skan0220

Kinetyka chemiczna 223
Po jego scałkowaniu otrzymamy wyrażenie
cB = akt cxp (-kt). (5.32)
Maksymalne stężenie produktu pośredniego osiągnie się, gdy
' = f (5.33)
Jeśli kb » ka (B natychmiast przechodzi w C), to wyrażenie (5.28) daje się łatwo przekształcić w
cc = a(] - exp(~kat)\ (5.34)
gdyż
K exp (~kh t) < kb exp (~ka t).
W tym przypadku etapem decydującym o kinetyce całego procesu jest więc reakcja A —> B.
Przykład 5.10. Okresy połowicznego rozpadu izotopu 29oTh i ^Pa wynoszą
29oTh 2^Pa + (S t\/2 = 24,1 dni,
29]Pa % 2l42U + p tm = 6,75 h.
Wychodząc z 2000 atomów 29oTh w chwili t = 0, obliczyć liczbę atomów Th, Pa i U po 12 h.
Rozwiązanie. Reakcja rozpadu Th jest reakcją następczą, której pierwszy etap opisany jest przez równanie (5.25)
N= N0&xp(-kat),
gdzie
ln 2
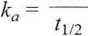
ln 2
24,1 • 24
1,198 • 10_3łrl.
Po czasie t = 12 h
JVTh = 2000 • exp (-1,198 • 10-3 • 12) = 2000 • 0,9857 = 1971 atomów.
Liczbę atomów Pa obliczymy z równania (5.27)
Npa -
Móka
kb - kt
(exp (~ka i) - exp (~kh t)).
Wyszukiwarka
Podobne podstrony:
68830 skan0219 222 Kinetyka chemiczna Stąd po scałkowaniu mamy 222 Kinetyka chemiczna CB k„ a a h -
skan0205 208 Kinetyka chemiczna więc po zlogarytmowaniu ln/1/2 = const + (1 - ń) ln c0 powinno się o
skan0218 Kinetyka chemiczna 221 w którym po etapie (1), z szybko ustalającą się równowagą, następuje
482 [1024x768] 492 KINETYKA CHEMICZNA to po wstawieniu (6.61) do (6.60) otrzymamy ((ES)*)
50717 skan0204 Kinetyka chemiczna 207 D = 1 Dla x = 0 otrzymamy Wab = 1 + a stąd ( b - 2 a)2 2 a&nbs
36100 skan0214 Kinetyka chemiczna 217 W chwili t spełnione są równocześnie dwa równania: 1) Pno2(0 =
65470 skan0230 Kinetyka chemiczna 233 Przykład 5.15. W kilku temperaturach dla reakcji *1 H2(g) + l2
skan0228 Kinetyka chemiczna 231 W przybliżeniu stanu stacjonarnego mamy = ki[A]" - *2[L][A] + a
więcej podobnych podstron