Image3 (70)

86 Rozwiązania zadań ze zbioru "MENDLA "
Punkty D i B leżą na tej samej izobarze, więc ciśnienie Pd = Pb, a więc róvvnj" zachodzi nierówność: *
Pa < pe
Podobnie porównamy ciśnienia i temperatury punktów D i E.
PD • Vp PE • Ve
Td
PD • VD
Td
Te ’
PE • VP
/: Vd
ale
Ve = Vd,
PD PE
Td Te PD = PE •
/•Td
Td
Te
Z wykresu mamy:
Te >Td -» 1
Te
Stąd również musi zachodzić:
Pd < Pe
Punkty E i C leżą na jednej izobarze, więc pe = pc. Po podstawieniu mamy:
Pd <pc
Z wykresu odczytaliśmy również, że Pd = Pb stąd pb< pc-Ostatecznie otrzymamy:
Pa < Pb < pc
Odp.: Między ciśnieniami przemian zachodzi związek pa < pb < pc.

Z treści zadania wynika, że :
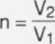
stąd V2 = n • Vi
Dla przemiany izobarycznej możemy zapisać:
Vl_ Vg
Ti " T2
Vi-T2 = V2-Ti /: Vi
stąd
_V2Ti
Vi
Aby znaleźć związek między temperaturą końcową T2 i początkową Ti wystarczy obliczyć ich stosunek.
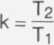
Po podstawieniu:
V2 • Ti
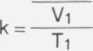
k = , lecz V2 = n • Vi
Vi T1
n • Vi . ,
stąd k = —-— , a więc k = n = 3
Vi
Odp.: Temperatura gazu wzrosła trzykrotnie.
Zadanie 597 str.120
Dane: Szukane:
S = 0,01 nr£ - pole przekroju cylindra Ah = ? - przesunięcie tłoka
po ogrzaniu gazu
Ti = 300K
Vi =2-10 3m3 S- pole przekroju cylindra
T2 = 330K
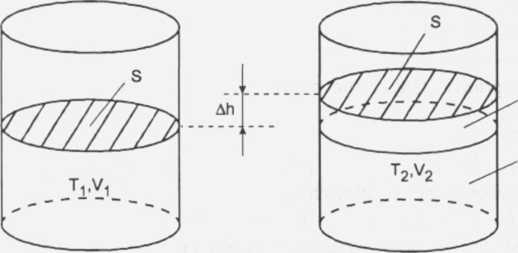
AV
V1
V2=V1+AV
Ciśnienie pod tłokiem w obu przypadkach jest równe ciśnieniu atmosferycznemu, więc zgodnie z prawem Gay-Lussaca mamy:
|
V1 v2 | ||
|
Ti "T2 | ||
|
< —i ro II H < ro |
lecz |
V2 = Vi + AV |
|
gdzie |
AV = Ah•S | |
|
stąd |
V2 = Vi + Ah • S |
Po podstawieniu za V2 mamy:
Wyszukiwarka
Podobne podstrony:
Image30 (23) 147 Rozwiązania zadań ze zbioru "MENDLA Dane: V = 5000 dm3 = 5 ni3Zadanie 648 str.
Image32 (23) 151 Rozwiązania zadań ze zbioru "MENDLA N ■ m = J 3 • 100000Pa • 1 rr? U = 150000-
Image34 (23) 155 Rozwiązania zadań ze zbioru "MENDLA ale Eśr = U = N • Eśr m • v§r stąd U = N 2
Image31 (21) 149 Rozwiązania zadań ze zbioru "MENDLA" 4200- J (0.1 kg ■ 39.33°C- 0,05kg •
Image36 (16) 159 Rozwiązania zadań ze zbioru "MENDLA 0,209 Q =- Q = 5112 J m2 mol •
Image38 (17) 163 Rozwiązania zadań ze zbioru "MENDLAZadanie 670 str.133 Dane:
Image3 (72) 10 Rozwiązania zadań ze zbioru "MENDLA o mv£ T = - • —2— = 3 k m • v. 3kJednostki:
więcej podobnych podstron