430 [1024x768]

439
POLARYZACJA ELEKTROLITYCZNA I NADNAPIĘCIE
elektrody kalomelowej) w połowie wysokości pólfali. Sens fizyczny potencjału półfali wynika z równania opisującego zależność potencjału kroplowej elektrody rtęciowej od natężenia prądu. Równanie to zwane równaniem Hey-rovsky’ego-ilkovića ma dla redukcji katodowej na kroplowej elektrodzie rtęciowej postać:
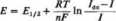
(5.212)
gdzie
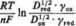
(5.213)
zaś: /d0 — maksymalne natężenie katodowego prądu dyfuzyjnego; I—natężenie prądu; Dre<l i Dox — współczynniki dyfuzji postaci zredukowanej i utlenionej badanej substancji; El/2— potencjał półfali; E° — standardowy potencjał oksydacyjno-redukcyjny badanej substancji.
Jak widać, potencjał półfali El/2 mający ścisły związek zc standardowym potencjałem oksydacyjno-redukcyjnym badanej substancji, jest dla danej substancji wielkością charakterystyczną, niezależną od stężenia, a wyznaczenie go metodą analizy polarograficznej stanowi podstawę jakościowej analizy składu roztworów metodą polarograficzną.
Wyszukiwarka
Podobne podstrony:
420 [1024x768] POLARYZACJA ELEKTROLITYCZNA I NADNAPIĘCIE 429 (5.181) zaś szybkość procesu rozpuszcza
422 [1024x768] POLARYZACJA ELEKTROLITYCZNA I NADNAPIĘCIE 431 Napięcie rozkładu powinno być w tym prz
424 [1024x768] POLARYZACJA ELEKTROLITYCZNA I NADNAPIĘCIE 433 Całkowita szybkość docierania jonów do
428 [1024x768] POLARYZACJA ELEKTROLITYCZNA I NADNAPIĘCIE 437 na oczywisty fakt, że jony, które przen
419 [1024x768] Polaryzacja elektrolityczna i nadnapięcieSzybkość procesów elektrodowych Elektroda me
SEMINARIUM XIWŁAŚCIWOŚCI ELEKTRYCZNE MATERIAŁÓW -POLARYZACJA ELEKTRYCZNA I PRZEWODNICTWO
bipol pol dla stanu inwersyjnego ł i. Podaj polaryzację elektrod tranzystora bipolarnego dla mwersyj
bipol pol dla stanu przewodzenia 9. Podaj polaryzację elektrod tranzystonTbipoiarnego dla stanu prze
CCF20110325�002 Rys. 1 Dielektryk w polu elektrycznym 2.2 Polaryzacja elektronowa Polaryzacja elektr
304 [1024x768] część pięta elektrochemia
312 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 321 Zatem współczynnik izotermiczny van’t Hoffa wy
320 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 329 przestrzeni środkowej, a stąd do przestrzeni k
322 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW W równaniu tym liczby przenoszenia /J i /£ są wart
324 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 333 zakrcskowaną płaszczyznę na rys. 5.4. W ciągu
więcej podobnych podstron