324 [1024x768]

WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 333
zakrcskowaną płaszczyznę na rys. 5.4. W ciągu 1 s do płaszczyzny tej dotrą wszystkie aniony znajdujące się w odległości v-. Ponieważ cała długość naczyńka, w którym znajduje się 1 gramorównoważnik wynosi / cm, więc w ciągu I s przez zakreskowaną płaszczyznę na rys. 5.4 przepłynie ułamek równoważnika kationów równy t>+// oraz ułamek równoważnika anionów równy v-//. Odpowiednie liczby kationów i anionów, które w ciągu 1 s przepłyną przez za-
kresowaną płaszczyznę wynoszą: ~ • ~ oraz Natężenie płyną
cego prądu otrzymamy mnożąc liczby tych jonów przez ich ładunki:
T Nl e -iVA-v+
/+ - — * -y- * *+ * e - -.—
(5.24)
Z+ / /
/ _ . z e _ 6 ' Ną ‘ V-
Oznaczając przez i szybkość poruszania się jonów w roztworze nieskończenie rozcieńczonym, otrzymujemy przez przyrównanie równań (5.23) i (5.24):
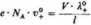
Ponieważ: e - Nx = F (stała Faradaya), zaś • j = E(E— natężenie pola elektrycznego wyrażone w V • cm-1), zatem:
(5.25)
(5.26)
EX%
F
Analogiczne postępowanie dla anionu daje:
-o « E X°-
®- * p
Otrzymane szybkości poruszania się jonów są więc ściśle uzależnione od gra- ruchliwości nicznych przewodnictw jonowych a takie od natężenia pola elektrycznego. ,ONÓW Kładąc E = 1 V*cm-1(100 V- m-1) otrzymujemy szybkości jonów w polu o natężeniu jednostkowym, zwane ruchliwościami:

Wyrażając graniczne przewodnictwa jonowe za pomocą ruchliwości, można
Wyszukiwarka
Podobne podstrony:
312 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 321 Zatem współczynnik izotermiczny van’t Hoffa wy
314 [1024x768] 323 WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW po rozpuszczeniu kryształu w wodzie mogłoby do
316 [1024x768] 325 WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW Kation H+ po zaadsorbowaniu na powierzchni ele
320 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW 329 przestrzeni środkowej, a stąd do przestrzeni k
322 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW W równaniu tym liczby przenoszenia /J i /£ są wart
308 [1024x768] 317 WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓW Tabela 5.1 Przewodnictwa równoważnikowe wodnyc
310 [1024x768] 31* WŁAŚCIWOŚCI ROZTWORÓW ELEKTROLITÓWTeoria dysocjacji elektrolitycznej Początki wsp
318 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW E1ZJLTR0UTÓW 327 Elektroliza wodnego roztworu NaCi jest przykła
274 [1024x768] WŁAŚCIWOSO ROZTWORÓW 283 mm Hg. Obliczyć masę cząsteczkową benzaldehydu. Zakładamy, ż
276 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW 285 przy czym m2 — masa substancji rozpuszczonej, m, — masa
280 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW 289 Obliczmy bracę maksymalną dla procesu przeniesienia I mola
282 [1024x768] WŁAŚCIWOŚCI ROZTWORÓW 291 rtijRT ^ m2RT Mty ’ * " /IV 3
80525 skan0262 6. Elektrochemia Właściwości roztworów elektrolitów różnią się od właściwości roztwor
270 [1024x768] Właściwości roztworówTermodynamiczna charakterystyka roztworów Zgodnie z definicją (p
larsen0744 744 II Anestezjologia ogólna roztwory elektrolitów, których skład jest jeszcze bardziej z
53 Zeszyty Problemowe - Maszyny Elektryczne Nr 73/2005 Na rys. 6 zostały przedstawione wyniki pomiar
więcej podobnych podstron