1
Z W I Ą Z K I F O S F O R O O R G A N I C Z N E
Aleksander Kołodziejczyk styczeń 2007.
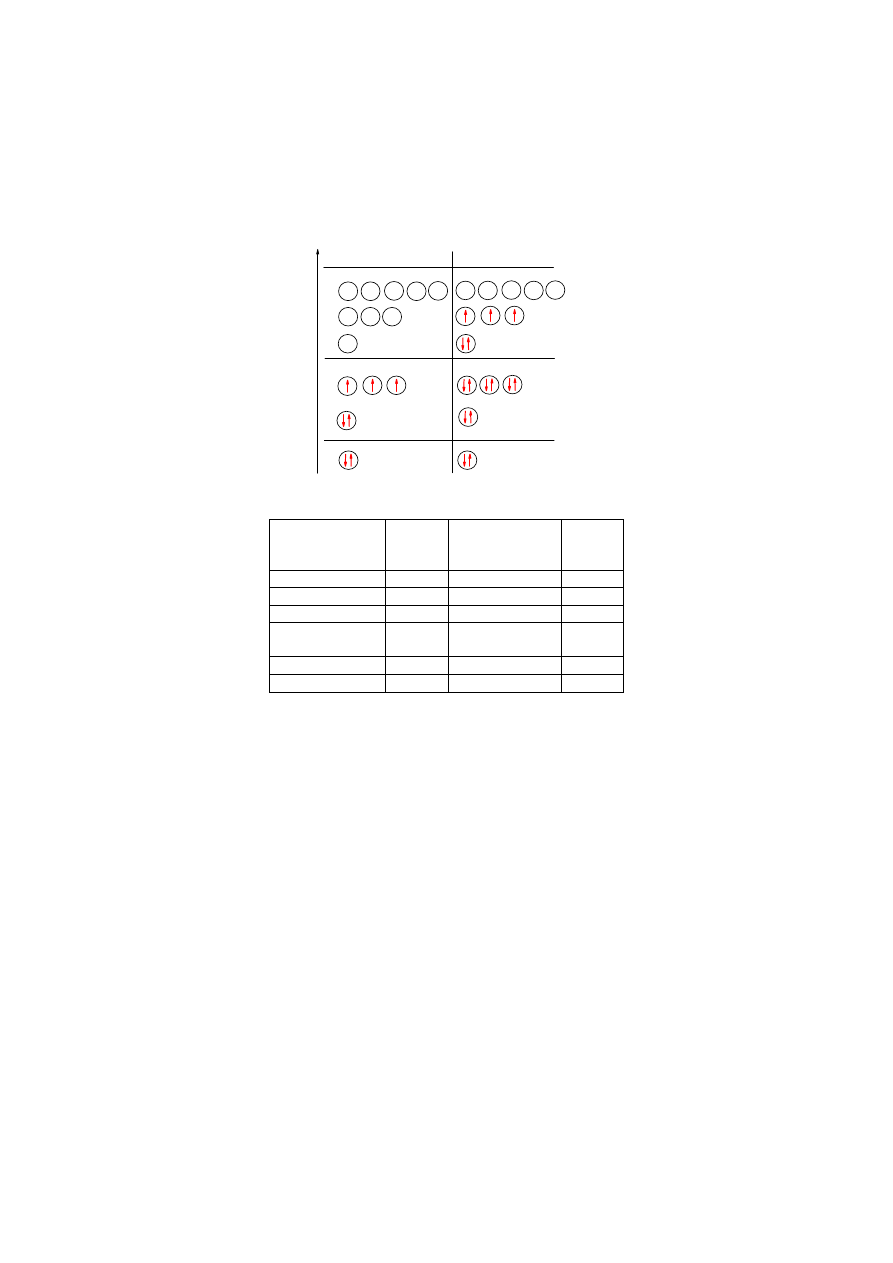
Struktura elektronowa atomów azotu i fosforu
1s
2s
2p
3s
3p
3d
azot
fosfor
K
L
M
Energia wiązań w związkach azotu i fosforu
Wiązanie N-Z
Energia
wiązania
kcal/mol
Wiązanie P-Z
Energia
wiązania
kcal/mol
P-H w PH
3
77
N-H w NH
3
93,4
P-C w P(CH
3
)
3
63
N-C w N(CH
3
)
3
72
P-O
95
N-O
50
P=O
140
N=O w R-O-
N=O
145
P-Cl
78
N-Cl
46
P-P
48
N-N
30
Wnioski
1. Wiązanie fosfor-wodór (P-H) jest znacznie słabsze niż wiązanie azot--wodór (N-H);
77 w porównaniu do 93,4 kcal/mol.
2. Pojedyncze wiązanie fosfor-tlen (P-O) jest wiązaniem bardzo mocnym, mocniejszym niż
pojedyncze wiązanie C-O i znacznie mocniejszym, niż wiązanie N-O;
odpowiednio 95, 90.9 i 50 kcal/mol.
3. Wiązanie podwójne fosfor-tlen (P=O) (
fosforylowe
, z udziałem orbitali d
ππππ
-p
ππππ
), jest około 45
kcal mocniejsze od pojedynczego wiązania P-O. Energia tworzenia grupy fosforylowej (P=O)
stanowi siłę napędową wielu reakcji tworzenia związków fosforu.
4. Wiązania fosfor-chlorowiec (P-X) są znacznie mocniejsze niż wiązania azot-chlorowiec,
energia wiązań P-X jest porównywalna do energii wiązań węgiel-chlorowiec (C-X).
Są to więc stosunkowo trwałe, ale i reaktywne wiązania.
5. Energia wiązań fosfor-węgiel (P-C) jest porównywalna z energią wiązań węgiel-węgiel (C-C).
Są to trwałe wiązania i rzadko dochodzi do ich rozerwania.
2
Fosfiny - alkilofosfory
Otrzymywanie
PX
3
+ RMgX
R-PX
2
- MgX
2
LiAlH
4
R-PH
2
fosfina 1
o
..
..
..
(monoalkilofosfor)
PX
3
+ 2 RMgX
R
2
PX
- 2 MgX
2
LiAlH
4
R
2
PH
fosfina 2
o
..
..
..
(dialkilofosfor)
P H
R
R
R
R
P CH
3
R
R
BuLi
..
..
P:
-
CH
3
I
..
fosfina 3
o
(trialkilofosfor)
Obecnie zamiast fosfin zalecane jest nazywanie tego typu związków alkilo(arylo)fosforami.
Jednak fosfiny są nadal w powszechnym użyciu.
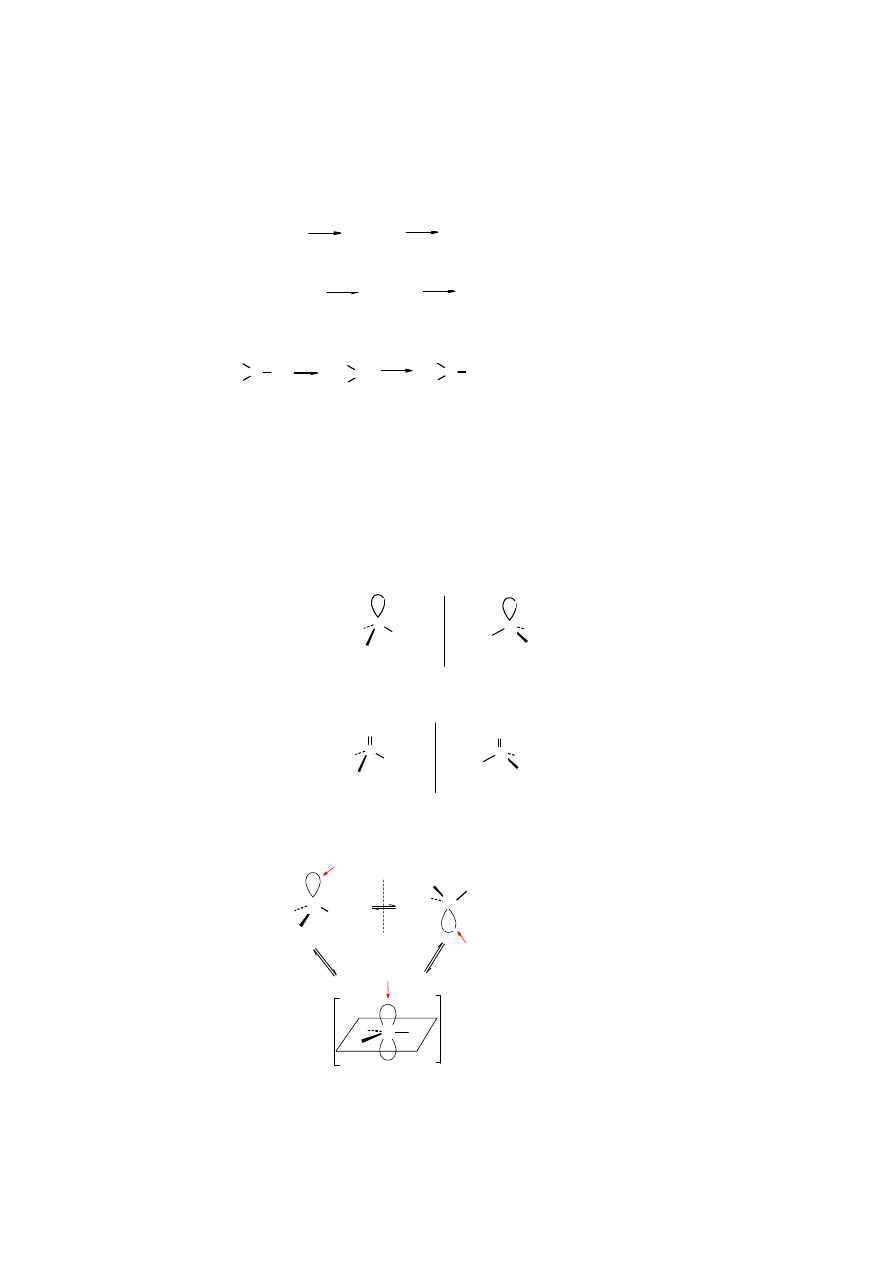
Chiralność fosfin
Fosfiny zawierające trzy różne podstawniki są chiralne. Czwartym podstawnikiem jest wolna
para elektronowa na atomie fosforu. W odróżnieniu od 3
o
chiralnych amin 3
o
chiralne fosfiny są
konfiguracyjnie trwałe, tzn. można je rozdzielić na enancjomery; nie ulegają one
racemizacji
w
normalnych warunkach. Wolna para elektronów na orbitalu d w związkach fosforu jest przyczyną
stabilnej konfiguracji enancjomerów.
P
CH
2
Ph
C
2
H
5
C
H
3
C
2
H
5
PhCH
2
CH
3
..
3d
..
3d
P
(R)-benzylo-
etylometylofosfina
(S)-benzylo-
etylometylofosfina
(R)-benzyloetylometylofosfor (S)-benzyloetylometylofosfor
Konfiguracyjnie trwałe są też chiralne tlenki fosfin.
P
CH
2
Ph
C
2
H
5
C
H
3
C
2
H
5
PhCH
2
CH
3
O
O
3d
3d
P
tlenek (R)-benzylo-
etylometylofosforu
tlenek (S)-benzylo-
etylometylofosforu
3
o
Chiralne aminy ulegają szybkiej racemizacji poprzez płaską formę, w której atom azotu
przyjmuje hybrydyzację sp
2
, a wolna para elektronowa obsadza orbital p.
R
R''
R'
R
R'
R''
R
R''
R'
N sp
3
N sp
3
N sp
2
w aminach następuje
szybka zmiana konfiguracji,
dlatego ich enancjomery nie
są trwałe, ulegają szybkiej
racemizacji
orbital sp
3
orbital sp
3
orbital p
..
N
..
N
..
N
3
Szybka racemizacja chiralnych amin zachodzi poprzez zmianę hybrydyzacji atomu azotu.
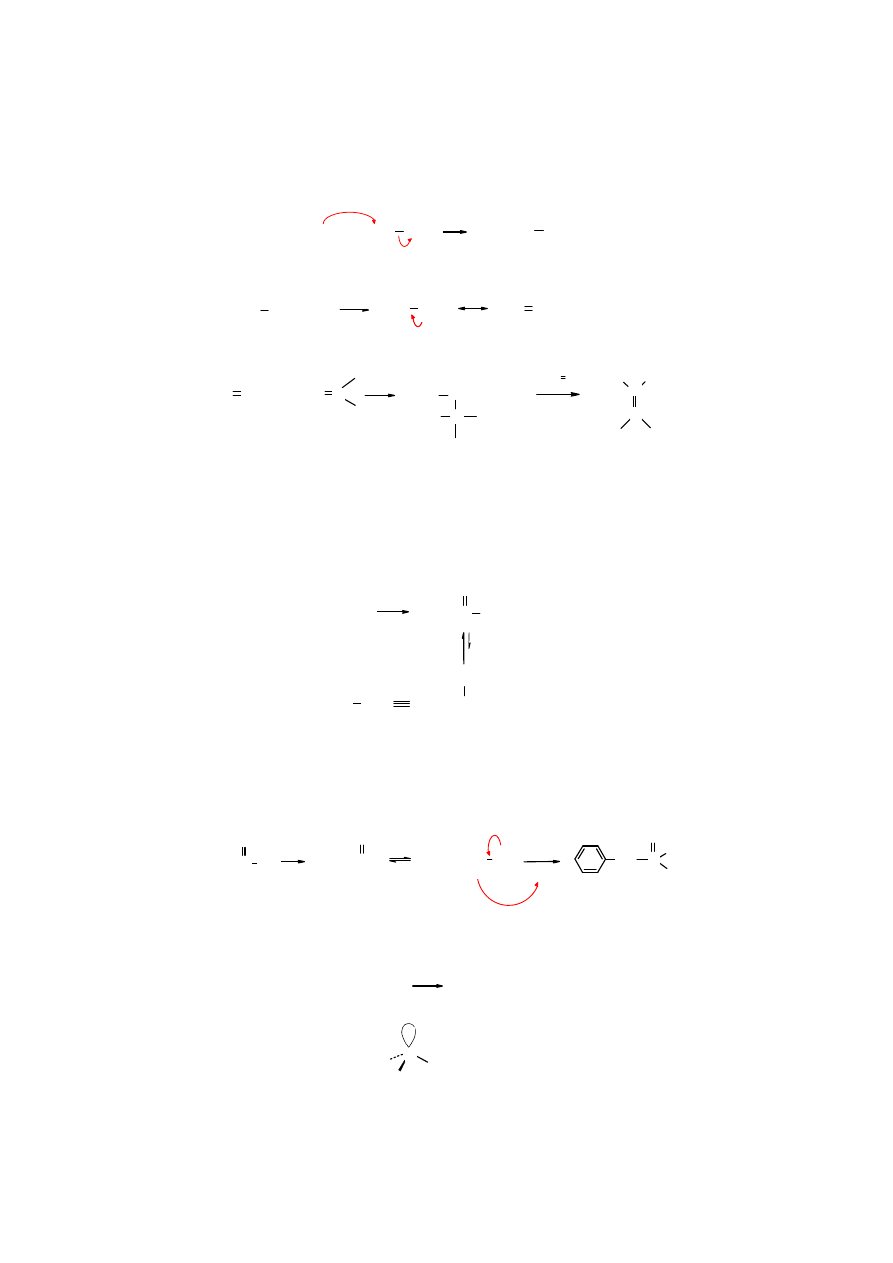
Trifenylofosfina
służy jako reagent w
reakcji Wittiga
. Z niej powstaje ylid fosforowy.
X
CH
2
R
Ph
3
P
Ph
3
P: + RCH
2
S
N
2
+
X
-
trifenylofosfina
halogenek alkilu sól fosfoniowa
CH
2
R
Ph
3
P
CHR
Ph
3
P
CHR
Ph
3
P
+
X
-
BuLi
+
-
..
ylid fosforanowy
Reakcja Wittiga
CHR
Ph
3
P
O
CHR
O
PH
3
P
R
H
O
Ph
3
P
-
+
+
C
C
C
betaina
ylid fosforanowy
zwiazek
karbonylowy
C
-
tlenek
trifenylofosfiny
alken
Tlenowe pochodne związków fosforoorganicznych
Związki fosforoorganiczne zawierające atom lub atomy tlenu wywodzą się odpowiednio od
kwasu fosforowego(III) – fosforawego lub fosforowego(V) – fosforowego.
Estry kwasu fosforowego III (fosforyny) powstają w reakcji trichlorku fosforu z alkoholem.
Alkoholiza
w środowisku kwaśnym prowadzi do H-fosforynów.
H
O
OH
OH
PCl
3
+ 3 ROH
(RO)
2
P
fosforyn dialkilowy
(
dialkoksyoksyfosfor
lub dawniej H-fosforyn
)
(RO)
2
P:
forma tautomeryczna,
mniej trwała
(RO)
2
P
..
..
:
:
:
..
..
..
- HCl
Zalecana obecnie nazwa dla fosforynu dialkilowego:
dialkoksyoksofosfor
.
Pod wpływem silnych zasad atom wodoru przy atomie P zostaje oderwany, a powstały anion
ulega
alkilowaniu
na atomie fosforu. W ten sposób powstają P-podstawione fosforyny
dialkilowe.
H
O
O
O
CH
2
O
OEt
OEt
-
(EtO)
2
P
..
NaH
:
:
:
:
..
..
..
..
..
-
PhCH
2
-Cl
- Cl
-
P
(EtO)
2
P
(EtO)
2
P
benzylofosfonian
dietylu
fosforyn
dialkilowy
Alkoholiza
halogenków fosforu(III) prowadzi do fosforynów trialkilowych.
RO
RO
OR
PCl
3
+ 3 EtOH
P(OEt)
3
fosforyn trietylu
:
- Cl
-
:B
:
ester kwasu
fosforawego
P
..
4
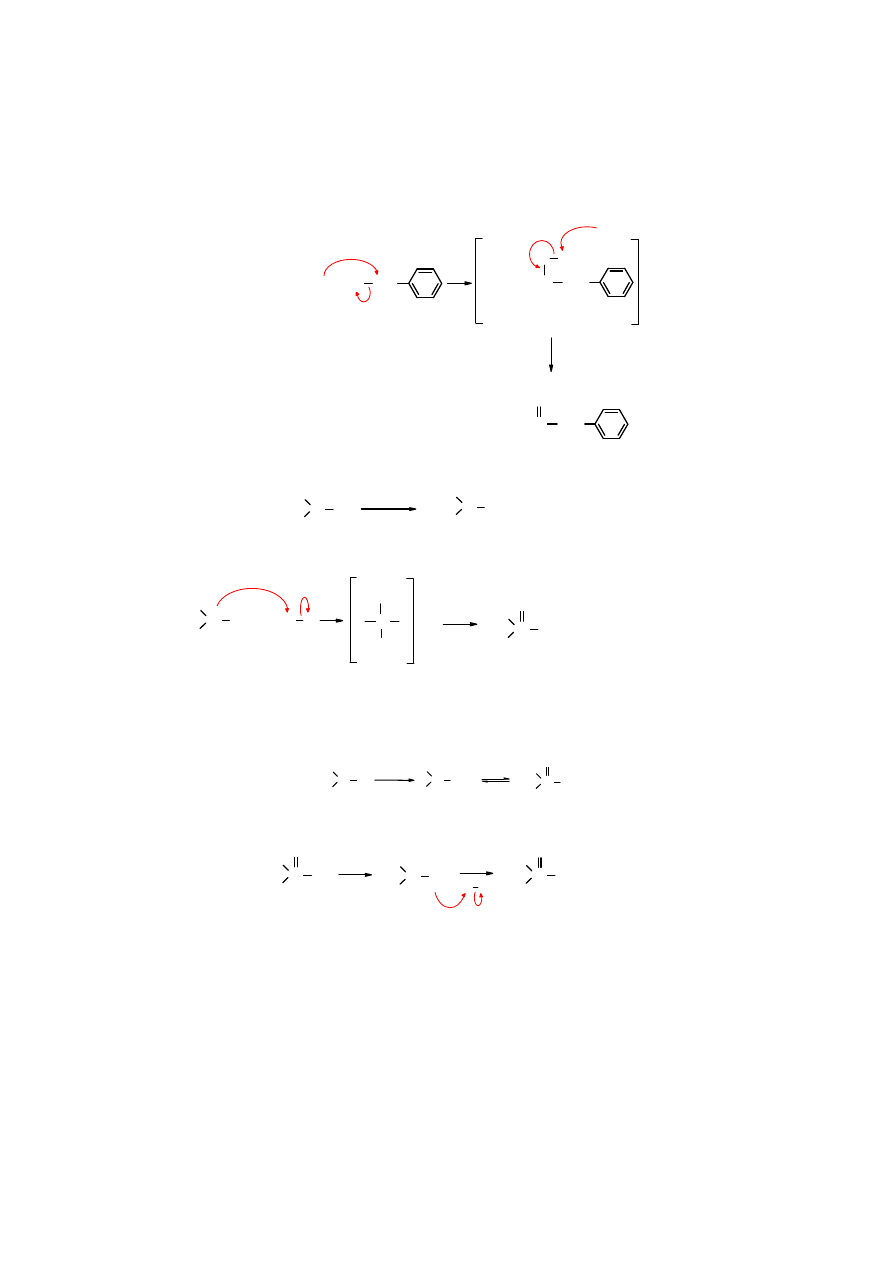
Fosforyny trialkilowe stosuje się w reakcji Arbuzowa do otrzymywania P-podstawionych
fosfonianów.
CH
2
CH
2
O C
2
H
5
CH
2
O
fosforyn trietylu
(C
2
H
5
O)
3
P: + Cl
(C
2
H
5
O)
2
P
Cl
-
+
- C
2
H
5
Cl
(C
2
H
5
O)
2
P
benzylofosfonian dietylu
Znane są również estry kwasu fosfinawego, otrzymuje się je z chlorodialkilofosfin.
Cl
R
R
OEt
R
R
P
..
EtOH, :B
- HCl
P
..
fosfinian etylu
Fosfiniany alkilowe można
alkilować
, powstaje przy tym tlenek trialkilofosfiny.
OEt
R
R
X
OEt
R
R
R
R
R
R
O
P
..
fosfinian etylu
+ R
P
X
+
-
sól alkoksy-
fosfoniowa
- EtX
P
tlenek trialkilofosfiny
trialkilooksofosfor
(wg zaleceń współczesnej nomenklatury)
Tlenek trialkilofosfiny może być też otrzymany poprzez
alkilowanie
tlenku dialkilofosfiny.
Cl
R
R
OH
R
R
H
R
R
O
P
..
HOH
- HCl
P
..
tlenek 2
o
fosfiny
P
H
R
R
O
O
R
R
R X
R
R
R
O
..
P
tlenek dialkilofosfiny
(tlenek 2
o
fosfiny)
NaH
P
:
-
..
.. :
P
:
..
tlenek trialkilofosfiny
(
dialkilooksofosfor
)
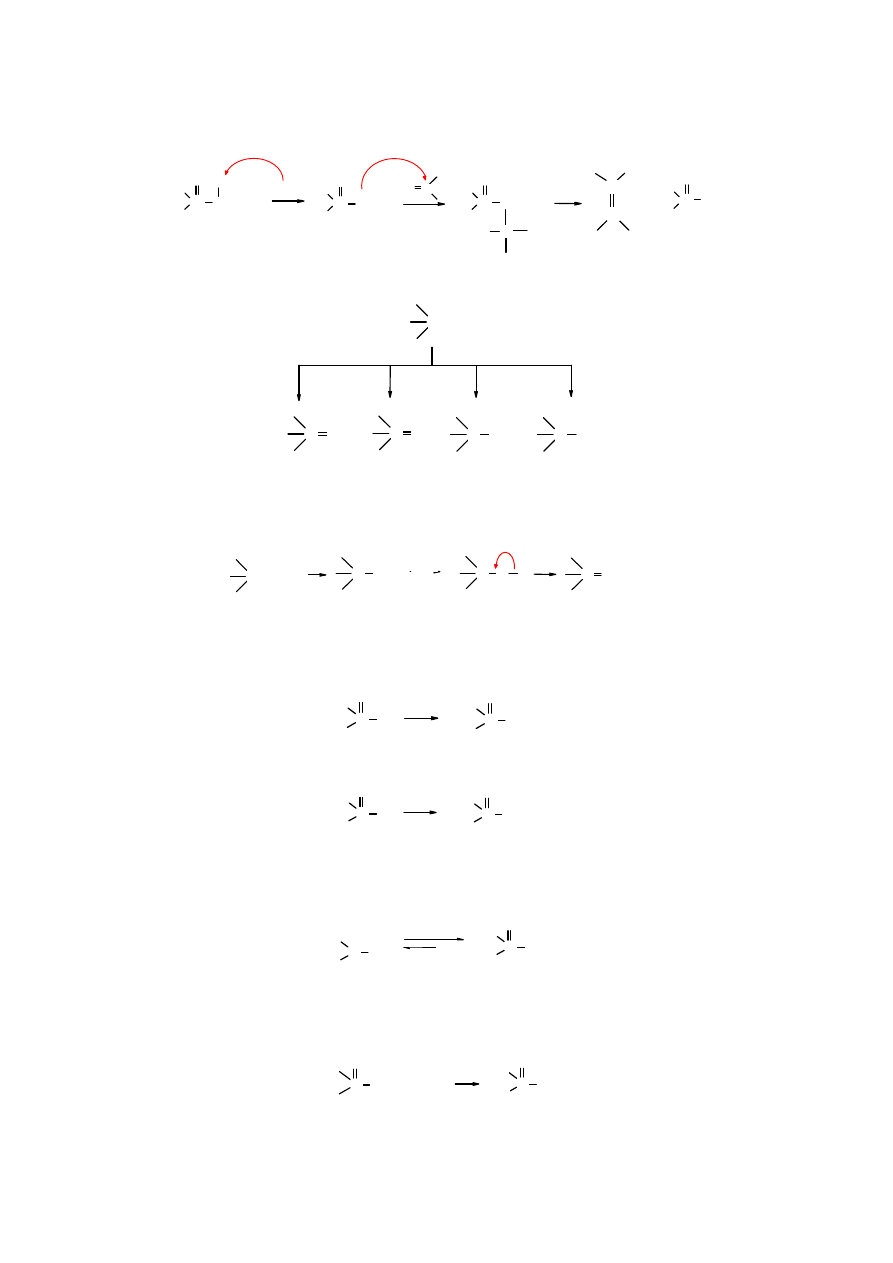
Reakcja Wittiga-Hornera
Reakcja Wittiga-Hornera podobnie jak reakcja Wittiga służy do przekształcania związków
karbonylowych w alkeny, przy współudziale związków fosforoorganicznych. Reakcje różnią się
stosowanym reagentem fosforoorganicznym; w reakcji Wittiga wykorzystywane są ylidy
fosforowe, a w reakcji Wittiga-Hornera tlenki fosfin (alkilooksofosfory).
5
CH-R'
R
R
O
CH-R'
R
R
O
H
CH-R'
R
R
O
O
R'
H
R
R
O
O
O
..
:
P
tlenek trialkilofosfiny
BuLi
P
-
- BuH
..
P
-
C
..
C
C
alken
+
P
-
..
.. :
C
Reaktywność fosfin
S
O
R
X
P:
S
[O]
RX
X
2
P
P
trialkilo-
tiofosfor
trialkilo-
oksofosfor
P
X
+
-
P
X
+
-
halogenek
fosfoniowy
sól halogeno-
fosfoniowa
Sól kationu halogenofosfoniowego powstaje w wyniku działania halogenu na fosfinę. Służy do
otrzymywania tlenków fosfin.
X
O H
O
P: + X
2
P
X
+
-
HOH
OH
-
P
+
OH
-
P
tlenek fosfiny
fosfina
halogenek
halogenofosfoniowy
2
o
Tlenek fosfiny może być utleniony do kwasu fosfinowego, najdogodniej za pomocą nadtlenku
wodoru.
H
O
R
R
OH
O
R
R
P
H
2
O
2
P
dialkilookso-
fosfor
kwas
dialkilofosfinowy
Natomiast fosforyn pod wpływem utleniacza zostaje przekształcony w fosforan.
H
O
EtO
EtO
OH
O
EtO
EtO
P
[O]
P
dietoksy-
oksofosfor
fosforan dietylowy
Kwas fosforowy(III) (H
3
PO
3
), dawniej nazywany kwasem fosforawym wg obecnej
nomenklatury – kwas trihydrydotrioksofosforowy(2-) – jest w równowadze z kwasem
dihydroksyoksofosforowym [HPO(OH)
2
], dawniej nazywanym kwasem fosfonowym.
OH
O
H
O
H
H
O
O
H
O
H
P
P
kwas
fosforawy
kwas dihydroksy-
oksofosforowy
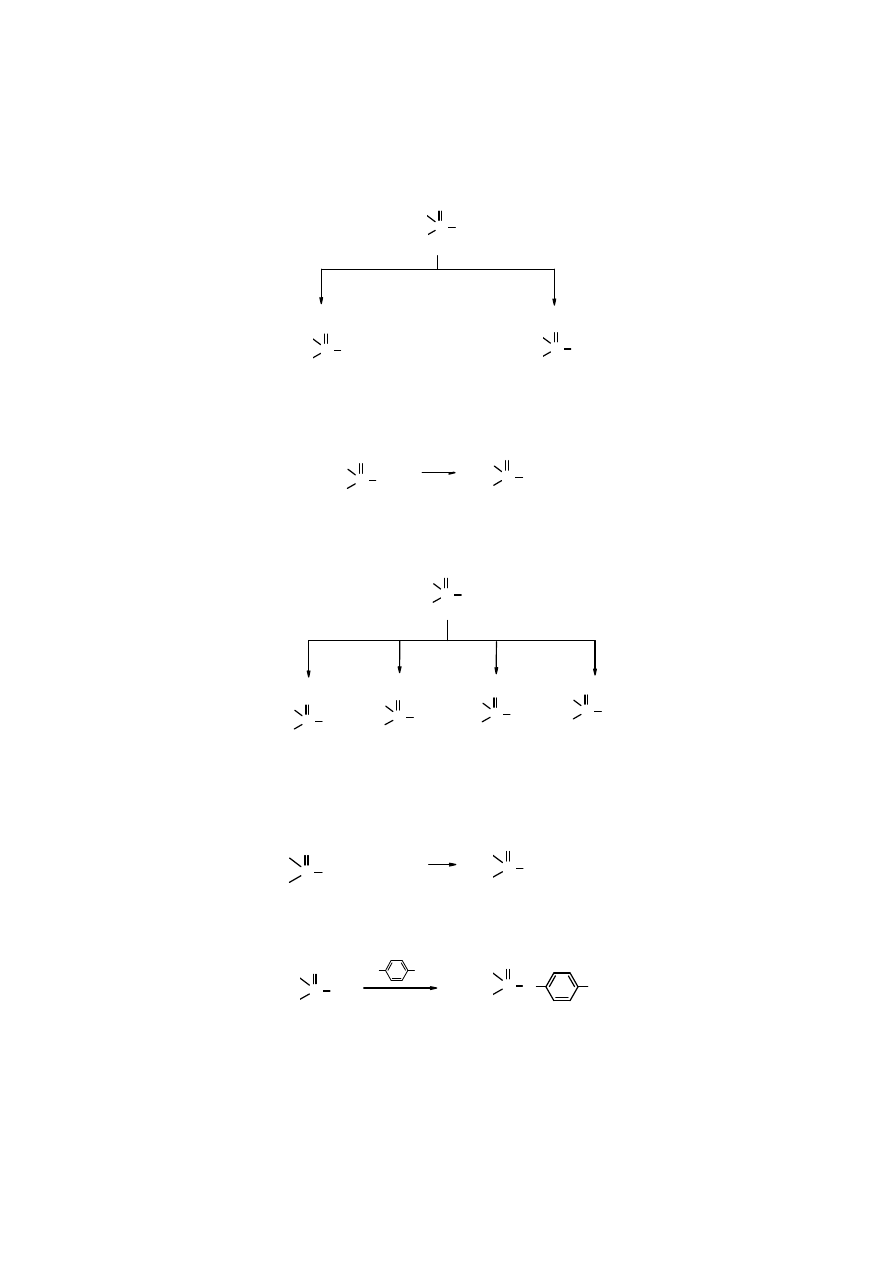
Estry kwasu fosforowego to fosforany. Znane są estry tego kwasu zawierające atom chloru
zamiast grupy hydroksylowej. Te chlorofosforany dialkilowe (arylowe) mają właściwości
chlorków kwasowych. Otrzymuje się je poprzez
alkoholizę
oksochlorku fosforu – OPCl
3
.
Cl
O
Cl
Cl
Cl
O
P
+ 2 ROH
:B
P
RO
RO
oksochlorek
fosforu
chlorofosforan
dialkilowy
6
Tego typu chlorki, podobnie jak chlorki kwasów karboksylowych, ulegają
amonolizie
przechodząc w amidy lub
alkoholizie
dając mieszane estry.
Cl
O
OR'
O
NHR'
O
P
RO
RO
R'OH
:B
:B
R'NH
2
P
RO
RO
P
RO
RO
fosforan trialkilowy dialkoksyoksyfosfonoamid
Chlorki organicznych kwasów fosforowych można otrzymać również działając pięciochlorkiem
fosforu na kwasy fosfinowe.
OH
O
R
R
Cl
O
R
R
P
PCl
5
P
kwas
fosfinowy
chlorek
kwasu
fosfinowego
Ulegają one
hydrolizie
,
amonolizie
,
alkoholizie
i
redukcji
, podobnie jak chlorki kwasów
karboksylowych.
Cl
O
R
R
OH
O
R
R
NR'
2
O
R
R
OR'
O
R
R
H
O
R
R
P
chlorek
kwasu
fosfinowego
HOH
:B
HNR'
2
:B
R'OH
LiAlH
4
P
P
P
P
kwas fosfinowy fosfinoamid dialkilofosfinian tlenek fosfiny
alkilu
Znane są też tlenowosiarkowe pochodne fosforu, np. w wyniku
alkoholizy
chlorku tiofosfonylu
powstają estry kwasu tiofosforowego.
Cl
S
Cl
Cl
OR
S
P
+ 3 ROH
:B
P
RO
RO
tiofosforan
trialkilowy
Można również startować z estrów kwasu tiochlorofosforowego.
Cl
S
O
H
NO
2
O
S
NO
2
P
RO
RO
:B
P
RO
RO
tiofosforan dialkilo-4-nitrofenylu
Z dioli i halogenków fosforu tworzą się estry cykliczne.

7
OH
OH
O
P
O
Cl
+ PCl
3
O
P
O
Cl
O
P
O
Cl
S
S
Estry kwasu fosforowego są popularne pośród ważnych związków organicznych biologicznie
czynnych. Znajdują się w kwasach nukleinowych, a także w
fosfolipidach
, ważnym elemencie
chociażby błony komórkowej. Fosfolipidy, podobnie jak tłuszcze (triacyloglicerole) są estrami
glicerolu
. W fosfolipidach tylko dwie grupy hydroksylowe
glicerolu
są acylowane resztami
kwasów tłuszczowych, trzecia zaś jest estrem kwasu fosforowego, zawierającego dodatkowo
jeszcze inną związaną estrowo cząsteczką organiczną, np.
etanoloaminę
,
serynę
,
cholinę
lub
linozyt
.
CH
2
OCOR
H
R'CO-O
CH
2
O P O
O
OH
R''
O
H
O
H
OH
OH
OH
C
-COR i R'CO-:
reszty acylowe
kwasów tłuszczowych
R'': reszty
-CH
2
-CH
2
-NH
2
,
-CH
2
-CH(NH
2
)COOH,
-CH
2
CH
2
-N
+
(CH
3
)
3
,
,
inozytu
etanoloaminy
seryny
choliny
fosfolipid
Glicerol
estryfikowany
tylko jedną cząsteczką kwasu fosforowego nosi nazwę
kwasu
glicerofosforowego
, a fosfolipid pozbawiony dodatkowej reszty organicznej R
’’ nazywany jest
kwasem fosfatydowym
.
CH
2
OH
H
CH
2
O P OH
O
OH
CH
2
OCOR
H
R'CO-O
CH
2
O P OH
O
OH
O
H
C
C
kwas glicerofosforowy
kwas fosfatydowy
Wyszukiwarka
Podobne podstrony:
Związki fosforu w organizmie człowieka, Chemia Przydatne dla studentów
25 Zwiazki fosforoorganiczne
ZWIĄZKI FOSFOROORGANICZNE
Związki fosforu w środkach myjących czyszczących i piorących
izomeria zwiazkow organicznych
Ostre Zatrucie Związkami Rtęci
3 ch org zwiazki funkcyjne
7 władza w bliskim związku
zwiazki kompleksowe 2
Związki chemiczne
ZWIAZKI AROMATYCZNE
25 Wyklad 1 Dlaczego zwiazki sa wazne
Patomechanizmy zaburzeń gospodarki wapniowo fosforanowej; osteoporoza
Hydroliza zwiazkow wielkoczasteczkowych 1
Ostre Zatrucie Związkami Żelaza
ZWIAZKI ZLOTA
więcej podobnych podstron