Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin 2008
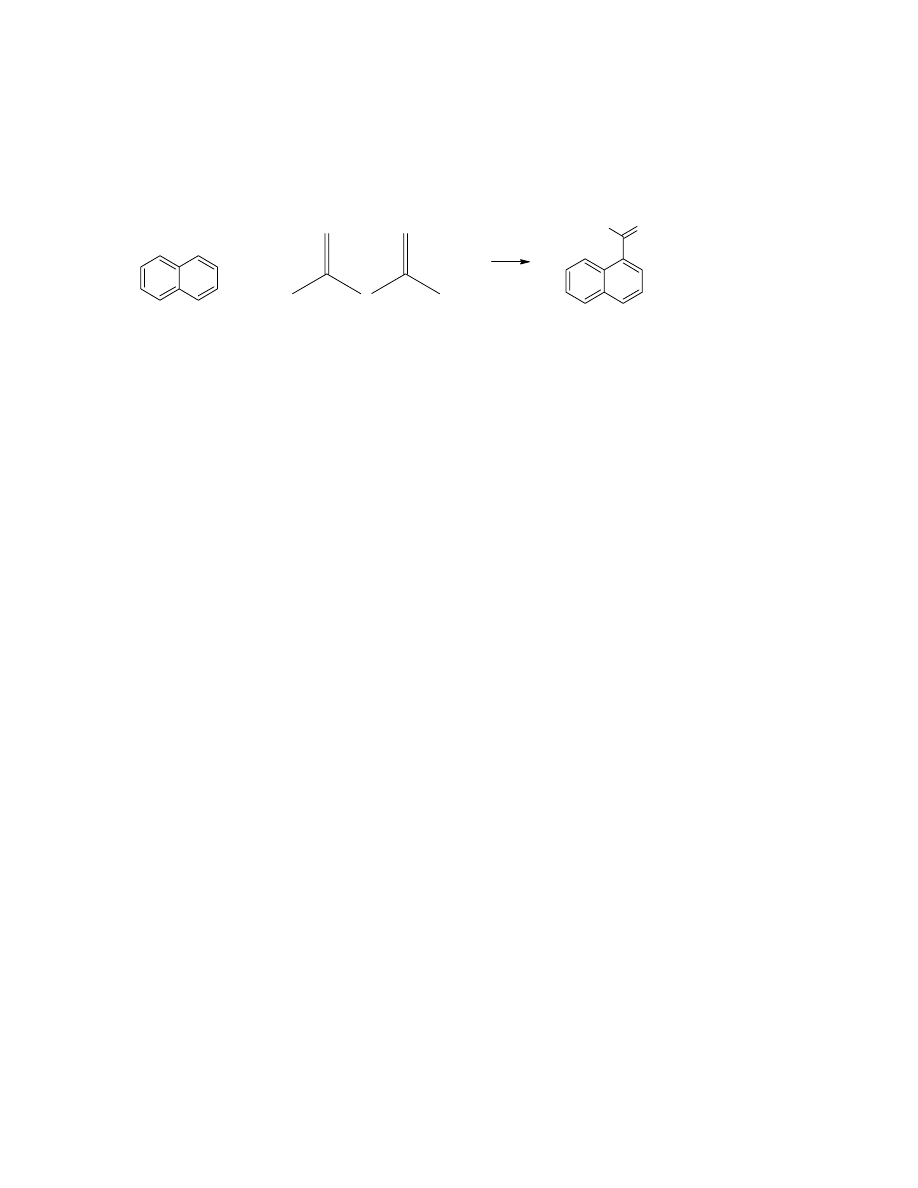
3. Synteza acetonaftonu
C
H
3
O
O
O
CH
3
+
AlCl
3
CHCl
3
C
H
3
O
W kolbie okrągłodennej 250mL rozpuszczono 7g (0.0524mola) chlorku
glinu w 15mL chloroformu. Dodano 2,6g bezwodnika octowego. Chłodzono w
łaźni wodnej z lodem przez pół godziny. Wkroplono roztwór naftalenu w
chloroformie (3,2g w 16mL). Chłodzono w łaźni wodnej. Roztwór zabarwił się na
pomarańczowo. Następnie (powoli, po kilku godzinach) zmienił kolor na
ciemnozielony. Pozostawiono na noc. Dodano 20mL 20% HCl celem rozłożenia
nadmiaru chlorku glinu. Dodano 20mL wody. Osad uległ rozpuszczeniu.
Wydajność: 60,48%
Pytanie kontrolne:
Jakich produktów można się spodziewać w tej reakcji oprócz 1-naftylo-
metyloketonu? Jaki wpływ mogą mieć warunki reakcji na stosunek
otrzymywanych produktów i dlaczego?
97
Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin 2008
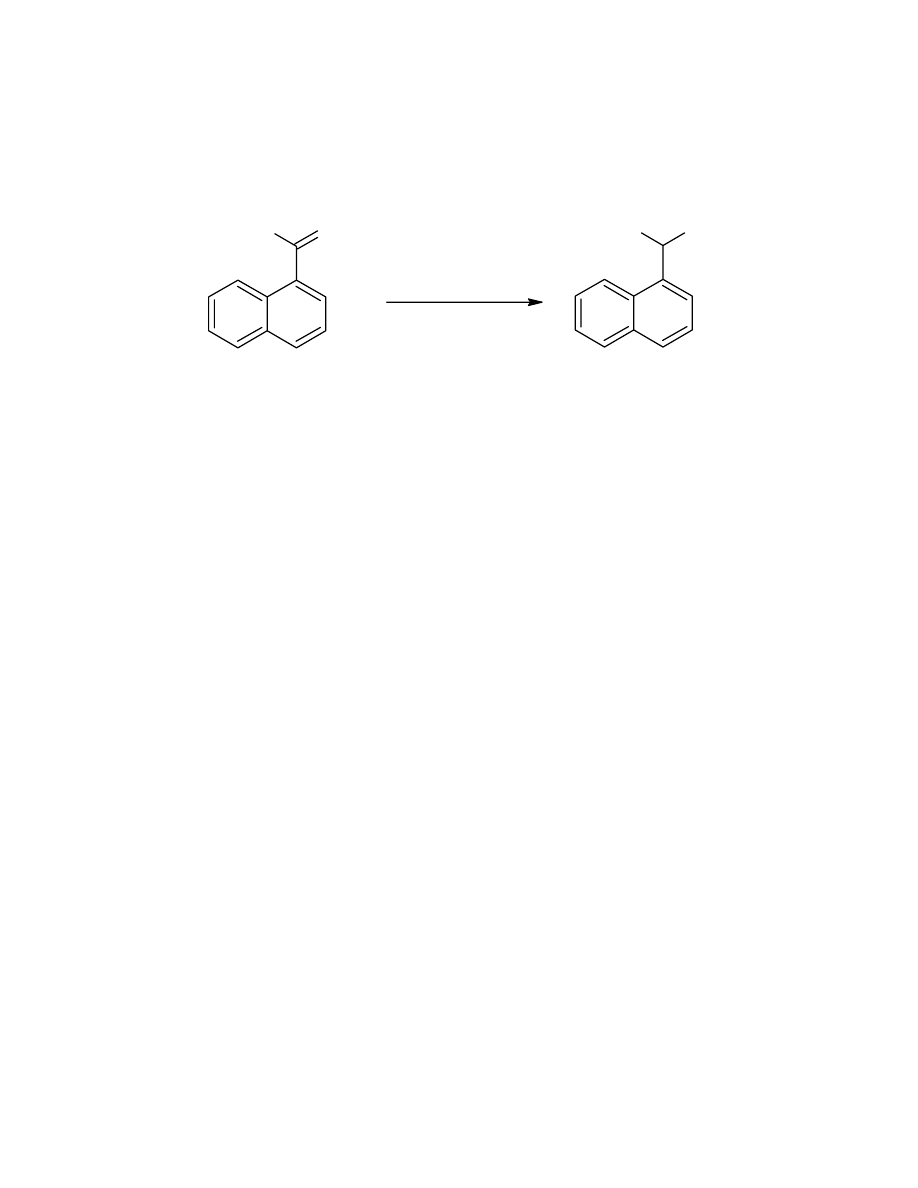
4. Otrzymywanie α-(1-naftylo)etyloaminy
C
H
3
O
C
H
3
NH
2
HCOOH, (NH
4
)
2
CO
3
(lub HCO
2
H, HCONH
2
)
Szkło laboratoryjne: kolba 100mL, wkraplacz 10mL, erlenmajerka
100mL, rozdzielacz 250mL, zestaw do sączenia, chłodnica zwrotna.
Aparatura: płaszcz grzejny elektryczny, pompka wodna.
Odczynniki:
Eter dietylowy (R12, R19, R22, R66, R67) – 140mL
Acetonafton (R22) – 9,12mL
Formamid (R61, S45, S53) – 8,81mL
Kwas solny (R34, S26, S45) – 25mL
Wodorotlenek sodu (R35, S26, S37/39, S45) – 20g
Kwas mrówkowy (R10, R35, S23, S26, S45) – 2,76mL
W kolbie o pojemności 50mL zaopatrzoną w krótką chłodnicę zwrotną z
umieszczonym nad nią wkraplaczem ogrzano 9,12mL acetonaftonu (60mmol) i
8,81mL formamidu (220mmol) za pomocą płaszcza elektrycznego do ok. 190°C.
Do tak przygotowanego roztworu (temperatura łagodnego wrzenia) wkroplono
w ciągu dwóch i pół godziny 2,76g kwasu mrówkowego 90%. Ogrzewano jeszcze
90minut. Pozwolono mieszaninie reakcyjnej ostygnąć, po czym dodano 25mL
98

Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin 2008
HCl. Roztwór ogrzewano 1 godzinę, schłodzono i dodano ok. 120mL wody ( w
rozdzielaczu 250mL). Ekstrahowano resztki nieprzereagowanych substratów ok.
20mL eteru dietylowego. Warstwę eterową odrzucono. Dodano NaOH, aż do
uzyskania pH silnie zasadowego (sprawdzono za pomocą papierka
uniwersalnego). Aminę ekstrahowano trzykrotnie porcjami po 40mL eteru
dietylowego. Suszono MgSO
4
, Odsączono, rozpuszczalnik odparowano. Uzyskano
6,80g aminy (wydajność 80%).
Gül N., Nelson J. H., J. Mol. Struct. 475 (1999), 121-130.
Pytanie kontrolne:
Jaka jest rola HCl, podać prawdopodobne produkty pośrednie tej
reakcji.
Dlaczego powinno sie stosować nadmiar HCOOH, (NH4)2CO3 (lub
HCOOH, HCONH2)?
Scharakteryzuj technikę ekstrakcji na przykładzie opisanego
doświadczenia i wyjaśnij, dlaczego produkt znajduje się raz w warstwie wodnej,
raz eterowej – organicznej.
99
Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli
Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin
2008
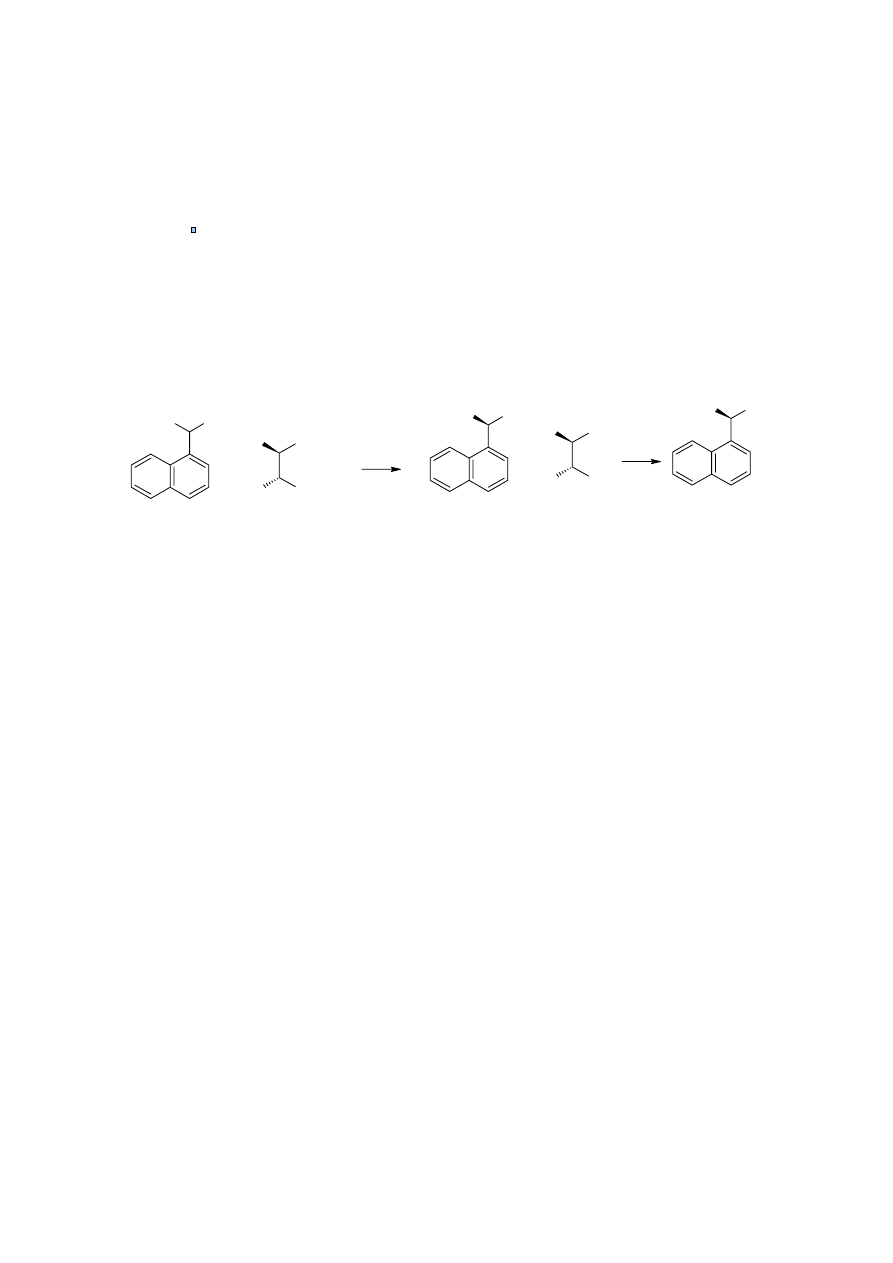
5. Rozdział α-(1-naftylo)etyloaminy na enancjomery. Budowanie
krzywej zależności skręcalności właściwej aminy i jej soli od ich czystości
optycznej. Praktyczna obserwacja efektu nieliniowości wzrostu skręcalności
wraz ze wzrostem czystości optycznej
C
H
3
NH
2
+
COOH
O
H
O
H
COOH
C
H
3
NH
3
+
COO
-
O
H
O
H
COOH
C
H
3
NH
2
MeOH
NaOH
Szkło laboratoryjne: kolba okrągłodenna 250mL,
chłodnica zwrotna, wkraplacz 25mL, fiolka, zestaw do sączenia,
rozdzielacz 250mL.
Aparatura: płaszcz grzejny elektryczny, pompka
wodna, łaźnia wodna.
Odczynniki:
Naftyloetyloamina (R36/37/38, S26, S36) – 3,4g
Kwas winowy (R36/37/38, S26, S37/39) – 3g
Metanol (R11, R23/24/25, S16, S36/37, S45, S7) – 40mL
W kolbie okrągłodennej 100mL wyposażonej w chłodnicę zwrotną i
kamyczki wrzenne rozpuszczono 3g kwasu L-winowego w 40mL metanolu,
ogrzewając płaszczem grzejnym.
1

Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli
Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin
2008
Następnie powoli, w ciągu pięciu minut wkroplono 3,4g
naftyloetyloaminy przy pomocy pipety.
Przeniesiono na uprzednio przygotowaną łaźnię wodną o
temperaturze 50°C. Po ochłodzeniu do temperatury pokojowej
zaobserwowano wzrost kryształów. Po 30 minutach krystalizacji odsączono
kryształy na lejku Schotta i przemyto 10mL metanolu. Kryształy suszono za
pomocą wodnej pompki próżniowej. Po wysuszeniu uzyskano 1,51g
kryształów. Przesącz pozostawiono do dalszej krystalizacji. W wyniku
analogicznego postępowania po drugiej krystalizacji (3 dni) uzyskano 1,95g
kryształów. Zmierzono skręcalności.
Za pomocą 10% wodnego roztworu NaOH (10mL) wydzielono wolną
aminę. Ekstrahowano eterem dietylowym (2x20mL), przemyto dwukrotnie
wodą (2x20mL), wysuszono i odparowano. Zmierzono skręcalności właściwe
dla wydzielonej aminy.
Zestawiono zmierzone przez studentów wyniki skręcalności soli aminy
z kwasem winowym i czystej aminy.
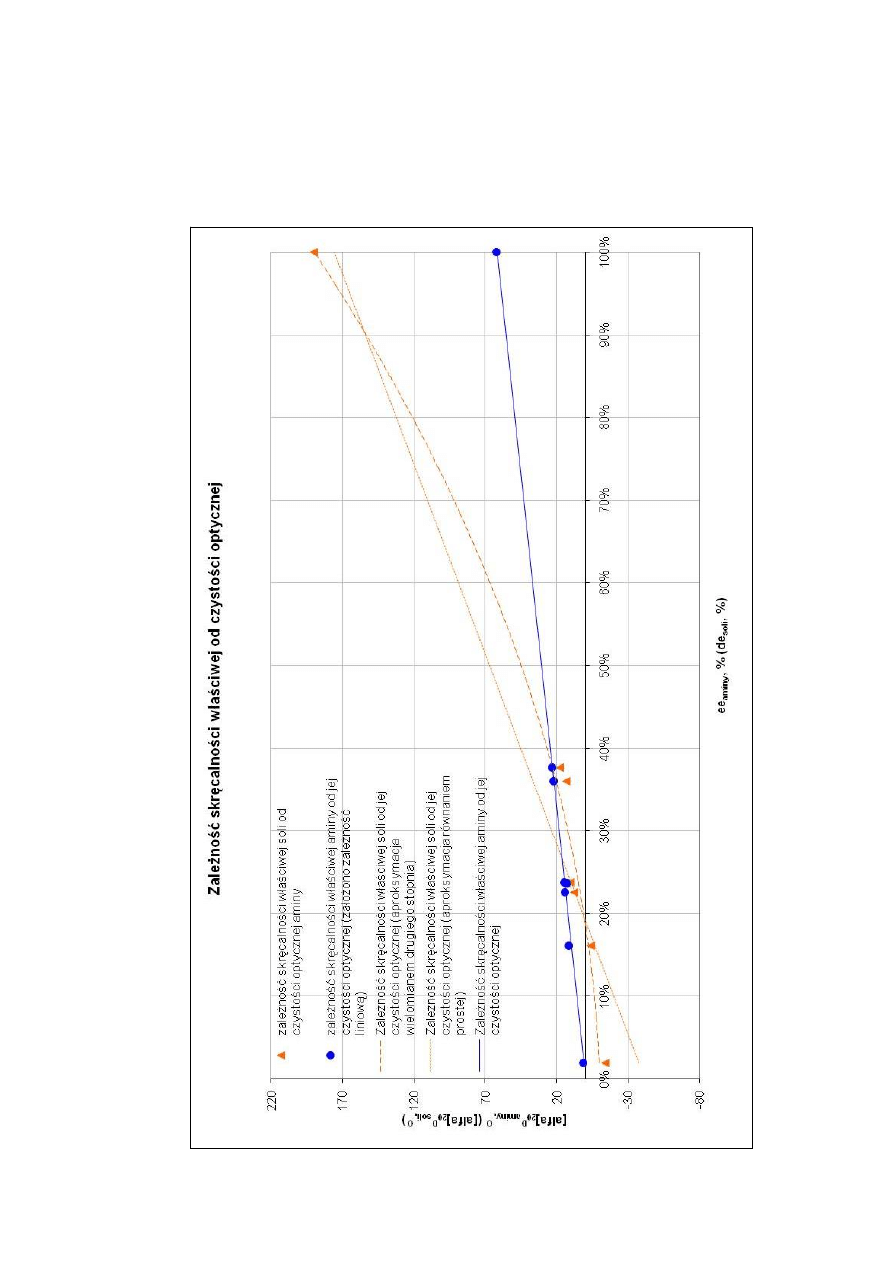
Wyniki przedstawiono graficznie sporządzając wykres zależności
skręcalności właściwej naftyloetyloaminy i skręcalności właściwej jej soli z
kwasem winowym od czystości enancjomerycznej aminy. Przy budowaniu
wykresu tej zależności w praktyce przyjmuję prostoliniowy przebieg zależności
skręcalności właściwej aminy od jej czystości optycznej (nie jest możliwe
pominięcie tego uproszczenia, gdyż czystość optyczną określam właśnie na
podstawie skręcalności; rzeczywisty przebieg tej zależności można uzyskać
wykorzystując techniki chromatograficzne lub NMR). W przypadku zależności
skręcalności właściwej soli od jej czystości optycznej (zakładam jednakową
2

Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli
Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin
2008
czystość optyczną soli i wydzielonej z niej aminy) wyraźnie widać, że równanie
drugiego rzędu opisuje tę zależność znacznie lepiej, aniżeli funkcja liniowa.
Przykładowy przebieg zależności przedstawiam na wykresie poniżej.
3
Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli
Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin
2008
4

Aneks 3 – (Skrypty studenckie) do pracy Adama Formeli
Opracowanie
doświadczeń laboratoryjnych na potrzeby pracowni studenckiej, Lublin
2008
5
Wyszukiwarka
Podobne podstrony:
2 Synteza acetonaftonu i otrzym Nieznany
Chemia związków wanadu Synteza i analiza chemiczna otrzymanych izopoliwanadów
SYNTEZA KWASU α-KAMFOLENOWEGO
Chemia, Chemia - Systematyka związków nieorganicznych, OTRZYMYWANIE TLENKÓW:w drodze bezpośredniej s
1 Synteza a fenyloetyloaminy i rozdział racemicznej α – fenyloetyloaminy (α PEA)
SYNTEZA KWASU α KAMFOLENOWEGO
Rodzaj alkoholu otrzymywanego w syntezie metodą Grignarda zależy od typu użytego związku karbonylowe
10 Metody otrzymywania zwierzat transgenicznychid 10950 ppt
06 Podstawy syntezy polimerówid 6357 ppt
6 wykad WiĄzania chemiczne[F]
8a Syntezy prostych aminokwasów
Wykład VIII Synteza układów sekwencyjnych
31 Metody otrzymywania i pomiaru próżni systematyka, porów
Wyk%c5%82ad Niepewno%c5%9b%c4%87 pomiaru
otrzymywanie soku jablkowego(1)
otrzymywanie polprzewodnikow
02 Metody syntezy organicznej VI s1id 3675
0002 Aceton
więcej podobnych podstron