Patofizjologia układu wydalniczego
M.P.
1
FUNKCJE NEREK
1. Wydzielnicza
• synteza
reniny
• hydroksylacja
25(OH)D
3
do 1,25(OH)
2
D
3
(aktywna forma witaminy D
3
-‐ kalcytriol)
• synteza
erytropoetyny
• synteza:
prostaglandyn,
kinin,
urodylatyny,
urokinazy
• synteza
insulinopodobnego
czynnika
wzrostu
(IGF-‐1),
czynnika
martwicy
nowotworów
(TNF),
transformującego czynnika wzrostu β (TGFβ), interleukiny 1, 6 i 8 (IL-‐1, IL-‐6, IL-‐8)
2. Metaboliczna
• degradacja:
− insuliny
− glukagonu
− parathormonu
(PTH)
− hormonu
wzrostu
(GH)
− prolaktyny
(PRL)
− hormonów
steroidowych,
tarczycowych,
amin
katecholowych
• synteza
elementów
strukturalnych
kłębuszka
nerkowego
• zachodzenie
glukoneogenezy
3. Funkcja wydalnicza
• wydalanie toksycznych produktów przemiany materii (toksyn mocznicowych):
− mocznik
− kreatynina
− kwas
moczowy
− cyjanki
− guanidyny
− indole,
fenole,,
imidazole
4. Utrzymanie równowagi wodno – elektrolitowej
• utrzymanie:
− izojonii
− izotonii
− izohydrii
− izowolemii
• rola
układu
RAA
• rola
antydiuretyny
• regulacja
gospodarki
wapniowo
–
fosforanowej
5. Utrzymanie równowagi kwasowo – zasadowej
• regeneracja jonów HCO
3
-‐
• buforowanie przy wykorzystaniu jonów PO
4
3-‐
(kwaśność miareczkowa)
• produkcja jonów NH
4
+
PATOMECHANIZMY NASTĘPSTW ZABURZONEJ CZYNNOŚCI NEREK
Zmiany diurezy
Tworzenie
moczu
przez
nerki
jest
zależne
od
prawidłowego
przepływu
krwi
i
skoordynowanej
czynności
wszystkich
części
nefronu.
Około
20-‐30
%
krwi
wyrzucanej
z
serca
przepływa
przez
nerki,
oznacza
to
że
u
dorosłej
osoby
nerkowy
przepływ
osocza
(RPF)
wynosi
ok.
600
ml/min.
Przepływ
krwi
przez
nerki
podlega
autoregulacji
przez
czynniki
humoralne,
takie
jak
angiotensyna
II
(obkurcza
naczynia)
oraz
prostaglandyny
(działają
rozkurczająco).
Przy
stałym
napływie
osocza
do
kłębuszków
wielkość
filtracji
kłębuszkowej
również
utrzymywana
jest
na
stałym
poziomie,
wynosi
ona
około
120 ml/min (GFR).

Patofizjologia układu wydalniczego
M.P.
2
1. Przyczyny zmniejszonej filtracji kłębuszkowej
2. Nerki oszczędzają lub wydalają wodę zależnie od potrzeb organizmu
Jakkolwiek
nerki
mają
zdolność
zagęszczania
moczu,
ich
wydajność
w
tym
zakresie
nie
jest
nieograniczona.
Prawidłowa
nerka
zagęszcza
mocz
maksymalnie
do
1200
mOsm/kg.
Stąd
dla
wydalenia
resztkowych
produktów
przemiany
materii
nerki
muszą
wydalić
od
500
do
700
ml
wody
w
ciągu
doby.
• nerki resorbują większość filtrowanej w kłębuszkach wody powyżej wielkości obligatoryjnej minimalnej
objętości moczu, co umożliwia jej wykorzystanie do innych celów w organizmie
• gdy natomiast organizm jest przewodniony, nerki wydalają nawet kilka litrów moczu
Hormonem regulującym ilość wydalanego moczu jest przez podwzgórzowy
hormon antydiuretyczny
(
ADH;wazopresyna
), który:
• pobudza wchłanianie wody zwrotne wody i Na
+
w kanalikach zbiorczych nerek → ↓ ilości
wydalanego moczu
• działa zwężająco na naczynia krwionośne → ↓ nerkowego przepływu krwi → ↓ GFR → ↓ ilości
moczu
Uwalnianie
ADH
jest
spowodowane
zwiększeniem
ciśnienia
osmotycznego
osocza,
co
stymuluje
osmoreceptory
przedniej
części
podwzgórza.
Ponadto
na
uwalnianie
ADH
ma
wpływ
objętość
krwi
krążącej,
a
w
mechanizmie
tym
biora
udział
baroreceptory
wrażliwe
na
obniżone
ciśnienie
krwi.
• nadciśnienie tętnicze, hiperkapnia, hipoksja, ból, wymioty mogą zwiększać uwalnianie ADH, prowadząc do
skurczu naczyń i zahamowania diurezy
3.
Moczówka prosta
charakteryzuje się występowaniem
poliurii
, prowadzącej do nadmiernej utraty wody przez
nerki. Wyróżnia się dwa typy moczówki prostej:
a) Moczówka prosta centralna – niezdolność do zagęszczania moczu jest związana z niedoborem ADH. Jest
ona
rzadką
chorobą
spowodowana
uszkodzeniem
jąder
podwzgórza
lub
tylnego
płata
przysadki
przez
nowotwór,
uraz
bądź
zabieg
chirurgiczny.
b) Moczówka prosta nerkowa – w tej postaci niezdolność do zagęszczania moczu jest związana z zaburzoną
czynnością
nerek,
przewlekłą
niewydolnością
nerek,
niewrażliwością
nerek
na
ADH
(np.
brak
receptora
dla
ADH)
lub
lekami,
takimi
jak
np.
lit
Moczówka
prosta
charakteryzuje
się
występowaniem
poliurii,
a
wydalanie
moczu
może
sięgnąć
nawet
5-‐15
litrów/dobę,
mocz
jest
hipoosmotyczny.
Nadmierna
utrata
wody
przyczynia
się
do
wystąpienia
hipernatremii
i
wzrostu osmolarności osocza.
Patogeneza
Choroba
Zmniejszony nerkowy przepływ krwi
niewydolność serca
Hipotensja – hipoperfuzja nerek
masywny krwotok
Skurcz tętniczki doprowadzającej kłębuszka
• nadciśnienie tętnicze (angiotensyna II)
• uraz, uszkodzenie mózgu
• inne stany powodujące aktywację układu
współczulnego → ↑noradrenaliny → skurcz
naczyń
Stan zapalny kłębuszków nerkowych
ostre zapalenie kłębuszków nerkowych
Zakrzepica w kłębuszku nerkowym
• DIC (zespół rozsianego wykrzepiania
wewnątrznaczyniowego)
• IPM (idiopatyczna plamica małopłytkowa)
• ZPM (zakrzepowa plamica małopłytkowa)
Zwiększone ciśnienie hydrostatyczne w drogach
nerkowych
obturacja dróg moczowych
Zmniejszenie łożyska naczyń włosowatych
kłębuszka
przewlekłe kłębuszkowe zapalenie nerek

Patofizjologia układu wydalniczego
M.P.
3
• utrata
wody
prowadzi
do
polidypsji,
w
wyniku
której
osmolarność
osocza
może
wrócić
do
normy
• moczówka
jest
rzadkim
zaburzeniem
hormonalnym,
które
należy
różnicować
z
wielomoczem
występującym w cukrzycy i polidypsji/poliurii o podłoży psychogennym
Ø
Poliuria
występująca
w
cukrzycy
–
charakteryzuje
się
wytwarzaniem
hiperosmotycznego
moczu,
hiperglikemią
i
glikozurią
Ø
Polidypsja
/
poliuria
o
podłożu
psychogennym
–
jest
chorobą
psychiczną
o
charakterze
natręctwa,
polegająca
na
przyjmowaniu
dużej
ilości
płynów,
przypominająca
moczówkę
prostę,
w
której
dochodzi
do
wytwarzania
dużych
ilości
hipotonicznego
moczu.
Osmolalność
osocza
jest
jednak
normalna
lub
obniżona,
a
stężenie
ADH
we
krwi
prawidłowe.
4.
Zespól nieadekwatnego wydzielania ADH
(SIADH – syndrome of inappropriate antidiuretic hormone secretion)
Charakteryzuje
się
podwyższonym
stężeniem
ADH
pomimo
obniżonej
osmolalności
osocza.
Zespół
ten
może
być
wynikiem:
• nieprawidłowej
syntezy
ADH
w
nowotworach
złośliwych
• wytwarzania
ADH
przez
zmienioną
nowotworowo
tkankę
płuc
przewlekłych
chorobach
płuc
• zwiększenia
wytwarzania
ADH
przez
podwzgórze
w
chorobach
mózgu
• leki:
przeciwdepresyjne,
diuretyki,
cytotoksyczne,
narkotyki
5. Prawidłowe nerki wytwarzają około
1500 ml moczu w ciągu doby
. Ponieważ przeciętnie pojemność pęcherza
moczowego wynosi około 500 ml, zdrowa osoba oddaje mocz cztery do sześciu razy w ciągu doby.
Częstość oddawania moczu i jego całkowita objętość zależą od wielu czynników, takich jak:
• podaż
płynów
• pozanerkowe
utraty
płynów
(parowanie,
pocenie
się,
biegunka,
wymioty)
• stan
czynnościowy
nerek
• pojemność
pęcherza
moczowego
• leki
(np.
diuretyki
modyfikują
resorpcję
i/lub
sekrecję
wodu
i
elektrolitów
w
nerkach)
• czynniki
miejscowe
wpływające
na
odruch
oddawania
moczu
(mikcji)
-‐
np.
przerost
gruczołu
krokowego
u mężczyzn
a) Wielomocz (poliuria) – jest to wytwarzanie moczu w ilości przekraczającej 3000 ml/dobę. Przyczyną tego
może być:
• nadmierna
podaż
wody
(polidypsja)
•
diureza osmotyczna
-‐ wydalanie dużych ilości moczu wywołane obecnością w moczu substancji
osmotycznie
czynnych,
nie
podlegających
resorpcji
kanalikowej
(np.
hiperglikemia
w
przebiegu
cukrzycy)
• nadmierne wydalanie wody – niewydolność nerek prowadząca do moczówki prostej pochodzenia
nerkowego
b) Nykturia/nokturia
–
jest
postacią
wielomoczu
polegającą
na
konieczności
oddawania
moczu
w
nocy
c) Dyzuria
–
polega
na
odczuwaniu
bólu,
pojawiającego
się
podczas
oddawania
moczu
lub
bezpośrednio
po
nim.
d) Skąpomocz – wydalanie zmniejszonej ilości moczu, poniżej 400 ml/dobę. Może być jednym z wykładników
niewydolności nerek pochodzenia przednerkowego, nerkowego czy pozanerkowego.
Białkomocz (proteinuria)
Zdrowe
osoby
wydalają
mniej
niż
150
mg
białka
w
moczu.
Wśród
wydalonych
białek
znajdują
się
przesączone
w
kłębuszkach
nerkowych
albuminy
i
inne
niskocząteczkowe
białka
osocza
(immunoglobuliny,
niektóre
hormony,
enzymy).
• 30% wydalanego białka stanowią glikoproteiny (białko Tamma – Horsfalla) będące podstawą strukturalną
formowania wałeczków w chorobach nerek.
Patofizjologia układu wydalniczego
M.P.
4
1.
Zwiększone wydalanie białek
(> 250 mg/dobę) może być spowodowane:
• nadmierną syntezą białek o małej masie cząsteczkowej w przebiegu takich chorób jak szpiczak mnogi,
gammapatie, hemoglobinouria (
białkomocz z przeładowania
)
• uszkodzeniem bariery filtracyjnej kłębuszków nerkowych (glomerulopatie pierwotne lub wtórne, zaburzenia
hemodynamiczne ze wzrostem ciśnienia śródkłębuszkowego)
• zmniejszeniem
reabsorpcji
cewkowej
nerek
(śródmiąższowe
choroby
nerek)
• nadmiernym
wytwarzaniem
białka
przez
nabłonek
dróg
moczowych
np.
w
przebiegu
stanów
zapalnych
dróg
moczowych.
2. Białkomocz możemy podzielić na:
a) Przednerkowy – powstaje w skutek przedostawania się do moczu białek występujących w nadmiarze w
osoczu. Nerki funkcjonują prawidłowo. Wystepuje w przebiegu:
• szpiczaka
mnogiego
(białko
Bence
–
Jones’a)
• hemoglobinourii,
mioglobinourii
b) Nerkowy
• organiczny – zależny od chorób kłębuszków –
glomerulopatii
(nefropatie toksyczne, polkowe,
zaburzenia nerkowego przepływu krwi, choroby śródmiąższowe nerek),
cewek
(↓ reabsorpcji białek)
• wzrasta przepuszczalność bariery filtracyjnej przez:
− zanik
ujemnego
ładunku
− ubytki
strukturalne
− wzrost
ciśnienia
śródkłębuszkowego
c) Pozanerkowy (tkankowy) – jest to obecność białka w uformowanym
moczu. Do najczęstszych przyczyn należą:
• zapalenia
dróg
moczowych
• zapalenia
gruczołu
krokowego
Obrzęki nerkopochodne
Jest
to
stan,
w
którym
dochodzi
do
nadmiernej
akumulacji
płynu
w
przestrzeni
śródmiąższowej.
W
zależności
od
umiejscowienia
dzieli
się
je
na:
• obrzęki
nefrytyczne
(pierwotne)
–
przelotne,
dotyczą
tkanek
miękkich
twarzy
(powiek)
• obrzęki
nerczycowe
(wtórne)
–
rozległe,
z
przesiękami
do
jam
ciała
1.
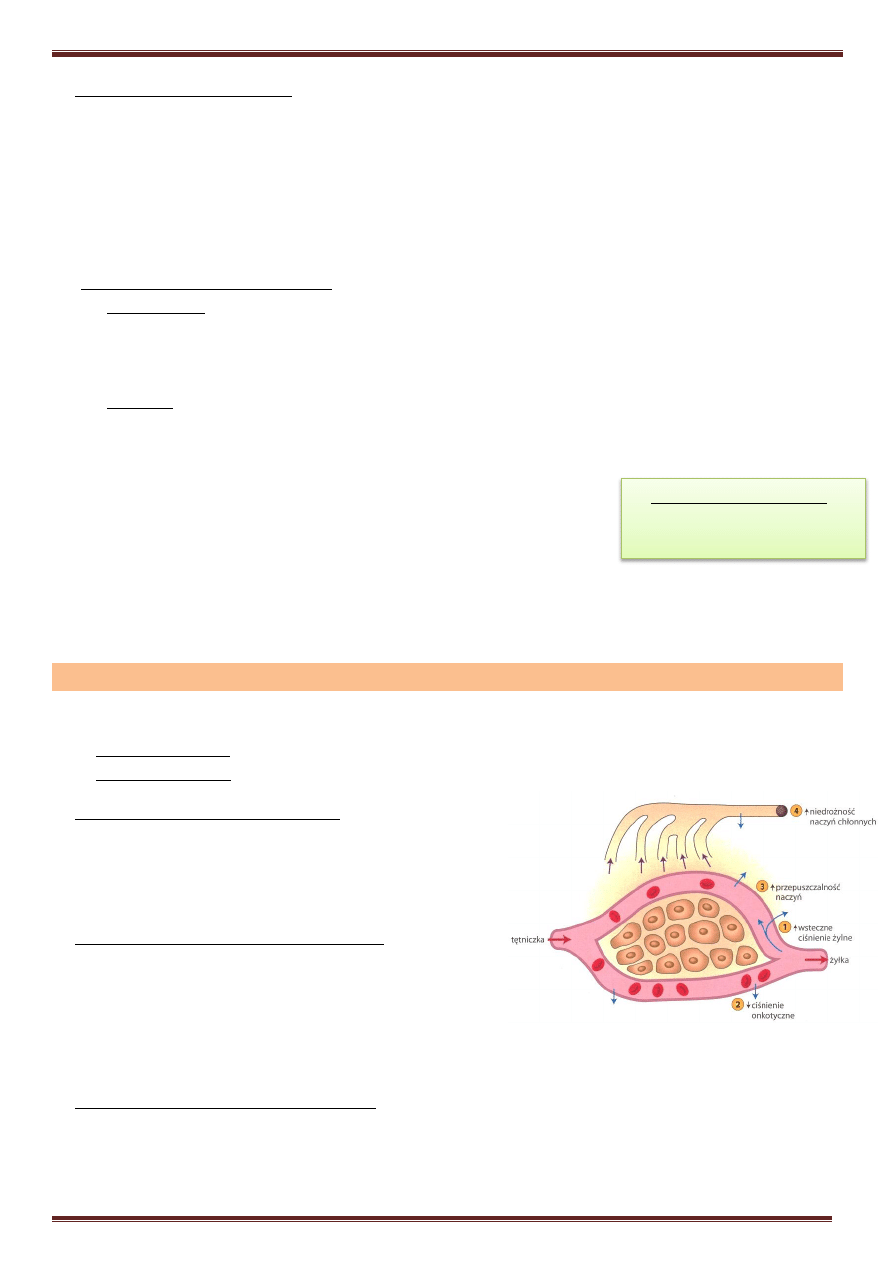
Mechanizm wytworzenia obrzęków
obejmuje:
• ↑
ciśnienia
wewnątrzkapilarnego
• ↑przepuszczalności
ściany
naczynia
• ↓
ciśnienia
onkotycznego
surowicy
krwi
–
przyczyną
jest białkomocz doprowadzający do hipoalbuminemii
2. Teorie obrzęków w zespole nerczycowym
a) Białkomocz prowadzący do hipoalbuminemii i niskiego
ciśnienia onkotycznego, a w następstwie do obrzęków
b) Pierwotny defekt nerkowy ze zwiększeniem wydalania
sodu.
Nadmierna
aktywność
kanałów
sodowych
i
Na-‐K-‐
ATP-‐azy
oraz
nabyta
oporność
na
działanie
ANP.
Przy
wystąpieniu
białkomoczu
dochodzi
do
zaburzenia
funkcjonowania
komórek
cewkowych,
które
obładowane
są
wchłanianymi
zwrotnie
albuminami.
3. Mechanizmy chroniące przed obrzękami
• zwiększenie
ciśnienia
hydrostatycznego
płynu
śródmiąższowego
• zwiększenie
przepływu
limfatycznego
• zmniejszenie
ciśnienia
onkotycznego
płynu
pozanaczyniowego
• zmniejszenie
przepuszczalności
ściany
naczyniowej
kapilar
Białkomocz ortostatyczny –
obecność białka w moczu u
osoby w pozycji stojącej.
Patofizjologia układu wydalniczego
M.P.
5
4. Różnicowanie obrzęków
d
Sercowe
Wątrobowe
Nerkowe
Obecność obrzęków
++++
+++
++
Obrzęk twarzy
-‐
-‐
obecny
Wodobrzusze
+
++++
+
Hipoalbuminemia
-‐
++
++++
Białkomocz
śladowy
śladowy
++++
Niedokrwistość
Anemia
pojawia
się
w
przebiegu
przewlekłej
niewydolności
nerek,
wówczas
gdy
GFR
obniży
się
do
wartości
25
–
30
ml/min,
najczęściej
ma
ona
charakter
normocytarny.
Przyczyny
niedokrwistości:
• z punktu widzenia patofizjologii nerek najważniejszą przyczyną jest niedostateczna synteza i uwalnianie przez
komórki nerek hormonu erytropoetyny, która pobudza szpik kostny do tworzenia erytrocytów
• skrócenie czasu przeżycia erytrocytów wywołane przez: toksyny mocznicowe, hipersplenizm, czynniki
wewnątrzkrwinkowe (zmniejszona oporność)
• przewlekła
utrata
krwi
(jatrogenna;
krwawienia
z
przewodu
pokarmowego)
• niedobór
wit.
B
12
(kobalamina) i żelaza w diecie
PATOMECHANIZM CHORÓB NEREK I UKŁADU MOCZOWEGO
Objawowo zespoły kliniczne chorób nerek dzieli się na dwie zasadnicze grupy:
• zespół
nefrytyczny
(objawy:
nadciśnienie,
oligouria,
proteinuria,
obrzęki)
• zespół
nerczycowy
(objawy:
masywna
proteinuria,
hipoproteinemia,
obrzęki,
hiperlipidemia)
Zespół nefrytyczny – kłębuszkowe zapalenie nerek
Jest to zbiór klinicznych objawów, które u pacjentów z
kłębuszkowym zapaleniem nerek
występują na podłożu
immunologicznym. Do objawów zalicza się:
• białkomocz
• krwiomocz
pochodzenia
kłębuszkowego
• oligouria
(skąpomocz)
• nadciśnienie
tętnicze
• obrzęki
1.
Zespół nefrytyczny
może być wynikiem pierwotnej choroby nerek lub może być wtórnym zaburzeniem w
stosunku
do
zakażenia
w
innym
miejscu
organizmu.
Może
również
wystąpić
w
przebiegu
układowych
chorób
o
podłożu
immunologicznym,
takich
jak:
toczeń
rumieniowaty
układowy,
choroba
Wegenera,
choroba
Schönleina-‐Henocha.
2. Pod względem obrazu i przebiegu klinicznego kłębuszkowe zapalenia nerek dzieli się na:
a) Ostre kłębuszkowe zapalenie nerek – charakteryzujące się nagłym początkiem, zazwyczaj poprzedzone
zakażeniem bakteryjnym.
b) Gwałtownie postępujące kłębuszkowe zapalenie nerek – charakteryzujące się nagłym początkiem, ciężkim
przebiegiem
i
rozwojem
w
ciągu
kilku
tygodni
lub
miesięcy
nieodwracalnej
niewydolności
nerek
wymagającej
dializacji
c) Przewlekłe postępujące kłębuszkowe zapalenie nerek – w tej chorobie do schyłkowej niewydolności nerek
dochodzi zwykle w ciągu kilkunastu lat
3. Ostre kłębuszkowe zapalenie nerek
Jego
najlepsza
ilustracją
są
zmiany
występujące
w
popaciorkowcowym
zapaleniu
kłębuszków
nerkowych.
Jest
to
ostra
choroba
rozwijająca
się
w
ciągu
2
tygodni
po
ostrym
paciorkowcowym
zapaleniu
gardła.
Patofizjologia układu wydalniczego
M.P.
6
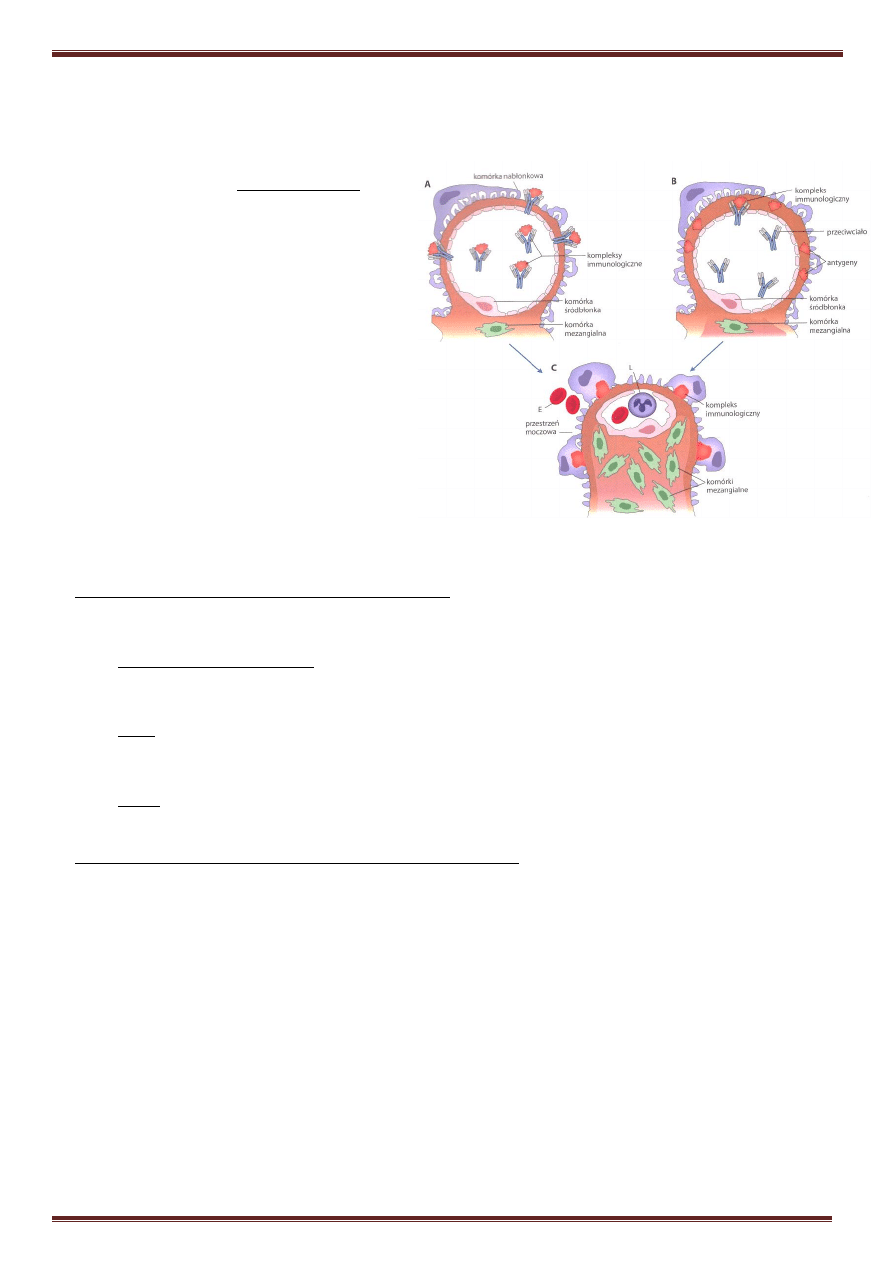
• zakażenie bakteryjne wywoływane przez „nefrytyczne” szczepy z grupy paciorkowców β-‐hemolitycznych
typu A powodują powstanie przeciwciał skierowanych przeciwko antygenom bakteryjnym
• kompleksy immunologiczne stworzone z przeciwciał i antygenów bakteryjnych krążące we krwi mogą się
odkładać
w
kłębuszkach
nerkowych,
aktywując
w
nich
układ
dopełniacza
i
w
ten
sposób
powodując
powstanie
kłębuszkowego
zapalenia
nerek
• antygeny bakteryjne mogą także zostać
wbudowane
podczas
procesu
filtracji
w
błonę
filtracyjną
kłębuszka
nerkowego,
co
może
doprowadzić
do
powstawanie
kompleksów
immunologicznych
w
błonie
podstawnej
kłębuszka
i
między
komórkami
mezangium
• aktywacja dopełniacza powoduje
tworzenie
czynników,
które
przyciągają
komórki
zapalne
i
pobudzają
proliferację
komórek
mezangium,
które
z
kolei
wytwarzają
silne
mediatory
zapalne
(interleukiny,
interferon,
TNF,
prostaglandyny)
wywołujące
uszkodzenie
błony
podstawnej,
powodując
wzrost
jej
przepuszczalności
4. Gwałtownie postępujące kłębuszkowe zapalenie nerek
Ta
choroba
może
mieć
charakter
pierwotny
lub
może
też
być
objawem
nerkowym
choroby
układowej.
Wyróżnia
się
3
typy
gwałtownie
postępującego
kłębuszkowego
zapalenia
nerek:
a) Typ I (zespół Goodpasture’a) – charakteryzuje się obecnością przeciwciał przeciwko błonie podstawnej
kłębuszków
nerkowych,
które
często
współistnieją
z
przeciwciałami
przeciwko
błonie
podstawnej
pęcherzyków
płucnych
b) Typ II – charakteryzuje się obecnością kompleksów immunologicznych tworzących „garby” w błonie
podstawnej
kłębuszka
(toczniowe
zapalenie
nerek,
popaciorkowcowe
kłębuszkowe
zapalenie
nerek,
nefropatia
IgA)
c) Typ III – przebiega bez złogów immunologicznych, natomiast we krwi stwierdza się obecność przeciwciał
przeciwko antygenom cytoplazmy leukocytów i monocytów.
5. Konsekwencjami zapalenia w obrębie kłębuszków nerkowych są:
• Zwiększona
przepuszczalność
błony
podstawnej
kłębuszka
→
białkomocz
• Zmiany
mikroskopijne
w
błonie
podstawnej
kłębuszka
→
przenikanie
erytrocytów
przez
barierę
kłębuszkową → krwiomocz
− erytrocyty przenikające przez błone podstawną kłębuszka nerkowego ulegają deformacji i
fragmentacji („dysmorficzne krwinki czerwone”)
− niektóre krwinki czerwone zostają wbudowane do wałeczków powstających w kanaliku bliższym w
środowisku wysokobiałkowego płynu
• Zmniejszona
filtracja
kłębuszkowa
→
skąpomocz
(oligouria)
• Zmniejszona
filtracja
sodu
→
mniej
jonów
Na
+
dopływa do komórek receptorowych plamki gęstej →
wydzielanie
reniny
→
aktywacja
układu
RAA
→
skurcz
tętniczek
doprowadzających
oraz
nadciśnienie
tętnicze
• Obrzęki ( najbardziej widoczne na twarzy oraz na rękach i stopach; ponadto obrzęk mózgu może
wywoływać
senność
oraz
być
przyczyna
śpiączki;
obrzęk
płuc
powoduje
uczucie
duszności)
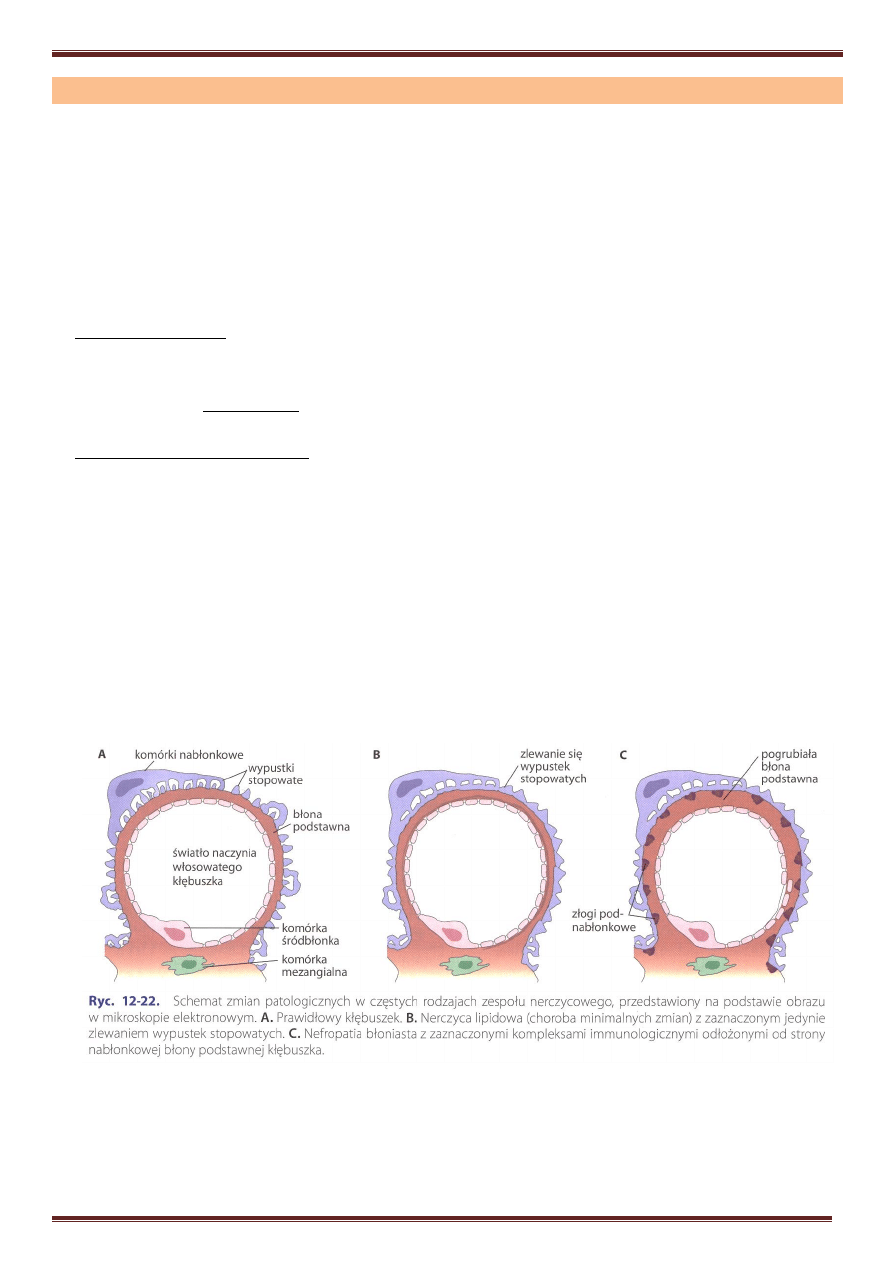
Patofizjologia układu wydalniczego
M.P.
7
Zespół nerczycowy
Zespół objawów klinicznych
wywołanych białkomoczem
(> 3,5 mg/dobę) przekraczającym możliwości
kompensacyjne organizmu. Objawy te stanowią:
• uogólnionymi obrzękami
• hiperlipidemia
• hipoproteinemia
• lipiduria
Występuje on w chorobach, które powodują zwiększenie przepuszczalności naczyń włosowatych kłębuszka. Może
on wystąpić w przebiegu glomerulopatii pierwotnych jak i wtórnych.
1.
Zaburzenia lipidowe
występujące w przebiegu zespołu nerczycowego obejmują:
• zmniejszenie
stężenia
w
surowicy
krwi
protein
o
wysokiej
gęstości
(HDL)
•
wzrost
frakcji
lipidowych
o
niskiej
i
bardzo
niskiej
gęstości
(LDL,
VLDL)
• dochodzi
do
hiperlipidemii,
a
przez
co
do
wzrostu
stężenia
cholesterolu
co
skutkować
może
miażdżycą
przy
długotrwałym zespole nerczycowym
2. Objawy zespołu nerczycowego:
• obrzęki,
przesięki
(wodobrzusze,
duszność)
• pienienie
się
moczu
• osłabienie,
bóle
głowy
• hipotonia
ortostatyczna
• ONN
przednerkowa
• zakrzepy
(10-‐40
%)
• infekcje
• niedobór
witaminy
D
3
→ osteomalacja, wtórna nadczynność przytarczyc
• wyniszczenie,
zahamowanie
wzrostu
• zaburzenia
miesiączkowania
• hiperlipidemia
Patofizjologia układu wydalniczego
M.P.
8
Ostra niewydolność nerek
Jest
to
zespół
chorobowy
o
różnej
etiologii,
charakteryzujący
się
szybkim
pogorszeniem
czynności
nerek,
cechujący
się:
• zmniejszonym wytwarzaniem moczu (skąpomocz lub bezmocz) – rzadko, ale
może przebiegać również z
wielomoczem
• retencją w organizmie wody, H
+
i elektrolitów,
kwasicą metaboliczną
, retencją resztkowych produktów
przemiany materii we krwi, głównie mocznika i kreatyniny
Ostra
niewydolność
nerek
może
być
następstwem
zarówno
wielu
chorób
samych
nerek,
jak
i
chorób
układowych,
ale
także
może
być
spowodowana
przez
uraz,
oparzenia,
odwodnienie
czy
zabieg
chirurgiczny.
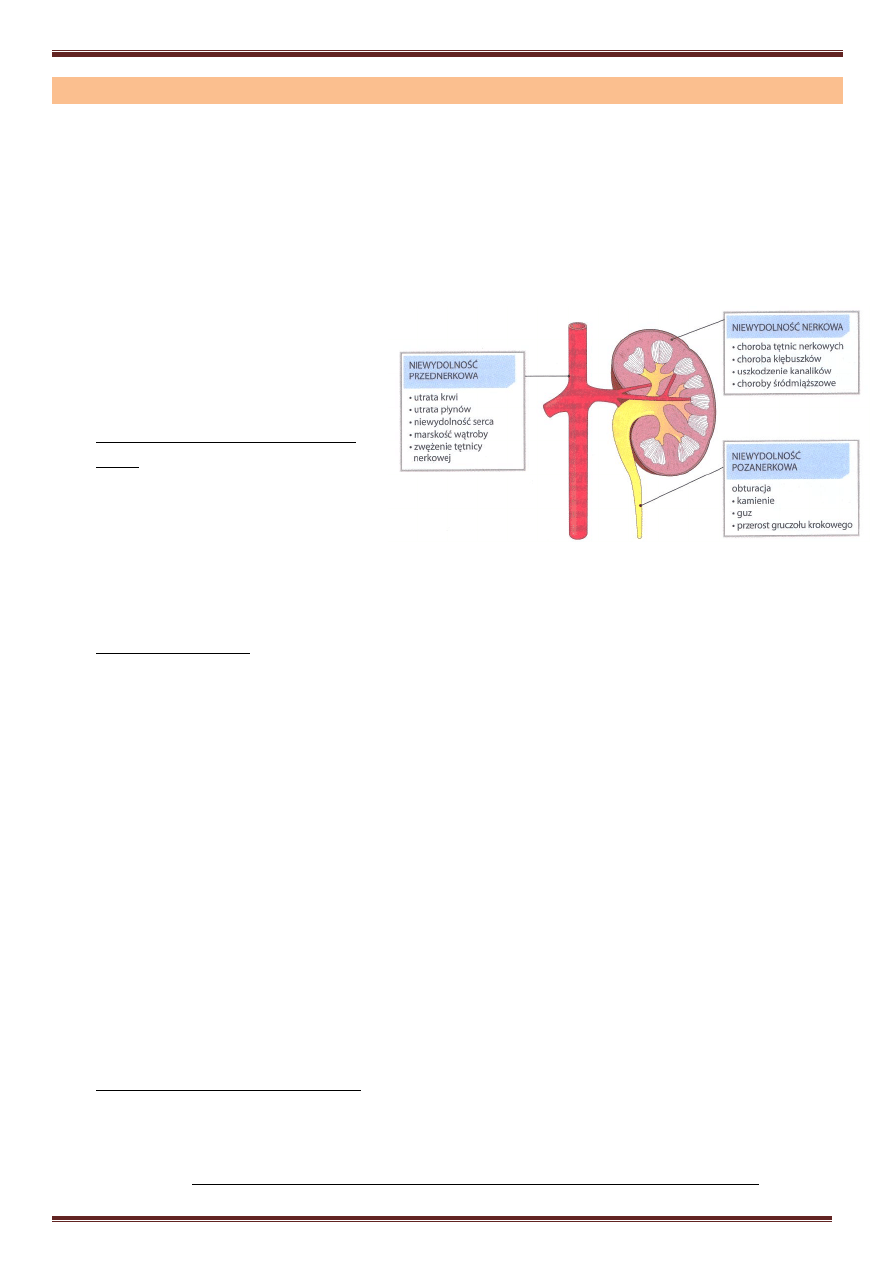
1. Dla celów klinicznych ostrą niewydolność
nerek dzieli się na:
• przednerkową
• nerkową
• pozanerkową
a)
Ostra
przednerkowa
niewydolność
nerek
– jest zespołem wywołanym
pogorszeniem
ukrwienia
nerek
z
następowym
obniżeniem
filtracji
kłębuszkowej
, co przy zachowanej
dobrej
czynności
cewek
moczowych
prowadzi
do
wchłonięcia
znacznej
ilości
moczu
pierwotnego.
Dochodzi
do
zachwiania
równowagi
kłębuszkowo
–
cewkowej
z
następowym
zmniejszaniem
ilości
moczu,
zatrzymaniem
w
organizmie
wody,
elektrolitów
i
produktów
przemiany
białkowej.
Najczęstsze
przyczyny
przednerkowej
niewydolności
nerek
są
następujące:
a) Hipowolemia
• wymioty,
biegunka,
moczówka
prosta,
niewydolność
kory
nadnerczy
• jatrogenna:
furosemid,
krwotok,
uraz,
zespół
zmiażdżenia,
rozległe
oparzenia
• „trzecia
przestrzeń”:
zapalenie
otrzewnej,
wodobrzusze,
OZT
b) Spadek objętości wyrzutowej serca
• zawał serca, tamponada, niewydolność krążenia, wady serca
c) Wzrost oporów naczyniowych naczynia nerkowe / naczynia systemowe
• skurcz
naczyń
nerkowych:
noradrenalina,
ergotamina,
hiperkalcemia
• rozkurcz
naczyń
systemowych:
leki
hipotensyjne,
sepsa,
wstrząs
anafilaktyczny,
znieczulenie
ogólne,
przedawkowanie narkotyków, niewydolność wątroby
d) Zmiany w tętnicach i żyłach nerkowych
• miażdżyca, zakrzepica, zatory, zapalenie, tętniak rozwarstwiający, ucisk z zewnątrz
e) Zmiany w drobnych naczyniach i naczyniach kłębuszkowych
• DIC, zespół hemolityczno-‐mocznicowy, kłębuszkowe zapalenie nerek, zatrucie ciążowe, nadciśnienie
złośliwe, uszkodzenie popromienne
f) Wzmożona lepkość krwi
• szpiczak, poliglobulia
b) Ostra nerkowa niewydolność nerek
Może być następstwem
uszkodzenia naczyń krwionośnych, kłębuszków lub kanalików nerkowych
. Nerkowe
przyczyny ostrej niewydolności nerek dzieli się na zapalne oraz niezapalne
a) Przyczyny zapalne – zapalenia kłębuszków nerkowych, zapalenie cewkowo – śródmiąższowe
• wyeliminowanie
czynnika
sprawczego
nie
odwraca
natychmiast
niewydolności
nerek
• dominują
nacieki
komórkowe

Patofizjologia układu wydalniczego
M.P.
9
b) Przyczyny niezapalne
• uszkodzenie kanalików – może być spowodowane nefrotoksyny:
− egzogenne: antybiotyki (aminoglikozydy, cefalosporyny), środki znieczulające i
kontrastujące,
inne
leki
(chemioterapeutyki,
immunosupresanty),
rozpuszczalniki
organiczne
(glikol
etylenowy,
nafta,
terpentynę,
toluen),
metale
ciężkie
(arsen,
bizmut,
kadm,
lit,
rtęć,
chrom,
ołów),
herbicydy,
muchomor
sromotnikowy,
toksyny
bakteryjne
− endogenne: mioglobina, hemoglobina, methemoglobina, kwas moczowy, kryształy
wapniowe, szczawianowe
• obturacja naczyń krwionośnych – u chorych z zapaleniem wsierdzia światło głównych naczyń
nerkowych
może
zostać
zamknięte
przez
zatory
skrzeplinami
pochodzącymi
z
zastawek
serca.
Zatory
cholesterolowe
pochodzące
z
pękniętych
blaszek
miażdżycowych
aorty
mogą
całkowicie
zamknąć
tętnice
nerkowe
i
doprowadzić
do
ostrej
niewydolności
nerek.
c) Ostra pozanerkowa niewydolność nerek
Pozanerkowa postać ostrej niewydolności nerek jest powodowana
blokadą odpływu moczu.
a) Obturacja dróg moczowych może wystąpić na poziomie moczowodów, szyi pęcherza moczowego lub
cewki.
• w przypadku bloku jednostronnego – w jednym z moczowodów druga nerka może kompensować
ten stan.
• całkowita obturacja na poziomie szyi pęcherza lub cewki moczowej może doprowadzić do ostrej
niewydolności nerek, wymagającej natychmiastowego leczenia
• zablokowanie moczowodu w jedynej nerce pacjenta lub w nerce po przeszczepie jest również
stanem zagrażającym życiu wymagająca natychmiastowej interwencji
b) Do przyczyn zatorowania pozanerkowych dróg moczowych zalicza się:
• u
mężczyzn
najczęstszą
przyczyną
jest
łagodny
lub
nowotworowy
rozrst
gruczołu
krokowego
• u
kobiet
najczęściej
obserwuje
się
nowotwory
narządu
rodnego,
rzadziej
kamicę
układu
moczowego
• zaburzenie
w
świetle
moczowodu:
guzy,
kamienie
• choroby
w
przestrzeni
zaotrzewnowej:
guzy,
włóknienia,
krwiaki,
przyczyna
jatrogenna
• zaburzenia
czynnościowe:
odpływ
pęcherzykowo
–
moczowodowy,
pęcherz
neurogenny
• zaburzenia
pęcherza:
rak,
kamienie
• zaburzenia
cewki
moczowej:
guzy,
zwężenia,
zastawki
2. Powikłania ostrej niewydolności nerek
Ostra niewydolność nerek powoduje
retencję wody, elektrolitów i metabolitów
, które w prawidłowych
warunkach są wydalane w moczu, a także
kwasicę.
Cechą
charakterystyczną
jest
zmniejszenie
wytwarzania
moczu
(skąpomocz),
a
z
czasem
dochodzi
do
bezmoczu.
W
obrazie
klinicznym
dominują
symptomy
stanu,
który
doprowadził
do
niewydolności
nerek.
Zmiany
parametrów
biochemicznych
krwi
i
moczu
są
najważniejszymi
dowodami
potwierdzającymi
niewydolność
nerek.
Typowe
odchylenia
obejmują:
a) Azotemia – np. podwyższony poziom resztkowych, organicznych produktów przemiany materii, takich jak:
− azot
białkowy
(mocznik)
− kreatynina
− kwas
moczowy
b) Retencja
wody
–
zwiększona
objętość
wewnątrznaczyniowa
c) Zaburzenia
elektrolitowe
− hiperkalemia
(bardzo
groźne
–
może
być
przyczyną
migotania
komór)
− hiponatremia
− hiperfosfatemia
− hipokalcemia
d) Kwasica metaboliczna – obniżony poziom HCO
3
-‐
Patofizjologia układu wydalniczego
M.P.
10
Ostra niewydolność nerek zaburza funkcję wielu narządów, powodując zaburzenia metaboliczne:
a) Powikłania płucno – sercowe
• niewydolność
serca
(przewodnienie
organizmu)
• zaburzenia
rytmów
serca
(hiperkaliemia,
hipokalcemia)
• nadciśnienie
tętnicze
(wysoki
poziom
reniny)
• niewydolność
lewokomorowa
→
obrzęk
płuc
b) Powikłania neurologiczne
• mocznik oraz inne azotowe produkty wspólnie z zaburzeniami elektrolitowymi i kwasicą powodują
depresję ośrodkowego układu nerwowego, drgawki lub w stanach skrajnych śpiączkę i śmierć
c) Zaburzenia
krzepnięcia
–
w
skutek
zmian
metabolicznych
w
płytkach
krwi
i
ścianie
naczyń
krwionośnych
d) Predyspozycja
do
zakażeń
–
niekorzystny
wpływ
zaburzeń
metabolizmu
na
mechanizmy
obronne
Przewlekła niewydolność nerek (PNN)
Jest
to
nieodwracalny
w
większości
wypadków,
postępujący
proces
chorobowy,
który
powoduje
uszkodzenie,
a
następnie
zmiany
w
czynności
nerek.
Prowadzi
do
zmiany
składu
moczu
oraz
objętości
płynów
ustrojowych,
a
także
upośledzenia
czynności
innych
narządów
i/lub
układów.
• klinicznie rozpoznaje się PNN gdy GFR spadnie poniżej 60 ml/min na dłużej niż 3 miesiące
1. Do najczęstszych przyczyn PNN zalicza się:
• nefropatię
cukrzycową
• przewlekłe
kłębuszkowe
zapalenie
nerek
• śródmiąższowe
zapalenie
nerek
• zwyrodnienie
trobielowate
nerek
• choroby
układowe
• amyloidozę
wtórną
• nowotwory
układu
moczowego
• szpiczak
• dna
moczanowa
2. W przebiegu PNN wyróżnino
5 stadiów choroby:
Stadium 1 – uszkodzenie nerek w przypadku prawidłowego lub zwiększonego GFR
• GFR > 90 ml/lin
Stadium 2 – niewielkiego stopnia upośledzenie GFR, tzw. utajona PNN
• GFR
60
–
89
ml/min
• zwykle
brak
objawów
klinicnzych
Stadium 3 – średniego stopnia upośledzenie GFR, tzw. wyrównana PNN
• GFR
30
–
59
ml/min
• niewielkie
objawy
kliniczne
• wielomocz
• niewielki
wzrost
poziomu
kreatyniny
w
surowicy
krwi
Stadium 4 – znacznego stopnia upośledzenie GFR, tzw. niewyrównana PNN
• GFR
15
–
29
ml/min
• objawy
kliniczne:
niedokrwistość,
neuropatia,
kardiomiopatia,
zaburzenia
metaboliczne
(↑
kreatyniny,
mocznika, kwasu moczowego; kwasica metaboliczna, wzrost stężenia fosforanów)
Stadium 5 – niewydolność nerek, tzw. schyłkowa niewydolność nerek / mocznica
• GFR
<
15
ml/min
• pełnoobjawowa
postać
zejściowa
niewyrównanej
PNN
Patofizjologia układu wydalniczego
M.P.
11
3. Patogeneza
• obniża się liczba czynnych nefronów (upośledzenie funkcji wydalniczej nerki) – wzrastają stężenia
końcowych
produktów
przemiany
materii
(białek
i
puryn),
rośnie
retencja
fosforanów,
toksyn
mocznicowych
• uszkodzenie
cewek
nerkowych
jest
wtórne
do
uszkodzenia
kłębuszków
nerkowych
(glomerulopatie)
• uszkodzenie
kłębuszków
nerkowych
i
cewek
nerkowych
zawsze
współistnieją
w
zaawansowanej
niewydolności nerek wpływając na pogarszanie się filtracji oraz upośledzenie reabsorpcji zwrotnej
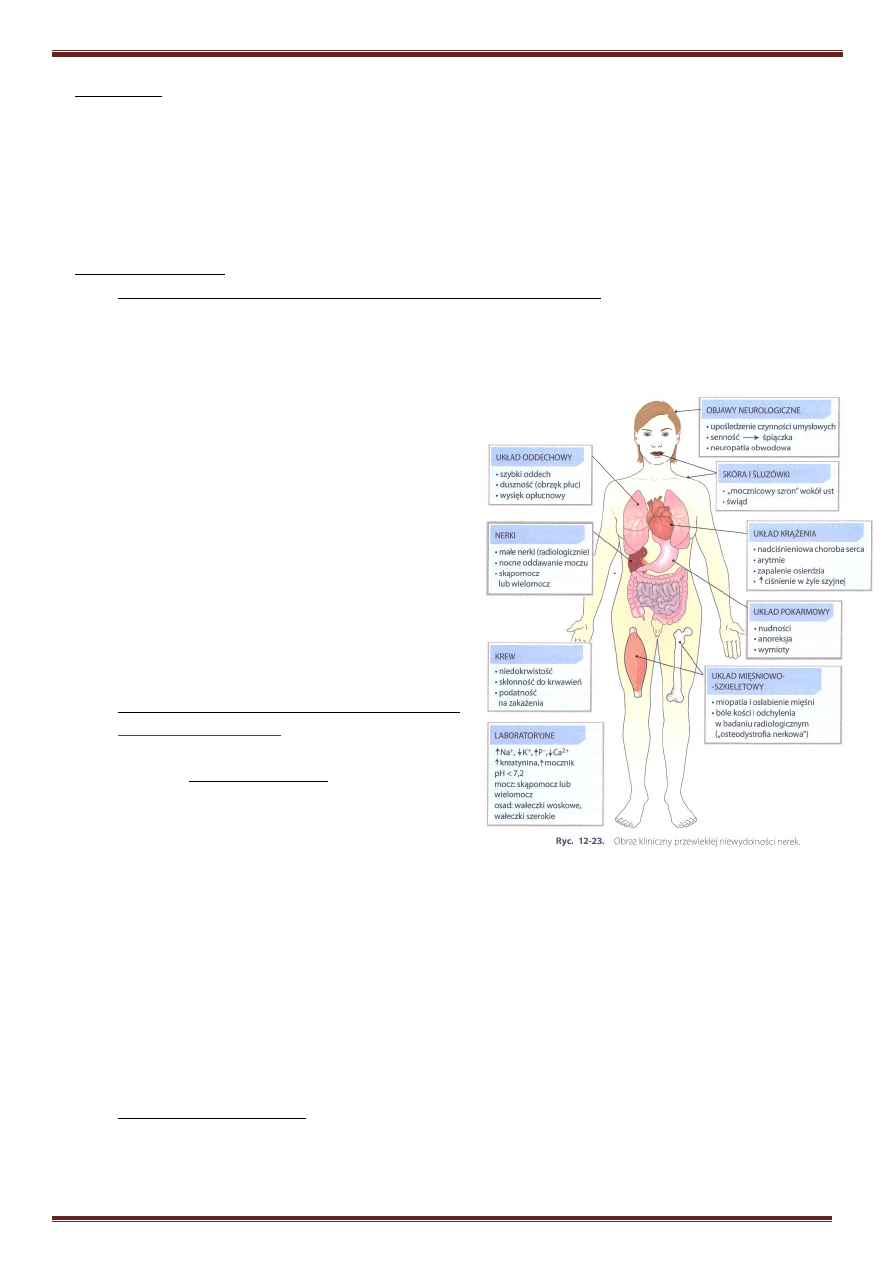
4. Obraz kliniczny PNN
a) Zaburzenia gospodarki wodno – elektrolitowej i kwasowo – zasadowej
•
początkowo wielomocz
, następnie ilość wydalanego moczu sukcesywnie spada
• gdy dobowa objętość wydalanego moczu spadnie poniżej 2 litrów, nadmierna podaż wody może być
przyczyną zatrucia wodnego, nadciśnienia tętniczego, obrzęków oraz niewydolności krążenia
•
hiperkaliemia
•
kwasica metaboliczna
-‐ spowodowana
zmniejszonym
wydalaniem
jonów
wodorowych,
powoduje:
− nasilenie proteolizy i zmniejszenie
syntezy białek
− nasila
insulinoporność
− zmienia
metabolizm
kości
–
upośledza
funkcje
osteoblastów,
nasila
funkcje
osteoklastów
− nasila produkcję i uwalnianie β2 –
mikroglobuliny
− nasila hipertriglicerydemię
b) Zaburzenia gospodarki wapniowo – fosforanowej,
osteodystrofia nerkowa
Zmniejszenie
masy
czynnego
miąższu
nerek
powoduje
retencję
fosforanów
oraz
upośledza
biosyntezę
aktywnego
metabolitu
witaminy
D
3
–
1,25(OH)
2
D, warunkującego wchłanianie wapnia w
przewodzie pokarmowym. Czynniki te prowadzą do
hipokalcemii
, pobudzającej przytarczyce do tworzenia PTH, poza hipokalcemią wydzielanie PTH jest
niezależnie
stymulowane
przez
współistniejącą
hiperfosfatemię.
Niedobór
aktywnej
formy
wit.
D3
oraz
hiperfosfatemia
są
głównymi
ogniwami
patogenetycznymi
wtórnej nadczynności przytarczyc u chorych na
PNN
. Dodatkowo w etiopatogenezie tej endokrynopatii uczestniczy kwasica metaboliczna i oporność kości
działanie PTH
• wtórna nadczynność przytarczyc jest ważnym czynnikiem w patogenezie
osteodystrofii nerkowej
przebiegającej z przyspieszonym obrotem tkanki kostnej
• u chorych na PNN może występować inny rodzaj patologii kostnej, która przebiega ze zwolnionym
obrotem tkanki kostnej, zaliczyć tu należy „
adynamiczną chorobę kości
” oraz
osteomalację
spowodowaną niedoborem aktywnych metabolitów wit. D
3
lub opornością na działanie tej witaminy
c) Zaburzenia hematologiczne
• niedobór
wydzielania
EPO
• niedobór
żelaza
• nieprawidłowa
czynność
płytek
Patofizjologia układu wydalniczego
M.P.
12
• niedobór
czynników
krzepnięcia
• defekt
odporności
komórkowej
d) Układ oddechowy
• oddech
kwasiczy
• mocznicowe
zapalenie
opłucnej
• płuco
mocznicowe
e) Układ pokarmowy
• utrata
łaknienia
• nudności
i
wymioty
• zaburzenia
smaku
• zapalenie
błony
śluzowej
żołądka
i
jelit
• wrzód
trawienny
żołądka
lub
dwunastnicy
• krwawienie
z
przewodu
pokarmowego
f) Układ krążenia
• nadciśnienie
tętnicze
lub
hipotensja
• przerost
lewej
komory
• zaburzenia
rytmu
• zapalenie
osierdzia
• przyspieszona
miażdżyca
• niewydolność
serca
g) Zaburzenia skórne
• bladość
• suchość
• ziemisto-‐brunatny
odcień
skóry
• wybroczyny
• świąd
• „szron
mocznicowy”
h) Objawy ze strony innych narządów
• zespół
cieśni
nadgarstka
(nagromadzenie
β2
–
mikroglobuliny
w
tkance
otaczającej
kanał
nadgarstka)
• upośledzona
czynność
endokrynna
gonad
(↓
testosteronu
/
estrogenów)
• zaburzenia
gospodarki
węglowodanowej
(hiperinsulinizm,
insulinooporność)
5. Mechanizmy adaptacyjne PNN
W
przewlekłych
chorobach
nerek,
bez
względu
na
czynnik
etiologiczny
dochodzi
do
uszkodzenia
wszystkich
struktur
nerki.
Jeżeli
pierwotny
proces
chorobowy
toczy
się
w
kłębuszku
nerkowym,
to
z
czasem
zmiany
pojawią
się
w
tkance
śródmiąższowej.
W
dalszym
przebiegu
procesu
chorobowego
zmiany
w
śródmiąższu
nasilają
uszkodzenie
kłębuszków.
W
wyniku
zmian
chorobowych
toczących
się
w
nerkach
dochodzi
do
utraty
funkcji
czynnych
nefronów,
a
pozostałe
nefrony
przejmują
ich
funkcje.
Procesy
adaptacyjne
w
czynnych
nefronach
polegają
na:
• zwiększeniu
przepływu
krwi
w
kłębuszkach
(rozszerzenie
tętniczek
doprowadzających)
• zwiększeniu
ciśnienia
wewnątrzkłębuszkoweg
oraz
filtracji
kłębuszkowej
–
jest
to
tzw.
hiperperfuzja
i
hiperfiltracja.
• wzrasta reabsorpcja sodu, wody i fosforanów oraz wydalanie jonów K
+
i H
+
.
Początkowo
te
procesy
pozwalają
na
utrzymanie
homeostazy,
lecz
hiperfiltracja
kłębuszków
przyczynia
się
do
ich
autodestrukcyjnego
uszkodzenia.
W
przerośniętych
kłębuszkach
zwiększa
się
liczba
komórek
mezangium
i
śródbłonka.
Innym
czynnikiem
przyspieszającym
progresję
PNN
jest
białkomocz.

Patofizjologia układu wydalniczego
M.P.
13
Kamica moczowa
Jest to tworzenie się kamieni nerkowych, będące bardzo częstą przyczyną zaburzeń w obrębie dróg moczowych.
1. Większość kamieni moczowych zawiera w swoim składzie wapń pod postacią:
• szczawianu
wapnia
(35
–
70%
kamieni)
• fosforanu
wapnia
(6
–
20%)
• mieszanina
obu
w/w
związków
(30%)
a) Kamienie
zbudowane
wyłącznie
z
kwasu
moczowego
stanowią
10%
wszystkich
kamieni
b) Kamienie
struwitowe
(fosforan
magnezowo
–
amonowy,
MgNH
4
PO
4
) stanowią 1 -‐20% kamieni
c) Złogi cystynowe stanowią nie więcej niż 1% kamieni
2. Tworzenie kamieni moczowych
Proces
tworzenia
się
kamieni
moczowych
zachodzi
wówczas,
gdy
wytrącają
się
w
moczu
prawidłowo
występujące
krystaloidy,
z
których
zbudowane
są
kamienie.
• krystaloidami, z których najczęściej tworzą się kamienie moczowe, są:
− szczawian
wapnia
− fosforan
wapnia
− kwas
moczowy
− fosforan
magnezowo
–
amonowy
− cystyna
Istotną
rolę
w
zapobieganiu
tworzenia
się
złogów
w
drogach
moczowych
odgrywają
inhibitory
krystalizacji,
które
tworzą
rozpuszczalne
kompleksy
z
krystaloidami,
albo
też
działają
jako
koloidy
ochronne
przeciwdziałając
agregacji,
zalicza
się
do
nich:
− uropontyna
− nepfrokalcyna
− białko
Tamma
–
Horsfalla
− cytryniany
− magnez
− pirofosforany
3. Czynniki sprzyjające tworzeniu złogów w drogach moczowych:
a) mała
objętość
moczu
b) zwiększone
wydalanie
z
moczem
składników
kamieni
nerkowych
(wapnia,
szczawianów,
kwasu
moczowego, cystyny)
• ↑ wydalania szczawianów (hiperoksaluria) – występuje w chorobach przewodu pokarmowego z
zaburzeniem
wchłaniania
kwasów
tłuszczowych,
nadmiar
k.
tłuszczowych
w
jelicie
wiąże
jony
Ca
2+
co powoduje, że zwiększa się ilość rozpuszczalnych szczawianów (fizjologicznie związanych z
wapniem), które są wchłaniane a następnie wydalane z moczem
• ↑ wydalania kwasu moczowego, sprzyja odkładaniu kamieni szczawianowych, na skutek
ułatwienia krystalizacji szczawianów w przesyconym roztworze moczanu.
• nieprawidłowe pH moczu
(kwas moczowy i cystyna słabo rozpuszczają się w kwaśnym moczu,
natomiast struwit i fosforan wapnia słabo rozpuszczają się słabo w moczu zasadowym)
• obecność jąder krystalizacji dla precypitacji kryształów (krystalizacja moczanu sodu ułatwia
krystalizację
szczawianu
wapnia
na
niektórych
kryształach
moczanowych
i
przyspiesza
ich
formowanie)
• niedobór
inhibitorów
krystalizacji
• zakażenia
dróg
moczowych
bakteriami
wytwarzającymi
ureazę
i
rozkładającymi
mocznik
(Klebsiella, Pseudomonas, Proteus) → tworzenie NH
3
→ ↓pH + NH
3
→ tworzeni kamieni
struwitowych
Patofizjologia układu wydalniczego
M.P.
14
• długotrwałe unieruchomienie (nadmierna mobilizacja wapnia z kości)
4. Najczęstszym zaburzeniem metabolicznym u chorych na kamicę nerkową jest
hiperkalciuria
a) zwiększone wydalanie wapnia z moczem może być spowodowane nadmiernym jego wchłanianiem z
przewodu pokarmowego (hiperkaciuria absorpcyjna) → przejściowy hiperkalcemia i ↓ PTH
• ↓ PTH obniża wchłanianie zwrotne wapnia w cewkach nerkowych i prowadzi do hiperkalciurii
b) zwiększone wchłanianie Ca
2+
w przewodzie pokarmowym stwierdza się też w hiperkalciurii
hiperfosfaturycznej
• nadmierne wydalanie fosforanów z moczem (defekt cewek nerkowych) dochodzi do
hipofosfatemii
, która stanowi silny bodziec pobudzający tworzenie 1,25(OH)
2
D
• pod wpływem 1,25(OH)
2
D zwiększa się wchłanianie wapnia w przewodzie pokarmowym i
wydalanie tego jonu z moczem
c) hiperkalciuria nerkowa – jest wynikiem upośledzonego wchłaniania zwrotnego wapnia w cewkach
nerkowych (pierwotny defekt cewek nerkowych), co prowadzi do:
• przejściowej
hipokalcemii
• wtórny
↑PTH
• ↑
1,25(OH)
2
D
• w efekcie: wzrost stężenia Ca
2+
d) hiperkalciuria towarzyszy również pierwotnej nadczynności przytarczyc, ma ona charakter:
• resporpcyjny
–
ze
względu
na
nadmierne
wchłanianie
wapnia
z
kości
• absorpcyjny
–
zwiększone
działanie
wit.
D
3
powoduje zwiększenie wchłaniania wapnia w
przewodzie pokarmowym
ZAKAŻENIA UKŁADU MOCZOWEGO
1. Do mechanizmów obronnych
zapobiegających zakażeniom układu moczowego należą:
• kwaśne
pH
moczu
i
pochwy
• prawidłowa
flora
bakteryjna
w
okolicy
okołocewkowej
• genetycznie
uwarunkowana
oporność
nabłonka
dróg
moczowych
na
adhezję
• warstwa
mukopolisacharydów
wyściełająca
pęcherz
• białko
Tamma-‐Horsfalla
• przeciwciała
IgA
wydzielana
w
drogach
moczowych
2.
Zakażenia
układu
moczowego
są
częstym
jego
schorzeniami.
W
ich
patogenezie
istotne
są
drogi,
jakimi
drobnoustroje
mogą
dostać
się
do
układu
moczowego.
Drogi
te
mogą
być:
• zależne
od
przepływu
krwi
(zakażenie
hematogenne)
• zależne
od
przepływu
limfy
lub
moczu
(zakażenie
urogenne
lub
wstępujące)
3.
Najprostszy podział zakażeń dzieli je na:
• pierwotne
–
bakteriuria
utrzymująca
się
w
czasie
leczenia
• nawracające
zakażenia
dróg
moczowych
4. Kliniczny podział
dzieli zakażenia dróg moczowych na:
a) Zakażenia górnych dróg moczowych
• ostre odmiedniczkowe zapalenie nerek – czynniki predysponujące: ciąża, utrudnienie odpływu,
zatrzymanie
moczu.
Jest
ono
wynikiem
hematogennego
lub
wstępującego
zakażenia
miąższu
nerki,
najczęściej
przez
bakterie
E.coli
oraz
Proteus
i
Klebsiella.
Może
ono
doprowadzić
do
uogólnienia
zakażenia,
wstrząsu
septycznego
oraz
przewlekłej
niewydolności
nerek.
Objawy:
nagła
wysoka
gorączka
z
dreszczami,
bezmocz,
ból
w
okolicy
lędźwiowej,
w
osadzie
moczu
obecne
wałeczki
leukocytarne,
bakterie
oraz
białko
i
erytrocyty.

Patofizjologia układu wydalniczego
M.P.
15
• przewlekłe odmiedniczkowe zapalenie nerek – występują okresowe nasilenia dolegliwości w postaci
bólów
w
okolicy
lędźwiowej
z
nadciśnieniem
i
bólami
głowy,
utratą
wagi
ciała,
nudnościami
i
bezmoczem.
Przewlekłe
zapalenie
miąższu
nerek
powoduje
spadek
zdolności
nerek
do
zagęszczania
moczu
wskutek
zaburzeń
zwrotnego
wchłaniania
NaCl
(diureza
osmotyczna),
oporności
kanalików
dystalnych
na
działanie
ADH
b) Zakażenia dolnych dróg moczowych
• zapalenie pęcherza moczowego – wywoływane przez drobnoustroje dostające się droga wstępującą z
cewki
moczowej.
Występują
objawy
podrażnienia
pęcherza
z
poliurią,
parciami
naglącymi
i
bezmoczem.
Analiza
moczu
wykazuje
ropomocz,
bakteriomocz,
krwiomocz,
a
posiewy
zwykle
wykazują
obecność
szczepów
E.Coli.
Zakażenie
pałeczką
odmieńca
zazwyczaj
sugeruje
obecność
kamicy
struwitowej.
Wyszukiwarka
Podobne podstrony:
Znaczenie prognostyczne zaburzeń czynności nerek u pacjentów z
Zaburzenia czynności śródbłonka, a przewlekła choroba nerek
Patomechanizm nadciśnienia tętniczego w niewydolności nerek Ż Chatys
Objawy zaburzeń czynnościowych narządu żucia
01 - AFAZJA, V rok, Neurologia, Sem. V rok, Otępienie i zaburzenia czynności wyższych układu nerwowe
objawy zaburzeń czynnościowych narządu żucia
Ojawy zaburzeń czynnościowych narządu żucia, Naika, stomatologia, Normy okluzji
2 Zaburzenia czynności tarczycy w ciąży
Patomechanizm nadciśnienia tętniczego w niewydolności nerek A Sankowska
2 2 Zaburzenia czynności tarczycy w ciąży
Zaburzenia czynnościowe przewodu pokarmowego
1 12 Zaburzenia czynnościowe biegunka ostra ppt
2 2 Zaburzenia czynności tarczycy w ciąży
1 11 Zaburzenia czynnościowe pp id 8862 ppt
Testy laboratoryjne zaburzeń czynności tarczycy
2 3 Zaburzenia czynności tarczycy w ciąży
mord psychologia i psychiatria zaburzenia czynności myślowych
więcej podobnych podstron