1
Funkcje falowe w atomie wodoru
Wartości przyjmowane przez liczby kwantowe
n, l, m
mają wpływ na postać funkcji falowej
)
,
,
(
)
,
,
(
)
,
,
(
m
l,
n,
ϕ
ϑ
ϕ
ϑ
r
r
z
y
x
Ψ
=
Ψ
=
Ψ
)
,
(
Y
)
(
R
)
,
,
(
m
l,
l
n,
m
l,
n,
ϕ
ϑ
ϕ
ϑ
⋅
=
Ψ
r
r
Funkcja
, która spełnia równanie Schrödingera, nosi nazwę
ORBITALU
ORBITAL ATOMU WODORU
= Funkcja falowa elektronu
w atomie wodoru
Orbitale atomu wodoru (1)
Poboczna liczba kwantowa
ma oznaczenia literowe:
g
f
f
unda-
mental
d
d
iffuse
p
p
rincipal
s
s
harp
4
3
2
1
0
l
l
l
l
Uwaga! Nie kryje się za tym żaden głęboki sens, to
jest po prostu sposób na łatwiejsze pamiętanie ...
2
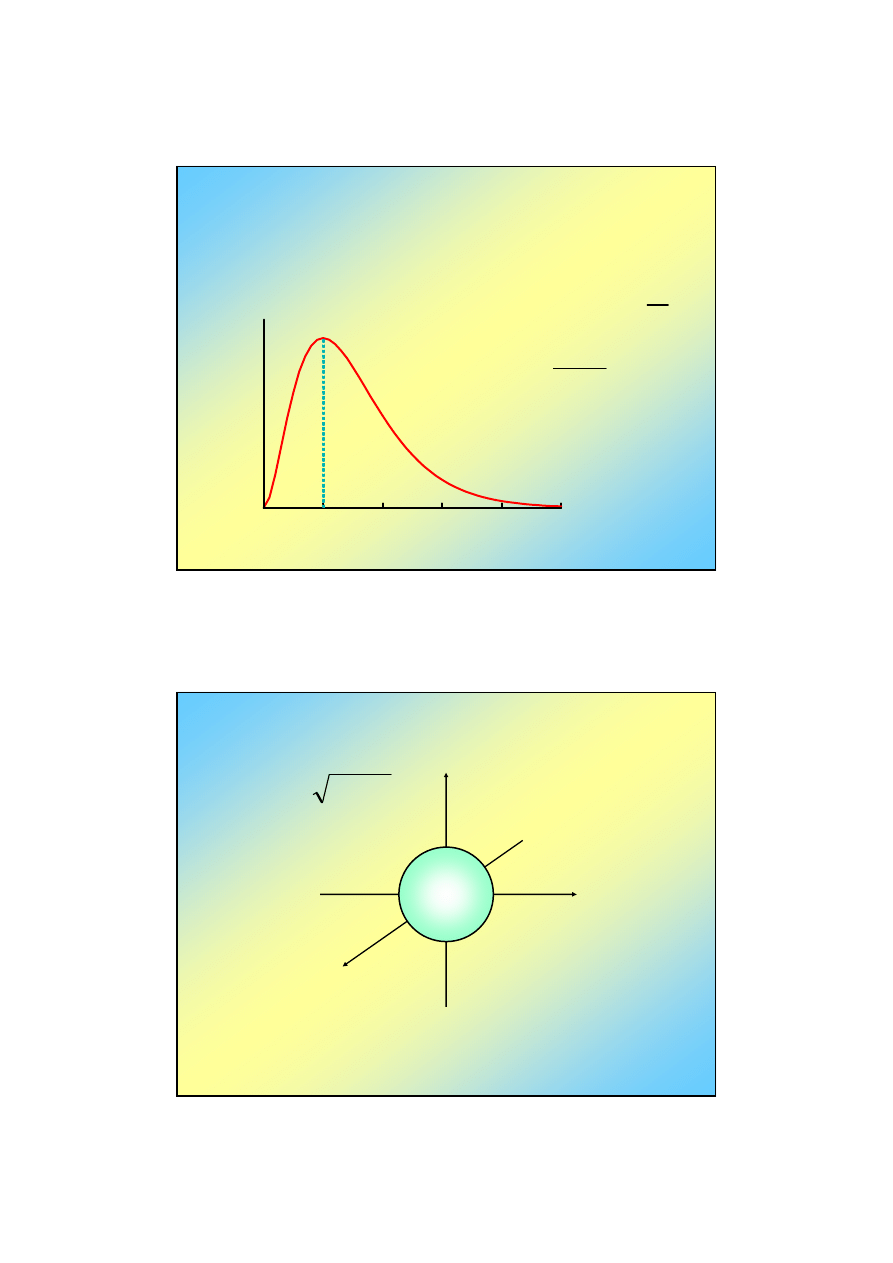
Orbitale atomu wodoru (2)
• Orbital 1s: n=1, l=0, m=0
)
,
(
Y
)
(
R
)
,
,
(
)
,
,
(
00
10
100
100
ϕ
ϑ
ϕ
ϑ
⋅
=
Ψ
=
Ψ
r
r
z
y
x
R( )
exp(
)
/
r
a
r
a
=
⋅
−
−
2
0
3 2
0
a
h
m e
pm
o
e
0
2
2
52 9
=
=
ε
π
,
0
1
2
3
4
5
r/a
0
r
2
R
2
1 s
Część radialna, R
1,0
(r)
E
1
= -13,6 eV
• Część kątowa
Orbitale atomu wodoru (3)
)
,
(
Y
00
ϕ
ϑ
ns
1s
Y( , )
/
ϑ ϕ
π
=
1 4
wykres łączy punkty o
jednakowej wartości
funkcji kątowej, czyli
jednakowej gęstości
prawdopodobieństwa
znalezienia elektonu
3
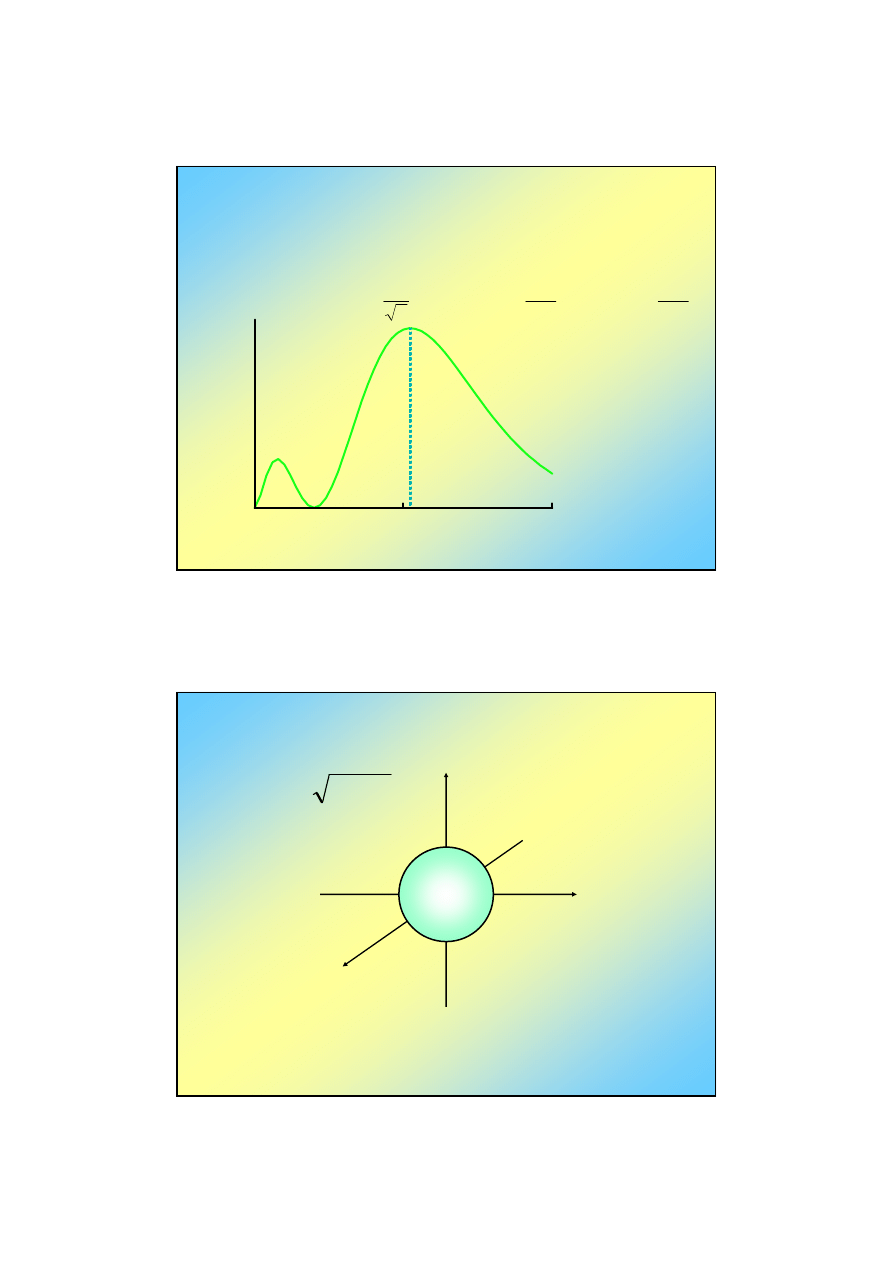
Orbitale atomu wodoru (4)
•
Orbital 2s: n=2, l=0, m=0
)
,
(
Y
)
(
R
)
,
,
(
)
,
,
(
00
20
200
200
ϕ
ϑ
ϕ
ϑ
⋅
=
Ψ
=
Ψ
r
r
z
y
x
0
5
10
r/a
0
r
2
R
2
2 s
R( )
(
) exp(
)
/
r
a
r
a
r
a
=
−
⋅
−
−
1
2
0
3 2
2
2
1
0
0
E
2
= -3,4 eV
Część radialna, R
2,0
(r)
• Część kątowa
Orbitale atomu wodoru (5)
)
,
(
Y
00
ϕ
ϑ
ns
2s
Y( , )
/
ϑ ϕ
π
=
1 4
E
2
= -3,4 eV
4
0
5
10
15
r/a
0
r
2
R
2
2 p
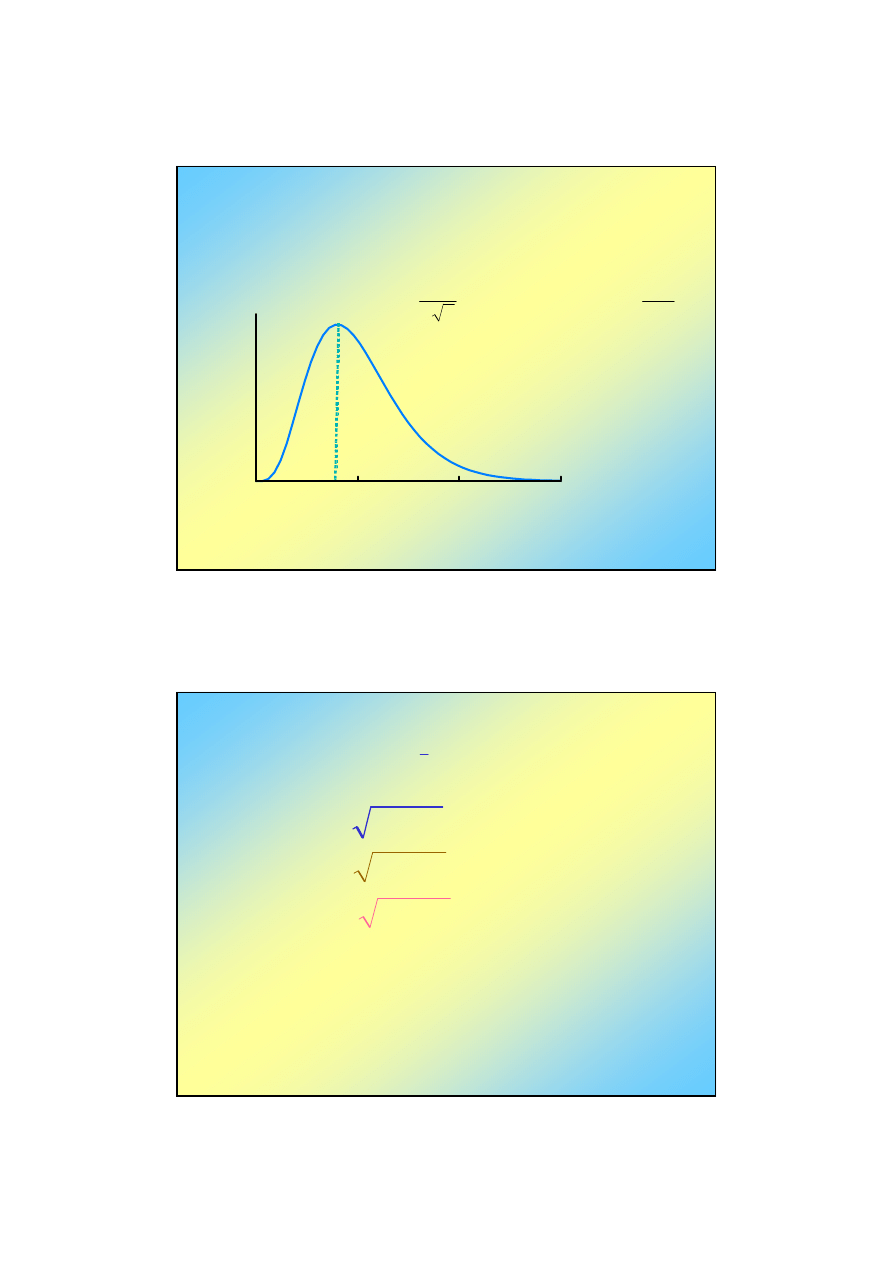
Orbitale atomu wodoru (6)
Orbitale 2p: n=2, l=1, m=0, ±1
Ψ
210
(x,y,z), Ψ
211
(x,y,z), Ψ
21,-1
(x,y,z) ; R
21
(r)
R
2,1
( )
exp(
)
/
r
a
r
r
a
=
⋅ ⋅
−
−
1
2 6
0
5 2
2
0
E
2
= -3,4 eV
Część radialna, R
2,1
(r)
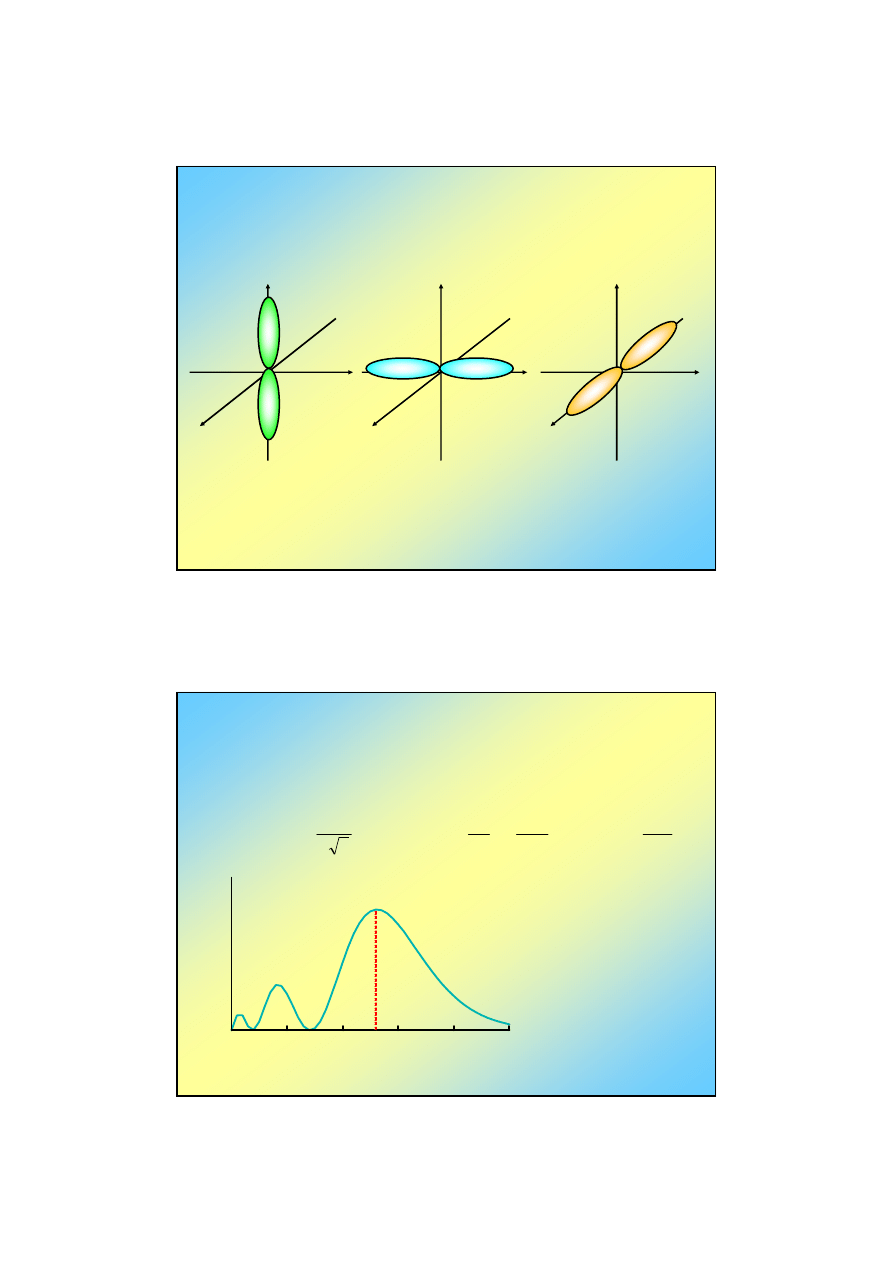
Orbitale atomu wodoru (7)
)
,
(
Y
),
,
(
Y
),
,
(
Y
1
1
11
10
ϕ
ϑ
ϕ
ϑ
ϕ
ϑ
Y (
2p
1,0
z
ϑ ϕ
π
ϑ
, )
/
cos
=
3 4
Y
2p
1,1
x
( , )
/
sin cos
ϑ ϕ
π
ϑ
ϕ
=
3 4
Y
2p
1,-1
y
( , )
/
sin sin
ϑ ϕ
π
ϑ
ϕ
=
3 4
x
r
y
r
z
r
M
M
M
= ⋅
⋅
= ⋅
⋅
= ⋅
cos
sin
sin
sin
cos
ϕ
ϑ
ϕ
ϑ
ϑ
E
2
= -3,4 eV
5
Orbitale atomu wodoru (8)
orbitale np (2p)
m=0
m=1
m= -1
płaszczyzna
węzłowa
xy
płaszczyzna
węzłowa
yz
płaszczyzna
węzłowa
xz
x
y
z
np
z
x
y
z
np
x
x
y
z np
y
Orbitale atomu wodoru (9)
)
,
(
Y
)
(
R
)
,
,
(
)
,
,
(
00
30
300
300
ϕ
ϑ
ϕ
ϑ
⋅
=
Ψ
=
Ψ
r
r
z
y
x
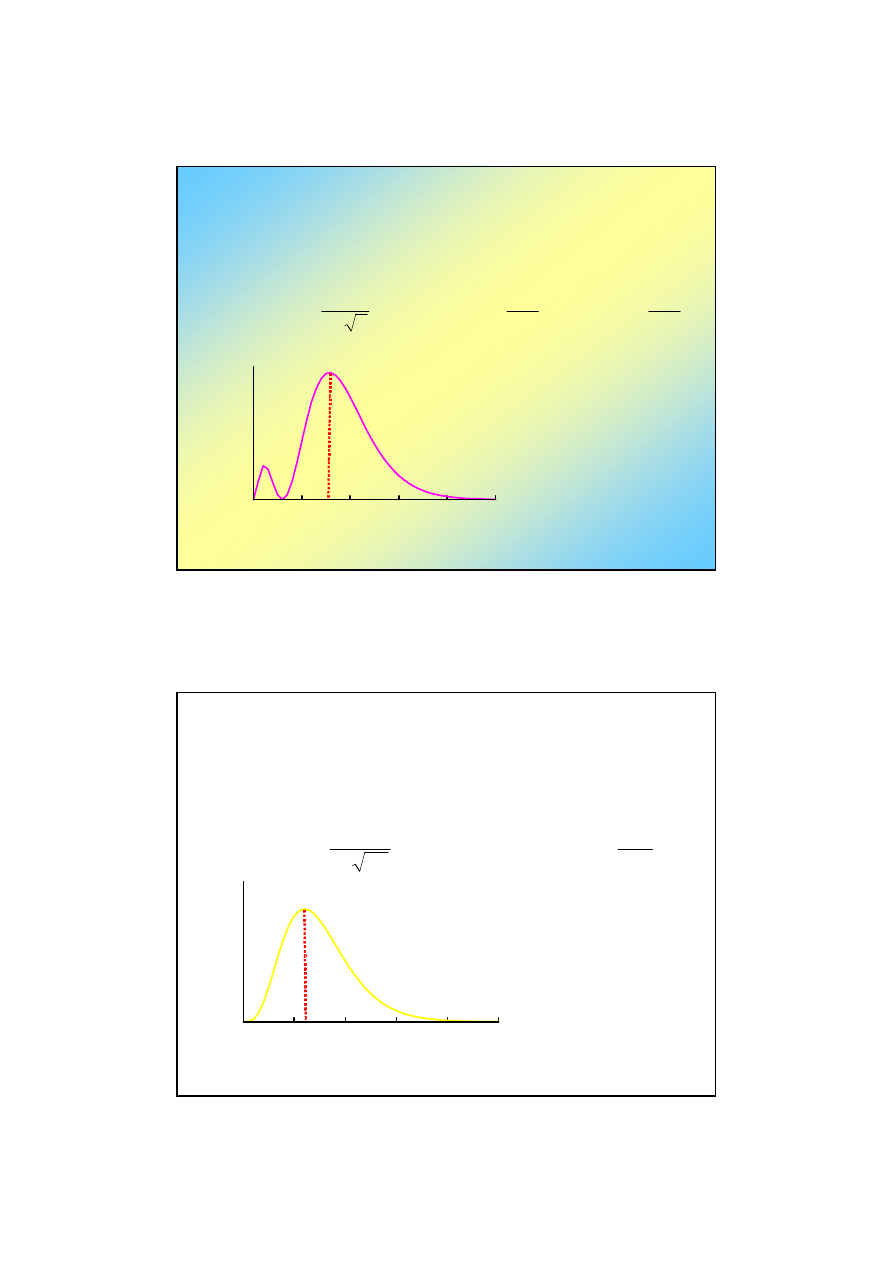
•
Orbital 3s: n=3, l=0, m=0
0
5
10
15
20
25
r/a
0
r
2
R
2
3 s
R
3,0
( )
[
] exp(
)
/
r
a
r
a
r
a
r
a
=
⋅ − +
⋅
−
−
2
9 3
0
3 2
2
2
9
3
3
0
2
0
2
0
E
3
= -1,5 eV
Część kątowa
jest taka sama
dla wszystkich
orbitali ns
Część radialna, R
3,0
(r)
6
Orbitale atomu wodoru (10)
Orbitale 3p: n=3, l=1, m=0, ±1
Ψ
310
(x,y,z), Ψ
311
(x,y,z), Ψ
31,-1
(x,y,z) ; R
31
(r)
3p
z
, 3p
x
, 3p
y
R
3,1
( )
(
) exp(
)
/
r
a
r
a
r
a
=
⋅ −
⋅
−
−
4
27 6
0
5 2
3
3
2
0
0
0
5
10
15
20
25
r/a
0
r
2
R
2
3 p
Część radialna, R
3,1
(r)
Część kątowa
jest taka sama
dla wszystkich
orbitali np
E
3
= -1,5 eV
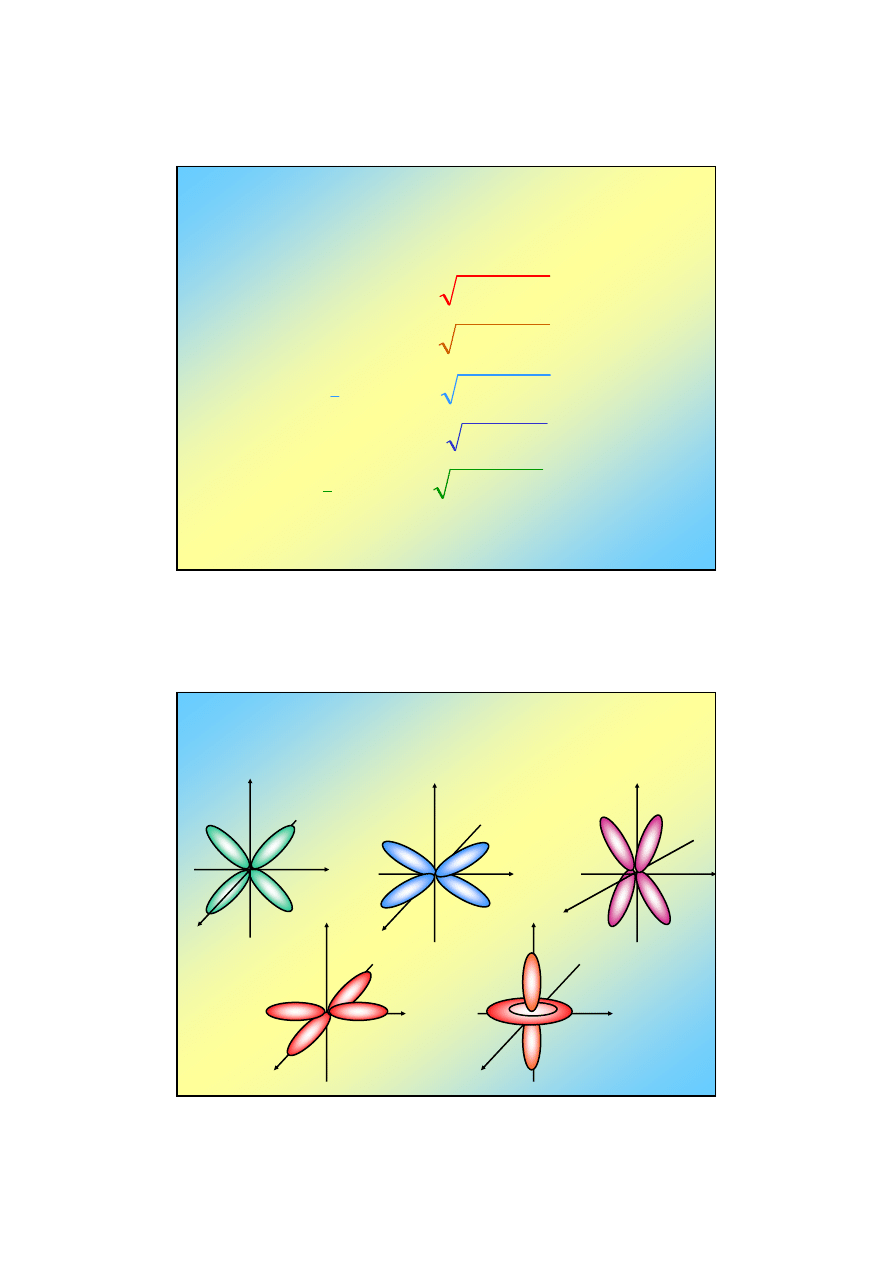
Orbitale atomu wodoru (11)
Orbitale 3d: n=3, l=2, m=0, ±1, ±2
Ψ
320
(x,y,z), Ψ
321
(x,y,z), Ψ
32,-1
(x,y,z), Ψ
322
(x,y,z),
Ψ
32,-2
(x,y,z) ; R
32
(r)
R( )
exp(
)
/
r
a
r
r
a
=
⋅ ⋅
−
−
1
81 30
0
7 2
2
3
0
0
5
10
15
20
25
r/a
0
r
2
R
2
3 d
Część radialna, R
3,2
(r)
E
3
= -1,5 eV
7
2
2
2
3
,
3
,
3
,
3
,
3
z
y
x
yz
xz
xy
d
d
d
d
d
−
Orbitale atomu wodoru (12)
część kątowa orbitali 3d
(
)
/
[ cos
]
3
45 16
3
1
2
2
d
z
Y ( , ) =
2,0
ϑ ϕ
π
ϑ
⋅
−
(
)
/
sin
cos
3
45 16
2
d
xz
Y ( , ) =
2,1
ϑ ϕ
π
ϑ
ϕ
⋅
(
)
( , )
/
sin
sin
3
45 16
2
d
yz
Y
2 1
ϑ ϕ
π
ϑ
ϕ
=
⋅
(
)
( , )
/
sin
cos
3
45 16
2
2
2
2
d
x
y
−
=
⋅
Y
22
ϑ ϕ
π
ϑ
ϕ
(
)
( , )
/
sin
sin
3
45 16
2
2
d
xy
Y
22
ϑ ϕ
π
ϑ
ϕ
=
⋅
Orbitale atomu wodoru (13)
część kątowa orbitali 3d
x
z
y
xz
d
3
x
z
y
xy
d
3
x
z
y
yz
d
3
x
z
y
2
2
3
y
x
d
−
x
z
y
2
3
z
d
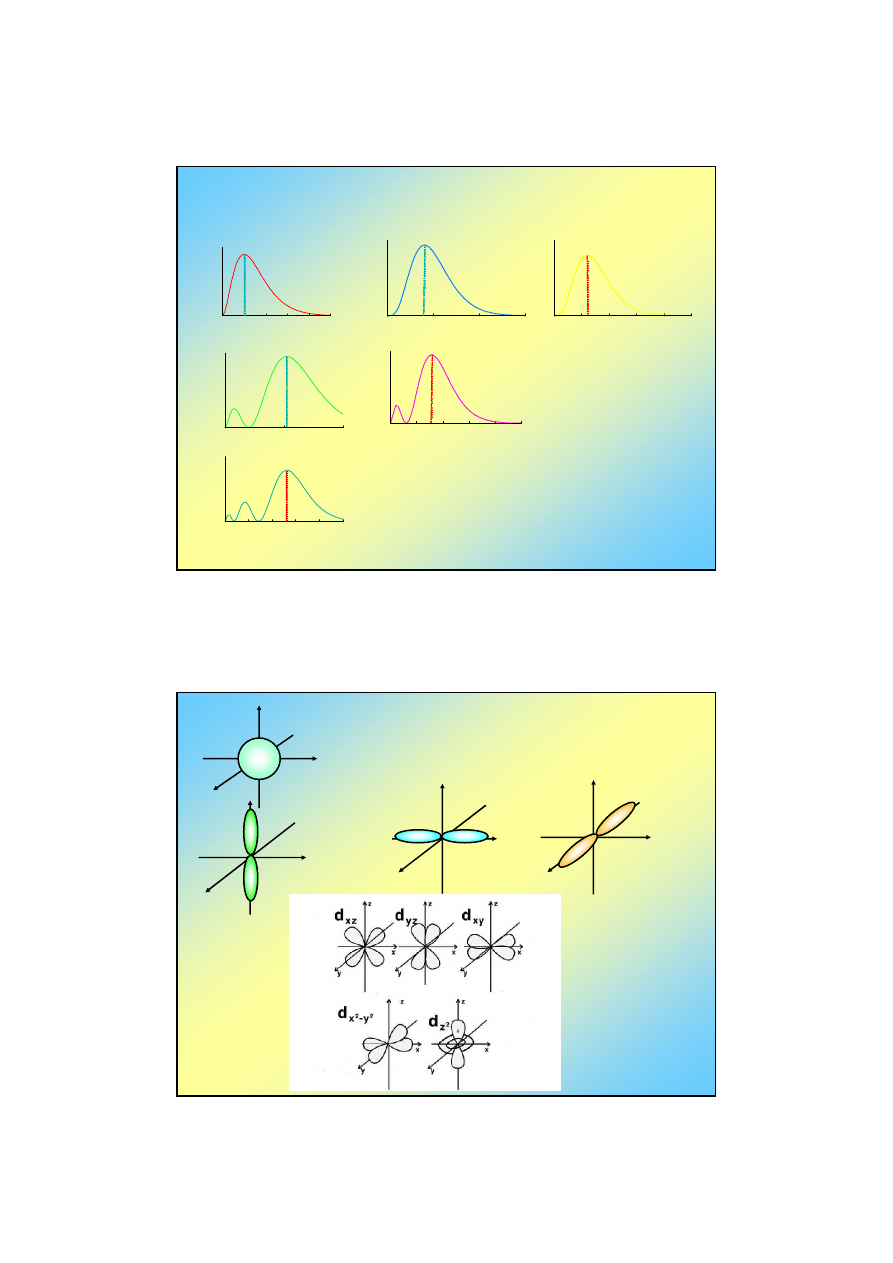
8
Orbitale atomu wodoru (14)
część radialna
0
1
2
3
4
5
r/a
0
r
2
R
2
1 s
0
5
10
r/a
0
r
2
R
2
2 s
0
5
10
15
20
25
r/a
0
r
2
R
2
3 s
0
5
10
15
r/a
0
r
2
R
2
2 p
0
5
10
15
20
25
r/a
0
r
2
R
2
3 p
0
5
10
15
20
25
r/a
0
r
2
R
2
3 d
liczba maksimów części radialnej
orbitalu wynosi zawsze n-l;
wysokość maksimów rośnie z r
Orbitale atomu wodoru (15)
część kątowa
ns
x
y
z
np
z
x
y
z
np
x
x
y
z
np
y
płaszczyzna xz
płaszczyzna xy,
na osiach
płaszczyzna xy
płaszczyzna yz
oś z,
w płaszczyźnie xy
9
Weryfikacja modelu
energie w atomie wodoru
Widmo emisyjne wodoru składa się z serii:
(
)
ν
q n
q n
H
n
q
E
h
R
−
−
=
=
−
1
1
2
2
gdzie:
n
- jest numerem kolejnej serii i najniższego
poziomu w danej serii
q
- jest numerem wyższego poziomu
R
H
- stałą Rydberga
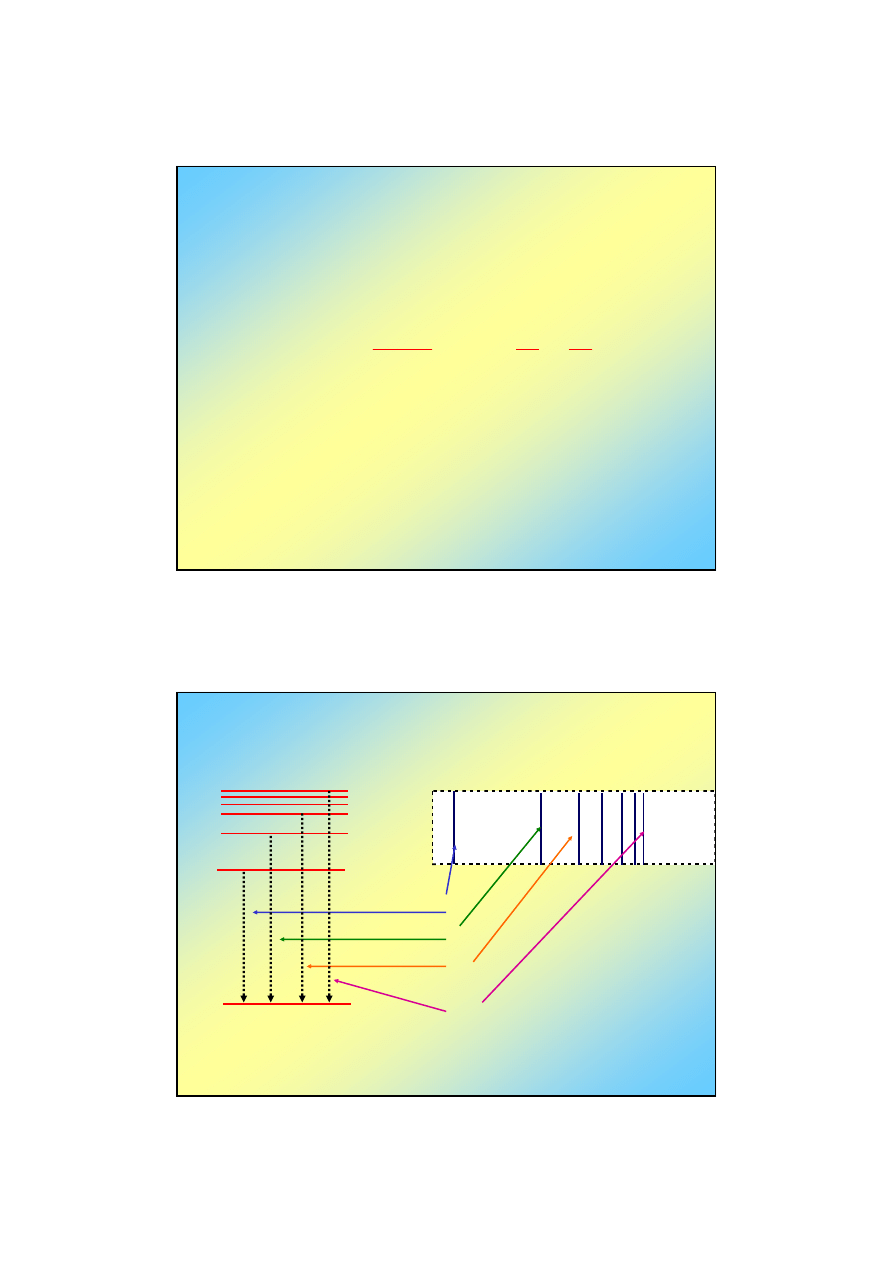
Poziomy energetyczne w atomie a widmo
promieniowania wodoru
<<<<
÷
÷
÷
÷
n = 3
n = 4
n = 7
n = 1
n = 2
Poziomy energetyczne w atomie wodoru, wynikające z
rozwiązania równania Schrödingera
E
1
E
2
E
3
E
4
E
7
<
1
<
2
<
3
<
4
<
7
21
1
2
1
E
E
E
h
∆
=
−
=
ν
31
1
3
2
E
E
E
h
∆
=
−
=
ν
41
1
4
3
E
E
E
h
∆
=
−
=
ν
71
1
7
6
E
E
E
h
∆
=
−
=
ν
10
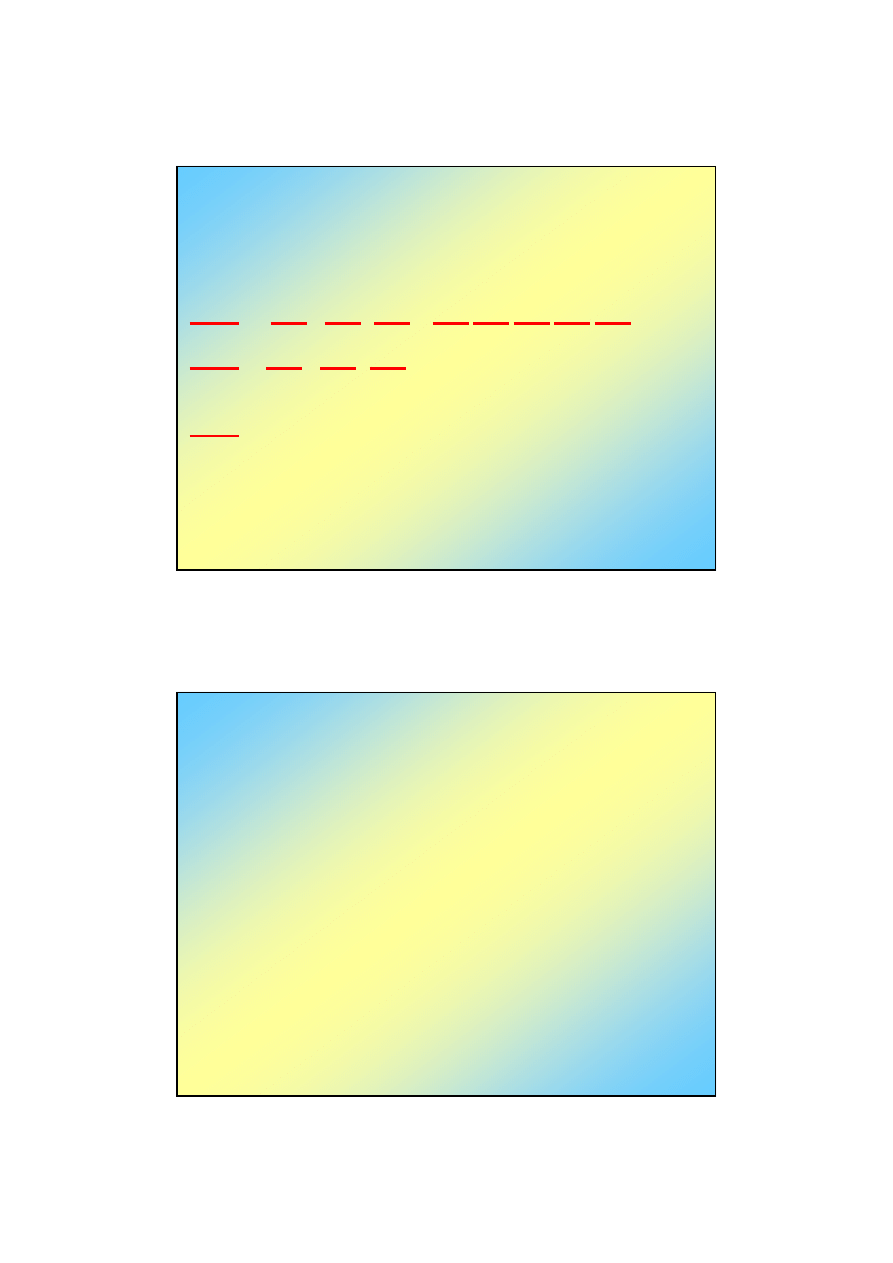
Degeneracja energii w atomie wodoru
Jeśli jednej wartości energii odpowiada kilka funkcji
własnych (orbitali), to mówimy, że ten poziom jest
zdegenerowany:
1s
1
2s
2p
x
2p
y
2p
z
4
3s
3p
x
3p
y
3p
z
xy
d
3
2
2
3
y
x
d
−
2
3
z
d
xz
d
3
yz
d
3
9
dla n=4 jest 1+3+5+
7
=
16 funkcji
dla n=5 jest 1+3+5+7+
9
=
25 funkcji
dla dowolnego n jest 1+3+5+7+
9...
=
n
2
funkcji
Degeneracja energii w atomie wodoru
E
E
E
E
E
E
E
E
E
E
E
E
E
E
s
s
p
p
p
s
p
p
p
d
d
d
d
d
x
y
z
x
y
z
xy
xz
yz
z
x
y
1
2
2
2
2
3
3
3
3
3
3
3
3
3
2
2
2
<
=
=
=
<
=
=
=
=
=
=
=
=
−
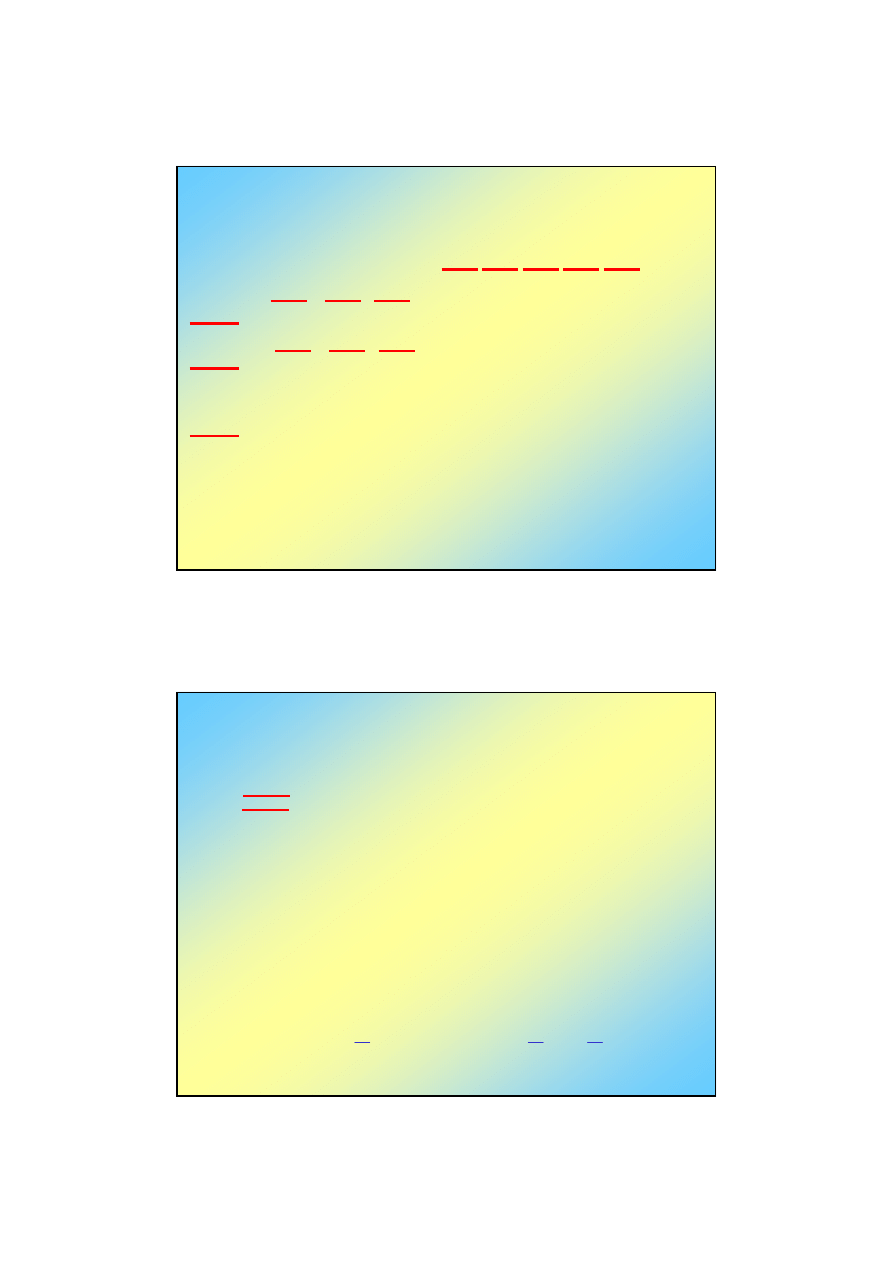
Cofnięcie degeneracji może zachodzić (częściowo
lub całkowicie) w silnym polu :
- elektrycznym (efekt Starka)
- magnetycznym (efekt Zeemana)
Cofnięcie degenracji można obserwować w widmie
emisyjnym lub absorpcyjnym
E
E
E
E
E
E
E
E
E
E
E
E
E
E
s
s
p
p
p
s
p
p
p
d
d
d
d
d
x
y
z
x
y
z
xy
xz
yz
z
x
y
1
2
2
2
2
3
3
3
3
3
3
3
3
3
2
2
2
<
<
=
=
<
<
=
=
<
=
=
=
=
−
11
Cofnięcie degeneracji =
rozszczepienie poziomów energii
2s
3s
3p
x
3p
y
3p
z
1s
1
2p
x
2p
y
2p
z
3
xy
d
3
2
2
3
y
x
d
−
2
3
z
d
xz
d
3
yz
d
3
5
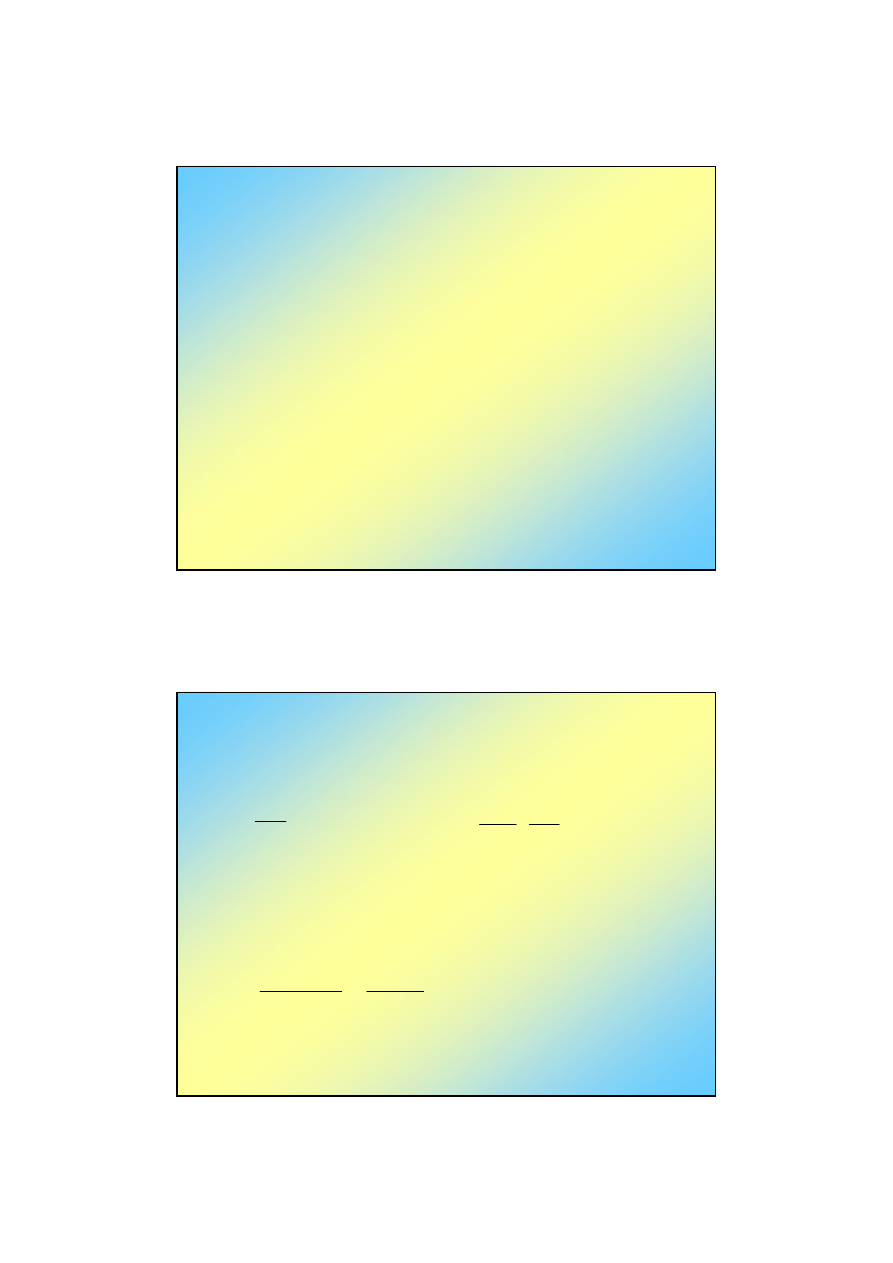
Jeśli elektron w atomie wodoru posiada najniższą
możliwą energię, to jego stan opisuje orbital 1s
Nawet poziomy 1s, 2s, .. mogą być
rozszczepione !
1s
w polu elektrycznym
i magnetycznym
Elektron zachowuje sie tak, jakby posiadał
"wewnętrzny moment pędu„
Ta własność elektronu nosi nazwę
spinu
(Dirac 1928)
Wartość spinu dla elektronu wynosi zawsze 1/2
s
m
s
=
= − +
1
2
1
2
1
2
,
12
Stan elektronu w atomie wodoru
Ψ
Ψ
Φ
n l m
s,m
n l m
s,m
n l m s,m
(x,y,z)
(x,y,z)
(x,y,z)
spinorbital
s
s
s
, ,
, ,
, , ,
- orbital +
- funkcja spinowa
-
σ
σ
⋅
=
Do określenia stanu elektronu w atomie wodoru
niezbędna jest znajomość 4 liczb (bo spin jest stały) -
n, l, m i m
s
W stanie podstawowym (minimum energii) stan
elektronu w atomie wodoru określa orbital 1s
(n=1, l=0, m=0, s=1/2, m
s
=±1/2)
Jony wodoropodobne
....
,
,
,
,
5
4
3
+
+
+
+
+
+
C
B
Be
Li
He
T
p
m
=
2
2
jak w atomie
wodoru
V
= −
⋅
Z
e
r
o
2
1
4
πε
gdzie Z - liczba
protonów w
jądrze
E
m
e
const
e
o
= −
=
π
ε
Z
2
4
2
2 h n
n
2
2
'
Wyniki:
orbitale jak w atomie wodoru,
energia uwzglednia wyższy ładunek jądra
M, M
z
, s, m
s
jak w atomie wodoru
Wyszukiwarka
Podobne podstrony:
podstawy chemii wyklad10 id 366 Nieznany
podstawy chemii wyklad12 id 366 Nieznany
podstawy chemii wyklad02 id 366 Nieznany
podstawy chemii kwantowej id 36 Nieznany
podstawy zarzadzania wyklady id Nieznany
Podstawy zarzadzania wyklad id Nieznany
LOGIKA wyklad 5 id 272234 Nieznany
ciagi liczbowe, wyklad id 11661 Nieznany
AF wyklad1 id 52504 Nieznany (2)
Neurologia wyklady id 317505 Nieznany
Podstawy logistyki wyk 3 id 367 Nieznany
Podstawy teologii Cz05 id 36844 Nieznany
ZP wyklad1 id 592604 Nieznany
CHEMIA SA,,DOWA WYKLAD 7 id 11 Nieznany
Podstawy Finansow egz id 367161 Nieznany
Podstawy Robotyki lab3 id 36832 Nieznany
więcej podobnych podstron