
TLENOMETRIA ERP IN VIVO
Cele ćwiczenia
a.
zapoznanie się z zastosowaniami techniki ERP w zakresie niskich częstotliwości do badania
obiektów biologicznych
b.
pomiar zmian w poziomie natlenowania tkanki prawidłowej podczas podawania zwierzęciu
do oddychania mieszanki gazowej bogatej w tlen, z użyciem sondy tlenometrycznej
Zagadnienia teoretyczne do opracowania
a.
znaczenie tlenu w procesach fizjologicznych i patologicznych w organizmie
b.
metody tlenometryczne stosowalne w układach biologicznych, ich wady i zalety
c.
podstawy ERP: efekt Zeemana, warunek rezonansowego pochłaniania mikrofal, parametry
widma ERP, relaksacja spinowo-sieciowa i spinowo-spinowa, oddziaływanie wymienne
Heisenberga (por. rozdział "Wstęp do ERP" tego skryptu)
d.
zasada pomiarów tlenometrycznych metodą ERP (opracować na podst. poz. 4 i 7 literatury,
por. także rozdziały "Znaczniki spinowe", "Tlenometria" i "Rozdzielcza czasowo detekcja
fosforescencji tlenu singletowego" tego skryptu)
e.
zastosowania spektroskopii ERP w pasmie S (przykłady w poz. 3 literatury)
Wprowadzenie
Znaczenie tlenu w procesach fizjologicznych i patologicznych w organizmie
Historia badań nad fizjologiczną rolą tlenu sięga aż XVII stulecia, kiedy to angielski uczony
Robert Hooke na jednym z pierwszych posiedzeń Królewskiego Towarzystwa Naukowego w 1667
roku wykonał doświadczenie, w którym udowodnił, że stały dopływ powietrza jest konieczny dla
wszystkich zwierząt do utrzymania życia. Po raz pierwszy otrzymał "powietrze zdeflogistonowane"
Joseph Priestley (1774), który stwierdził, że gazem tym oddycha się znacznie łatwiej i przyjemniej
niż powietrzem, oraz że mysz umieszczona pod szczelnym kloszem wypełnionym tlenem żyje dłużej
niż w tej samej objętości zwykłego powietrza. Nazwę "tlen" wprowadził Lavoisier (1743-1794),
który obalił teorię flogistonu i odkrył właściwy mechanizm procesu utleniania.
Tlen jest nam potrzebny głównie do oddychania, pod tym pojęciem rozumie się szereg

reakcji enzymatycznych, w wyniku których z substancji organicznych powstaje ostatecznie CO
2
i woda, a uwalnia się energia niezbędna dla opłacania kosztów innych reakcji metabolicznych.
W jednym spokojnym oddechu człowiek wdycha ok. 500 ml powietrza, w którym znajduje się ok.
100 ml tlenu. W ciągu jednej minuty przez płuca przechodzi ok. 1.6 litra tlenu. Wentylacja płuc
może wzrosnąć nawet 15-krotnie podczas intensywnego wysiłku fizycznego.
Stężenie tlenu wewnątrz naszego organizmu jest znacznie mniejsza niż w powietrzu, np. we
krwi żylnej ciśnienie parcjalne tlenu wynosi 53.3 hPa, co odpowiada stężeniu 53 µmola dm
-3
(14.4%). Ponieważ tlen 7-8 razy lepiej rozpuszcza się w rozpuszczalnikach organicznych niż
w wodzie, jego stężenie jest znacznie większe w błonach biologicznych niż w cytoplazmie.
Wewnątrz wielu komórek istnieją znaczne różnice w stężeniu tlenu: jest ono najwyższe w pobliżu
błony komórkowej, a najniższe w sąsiedztwie mitochondriów.
Od dawna wiadomo, że życiodajny tlen może także szkodzić, ale dopiero intensywne badania
nad metaboliczną rolą tlenu przeprowadzone w ostatnim ćwierćwieczu przyniosły wyjaśnienie
mechanizmów jego toksyczności. Wykazały one, że cząsteczka tlenu może ulegać zarówno pełnej
redukcji do cząsteczki wody (co jest podstawą oddychania), jak i stopniowej redukcji w etapach
jednoelektronowych lub wzbudzeniu. W wyniku tych procesów powstają reaktywne formy tlenu.
Reagują one w sposób niespecyficzny ze składnikami komórek, modyfikując je i uszkadzając (por.
rozdział "Wolne rodniki" tego skryptu).
Udziałem reaktywnych form tlenu są głównie, ale nie wyłącznie biochemiczne role
"czarnych charakterów". Organizmy wykorzystują je także do obrony przed patogenami. Komórki
fagocytujące wytwarzają je do zabicia wchłanianych mikroorganizmów. Udowodniono także, że
reaktywne formy tlenu mogą pełnić rolę przekaźników metabolicznych i brać udział w kontroli
ekspresji genów. Są więc potrzebne organizmom, lecz w stężeniach utrzymywanych na odpowiednio
niskich poziomach. Niekontrolowany wzrost stężeń reaktywnych metabolitów tlenu jest określany
mianem stresu oksydacyjnego i może mieć groźne konsekwencje. Wiadomo dziś, że stres
oksydacyjny jest elementem składowym molekularnych mechanizmów wielu chorób, takich jak
miażdżyca, cukrzyca i choroby nowotworowe, że przyczynia się do uszkodzenia serca i mózgu przy
zawałach i do uszkodzenia przeszczepianych narządów. Mechanizm działania wielu
ksenobiotyków, czyli egzogennych substancji dostającuch się do organizmu, wiąże się z
wytwarzaniem w komórkach reaktywnych form tlenu. Na tym polega szkodliwe działanie m. in.
dymu tytoniowego i alkoholu. Reakcje reaktywnych form tlenu mają też swój udział w procesie
starzenia się.

3
Niedobór tlenu u człowieka
W czasie wspinania się na coraz to większe wysokości zmniejsza się stale ciśnienie
atmosferyczne, a z nim i ciśnienie parcjalne tlenu. Na pewnej określonej wysokości, zazwyczaj
pomiędzy 3000 a 4300 m n.p.m., zaczyna odczuwać się brak tlenu. Do objawów należy: zasinienia
warg i twarzy, utrata łaknienia, nudności i wymioty, zaburzenia jelitowe, bóle głowy, czasami
omdlenia, oddech nieregularny oraz przyspieszone oddychanie w czasie wykonywania dużych
wysiłków fizycznych; występują również zaburzenia psychiczne, podobne do zaburzeń
występujących przy zatruciu alkoholowym. Wszystkie te objawy występują i w innych warunkach
przy braku tlenu.
Przy niskim ciśnieniu atmosferycznym ciśnienie parcjalne dwutlenku węgla w płucach
obniża się równolegle ze spadkiem ciśnienia tlenu, a ponieważ wentylacja płuc jest przede
wszystkim pod kontrolą ciśnienia parcjalnego CO
2
, obniżenie ciśnienia tego gazu wywołuje efekt
hamowania szybkości wentylacji koniecznej do zapewnienia odpowiedniej dostawy tlenu.
Po upływie kilku tygodni, a czasem nawet kilku dni pobytu na dużych wysokościach
człowiek się aklimatyzuje. W aklimatyzacji największe znaczenie mają dwa procesy. Pierwszym
z nich jest wzrost stężenia hemoglobiny we krwi w następstwie wzmożonej aktywności szpiku
kostnego i zwiększenia ilości krążących erytrocytów. Na wysokości 5500 m dochodzi do
podwojenia liczby krwinek czerwonych w stosunku do ich ilości normalnie występującej przy
poziomie morza. Dzięki temu dana objętość krwi może przenosić więcej tlenu z płuc do tkanek.
Powoduje to wzrost ciśnienia tego gazu w tkankach. Drugim procesem związanym z aklimatyzacją
jest wydzielanie przez nerki zasadowego moczu, w wyniku czego obniża się odczyn (pH) krwi,
która staje się bardziej kwaśna, niż wynikałoby to ze stężenia CO
2
. Stan taki powoduje pobudzenie
ośrodka oddechowego i zwiększenie szybkości wentylacji płuc, która staje się prawie wystarczająca,
mimo nieprawidłowo niskiego ciśnienia dwutlenku węgla. Ponadto różnego rodzaju komórki
"przyzwyczajają się" w nie wyjaśniony jeszcze sposób do zmniejszonego ciśnienia tlenu i dwutlenku
węgla i zachowują się w tych warunkach bardziej prawidłowo. Ostre objawy choroby górskiej
ustępują po paru dniach, a po aklimatyzacji zwiększa się zdolność wykonywania pracy fizycznej.
Stopień przystosowania różni się w zależności od osoby i, jak dotychczas, nie znamy sposobów
pozwalających przewidzieć, czy dany człowiek będzie się aklimatyzował szybko czy wolno.
U większości ludzi wyrównywanie skutków niskiego ciśnienia tlenu jest dalekie od doskonałości.

4
Odziaływanie tlenu hiperbarycznego na organizm człowieka
Wpływ zwiększonego ciśnienia tlenu na organizm ludzki poznano przy okazji badań
radiobiologicznych. Poszukiwano bowiem skutecznych sposobów zwiększania natlenowania tkanek,
w szczególności nowotworów, w celu uczulenia ich na promieniowanie jonizujące.
Na skutek oddychania czystym tlenem pod ciśnieniem 3 atm zawartość tlenu we krwi
wzrasta o ok. 25 %. Ta zwiększona ilość tlenu jest jednak szybko uwalniana z hemoglobiny, tak że
w rezultacie stosunkowo niewielka jego ilość dostarczana jest do słabo ukrwionych tkanek. Wyniki
testów klinicznych z zastosowaniem hiperbarycznego tlenu jako radiouczulacza przyniosły
nieznaczne pozytywne efekty w przypadku radioterapii guzów zlokalizowanych w okolicach głowy
i szyi oraz guzów pęcherza moczowego. Niestety zauważono także zwiększoną śmiertelność
pacjentów traktowanych hiperbarycznym tlenem oraz występowanie objawów związanych z
uszkodzeniami płuc i krtani.
W związku z niepowodzeniami w stosowaniu zwiększonego ciśnienia tlenu zaproponowano
stosowanie karbogenu, czyli mieszanki 95% O
2
i 5 % CO
2
. Wprowadzenie dodatku CO
2
przeciwdziała zwężaniu naczyń, które występuje podczas oddychania czystym tlenem, zwłaszcza
hiperbarycznym. Eliminuje to również występowanie bezdechu, który jest częstym skutkiem
oddychaniam czystym tlenem. Ponadto CO
2
może przesuwać równowagę dysocjacji
hemoglobina/tlen w ten sposób, że do tkanek będzie dostarczana większa ilość tlenu.
Metody tlenometryczne stosowane w układach biologicznych, ich wady i zalety
Ze względu na zasadę pomiaru metody tlenometryczne stosowane w układach biologicznych
można podzielić w następujący sposób:
a.
metody polarograficzne, oparte na zastosowaniu elektrod. Najpowszechniej stosowana jest
elektroda Clarka, której szczegółowe omówienie można znaleźć w poz. 2 literatury.
b.
metody manometryczne (omówienie j.w.)
c.
metody spektroskopowe, wykorzystujące wpływ cząsteczki tlenu na czas relaksacji stanów
wzbudzonych innych molekuł. Informację o czasach relaksacji molekuł można uzyskać
5
różnymi metodami: mierząc fluorescencję lub fosforescencję odpowiednich cząsteczek. Czas
relaksacji można też badać metodą NMR (mierzy się czasy relaksacji jąder wodoru, fosforu,
węgla związków obecnych w układzie) lub ERP.
d.
metody absorpcyjne, wykorzystujące zjawisko wpływu tlenu na własności spektralne
niektórych endogennych pigmentów, takich jak hemoglobina, mioglobina, cytochrom aa
3
,
flawoproteiny.
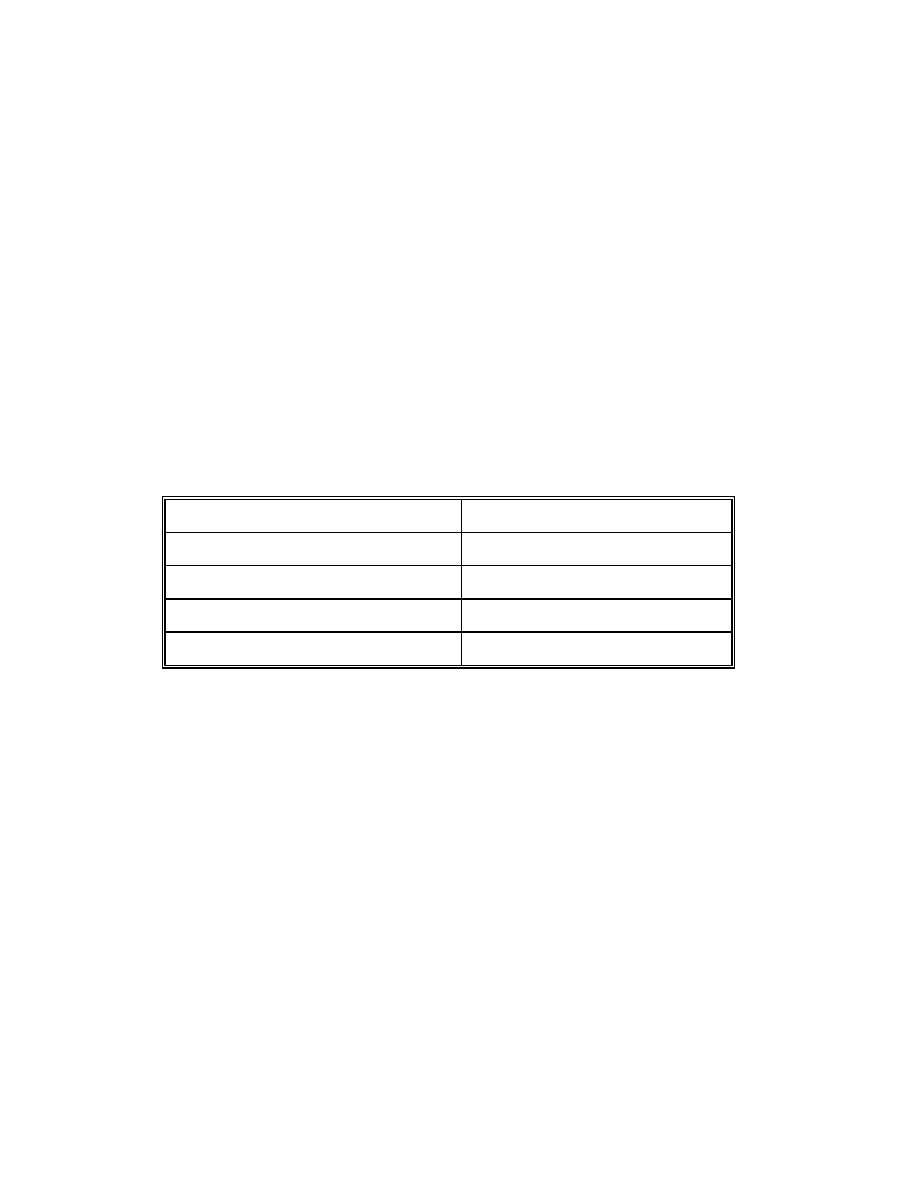
Tabela 1.
Porównanie wyników pomiarów tlenometrycznych różnymi metodami w tkance in
situ (mięsień sercowy u psa) [wg. 9].
Zastosowana metoda
PO
2
, [mmHg]
mikroelektroda platynowa
14.7 - 17.2
metoda gazometryczna
11 - 23
makroelektrody (37-275 µm śred.)
19.3 (2.5 - 9 mm głęb.)
nasycenie mioglobiny
4 - 6
Odczynniki i aparatura
Sonda tlenometryczna, metofan, butla z tlenem medycznym, igły i strzykawki jednorazowe,
rękawiczki chirurgiczne, spektrometr ERP z mostkiem mikrofalowym na pasmo S.
Wykonanie ćwiczenia
1. Zapoznanie się z aparaturą ERP do pomiarów w pasmie S
Aparatura ERP do pomiarów in vivo składa się ze spektrometru "Radiopan" oraz mostka
mikrofalowego "Jagmar" generującego mikrofale w zakresie częstotliwości od 2 do 4 GHz.

6
Po włączeniu aparatu umieścić standard DPPH we wnęce rezonansowej, dostroić mostek
mikrofalowy i zarejestrować sygnał ERP standardu przy następujących parametrach:
częstotliwość
- 2.89 GHz
tłumienie mocy mikrofal
- 8-10 dB
wartość pola magnetycznego - ok. 101 mT
przemiatanie pola
- 1 x 10 mT
amplituda modulacji
- 1 x 100 µT
2. Przygotowanie zwierzęcia do eksperymentu (pod nadzorem asystenta)
Mysz, której wcześniej podano sondę tlenometryczną (tusz chiński) wprowadzić w stan
płytkiej narkozy przy pomocy metofanu, a następnie umieścić w pojemniku pomiarowym.
3. Pomiar wyjściowego stanu natlenowania badanej tkanki
Pojemnik ze zwierzęciem włożyć do wnęki rezonansowej i dostroić mostek mikrofalowy.
Rejestrować sygnał ERP sondy co 5 minut aż do osiągnięcia stałego poziomu (ok. 30-40 min), przy
tych samych parametrach (za wyjątkiem częstotliwości) co standard.
4. Rejestrowanie zmian poziomu tlenu
Podawać zwierzęciu do oddychania mieszaninę 95% O
2
i 5% CO
2
przez ok. 30 minut,
rejestrując zmianę poziomu natlenowania tkanki i później powrót do stanu wyjściowego.
Opracowanie wyników
Narysować zależność szerokości połówkowej oraz amplitudy sygnału ERP sondy od czasu.
Na podstawie wybranych punktów kalibracyjnych oszacować stężenie tlenu w tkance. Jak szybko
po podaniu tlenu do oddychania można zaobserwować efekt zmiany poziomu tlenu w tkance? Ile
% w stosunku do wyjściowego poziomu stanowi ta zmiana? Jak szybko po zaprzestaniu podawania
tlenu poziom wraca do stanu wyjściowego? Jakie mogą być przyczyny tego zjawiska?

7
Literatura podstawowa
1.
G. Bartosz "Tlen - pierwiastek życia i śmierci", rozdz. 1.1 w monografii "Druga twarz
tlenu", PWN, Warszawa 1995, str. 13-16
2.
A. C. Giese "Fizjologia komórki", PWN Warszawa 1985, str. 367-373.
3.
S.J. Łukiewicz "Spektroskopia in vivo ERP w biologii i medycynie", rozdz. 5.5 w
monografii: "Problemy biocybernetyki i inżynierii biomedycznej", tom II "Biopomiary" (red.
M. Nałęcz), , Wyd. Komunikacji i Łączności, Warszawa, 1991, str. 357-362
4.
W.K. Subczyński "Zastosowanie ERP w badaniach stężenia i dyfuzji tlenu w układach
biologicznych", Zeszty Naukowe UJ, Prace z Biologii Molekularnej Z.10, Kraków 1984,
str.145-203.
Literatura uzupełniająca
5.
F. Goda et al. "In Vivo Oximetry Using EPR and India Ink", Magn. Res. Med. 33, 1995, str.
237-245,
6.
D.G. Hirst "Oxygen Delivery to Tumors", Int. J. Radiation Oncology Biol. Phys., 12, 1986,
str. 1271-1277
7.
M. Symons "Spektroskopia ERP w chemii i biochemii", PWN Warszawa, 1987.
8.
N. Vahidi et al. "In Vivo and in Vitro EPR Oximetry with Fusinite: A New Coal-Derived,
Particulate EPR Probe", Magn. Res. Med. 31, 1994, str.139-146
9.
N. Vanderkooi et al. "Oxygen in mammalian tissue: methods of measurement and affinities
of various reactions" Am. J. Physiol. 260, 1991, str. C1131-C1150.
Wyszukiwarka
Podobne podstrony:
PRK 23 10 2011 org
23 piątek
23 Metody montażu w mikroelektronice
23 Tydzień zwykły, 23 wtorek
Atrybucje 23 24
Cwiczenia 23 25 2007
23 sekcja
21 23
Doradztwo Podatkowe z 23 czerwca 08 (nr 121)
23 Pddzialywanie swiatla z materia
Podstawy rekreacji ćwiczenia 23 01 10x
brzuch i miednica 2003 2004 23 01
Dz U 2008 4 23
1996 07 23 1433
karta informacyjna do VAT 23
ISO128 23 lines technical
więcej podobnych podstron