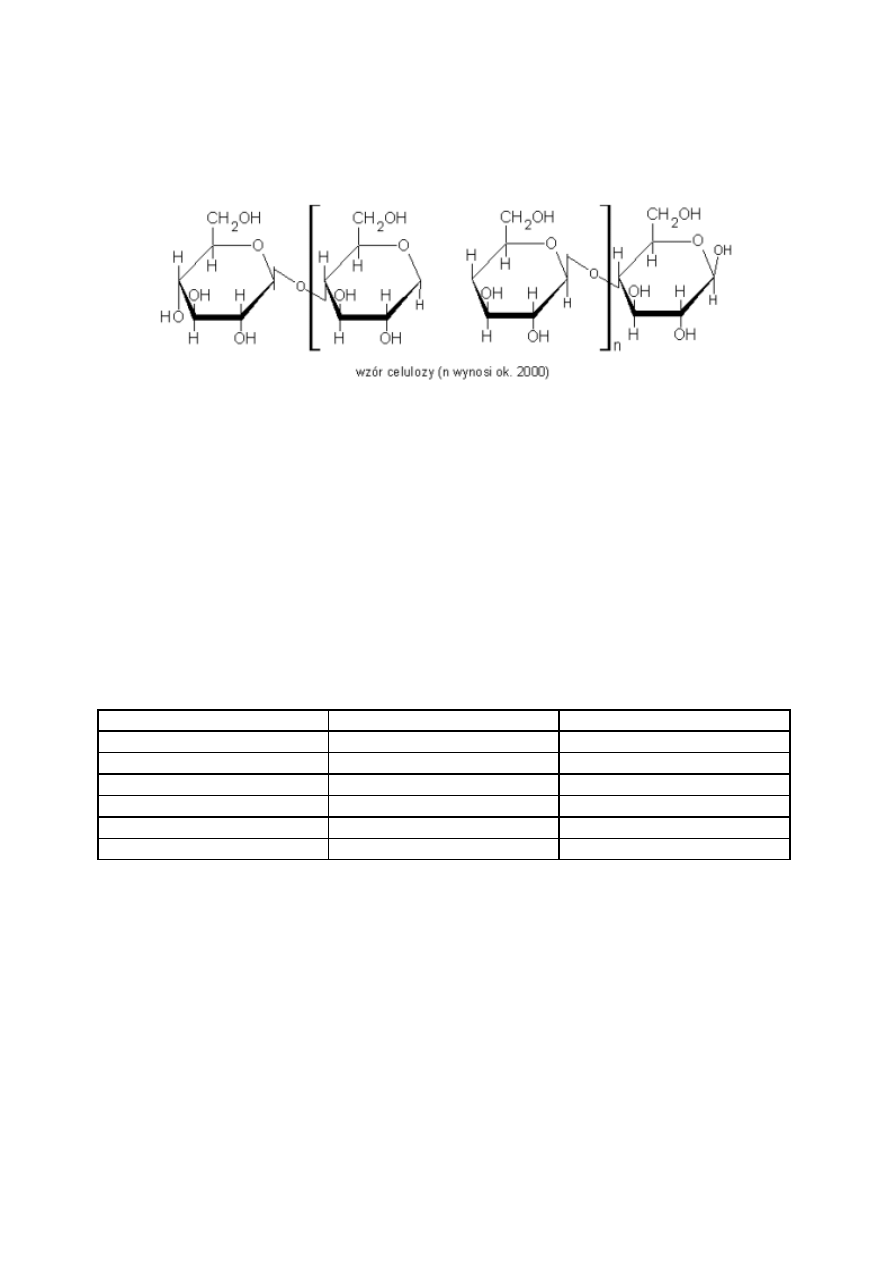
CELULOZA
Celuloza jest naturalnym polimerem zbudowanym z cząsteczek D-glukozy połączonych
wiązaniem ß-glikozydowym. Sposób połączenia jednostek przedstawiono na rysunku:
Masa cząsteczkowa materiałów celulozowych ma istotny wpływ na właściwości fizyczne
celulozy oraz produktów pochodnych i zależy od źródła pochodzenia i sposobów
przetwarzania materiału.
Przedstawione dane wskazują, że tak w procesach wydzielania, jak i na etapie produkcji
pochodnych następuje degradacja polimeru. Dlatego test lepkości, pozwalający na określenie
średniej masy cząsteczkowej, jest jednym z najważniejszych sposobów oceny surowca. Inny
sposób określania masy cząsteczkowej w przedziale 15 000 do 1 500 000 opiera się na
osmometrii.
Tabela 1. Przykładowe wartości mas cząsteczkowych celulozy i pochodnych celulozy
Materiał
Masa cząsteczkowa
Liczba jednostek cukru
Natywna celuloza
Ponad 600 000
Ponad 3 500
Bawełna
80 000 – 500 000
500 – 3 000
Drewno (pulpa)
80 000 – 210 000
600 – 1 300
Handlowa celuloza
30 000 – 80 000
200 – 600
Nitroceluloza
25 000 – 875 000
100 – 3 500
Octan celulozy
45 000
175 – 360
Jak już wspomniano, w trakcie operowania celulozą ulega ona degradacji (rozerwaniu wiązań
glikozydowych). Do najczęściej spotykanych czynników powodujących degradację należy
działanie kwasów, utleniaczy, ogrzewanie, działanie światła i tlenu z powietrza. Celuloza jako
produkt naturalny ulega degradacji pod wpływem niektórych mikroorganizmów. W wyniku
degradacji rośnie zawartość grup aldehydowych i tym samym zdolność do redukcji soli srebra
lub miedzi(II). Jak większość węglowodanów celuloza ma zdolność adsorpcji i desorpcji
wody. Zawartość wody w stanie równowagi zależy od wilgotności powietrza i temperatury.
Zawartość wody w celulozie ma znaczący wpływ na niektóre jej właściwości. I tak chemiczna

reaktywność grup wodorotlenowych w procesie estryfikacji jest znacznie niższa, gdy
całkowicie usunie się wodę. Właściwości mechaniczne włókien są znacznie lepsze, gdy
celuloza zawiera wodę.
Oznaczanie celulozy
Cukry, w tym i celulozę oznacza się przez utlenienie dwuchromianem w wodnym roztworze
kwasu siarkowego. Nadmiar dwuchromianu miareczkuje się siarczanem amonowo-
żelazawym.
Odczynniki
-
Dwuchromian potasu,
-
Kwas stężony siarkowy,
-
Fe(NH
4
)
2
(SO
4
)
2
x6H
2
O,
-
Kolba stożkowa 400 cm
3
,
-
Mieszadło magnetyczne,
-
Szkiełko zegarkowe,
-
Pipeta 25 cm
3
,
-
Cylinder miarowy,
-
Biureta
Roztwory do analizy
Dwuchromian potasu (0,5 N): - Dwuchromian potasu, cz.d.a. suszyć przez 8 h w temperaturze
100-105 °C. Odważyć 24,515 g dwuchromianu, rozpuścić w wodzie (500 cm
3
), przenieść
ilościowo do kolby miarowej i dopełnić wodą do 1 dm
3
. Roztwór w razie potrzeby przesączyć
i przechowywać w butelce z ciemnego szkła.
Siarczan amonowo-żelazawy (0,1 N): - Umieścić 300 ml wody destylowanej w 1-litrowej
kolbie miarowej. Rozpuścić w niej 39.20 g siarczanu amonowo-żelazawego. Dodaj ostrożnie
25 ml 7N kwasu siarkowego, dopełnij wodą do 1 litra. Roztwór przechowywać w butelce z
ciemnego szkła.
Sposób postępowania
Do kolby stożkowej o obj. 300 ml wprowadzić próbkę (0,25 g) i zawieś ją w 25 ml wody

destylowanej. Dodaj 50 ml roztworu 0.5N dwuchromianu potasu i intensywnie zamieszaj.
Następnie dodaj ostrożnie 100 ml stężonego kwasu siarkowego, przykryj małym lejkiem i
podgrzewaj do zagotowania na płytce azbestowej nad palnikiem. Odstaw z palnika, pozostaw
na 15 minut w temperaturze pokojowej, schłodź pod wodą wodociągową i przenieś ilościowo
do kolbki miarowej o obj. 250 ml. Dopełnij wodą destylowaną do kreski. Pobierz 50 ml,
dodaj kilka kryształków żelazicyjanku potasu jako wskaźnika i miareczkuj 0.1N roztworem
siarczanu amonowo-żelazowego do niebieskiej niezanikającej barwy. Jednocześnie wykonaj
próbę ślepą bez próbki z celulozą. Procentową zawartość celulozy określ ze wzoru:
% celulozy =
%
25
20
)
(
85
,
6
W
N
V
V
s
⋅
⋅
⋅
−
⋅
Gdzie: V – objętość siarczanu zużyta na miareczkowanie próby właściwej,
V
r
– objętość siarczanu zużyta na miareczkowanie próby ślepej,
N – normalność roztworu siarczanu amonowo-żelazowego (0,1 N)
W – masa próbki w g.
Oznaczanie zawartości alfa-celulozy
Celuloza, która jest poli-(1,4)-ß-D-glukopiranozą, zwykle zawiera pewne ilości
monosacharydów, ligninę, sole metali. Nawet po starannym oczyszczeniu nie jest ona
indywiduum chemicznym, lecz mieszaniną homopolimerów różniących się stopniem
polimeryzacji (DP). Zależy on od wielu czynników, takich jak pochodzenie materiału, sposób
wydzielania, sposób oczyszczania. Ponieważ nie można precyzyjnie określić rozkładu mas
cząsteczkowych składników celulozy, przyjęto podział cukru na frakcje uwzględniając
rozpuszczalność w roztworach wodnych zasad. I tak materiał, który po traktowaniu 17,5%
roztworem wodorotlenku sodu pozostaje nierozpuszczalny, nosi nazwę alfa-celulozy.
Materiał, który jest rozpuszczalny w alkaliach, lecz wytrąca się po zakwaszeniu, nosi nazwę
beta-celulozy. Jest to zwykle mieszanina polimerów mających DP około 200, tworzących się
w wyniku degradacji celulozy w czasie operacji izolacji i oczyszczania.
Odczynniki i aparatura
celuloza
17,5% r-r wodorotlenku sodu

10% r-r kwasu octowego
alkohol metylowy
kolba ssawkowa 300 cm
3
lejek ze spiekiem
naczyńko wagowe
łopatka
cylinder miarowy 50 cm
3
Wykonanie oznaczenia:
W kolbie stożkowej umieścić celulozę (3 g), dodać r-r wodorotlenku sodu (35 cm
3
) i
pozostawić na 10 min., delikatnie mieszając zawartość kolby do uzyskania zawiesiny.
Następnie dodać porcjami wodorotlenek sodu (4 x 10 cm
3
) mieszając zawartość kolby
mieszadłem magnetycznym w ciągu 30 minut. Następnie dodać wodę (75 cm
3
) i uzyskaną
zawiesinę przesączyć na lejku szklanym ze spiekiem lub na lejku Buchnera. Osad przemyć
750 cm
3
wody. Następnie osad na lejku zadać 40 cm
3
roztworu kwasu octowego, pozostawić
na 10 minut, po czym odfiltrować kwas pod próżnią i przemyć osad 200 cm3 wody.
Uzyskany osad przemyć trzema porcjami metanolu (3 x 30 cm3), odfiltrowując każdorazowo
alkohol po 5 min. Na koniec przenieść osad ilościowo do naczyńka wagowego i suszyć do
stałej wagi (około 1 h) w suszarce w temperaturze 100-105°C. Określić masę osadu.
Zawartość alfa-celulozy wyliczyć ze wzoru:
100
m
m
(%)
celuloza
alfa
p
o
=
−
gdzie: m
o
- masa osadu,
m
p
- masa próbki do analizy.
Wyszukiwarka
Podobne podstrony:
3 ćwiczenia BADANIE asfaltów
Ćwiczenie7
Cwiczenia 2
Ćwiczenia V
metody redukcji odpadów miejskich ćwiczenia
Ćwiczenia1 Elektroforeza
cwiczenia 9 kryzys
Ćwiczenia 1, cz 1
Ćwiczenie 8
9 ćwiczenie 2014
Cwiczenie 1
Ćwiczenie 2 Polska w europejskim systemie bezpieczeństwa
11 CWICZENIE 1 SEMESTR LETNIid 12747 ppt
więcej podobnych podstron