
1 - r z ę d o w ą s t r u k t u r ę b i a ł e k b a d a m y m e t o d ą - E d m o n a
A b y w y t w o r z y ć c z A T P z A D P i P i p o t r z e b a Δ G a = 9 0 0 0 c a l r ó ż n i c a p o t e n c j a ł u –
Δ g o ( e n s w o b o d n e j w y n o s i ) = 0 , 1 7 v
A c e t y l o C o A - p r z e m i a n y : m e t a b o l i c z n e , b i o s y n t e z a k w t ł u s z c z o w y c h
A D P + P + Δ G
o
= 3 3 , 5 k J = 0 , 8 k c a l
A k t y w a t o r : p r z e k s z t a ł c a p r o e n z y m w e n z y m
A k t y w a t o r y t o : C u
2 +
, Z n
2 +
, M n
2 +
, M g
2 +
A k t y w n o ś ć m o l e k u l a r n a t o : l i c z b a m o l i s u b s t r a t u k t ó r a m o ż e p r z e r e a g o w a ć
w c i ą g u 1 m i n z 1 m o l e m c e n t r ó w a k t y w n y c h e n z y m u d l a 3 0 s t C ( l i c z b a
o b r o t ó w e n z y m u )
A m i n o k w a s b i a ł k o w y w y s t ę p u j ą c y w n a j w i ę k s z y c h i l o ś c i a c h w m ą c e :
g l u t a t i o n
A m i n o k w a s n i e p o s i a d a j ą c y s t e r o i z o m e r u t o : g l i c y n a
A m i n o k w a s e m z b i o r c z y m n a z y w a m y - k w a s g l u t a m i n o w y .
A m i n o k w a s y e g z o g e n n e d l a ż y w y c h o r g : w a l i n a , l e u c y n a , f e n y l o a l a n i n a ,
l i z y n a , i z o l e u c y n a , t r y p t o f a n , m e t i o n i n a , t r e o n i n a ( t y r o z y n a - c z ł o w i e k )
A m i n o k w a s y e n d o g e n n e : t o a m i n o k w a s y k t ó r e o r g m o ż e s y n t e t y z o w a ć z
i n n y c h z w i ą z k ó w
A m i n o k w a s y m a j ą c e i s t o t n e z n a c z e n i e w b i o c h e m i i , t o z w i ą z k i r o d z a j ó w :
g l u k o z a m i n y i g a l a k t o z a m i n y . M a j ą o n e g r u p ę a m i n o w ą p o d s t a w i o n ą
z a m i a s t : g r u p y O H p r z y C 2
A m i n o k w a s y m o ż n a o d r ó ż n i ć o d p e p t y d ó w z a p o m o c ą r e a k c j i :
n i n h y d r y n o w e j
A m i n o k w a s y n a l e ż ą d o g r : s u b s t r a t ó w s t r u k t u r a l n y c h
A m i n o k w a s y n i e p o s i a d a j ą s t e r o i z o m e r u - g l i c y n a
A m i n o k w a s y n i e b i a ł k o w e : 5 - h y d r o k s y l i z y n a ; o r n i t y n a ; c y t r u l i n a ; b e t a
a l a n i n a ; k w a s a l f a a m i n o m a s ł o w y ; 4 - h y d r o k s y p r o l i n a ; 3 , 5 - j o d o t y r o z y n a
A m i n o k w a s y p o l a r n e b e z ł a d u n k u : s e r y n a , t r e o n i n a , t y r o z y n a , k w a s
a s p a r g i n o w y , c y s t e i n a , g l u t a m i n a , g l i c y n a
A m i n o k w a s y p o l a r n e z d o d a t k o w ą g r u p ą C O O
-
: k w a s g l u t a m i n o w y i
a s p a r g i n o w y
A m i n o k w a s y r o z p u s z c z a l n e w s o k a c h t r a w i e n n y c h s ą w c h ł a n i a n e w j e l i c i e
c i e n k i m . O b e c n o ś ć c u k r o w c ó w i t ł u s z c z ó w : z m n i e j s z a s z y b k o ś ć w c h ł a n i a n i a
A m i n o k w a s y z a w i e r a j ą w s w o i m s k ł a d z i e - C , N , H , O , S
A m i n o k w a s y z b i o r c z e : m e t i o n i n a , k w g l u t a m i n o w y , k w a s p a r g i n o w y
A m i n o k w a s y : e l e m e n t y s t r u k t u r a l n e b i a ł e k
A p a r a t c y k l u m o c z n i k o w e g o : z n a j d u j e s i ę w m i t o c h o n d r i o m
B i a ł k a m l e k a t o : k a z e i n a , g l o b u l i n a , a l b u m i n a
B i a ł k a o s o c z a k r w i : a l b u m i n y α 1 , α 2 , β γ g l o b u l i n y , f i b r y n o g e n
B i a ł k a o s o c z a k r w i : F i b r y n o g e n , β - a l b u m i n y ; γ - g l o b u l i n y
B i a ł k a w p u n k c i e i z o e l e k t r y c z n y m w y k a z u j ą r o z p u s z c z a l n o ś ć : n a j m n i e j s z ą
B i a ł k a z ł o ż o n e : m e t a l o - , b r o m o - , f o s f o - , g l i k o - , l i p o - , n u k l e o p r o t e i n y
B i a ł k a m i p r o s t y m i s ą e n z y m y n a l e ż ą c e d o g r u p y g ł ó w n e j : h y d r o l a z
B i a ł k o d o b o r o w e : z a w i e r a w s z y s t k i e a m i n o k w a s y
B i a ł k o g l o b u l a r n e : p r o t a m i n y n a l e ż ą c e d o p o l i p e p t y d ó w i b i a ł k a w ł a ś c i w e :
h i s t o n y , a l b u m i n y , g l o b u l i n y , p r o l a m i n y , g l u t e l i n y
B i a ł k o s i g m a : a k t y w i z u j e p r o c e s y R N A
B i l a n s e n e r g e t y c z n y c y k l u K r e b s a : 6 N A D H ; G T P ; F A D H 2
B i o t e c h n o l o g i c z n e d o s k o n a l e n i e ż y w n o ś c i o w o c u j e w y t w o r z e n i e m : G M O
B i o t y n a b i e r z e u d z i a ł w p r z e n o s z e n i u g r u p : k a r b o k s y l o w y c h
C e n t r u m a k t y w n e j e s t u t w o r z o n e z a m i n o k w a s ó w : p o ł o ż o n y c h w r ó ż n y c h
c z ę ś c i a c h ł a ń c u c h a p o l i p e p t y d o w e g o
C h o r o b o t w ó r c z e b i a ł k a n i s z c z ą c e m ó z g t o : p r i o n y
C h y m o t r y p s y n o g e n , t r y p s y n o g e n , p e p s y n o g e n - t o z y m o g e n y
C i a ł a k e t o n o w e p o w s t a j ą g d y : j e s t n a d m i a r a c e t y l o C o A
C o h y d r o l i z u j e β a m y l a z a : s k r o b i a
C o j e s t m a g a z y n o w a n e w a m y l o s o m a c h : s k r o b i a , a m i n o k w a s y n i e b i a ł k o w e
( b e t a a l a n i n a , o r n i t y n a , k w a s a m i n o m a s ł o w y , h y d r o k s y p r o l i n a ,
h y d r o k s y l i z y n a )
C o j e s t p r e k u r s o r e m d l a f o s f o l i p i d ó w : C D P - d i g l i c e r o l
C o j e s t s u b s t r a t e m g l u k o n e o g e n e z i e : p i r o g r o n i a n , m l e c z a n
C o k o d u j e 6 t r ó j e k : a r g i n i n a , s e r y n a , l e u c y n a , ( A R G , S E R , L E U )
C o k o d u j e w i ę c e j n i ż 3 t r ó j k i : s e r , l e u , a r g
C o m o ż e b y ć o p e r a t o r e m : b i a ł k o s t r u k t u r a l n e
C o o d p o w i a d a z a s p e c y f i c z n o ś ć e n z y m ó w : a p o e n z y m
C o o z n a c z a I I I c y f r a w k l a s y f i k a c j i e n z y m ó w : p o d p o d k l a s ę
C o p o w s t a j e w r e a k c j i k a t a l i z o w a n e j p r z e z l i a z ę z k w a r g i n i n o
b u r s z t y n o w e g o : a r g i n i n a + k w f u m a r o w y
C o p o w s t a j e w w y n i k u d z i a ł a n i a l i a z y i z o c y t r y n i a n o w e j n a i z o c y t r y n i a n -
b u r s z t y n i a n u : b u r s z t y n i a n , k w g l i o k s a l o w y
C o p o w s t a j e w w y n i k u r e a k c j i k a t a l i z o w a n e j p r z e z l i a z ę a r g i n i n o -
k w a r g i n o w y , k w b u r s z t y n o w y , a r g i n i n a , k w f u m a r o w y
C o p o w s t a j e z a c e t y l o C o A : m a l o n y l o C o A , k w t ł u s z c z o w e , a m i n o k w a s y ,
a m i n o k w a s y e k t o g e n i c z n e , 3 h y d r o k s y m e t y l o g l u t e n y l o C o A
C o p o w s t a n i e z a c e t y l o C o A w w y n i k u d z i a ł a n i a k a r b o k s y l a z y
a c e t y l o C o A : m a l o n y l o C o A , k w t ł u s z c z o w e , a m i n o k w a s y
C o s i ę d z i e j e g d y w z r a s t a s t ę ż e n i e e n z y m u : r e a k c j a u l e g a p r z y s p i e s z e n i u
C o t o j e s t a k t y w n o ś ć m o l e k u l a r n a : : l i c z b a o k r e ś l a j ą c a i l o ś ć m o l i s u b s t a n c j i ,
k t ó r a p r z e r e a g u j e z j e d n y m m o l e m e n z y m u w c i ą g u 1 m i n .
C o t o j e s t b i a ł k o z e i n a ? : b i a ł k o n a s i o n k u k u r y d z y , n i e z a w i e r a t r y p t o f a n u
C o t o j e s t d e l e c j a : 1 ) u b y t e k f r a g m e n t u n u k l e o t y d ó w , c z ę ś c i c h r o m o s o m ó w ;
2 ) u s u n i ę c i e j e d n e j z a s a d y z t r ó j k i k o d u g e n e t y c z n e g o , 3 ) u t r a t a p a r y
c h r o m o s o m ó w
c o t o j e s t g l u t a t i o n : t r i p e p t y d ( G l u - C y s - G l i )
Co to jest HOC-(CH
2 )7
-CH=CH-CH
2
-CH=CH (CH
2)4
COOH: kw linolowy
Co to jest katal: 1 katal odpowiada aktywności enzymu, która w ciągu 1s przekształca 1 mol substancji
w temp 30 st C przy optymalny pH stężeniu substratu
Co to jest kod genetyczny: układ zasad w DNA określający sekwencję aminokwasów w
syntetyzowanym łańcuchu polipeptydowym
Co to jest liczba obrotów enzymu: liczba określająca ilość moli substancji, która przereaguje z jednym
molem enzymu w ciągu 1 min.
Co to jest NADP: fosforan nukleotydu nikotynoamidoadeninowego
Co to jest plazmid: autonomiczna jednostka dziedziczna
Co to jest punkt izoelektryczny: 1) pH przy którym aminokwas wyst w formie jonu obojnaczego; 2) pH
przy którym aminokwas wypadkowy ma ładunek O, staje się jonem obojnaczym
Co to jest wysalanie: reakcja ze stężonym roztworem silnie dysocjowanej soli co powoduje wytrącanie
białka z roztworu bez utarty właściwości biologicznych i struktury.
Co to są aminokwasy : elementy strukturalne białek
Co to są kefaliny:fosfatydyloetanoloaminy
Co to są układy wieloenzymowe: multienzymy, skł się z kilku enzymów spełniających
wyspecjalizowane funkcje w 1 złożonej reakcji, nie uwalniają prod pośrednich
Co to za kwas COOH-(CH2)7-CH=CH—CH2-CH=CH(CH2)4-CH3-C16H1202: kwas linolowy
Co tworzy się gdy w kom jest nadmiar glukozy i ATP: skrobia i glikogen
Co zawiera FAD: ryboflawinę, Wit B2
Co zawiera FMN: ryboflawinę (Wit B2) i resztę ortofosforanową
Co zawiera kw pantotenowy: α γ dwuhydrolazy, ββ dwumetylomasłowy, β alanina
Co zawiera kwas pantelenowy: powstaje przez połączenie kwasu alfa i gamma
bihydroksybetadimetylomasłowego i beta alaniny połączonego wiązaniem peptydowym 2,4-
dihydroksy 3,3-dimetylomasłowy i 3 alaninę
Co zawierają ziarna aleuronowe: białko zapasowe, albuminy, globuliny
Cukier stosowany do celów spożywczych to: sacharoza
Cukrami redukującymi są-glukoza, fruktoza, mannoza, trioza, aldehyd glicerynowy.
Cukrowce różniące się konfiguracja wokół jednego C+ nazywamy: epimerami
Cukrowce trudniej dostępne dla człowieka to: lignina
Cukry redukujące to: maltoza, laktoza, celobioza, malibioza, izomaltoza, genojobioza
Cukry redukującymi są: glukoza, fruktoza, mannoza, trioza, aldehyd glicerynowy
Cukry złożone są z budowane z cukrów prostych połączonych wiązaniem glikozydowym utworzonym
pomiędzy: C1-C1;C1-C4; C1-C6
Cykl glioksalowy zużywa duże ilości : acetylo-CoA
Cykl ornitozy to: powstanie mocznika w wątrobie
Cykl ornitynowy(synteza mocznika) zachodzi w wątrobie
Cykl pentofosforanowy przebiega u zwierząt w cytoplazmie w: wątroba, gruczoł mlekowy
Cytochrom B: początek łańcucha oddechowego; Cytochrom b-> cytochrom c1-> cytochrom c-
>cytochroma i a3
Część niebiałkowa enzymu: koenzym, kofaktor, gr. prostetyczna
Czym różni się nukleotyd od nukleozydu: nukleozyd nie zawiera reszty fosforanowej
Czynnik redukcyjny powstaje w dużych ilościach na drodze: szlaku pentozafosforanowego i fotosyntezy
Czynnik redukcyjny powstaje w następujących procesach - fotosynteza, szlakpentozofosforanowy.
Czynnik redukujący z fosforylacji niecyklicznej redukuje Co
2
do: cukrów
Dehydrogenaza 6-fosfoglukonianowa katalizuje reakcję przekształcenia: 6-fosfoglukonian przekształca
się wrybozo-5 fosforan
Dehydrogenaza bursztynianowa ma: 17 izomerów
Dehydrogenaza mleczanowa drożdżowa: współdziała z FMNH
2
Dekarboksylacja oksydacyjna: pirogronian->acetyloCoA
Dla wytworzenia 1 kg masy mięśniowej zwierząt należy w pokarmie dostarczyć - 30mg fenyloalaniny;
30mg metioniny; 20 mg lizyny
Do aminokwasów egzogennych zaliczamy - walinę, leucynę, lizynę, histydynę.
Do aminokwasów rzadko występujących w białkach zaliczamy - cystynę i dermozynę.
Do czego odnosi się represja i indukcja: regulacja genetyczna-operon laktozowy
Do czego służy reakcja ninhydrynowa: do wykrywania gr α aminowych białek
Do jakich aminokwasów należą: walina, leucyna, izoleucyna: egzogenne
Do jakich związków odnosi się β oksydacja:kw tłuszczowe
Do utworzenia karbamoilofosforanu używanych jest: 2 ATP
Do wytworzenia cząsteczki glukozy w fotosyntezie potrzeba: 48 kwantów światła widzialnego
Duszenie bigosu w największym stopniu obniża zawartość witaminy: C
Działanie ureazy jest typowym przykładem specyficzności enzymów: absolutnej
Dzienne zapotrzebowanie człowieka na fenyloalanina:4,79; tryptofan:1,1; izoleucyna:3,7; leucyna: 12,6;
metionina: 4,1; treonina:3,6; tyrozyna:3,9, lizyna:5,2
Efekt energetyczny rozkładu glukozy do CO
2
: H
2
O- 683 kcal= 38ATP=2780kJ
Efekt Tyndala określa zjawisko - rozpraszania wiązki świetlnej.
Efekt Tyndala to: rozpraszania wiązki światła przy przejściu przez roztwór koloidalny
Enzym niezbędny do życia: karboksylazy rybulozo 1,5 bisfosforanu
Enzym o numerze E.C. 3.3.2.1. należy do klasy: hydrolazy
Enzym rozkładający nadtlenek wodoru: peroksydazy, katalazy
Enzym zwierzęcy: ketopsyn
Enzym, amoniakaliozaaspraginowa katalizuje: reakcje deaminacjiasparginianu do fumaranu
Enzymy są białkami: prostymi i złożonymi
Enzymy katalizujące reakcję bez udziału H
2
O: liazy
Enzymy o pH kwaśnym: pepsyna, karboksylaza pirogronianowa, kwaśna fosforowa
Enzymy umożliwiające rozcinanie DNA nazywamy - enzymami restrykcyjnymi.
Enzymy umożliwiające włączenie tlenu cząsteczkowego do jednego substratu: oksygenazy
Enzymy warunkujące życie na ziemi: karboksylaza, rybulozo 1,5 difosforan
Enzymy zwierzęce: ketopsyny
Fenyloalanina jest aminokwasem egzogennym dla zwierząt. Brak fenyloalaniny w komórkach w czasie
biosyntezy białek spowoduje (zaznacz najbardziej prawdopodobną odpowiedź): zahamowanie
biosyntezy wszystkich białek, w których składzie występuje fenyloalanina
Fosfatydyloseryny są zaliczane do grupy - fosfoglicerydów.
Fosforylacja substratowa w cyklu Krebsa: między sukcesyloCoA a bursztynianem/ powstaje ATP bez
udziału łańcucha oddechowego
Fosforylacja substratowa w glikolizie: 2 ATP
Fosforylazy należą do klasy: transferaz
Frakcje globuliny: alfa gliko i lipoproteiny
Funkcja biologiczna tRNA w komórce polega na: transporcie aktywnych aminokwasów na rybosany –
miejsce biosyntezy białka
Funkcje FAD to: przenoszenie protonów i elektronów, współdziałanie z reduktorami
Gdzie jest odszczepiana cząsteczka ATP w cyklu Krebsa (fosforylacja substratowa)- przy przejściu
sukcysyloCoA w bursztynian
Gdzie odbywa się wydłużanie łańcucha kw tłuszczowego- od 16 C w cytoplazmie , zasadniczo w
mitochondriom, acetylo Co-CoA
Gdzie powstaje pozamitochondrialny czynnik redukujący: cykl pentozo fosforanowym NADPH2,
powstaje w łańcuchu oddechowym w procesie, fosforylacji oksydacyjnej
Gdzie występuje wiązanie trio estrowe (bezwodnik): acetyloCoA
Gdzie zachodzi biosynteza białka: w rybosomach
Gdzie zachodzi biosynteza kw tłuszczowych: 7 enzymów – w cytoplazmie
Gdzie zachodzi cykl Krebsa: w matrix mitochondrialnym
Gdzie zachodzi łańcuch oddechowy: na wewnętrznej błonie mitochondriom
Gdzie zachodzi replikacja i transkrypcja: w jądrze komórkowym
Gdzie zachodzi synteza rRNA: w jąderku
Glikoliza to: kompleks 11 enzymów i 11 reakcji
Glutation to – 5-glutamylo-cysteinylo-glicyna; γ-glutamylocysteiloglicyna
Główna funkcją NAD
+
i NADP
+
jest współdziałanie z: dehydrogenazami
Główne zadania cyklu Krebsa: wytwarzanie protonów (H
+
) i elektronów na łańcuch oddechowy,
powstaje CO2 i 2 cząsteczki ATP
Głównym wielocukrem występującym w mięsie jest: glikogen
Głównym źródłem nienasyconych kwasów tłuszczowych są: tłuszcze roślinne
Głównymi cukrowcami w mleku są: glukoza, galaktoza i laktoza
Grupa prostetyczna enzymu pełni funkcję koenzymu, jeśli jest to: związek organiczny zdolny do
oddysocjowania od części białkowej
Grupę białek globularnych stanowią - albumina, globuliny, histony, prolaminy, gluteliny
Grupy funkcyjne tworzące wiązanie peptydowe to: aminowa i peptydowa
Hamowanie aktywności dehydrogenazy treoninowej jest przykładem mechanizmu -autoregulacji.
Heminy to: niebiałkowa część cytochromów
Hemoglobina składa się z : 4 podjednostek: 2 ciężkich i 2 lekkich
Hiperwitamonoza: nadmiar witamin
Hipowitaminoza to: niedobór witamin
Hydratazaakonitynowa katalizuje reakcję: izomeryzacji cytrynianu do izocytrynianu
Hydratazaenoilo-S-ACP uczestniczy w wytwarzaniu: Krotonylo-S-ACP
Hydrolazy nie wymagają współistnienia: koenzymów
Hydroliza podanego peptydu pod wpływem trypsynyendopeptydaza: tworzą krótkie łańcuchy
Hydrolizy to enzymy działające bez koenzymów
Hyrolazy: nie wymagają współistnienia koenzymów
Ile cząsteczek NH
3
bierze udział w obrocie jednego cyklu mocznikowego: 2NH
3
Ile cząstek alkoholu powstanie z 1 cz glukozy: 2 cząsteczki C
6
H
12
O
6
-> 2 C
2
H
5
+2CO
2
Ile enzymów bierze udział w syntezie kw tłuszczowego: 7
Ile fosforylacji substratowych wyst w glikolizie: 2
Ile fosforylacji substratowych występuje w cyklu Krebsa-1
Ile izomerów ma dehydrogenaza bursztynianowi – 17
Ile izomerów ma dehydrogenaza mleczanowa: 5 izomerów
Ile jest oksydazy w cyklu Krebsa: 1
Ile jest struktur białka: 5
Ile NH
3
bierze udział w jednym obrocie cyklu mocznikowego: 2 cząsteczki
Ile oksydacji substarowych występuje wystepuje podczas cyklu Krebsa : 1
Ile potrzeba zw do wytworzenia się 1kg masy mięśniowej: 6 związków: 30mg(fenyloalaniny, Metioniny,
Leucyny), 20mg(Lizyny); 14mg(Treoniny); 7mg(Tryptofan)
Ile procent wszystkich kwasów rybonukleinowych E.coli stanowi mRNA: 2
Ile procent wynosi wydajność rozkładu 1 cząsteczki glukozy w warunkach beztlenowych: 32,8%
Ile struktur opisuje budowę białek: 5
Inhibicja współzawodnicząca może być częściowo zniesiona przez: zwiększenie stężenia substratu
Inhibitor kompetencyjny dehydrogenazy bursztynianowej to: malonian
Insulina: cukry zapasowe fruktozan
Izoenzymy różnią się następującymi parametrami: wartością ładunku wartością KM specyficznością
substratową
Jaka reakcja jest katalizowana przez kinazę adenylową: reakcja fosforylacji ADP+ADP=ATP+AMP
Jaka reakcja ma bilans Δ6<1: endoeryfoz
Jaki enzym katalizuje przemianę aldehydu 3-fosfoglicynowego w 1,3-difosfoglicerynian: dehydrogenaza
aldehydu 3-fosfoglicerynowego
Jaki enzym katalizuje przemianę kw β fosfoliglicerynowego: aldehyd – fosfogliteromutaza,
dehydrogenaza aldehydu 3 fosfogliceryna
Jaki enzym katalizuje przemianę kwasu 3 policerynowego: fosfogliceromelaza dehydrogenaza aldehydu
3 fosfoglicerynowego
Jaki enzym katalizuje przeniesienie reszty ortofosforanowej z wydzieleniem ATP: kinaza
Jaki enzym katalizuje reakcję 3 fosfoglicerynian->2 fosfoglicerynian:fosfogliceromutaza
Jaki enzym katalizuje rozdzielanie DNA (helekaza):nukleotydylo transferaza DNA (enzym Kornberga)
Jaki enzym w cyklu Krebsa utlenia kw bursztynowy do kwfurmarowego: dehydrogenaza
bursztynianowi
Jaki roztwór powstaje w wyniku rozpadu białka w wodzie: koloidalny
Jaki związek jest inhibitorem kompetycyjnym dehydrogenazy bursztynianowej: HOOC-CHOH-CH2-COH
Jakich pierwiastków jest najwięcej w żywych organizmach: C, O, N, H – 99%
Jakie aminokwasy mają pierścienie aromatyczne: fenyloalanina, tyrozyna, tryptofan
Jakie aminokwasy mają pierścień endolowy: tryptofan
Jakie aminokwasy zawierają gr tiolowe: cysteina, glutation,
Jakie aminokwasy zawierają pierścień aromatyczny: fenyloalanina, tyrozyna, tryptofan
Jakie cukry należą do: triozaldehyd glicerynowy, dihydroksyaceton; pentoz- ksyloza, ryboza,
arabinoza; heksoz- galaktoza, fruktoza, mannoza, glukoza
Jakie są cukry redukujące zawierają grupę hemikatalową lub hemiacetylową: maltoza, melobioza,
celobioza, gemobioza, laktoza, izomaltoza
Jakie są inhibitory dla dehydrogenazy bursztynianowej: kw malonowy (malonian), szczawiooctowy ,
acetylooctan i fumaran
Jakie są inhibitory dla hydrogenazybursztynianowej: szczawian, szczawioocnat, malarian
Jakiego kw tłuszczowego jest najwięcej w smalcu tłuszczowym: kw oleinowy (stearynowego)
Jednostka kw nukleinowego: nukleotyd
Jeżeli w łańcuchu DNA adenina stanowi 20% zasad heterocyklicznych, to ile stanowi tymina- 20%.
Katepsyny: enzymy proteolityczne, wewnatrzkom i zwierzęce
Kodowanie jednego aminokwasu przez więcej niż jedną trójkę jest cechą kodu genetycznego określoną
jako: zwyrodnienie kodu
Koenzym F (kwas foliowy), witamina B
2
i witamina K wytwarzają: erytrocyty
Koenzym F, Wit B
6
i Wit H: wytwarzają krwinki czerwone
Koenzym NAD+ współdziała głownie z : dehydrogenazami
Koenzym: część niebiałkowa enzymu
Kofaktorem współdziałającym z α amylazą jest: C
1
-1
Kompleks dehydrogenazy pirogronianowej składa się: 3 enzymów i 5koenzymów
Kompleks syntetazy kwasów tłuszczowych tworzy - 7 enzymów.
Komplementarność zasad: A=T; G=C; A=U
Kto pierwszy użył terminu biochemia: 1903r. Neuberg;
Która witamina jest najbardziej zróżnicowana: H1
Która z reakcji jest katalizowana przez izomery: A-R-B+H20=A-B-R
Które aminokwasy zawierają peptyd 6IEDLCE : kwas glutaminowy, leucynę, izoleucynę, kwas
pioparaginowy, senjua cysteina
Które enzymy prosteolityczne są najczęściej stosowane w badaniu struktury białek: pepsyna, trypsyna,
karbopeptydaza.
Które reakcje mają bilans G < 0: egzoergiczne
Które reakcje mają bilans G < 1: endoergiczne
Które stwierdzenie jest prawdziwe: każdy koenzym jest gr prostetyczną
Którego kw RNA jest najwięcej: tRNA
Który aminokwas nie posiada stereo izomerów: beta alanina
Który aminokwas zawierają peptyd SIEDLCE: kwas glutaminowy, leucyna, izoleucyna, kwas
asparginowy, seryna, cysteina
Który produkt spożywczy zawiera najwięcej białka: mięso drobiowe (18-25); jajo kurze (12-13)
Który z kwasów nukleinowych jest najbardziej zróżnicowany: r-RNA
Kwas 3-fosfoglicerynowy pod wpływem fermentacji glicerynowej przechodzi w: kwas pirogronowy
Kwas amino lewulinowy występuje w: syntezie porfiryn
Kwas foliowy: (wit B9) wchodzi w skład CoF
Kwas karbamoilofosforanowy Jest produktem pośrednim podczas syntezy: nukleotydów
pirymidynowych
Kwas linolowy zawiera: witaminę G niezbędną dla rozwoju ssaków
Kwas linolowy zawiera: Wit F niezbędną do rozwoju ssaków
Kwas liponowy to: dwutiulowa pochodna kwasu oktanowego
Kwasy nukleinowe posiadają budowę: liniową
Kwasy tłuszczowe zawierają litofilną gr karboksylową lipofobną gr-> łańcuch węglowodorowy;
glikoprotaminy->krzępnięcie krwi
Kwasy uronowe powstają przez utlenienie OH przy węglu: najdalej oddalonym od węgla
anomerycznego
Malonian i szczawiooctan to inhibitorykompitycyjne: dehydrogenazy bursztynianowej
Maloninaszczawiooctan i acetylooctan to inhibitory : dehydrogenazy
Masa cząsteczkowa białka wynosi 30 000. Określić przybliżoną masę cząsteczkową odpowiedniego
mRNA (matrycowego dla tego białka): 270 000
Mechanizm biosyntezy okazaki? Jest związany z enzymem: ligazą DNA
Mechanizm represji dotyczy regulacji procesów - anabolicznych.
Mechanizm represji reguluje: anabolizm
Metionina to: aminokwas siarkowy egzogenny
Metionina: aminokwas egzogenny, niepolarny
Miejscem wiązania substratu z enzymem jest: centrum aktywne
Najmniejsza różnica potencjałów pomiędzy dwoma układami przy przenoszeniu elektronów powinna
wynosić: ok. 0,17r
Najpopularniejszy enzym deaminacji: dehydrogenaza glukaminowa
Najważniejszym enzymem podczas transportu aktywnego jest: ATP-aza Na
+
/K
+
Najważniejszym enzymem warunkującym istnienie życia jest: karboksylaza rybulozo-1,5 difosforanowa
(cykl Calvina)
Najwięcej błonnika pokarmowego występuje w: kaszach jęczmiennych
Najwięcej kwasów tłuszczowych wielonienasyconych zawierają oleje: lniany i słonecznikowy
Najwięcej nasyconych kwasów tłuszczowych występuje w: smalcu wieprzowym
Najwięcej w litosferze znajduje się: tlenu
Największa ilość energii jest uwalniana w reakcji - ATP+H20->AMP+PPn. (hydrolizy ATP)
Największa zmiana potencjału w łańcuchu oddechowym jest między: cytochromem a3 a tlenem
Największy spadek potencjału oksydacyjnego na drodze łańcucha oddechowego wystepuje podczas
przekazywania protonów i elektronów : Cyta
3
(Fe
2+
)O
2
Największy udział w budowie biomolekułposiadaja: O,,C N, H
Nauka o enzymach: enzymologia
Nukleotydy flawinowe są spokrewnione z: witaminą B2
O ile rośnie potencjał w łańcuchu oddechowym: 0, 16V
Obliczyć ilość energii w cząst. ATP z przemiany acetylo-CoA w cyklu Krebsa i łańcuchu oddechowym.:
Cykl Krebsa + łańcuch oddechowy (1x acetylo- CoA - 2x CO2) : 1 GTP = 1ATP;; 1 FADH
2
= 1,5 ATP; 3
NADH = 7,5 ATP; RAZEM = 10 ATP
Obliczyć zysk energetyczny powstający w wyniku całkowitego rozkładu kwasy:
a)
Kwas palmitynowy: zawiera 16 C;
Spirala β-oksydacji= utlenianie FAD
2
7x1x1,5=10,5 ATP
=utlenianie NADH= 7x1x2,5= 17,5ATP
Cykl Krebsa= fosforylacja substratowa 8x1=8 ATP
= fosforylacja oksydacyjna 8x9=72ATP
Zysk brutto = 108ATP
Aktywacja palmitylko-CoA= -2ATP
Zysk netto=106ATP
Kwas stearynowy: 120ATP (zawiera 18C)
Kwas laurynowy: 72 ATP (zawiera 12C)
Kwas mistyrynowy: 92 ATP (zawiera 14C)
Obniżenie świeżości mięsa skutkuje: wzrostem aktywności procesów katabolicznych
Oddychanie tlenowe dostarcza: 15 krotnie więcej energii niż fermentacja
Oksydaza cytochromowa skł się z: cytochromu a
3
Oksydazy to enzymy katalizujące reakcję: przenoszenia tlenu z nadtlenków na różne akceptory
Oleje schnące to: słonecznikowy i lniany
Optimum pH dla większości enzymów mieści się w granicach: 6-9
Optymalne pH dla α amylazy: pH=6,8
Optymalne pH dla: pepsyny 1; mioglobiny 7; hemoglobiny 7.07; cytochromu 9.5
Ostatni przenośnik H: koenzym Q
Peptyd o nazwie SIEDLCE zawiera:serynę, izoleucynę, leucynę, kw asparginowy, kwas glutaminowy,
cysteinę
Pirogronian i mleczan to: najlepsi prekursorzy glukoneogenezy
Pirogronian jest przekształcany w acetyloCoA jeżeli w kom. występuje zapotrzebowaniena: metabolity
CTK i biosyntezę kwasów tłuszczowych.
Podaj substraty dla danych enzymów: β-fruktofuranozydaza-skrobia; uraza-mocznik; αamylaza-skrobia
Podczas fermentacji alkoholowej u glukozy jest rozkładana do: 2 cząsteczek etanolu
Podczas rozkładu cząsteczek glukozy w warunkach aerobowych organizmu uzyskuje w porównaniu do
warunków anaerobowych : około 14,5-raza więcej energii
Podstawowym intermediatem podczas biosyntezy fosfolipidów jest: CDP –acetodiaglicerol
Podstawowymi wiązaniami chemicznymi występującymi w strukturze III-rzędowej białka są: siarczkowe,
estrowe, typu soli wewnętrznych oraz działania hydrofobowe
Podwójne wiązanie w kw tłuszczowych nienasyconych: dehydrogenazy
Podział aminokwasów na kwaśne, zasadowe i obojętne związany jest z: właściwościami
elektorforetycznymi
Poniższą reakcję katalizuje - dehydrogenaza izocytrynianowa.
Poniższą reakcję katalizuje -fosfoglicerolomaltaza. (3-fosfoglicerynian->2-fosfoglicerynian)
Pól białko złożone: metalo-, chromo-, gliko-, lipo-, fosfo-, nukleo-, hemo- proteiny
Prekursorem wszystkich fosfoglicerydów jest - CDP-diaglicerol.
Prekursorem związków aromatycznych jest: kwas benzoesowy
Priony to białka wywołujące chorobę - Creutzfelda-jacoba.
Proces biosyntezy białka rozpoczyna się do: N-formylometioniny
Proces biosyntezy kwasów tłuszczowych przebiega w - cytoplazmie.
Proces glikolizy przebiega w: cytoplazmie
Proces tłumaczenia informacji genetycznej zawartej w mRNA na język aminokwasów: translacja
Proces w którym następuje redukcja i synteza CO
2
:cykl Calvina Bens (CO
2
+1,5 rybulozobisfosforan)
Rrubisco
Produktami dehydrogenazy izocytrynianowej są: kwas α-ketoglutarowy i dwutlenek węgla
Produktami reakcji transami nacji: α-ketokwas i aminokwas
Produktami reakcji z udziałem liazy argininobursztynianowej są: arginina i kwas fumarowy
Produktami szlaku pentozo fosforanowego są: 6 cząstek CO
2
i 2 czast triozo fosforanu
Produktem działania karbamoilotransferazyornitynowej jest: cytrulina
Produktem działania ornitozy choryzmanowej jest: kwas prefenowy
Protaminy to: białka globularne (należą do polipeptydów), białka proste
Przekształcenie treoniny w izoleucynę stanowi doskonały przykład mechanizmu: autoregulacji
metabolizmu komórkowego
Przepisywanie informacji z mRNA na język aminokwasów: translacja
Przykładem białka o strukturze 4-rzędowej jest: hemoglobina
Pula AcetyloCoA: ciała ketonowe, cholesterol, amidy tłuszczowe
Reakcja ATP+H
2
OAMP+PPntowarzyszy G
o
równa 8kcl/mol
Reakcja ATP+H
2
OAMP+PPn towarzyszy ΔG
o
: 7,3 kcal
Reakcja glikogen->glukozo-1-fosforan katalizuje: fosforylaza
Reakcja najbardziej energetyczna: ATP+H
2
O->AMP+PPi+800kcal
Reakcja ninhydrynowa jest przykładem - reakcji na wykrywanie grup a-aminowych aminokwasów.
Reakcja ninhydrynowa: wykrycie grupy tiaminowej w białkach
Reakcja odszczepienia kreślonej grupy z utworzeniem wiązania podwójnego katalizują: liazy
Reakcja z rezorcyną służy do wykrywania- ketoz (odczynnik Seliwanowa)
Reakcje chemiczne w których wytwarzany jest ATP nazywamy - fosforyzacjami.
Reakcje katalizowane przez koenzym A: reakcja kw karboksylowych, biosynteza kw tłuszczowych, cykl
Krebsa, β oksydacji
Reakcję 2 H
2
O
2
-> 2H
2
O+O
2
jest katalizowana przez: katalazę
Reakcję H2C03 -> C02+H20 katalizuje: anhydroza węglanowa
Reakcję przemiany aldozy w ketozę katalizują: izomerazy
Regulator w glikolizie to: fosfofruktokinaza
Reowirusy RNA: dwuniciowy
Represja i indukcja to mechanizmy regulacji – wewnątrz kom. syntezy białek enzymatycznych.
Równanie glikolizy:glukoza+2ADP+2Pn+2NAD
+
-> 2 pirogronian+ 2ATP+ 2NADH + 2H
+
+ 2H2O(jest
egzoergiczna)
Równanie glukoneogenezy: 2 pirogronian+ 4 ATP+ 2GTP+2NADH +2H
+
+6H20-> glukoza +2NAD
+
+ 2H
+
+
4ADP + 2GDP + 6Pn(jest endogernicza)
Ruchomy zasób białek w organizmie zwierzęcym to: ruchliwa metaboliczna cześć strukturalnych białek
komórkowych
Sekwencję aminokwasów insuliny określił: Singer 1955r.
Skład pierwiastkowy aminokwasów: C, O, N, H, S
Skład wosku pszczelego: z alkoholi: C16-cetylowy; C26-cerylowy; C30-mirycylowy; C31-melisylowy
Skrobia jest hydrolizowana do maltozy i izomaltozy przez: β-amylazę i izoamylazę
Skrót TLC oznacza: chromatografie cienkokomorkową lub kolumnową
Smalec wieprzowy zawiera w największych ilościach kwas - oleinowy.
Spalanie w butli fotometrycznej daje: 1g białka: 17,6 kJ i 0,47g H
2
O; 1g węglowodanów- 23,4 kJ i 0,55g
H
2
O; 1g tłuszczu: 38,4g kJ i 1,07 H
2
O
Spirala β-oksydacji to - utlenianie kwasów tłuszczowych.
Stała MichaelisaKm=ISI Km+ISI=215 stężenie substratu M/dm
3
Stosunek A+C:T+G w cząsteczce DNA jest równy: 1
Stosunek wydzielanego Co2 do pobranego O2 nazywa się współczynnikiem oddechowym (WO).
Współczynnik WO dla glukozy jest równy: 1.0
Struktura II rzędowa białek – śruba prawoskrętna: α heliks; śruba lewoskrętna ustabilizowana wiązań
wodorowymi
Synteza glikogenu ma miejsce, gdy w kom. wyst. - nadmiar glukozo-6-P i ATP.
Synteza karbamoilofosforanowazuzywa: 2 czasteczki ATP
Synteza łańcucha polipeptydowego: N do C końca
Synteza RNA jest zlokalizowana w - jąderku.
Szalak Estera-Dandrofa pełni podobne funkcje jak : szlak pentozofosforanowy albo ma podobne
znaczenie jak cykl Krebsa
Szlak metaboliczny to przemiana w której: substrat jest przekształcany w produkt na drodze kolejnych
reakcji
Teoria fragm. Okuzaki-enzymy: prymasa, polimeraza RNA, DNA, ligazy, egzo-
Teoria Koshlanda to: teoria indukcyjnego dopasowania enzymu i substratu
Teoria pułapki wyjaśnia mechanizm katalizy - hydrolaz.
Teoria pułapki: działanie enzymu
Tioliza: to rozpad 3-oksoacylu pod wpływem 3-oksoliolazy z udziałem 2 cząstek CoA
Tłuszcze pochodzenia zwierzęcego. Jako źródła energii mogą być zastąpione przez: cukrowce
Tłuszcze zmagazynowane w zwierzęcej tkance tłuszczowej stanowią podstawowe źródło: energii
trypsyna łączy:Arginina, lizyna
Trypsyna rozbija wiązania: Arg, cys
Tworzenie glukozy z CO
2
i H
2
O wynosi 2870 kJ (686kcal)= 30%
Typowym enzymem wykazującym optimum w zakresie pH zasadowym jest arginina; arginaza
U bakterii substancje zapasowe są transportowane w postaci: estrów fosforanowych
Ubichinon: koenzym Q w mitochondriom COQH
2
Układy wieloenzymowe to - enzymy tworzące ciągi reakcji następczych.
Ureaza należy do klasy enzymów (podaj nr i nazwę klasy): hydrolazy; 3 klasa
Ureaza wykazuje specyficzność: absolutną
W wyniku denaturacji białka zostaje zniszczona struktura: 2 i 3 rzędowa
W białkach zwierząt występują wyłącznie konfiguracje w konfiguracji: α
W celu klasyfikacji enzymu podać: nazwę, kod, reakcję, pochodzenie enzymu
W celu poprawnego określenia enzymu należy podać: 4 cyfrowy kod, nazwę systemową, kod i
katalizowaną reakcję.
W glikogenezie omijane są reakcje: przekształcenie pirogronianu w fosfoenolopirogronian,
przekształcenie fruktozo-1-6difosforab w fruktozo-6-P, przekształcenie glukozo-6-P w glukozę
W glikoneogenezie nieodwracalna jest reakcja: przeniesienie fosforanu z fosfornolopirogronianu
napad a więc powstanie kw pirogronowego
W glukoneogenezie omija się reakcje: pirogronian – fosfoendopirogronian PEP 1,6 biofosfofruktozy- 6
fosf. frukto 6 glukozo (P)-glukoza
W jakich granicach mieści się pH aminokwasów: 2,5 – 11
W kodzie genetycznym 6 trójek koduje: argininę
W którym z poniższych wosków występuje agnosterol - lanolina.
W lokalizacji i mapowaniu genów ważną rolę odgrywają: restrykcyjne endonukleazy
W łańcuchu oddechowym ATP powstaje w trzech miejscach: między NADPH+H
+
i FADH
2
; cytochromem
C i B, oksydaza cytochromowi i tlen
W łańcuchu oddechowym potencjał przy przechodzeniu e
-
: wzrasta
W łańcuchu oddechowym potencjał wzrasta: 0,16 do 0,179 V
W organizmie zwierzęcym, w warunkach niedoboru tlenu, glukoza ulega fermentacji do kwasu
mlekowego, natomiast nigdy nie fermentuje do alkoholu etylowego z powodu braku: dekarboksylazy
pirogronianowej
W roku 2003 nagrodę nobla przyznano za zastosowanie badań –chromatografugazowego.
W skład puli metabolicznej acetylo-CoA wchodzą: aminokwasy ektogeniczne, pirogronian, 3-hydroksy-
3-metylko-glicerylo CoA
W skład RNA wchodzą zasady azotowe: guanina, uracyl, cytozyna, adenina
W skład sfingomieliny wchodzi: sfingozyna, kw tłuszczowy, kwlignocerynowy, fosforan choliny
W tRNA wyróżniamy: 61 rodzajów
W wyniku działania aldolazy fruktodifosforanowej powstają: aldehyd 3-fosfoglicerynowy i
fosfodihydroksyaldolaza
W wyniku działania aldozy fuktodifosforanowej powstają: aldehyd 3-fosfoglicerynowy i
fosfodihydroksyaceton
W wyniku fermentacji powstało 23g etanolu. Ile glukozy zużyto C
6
H
12
O
6
->2C
2
H
5
OH+2CO
2
W wyniku fosforylacji substratowej w cyklu Krebsa powstaje 1 cząsteczka ATP na etapie przekształcenia:
bursztynylo-CoA w bursztynian
W wyniku hydrolizy di cukru powstaje α glukopiranoza i β-galaktopiranoza. Di cukrem jest: laktoza
W wyniku mutacji polegającej na zmianie jednej zasady w triplecie gen: jest źródłem zmienionej
informacji genetycznej
W wyniku rozkładu cząsteczki glukozy powstaje - 2 cz etanolu.
W wyniku transminacji powstaje: aminokwasy i alfa keto kwasy
Wartości punktów izoelektrycznych cysteiny i tyrozyny są w zakresie pH: kwaśnego
Wartość G<0 dla reakcji - egzoergicznych.
Wartość G>0 jest dla reakcji: endoergicznych
Wartość pH cysteiny i tyrozyny są w zakresie ph: kwaśnego
Wellecja: ubytek pary chromosomów
Wiązania stabilizujące III rzędowe stukturę białek : wodorowe, jonowe, estrowe, trioestrowe,
disiarczkowe
Wiązania stabilizujące struktury białek to –I rzędowe- peptydowe; II rzędowe- wodorowe, III rzędowe-
wodorowe, jonowe, estrowe, trio estrowe, di siarkowe, sił Van Der Walsa; IV rzędowe:
dwusiarczkowe, kleszczowe, sił Van Der Walsa
Wiązanie bezwodnikowe fosforowo- fosforanowe: występuje w ATP
Wiązanie C02 i jego redukcję nazywamy - cyklem Calvina.
Wiązanie pomocnicze w białkach: wodorowe, peptydowe, siarkowe,
Wiązaniem makroergicznym nazywamy wiązanie, podczas hydrolizy którego wydzielana energia równa
co najmniej:24J
Witamina B
12:
cyjanokobalamina (zaw. Kobalt)
Witamina H: biotyna (pochodna moczniku)
Witamina PP (kwas nikotynowy): część składowa NAD
+
i NADP
+
Właściwości redukujące cukrów są uwarunkowane: obecnością półacetylowej grupy OH przy węglu C,
lub C2
Wosk pszczeli: kwas palmitynowy, ceratynowy, melizynowy i alkohole
Wśród tRNA wyróżniamy: 60 rodzajów
Wydajność egzegetyczna procesu fosforylacji oksydacyjnej wynosi: 60%
Wydajność energetyczna procesu glikolizy wynosi: 32%
Wydajność energetyczna procesu glukozy wynosi 32,8A
Wydajność łańcucha oddechowego wynosi: 40 %
Wydajność łańcucha oddechowego: 38 ATP
Wydzielanie w cyklu Krebsa dwie cząsteczki CO2 przechodzą z: szczawianuoctanu
Wymień białka tkanki mięśniowej: miogeny, globulina, miozyna, aktyna, kolagen
Wysoka aktywność hydrolaz występuje : sferosomach
Występujące w białku dwie formy struktury II-rzędowej różnią się od siebie: liczbą łańcuchów
Wytworzeniu jednego wiązania fosforanowego na drodze łańcucha oddechowego towarzyszy wzrost
potencjału oksydoredukcyjnego o : 0,16.
Wzory kw tłuszczowych i zysk ich utleniania: C
14
H
28
O
2
mirystynowy 113ATP; C
16
H
32
O
2
pulmitynowy130
ATP
Wzrost stężenia enzymu powoduje - wprost proporcjonalny przyrost reakcjienzymatycznej.
Z czego składa się lanolina: kw tłuszczowy, lanosterol, agnosterol
Z czego wywodzą się gibereliny: z kwmewalonowego
Z ilu enzymów składa się kompleks β oksydacji: 25 enzymów
Z jakich pierwiastków zbudowane są aminokwasy: C, O, H, N, S
Z podanych cukrów prostych do aldoz należą: aldehyd glicerynowy, erytroza i ryboza, mannoza,
glukoza
Z przedstawionych par cukrów epimerami są: glukoza-mannoza
Za co odpowiada sekwencja ułożenia aminokwasów: I rzęd., struktura białka
Za specyficzność substratowa enzymu odpowiada - apoenzym.
Zasady komplementarne to: A=T, C=G
Zdolność przenoszeniaelektronównatlen cząsteczkowy mają:cytochromy a i a
1
Ziarna aleuronowe magazynują - białka zapasowe.
Zymogeny trzustkowe to: trypsynogen, chymotrypsynogen, proelstaza, prokarboksypeptyd
Zysk energetyczny dla kwasu stearynowego:147 ATP
Zysk energetyczny dla rozkładu kw nienasyconych : kwmirystynowy – 113
Zysk energetyczny powstający w wyniku całkowitego rozkładu cząsteczki kwasumirystynowego - 108 cz
ATP
Zysk energetyczny z całkowietego rozpadu kw. kaprynowego wynosi: 64 cząsteczki ATP
Zysk energetyczny z rozpadu kw. kaprynowego wynosi: 79ATP (jest to kw 9-C)
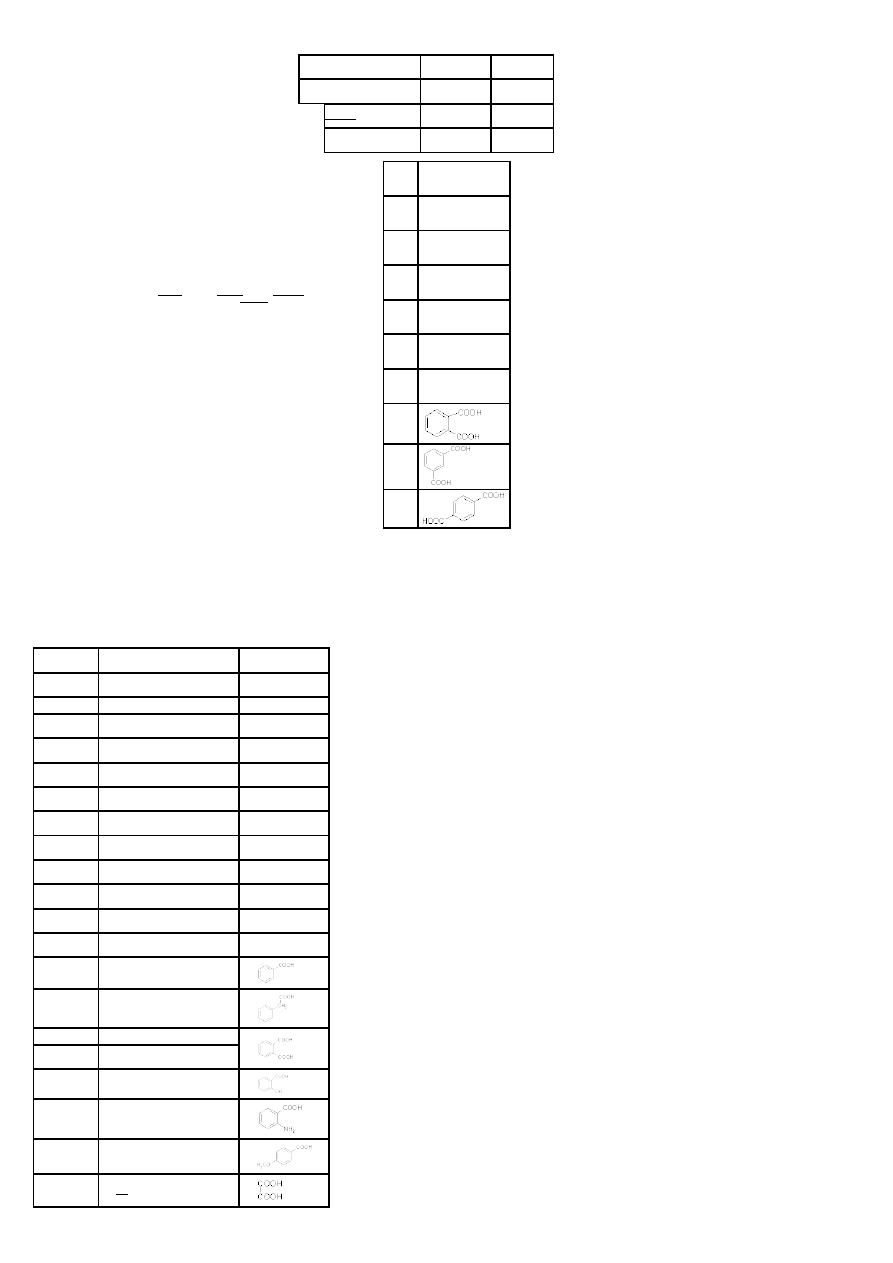
nazwa
zwyczajowa
nazwa systematyczna
wzór chemiczny
kwas
mrówkowy
kwas metanowy
H–COOH - kwas i
aldehyd jednocześnie!
kwas octowy
kwas etanowy
CH
3
COOH
kwas
propionowy
kwas propanowy
C
2
H
5
COOH
kwas
masłowy
kwas butanowy
C
3
H
7
COOH
kwas
walerianowy
kwas pentanowy
C
4
H
9
COOH
kwas
laurynowy
kwas dodekanowy
C
11
H
23
COOH
kwas
mirystynowy
kwas tetradekanowy
C
13
H
27
COOH
kwas
palmitynowy
kwas heksadekanowy
C
15
H
31
COOH
kwas
stearynowy
kwas oktadekanowy
C
17
H
35
COOH
kwas
oleinowy
kwas cis-9-oktadecenowy
C
17
H
33
COOH
kwas
linolowy
kwas cis, cis-9,12-oktadekadienowy
C
17
H
31
COOH
kwas
linolenowy
kwascis, cis, cis-9,12,15-oktadekatrienowy
C
17
H
29
COOH
kwas
benzoesowy
kwas fenylokarboksylowy
kwas
fenylooctowy
kwas fenylometanowy
kwas ftalowy
kwas o-benzenodikarboksylowy
kwas
izoftalowy
kwas m-benzenodikarboksylowy
kwas
salicylowy
kwas o-hydroksybenzoesowy
kwas
antranilowy
kwas o-aminobenzoesowy
kwas
anyżowy
kwas p-metoksybenzoesowy
kwas
szczawiowy
kwas malonowy
kwas
metanodikarboksylowy
kwas bursztynowy
kwas etano-1,2-
dikarboksylowy
1,2-
dihydroksydikarboksylowy
kwas węglowy
[H
2
CO
3
]
szczawiowy HOOC–COOH
malonowy
HOOC–CH
2
–COOH
bursztynowy HOOC–CH
2
–CH
2
–COOH
glutarowy
HOOC–CH
2
–CH
2
–CH
2
–COOH
adypinowy
HOOC–CH
2
–CH
2
–CH
2
–CH
2
–COOH
maleinowy
HOOC–CH=CH–COOH (cis)
fumarowy
HOOC–CH=CH–COOH (trans)
ftalowy
izoftalowy
tereftalowy
Wyszukiwarka
Podobne podstrony:
konta egzaminacyjne id 246765 Nieznany
algetra EGZAMINY id 57432 Nieznany
biochemia kolo id 86264 Nieznany (2)
ephl egzamin id 162318 Nieznany
Pisma Janowe egzamin id 359103 Nieznany
egzamin 2 id 153541 Nieznany
Biotechnologia egzamin id 89038 Nieznany
chemia fizyczna egzamin id 1122 Nieznany
logika egzamin id 272077 Nieznany
Na egzamin id 312078 Nieznany
biochemia egzam1 id 86330 Nieznany
konsta egzamin1 id 246146 Nieznany
Cw 2 Biochemia OS id 121642 Nieznany
CHEMIA EGZAMIN 2 id 112139 Nieznany
Na egzamin 2 id 312084 Nieznany
ped egzamin id 353250 Nieznany
Egzamin id 151498 Nieznany
BOF egzamin id 91316 Nieznany
więcej podobnych podstron