
ANTYGENY ZGODNOŚCI
TKANKOWEJ I
PODSTAWOWE
PROBLEMY
TRANSPLANTOLOGII

IMMUNOLOGIA - badanie
zjawisk odpornościowych
• Odporność dzieli się na
wrodzoną,
czyli
nieswoistą
lub naturalną i na
nabytą
czyli
swoistą
• Odporność
swoista
powstaje na skutek
zetknięcia się ustroju z antygenem
( pierwszy kontakt z antygenem daje
zdolność do reakcji wtórnej z tym samym
antygenem)
• Odporność
wrodzona
jest nieswoista i nie
ma pamięci immunologicznej

DOPEŁNIACZ
• Grupa ponad dwudziestu różnych
białek enzymatycznych
• Występują one w krążeniu w postaci
proenzymów, których właściwości
biologiczne ujawniają się po aktywacji
• Składniki dopełniacza są syntetyzowane
przez różne komórki (nabłonek jelit,
makrofagi, komórki tuczne)

SKŁADNIKI UKŁADU ODPORNOŚCIOWEGO –
CZĄSTECZKI BIOLOGICZNIE CZYNNE
• IMMUNOGLOBULINY
• ANTYGENY HLA
MEDIATORY REAKCJI IMMUNOLOGICZNYCH
(cytokiny-zdolność
zmiany ekspresji genów w komórkach docelowych i
wpływ na syntezę RNA
• INTERLEUKINY
• CZYNNIK MARTWICY NOWOTWORU
• CZYNNIK WZROSTU
KOMÓRKI UKŁADU IMMUNOLOGICZNEDGO
• LIMFOCYTY
• KOMÓRKI DENDRYTYCZNE
• MAKROFAGI
INNE KOMÓRKI
GRANULOCYTY
KOMÓRKI TUCZNE

Limfocyty
• Powstają w szpiku kostnym z
niezróżnicowanych komórek pnia
• W grasicy różnicują się limfocyty T
w szpiku limfocyty B

Komórki dendrytyczne
• Występują w zrębie węzłów i
grudek limfatycznych, błonach
śluzowych, skórze i tkance łącznej
większości narządów
• Prezentują antygen limfocytom
pomocniczym

Makrofagi
• Wywodzą się ze szpiku kostnego
• Prekursory makrofagów krążące we
krwi to monocyty(komórki
jednojądrzaste)
• Występują w wątrobie, płucach, CUN, w
śledzionie, skórze i jamach surowiczych
• Neutralizują antygeny, niszczą
drobnoustroje
• Prezentują antygeny komórkom

GRANULOCYTY
• Powstają w szpiku kostnym
Trzy rodzaje komórek
• neutrofile - obojętnochłonne
• Eozynofile - kwasochłonne
• Bazofile - zasadochłonne

Komórki tuczne
• Mastocyt, komórka tkanki łącznej i
błon śłuzowych

Układ immunologiczny
• Układ immunologiczny jest
identyfikowany anatomiczne z
układem chłonnym.
• U człowieka ważną rolę w
indukowaniu odporności
odgrywają struktury nie zaliczane
do tkanki chłonnej jak szpik czy
skóra.

Układ immunologiczny
• Układ chłonny zbudowany jest z narządów
ośrodkowych, obwodowych i naczyń chłonnych.
• W ośrodkowych narządach chłonnych zachodzi
namnażanie, różnicowanie i nabywanie
kompetencji immunologicznej zdolność
rozpoznawania i reagowania na określony
antygen)
• Komórki układu immunologicznego (limfocyty,
makrofagi i komórki dendrytyczne) pochodzą z
prekursorów występujących w szpiku
• U ludzi dojrzewanie limfocytów B zachodzi w
szpiku, a limfocytów T w grasicy

GRASICA-narząd
ośrodkowy
• Zbudowana z części korowej i rdzennej
• Prekursory limfocytów T (w grasicy
noszą nazwę tymocytów) zasiedlają
korę grasicy, gdzie proliferują i
różnicują się i wydostają się
naczyniami chłonnymi i krwionośnymi
na obwód

OBWODOWE NARZĄDY CHŁONNE
•
Węzły chłonne
(miejsce namnażania limfocytów i
tworzenia przeciwciał)
•
Śledziona
– w miazdze białej część grasiczozależną
z limfocytami T i obwodowo położona część
grasiczoniezależna z limfocytami B (pierwotne
grudki chłonne). Śledziona jest powiązana z
układem krwionośnym i jest głównym ośrodkiem
syntezy przeciwciał gdy antygen przenika do krwi
•
Migdałki
i
grudki chłonne
(pojedyncze i skupione)

SWOISTE REAKCJE USTROJU NA
CZYNNIKI INFEKCYJNE
•
Odpowiedź humoralna
- zniszczenie obcych
cząsteczek występujących w stanie wolnym
(pozakomórkowym). Główna rolę odgrywają
przeciwciała
•
Odpowiedź komórkowa
-uruchamia się gdy
drobnoustroje
pasożytują we wnętrzu komórek
•
Nadwrażliwość typu późnego
-uruchomiona w
przypadku gdy patogen nie indukuje ekspresji obcych
antygenów na powierzchni komórek w których
pasożytuje. Limfocyty w niej uczestniczące wydzielają
substancje niszczące zakażoną komórkę

Immunoglobuliny
(przeciwciała)
• Najważniejsze cząsteczki układu
immunologicznego - biorą udział w
odpowiedzi typu humoralnego
• Produkowane przez plazmocyty
• Należą do frakcji gamma-globulin
osocza krwi

immunoglobuliny
• 5 klas
– IgM, IgA, IgG, IgD, IgE
• Budowa
• Cztery łańcuchy polipeptydowe
• 2 lekkie L i 2 ciężkie H
• O klasyfikacji immunoglobulin decyduje
swoistość łańcuchów
ciężkich
alfa - α, gamma – γ , epsilon – ε
mi - μ, delta- δ ,
I lekkich
kappa – κ, lambda - λ

immunoglobuliny
• Budowa łańcucha immunoglobulin
• Część zmienna V, posiadająca wolne
grupy aminowe jest odpowiedzialna
za wiązanie antygenów
• Część stała C, na końcach posiada
grupy karboksylowe
(odpowiedzialne za funkcje
efektorowe )

Funkcje immunoglobulin
• Ig G
- uczestniczy w odpowiedzi
immunologicznej w infekcjach bakteryjnych i
wirusowych, przenika przez łożysko, wiąże
dopełniacz, wzmaga fagocytozę
• IgM
- uczestniczy w początkowej fazie
odpowiedzi immunologicznej, wiąże
dopełniacz, jest pierwszą immunoglobuliną
produkowaną w życiu płodowym człowieka od
6 miesiąca życia)

• IgA
-znajduje się przeważnie na powierzchni
błon śluzowych , wiąże antygeny wirusowe,
jest najważniejszym przeciwciałem w mleku
matek karmiących, występuje w łzach , ślinie i
wydzielinach
• IgD
– indukuje dojrzewanie przeciwciał
• IgE
– uczestniczy w reakcjach alergicznych i
atopowych, łączy się z komórkami tucznymi i
bazofilami,monocytami eozynofilami i
neutrofilami

GENY KONTROLUJĄCE SYNTEZĘ
IMMUNOGLOBULIN
• Geny znajdują się w trzech różnych,
autosomalnych loci
• Geny dla
łańcucha lekkiego
Lambda - chromosom 22 (22q11)
Kappa - chromosom 2 (2p12)
łańcucha ciężkiego
– chromosom 14 ( 14q32)

• Część zmienna łańcucha lekkiego
jest kodowana przez dwa rodzaje
genów : geny odpowiedzialne za
syntezę części zmiennych V i geny
odpowiedzialne za syntezę części
łączących J
• Część zmienną łańcucha ciężkiego
kodują trzy rodzaje genów V,D i J

GŁÓWNY UKŁAD ZGODNOŚCI
TKANKOWEJ
Główny układ zgodności tkankowej (Major
Histocompatibility Complex-MHC) odkryto przy
okazji
badań
dotyczących
odrzucania
przeszczepów
skóry
u
myszy.
Antygeny
odpowiedzialne za odrzucanie przeszczepu
allogenicznego
nazwano
antygenami
transplantacyjnymi lub antygenami zgodności
tkankowej.
Zespół
kodujących
je
genów
określono
jako
główny
układ
zgodności
tkankowej w odróżnieniu od genów kodujących
„słabe” antygeny zgodności tkankowej.
• pojęcie MHC wprowadził w 1956 roku G.D.
Snell
• w 1980 roku J. Dausset, G.D. Snell oraz B.
Benacerraf
otrzymali nagrodę Nobla za badania nad MHC

MHC I JEGO BIOLOGICZNE FUNKCJE
Do najważniejszych funkcji kontrolowanych przez
MHC należą, m.in.:
• wiązanie i prezentowanie antygenów limfocytom T
oraz inicjacja odpowiedzi immunologicznej
• odrzucanie przeszczepów
• reakcja przeszczepu przeciw gospodarzowi (GvHR)
• stymulacja limfocytów w mieszanej hodowli MLR
• regulacja poziomu niektórych składowych
komplementu, C2, C4, czynnik B oraz properdyna

GENY KOMPLEKSU MHC (HLA) U
CZŁOWIEKA
• układ HLA obejmuje ponad 100 genów
charakteryzujących się znacznym
polimorfizmem
• zlokalizowany jest na chromosomie 6p21.3
(geny sprzężone)
• obszar HLA podzielony jest na następujące
regiony:
region klasy I, II i III.

REGION KLASY I
• region ten obejmuje geny B, C, A, które kodują
łańcuchy ciężkie (α) antygenów klasy I
• łańcuch ciężki kodowany jest przez 8 eksonów.
Ekson pierwszy koduje sekwencję sygnałową-
usuwaną jeszcze w obrębie siateczki
śródplazmatycznej, drugi do czwartego-kodują
domeny od α1 do α3, a piąty do ósmego-odcinek
śródbłonowy i odcinek śródplazmatyczny.

• obejmuje geny zgrupowane w subregiony DP, DQ, DR
• każdy subregion zawiera gen A (kodujący łańcuch α)
oraz gen B (kodujący łańcuch β)
• każdy z genów składa się z 5 eksonów
• ekson pierwszy koduje peptyd prowadzący, ekson
drugi i trzeci kodują domeny α
1
, α
2
, β
1
, β
2
,
• ekson czwarty genu A zawiera informacje dotyczącą
syntezy domeny cytoplazmatycznej, przezbłonowej i
części regionu III, nie ulegającego translacji
• ekson czwarty genu B koduje domenę przechodzącą
przez błonę i część domeny cytoplazmatycznej
• ekson piąty koduje pozostałą część nie ulegającego
translacji genu A oraz resztę cytoplazmatycznej
domeny genu B
REGION KLASY II

• znajduje się pomiędzy regionem klasy I i II
• obejmuje geny kodujące cytokiny (m.in. TNF)
oraz składowe dopełniacza: C2, Bf i C4
Geny kompleksu MHC tworzą grupę
sprzężeniową z genem fosfoglukomutazy,
glioksalazy oraz pepsynogenu. Kompleks HLA
obejmuje również tzw. pseudogeny, nie ulegające
ekspresji z powodu nagromadzonych mutacji.
REGION KLASY III

• geny HLA-A, HLA-B, HLA-C
• obecne są na powierzchni wszystkich komórek
z wyjątkiem erytrocytów i plemników
• ich głównym zadaniem jest prezentacja
limfocytom T (CD8+) białek własnych,
egzogennych oraz pochodzących z komórek
nowotworowych
• antygeny klasy I są antygenami
transplantacyjnymi
ANTYGENY KLASY I
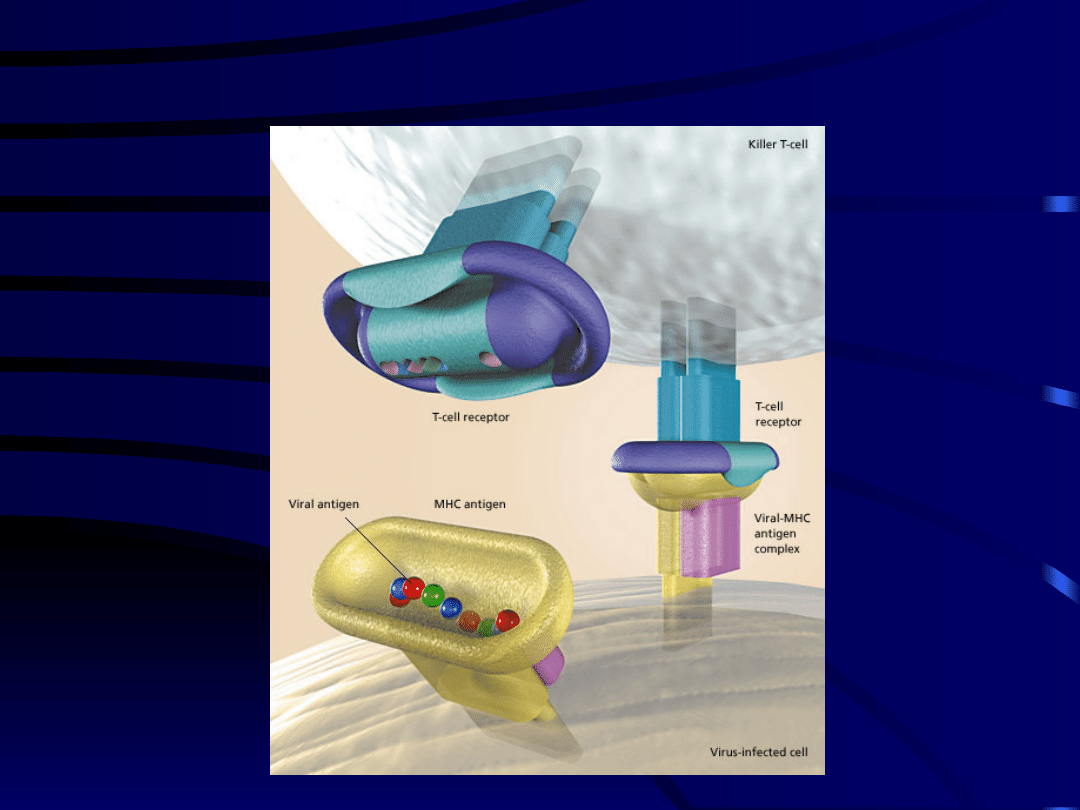
ANTYGENY KLASY I

• charakteryzują się dużym polimorfizmem
allelicznym i haplotypowym
• występują stale na limfocytach B, makrofagach,
komórkach dendrytycznych i komórkach
nabłonkowych grasicy
• pojawiają się okresowo na powierzchni śródbłonka
naczyń nerkowych i naczyń mięśnia sercowego oraz
na nabłonkach jelit, oskrzeli, tarczycy i
keratynocytach
• antygeny tej klasy to tzw. antygeny indukowane (ich
ilość wzrasta na powierzchni przeszczepionego
narządu w GvHR)
• prezentują limfocytom T (CD4+) antygeny
zewnątrzpochodne oraz autoantygeny
ANTYGENY KLASY II
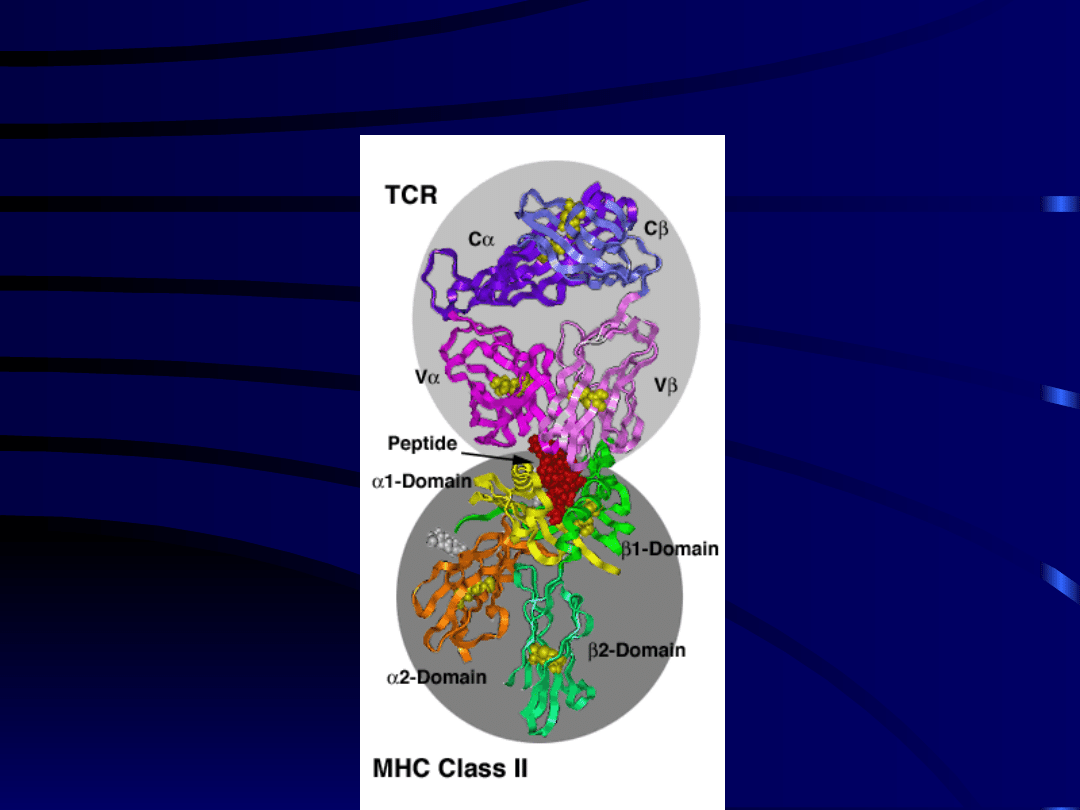
ANTYGENY KLASY II

• do antygenów klasy II zalicza się składniki
komplementu C2, Bf i C4 oraz cytokiny
• dopełniacz uczestniczy w obronie
przeciwzakaźnej na drodze cytolizy oraz w
usuwaniu kompleksów immunologicznych
• nie biorą udziału w prezentacji antygenów (nie
są białkami błonowymi)
ANTYGENY KLASY III

BUDOWA ANTYGENÓW MHC
KLASY I
• łańcuch ciężki (α) połączony niekowalencyjnie
z łańcuchem lekkim (β
2
-mikroglobuliną)
• łańcuch ciężki (α) posiada trzy domeny
zewnątrzkomórkowe (α
1
, α
2
, α
3
) tworzące pętlę,
segment transbłonowy i tzw. ogon cytozolowy
• różnice między białkami klasy I zależą od
polimorfizmu domen α
1
i α
2
• domenyα
1
i α
2
tworzą miejsce wiązanie peptydu
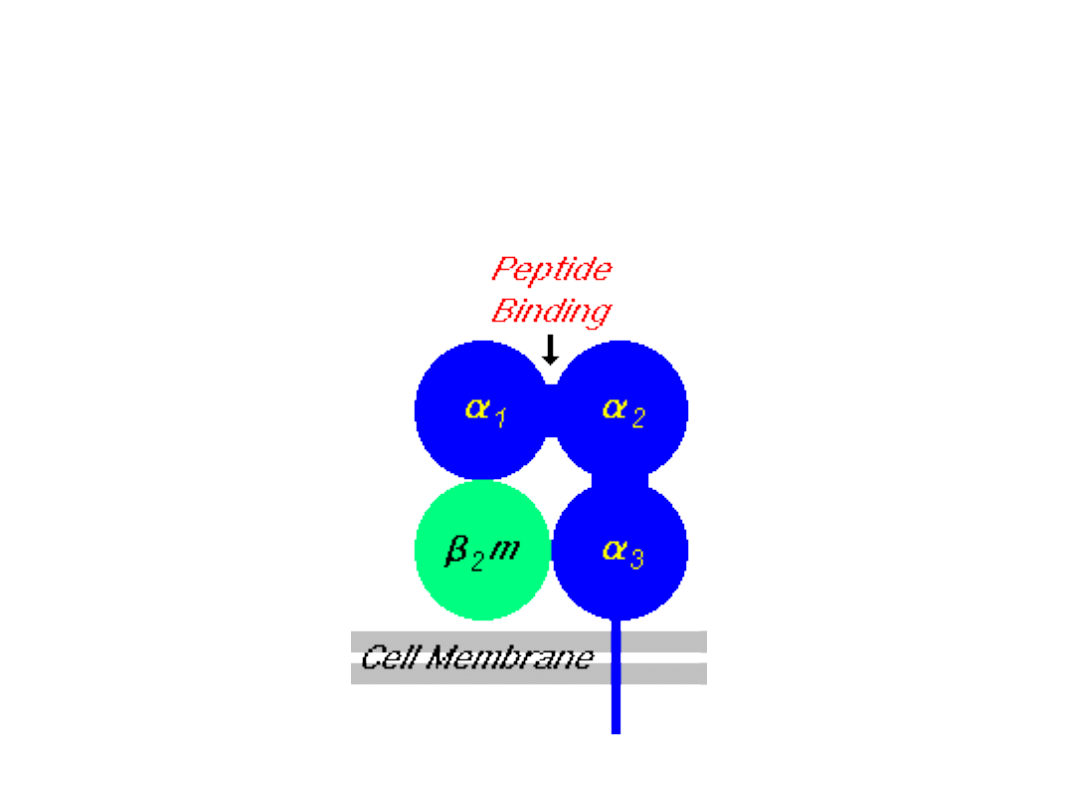
BUDOWA ANTYGENÓW MHC
KLASY I

• łańcuch α połączony niekowalencyjnie z
łańcuchem β
• każdy z łańcuchów ma dwie domeny
zewnątrzkomórkowe, segment transbłonowy i
krótki cytozolowy ogon.
• najbardziej zmienne są domeny zewnętrzne α
1
,
β
1
, które tworzą miejsce wiązania peptydu
BUDOWA ANTYGENÓW MHC
KLASY II
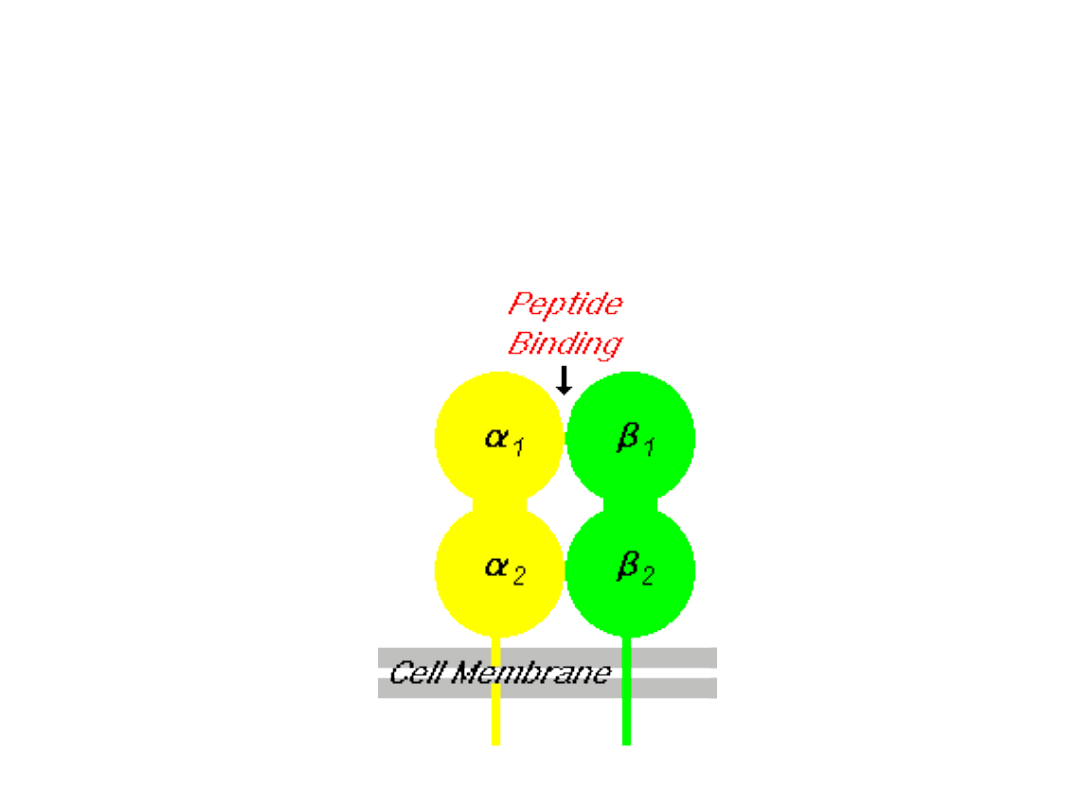
BUDOWA ANTYGENÓW MHC
KLASY II

• komponenty dopełniacza C2, Bf, C4,
properdyna oraz białka surowicy, m.in. Ss
(Serum serological)
BUDOWA ANTYGENÓW MHC
KLASY III

• dziedziczenie w sposób kodominujący, zgodnie z I
regułą Mendla
• człowiek posiada dwa haplotypy, po jednym od
każdego z rodziców
• w każdym haplotypie znajdują się 4 geny układu
HLA ułożone w kolejności (D, B, C, A)
• w populacji ogólnej niektóre haplotypy występują
z mniejszą lub większą częstotliwością (nielosowe
sprzężenie alleli w haplotypach-
niezrównoważenie sprzężeń)
• niezrównoważenie sprzężeń może wynikać z
wymieszania się różnych populacji o odmiennych
częstościach genowych, lub/i selekcji środowiska.
DZIEDZICZENIE ANTYFENÓW UKŁADU
HLA

METODY WYKRYWANIA HLA
• test mikrocytotoksyczny z limfocytami krwi
obwodowej (wykrywanie antygenów klasy I)
• metody komórkowe (wykrywanie antygenów
klasy II):
-mieszana hodowla limfocytów (MLC-Mixed
Lymphocyte Culture), jednostronny test
blastyczny w MLC
• metody bezpośredniej identyfikacji HLA (HLA
genotyping), przy użyciu odpowiedniej sondy
molekularnej
• identyfikacja za pomocą metod RFLP i PCR
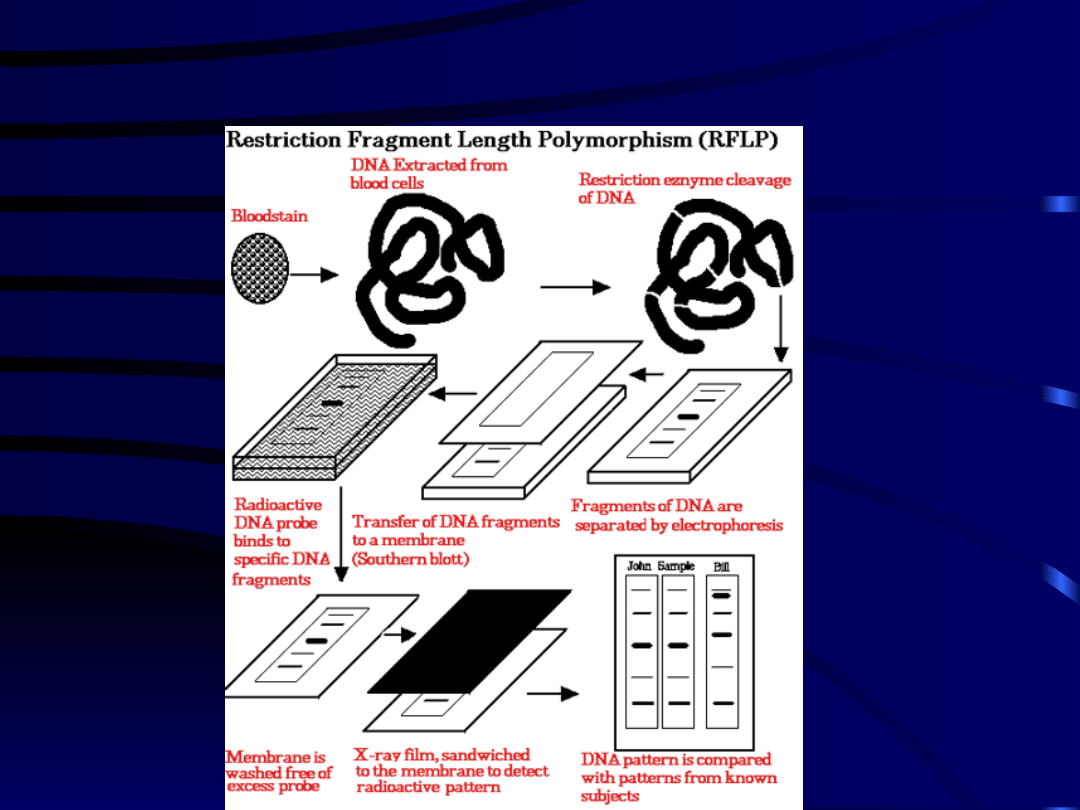
RFLP-polimorfizm długości
fragmentów restrykcyjnych
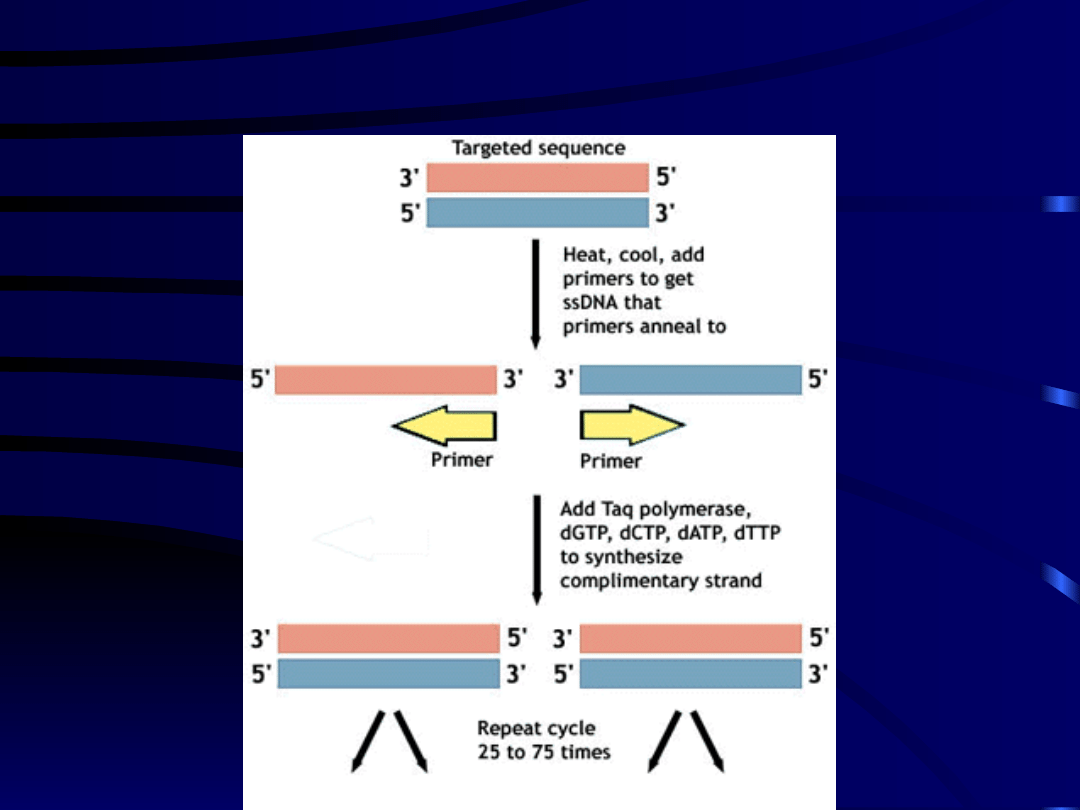
PCR-łańcuchowa reakcja polimerazy

PCR-specyficzna, szybka, wydajna
replikacja wybranego fragmentu genomu
• 1. Etap
- termiczna denaturacja dwuniciowego
DNA (94 °C)
• 2. Etap – przyłączenie do zdenaturowanego
jednoniciowego DNA primerów, krótkich
jednoniciowych oligonukleotydów Utworzenie
dwuniciowej struktury primer-DNA określa
miejsce rozpoczęcia replikacji (40-60 °C)
• 3. Etap
– na jednoniciowej matrycy DNA
synteza przez odporną na wysoka temperaturę
polimerazę nici potomnej (72 °C)
Każdorazowe powtórzenie trójetapowego cyklu
powinno powodować podwojenie ilości
namnażanego materiału
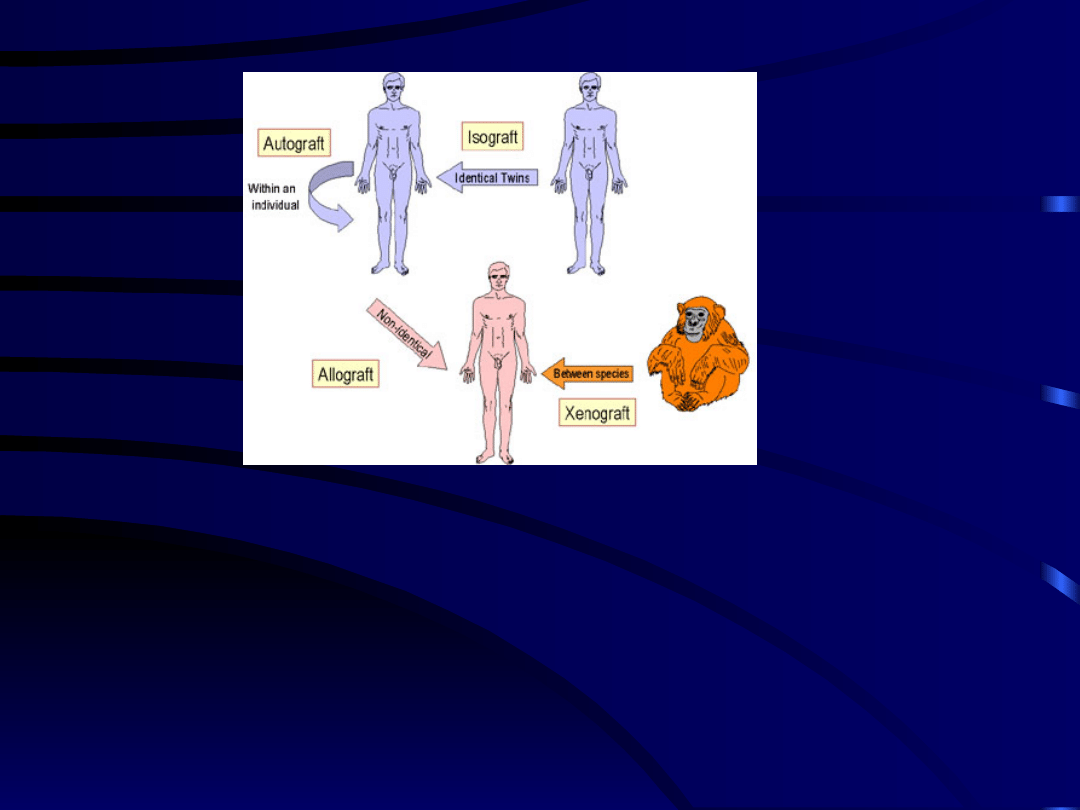
•
przeszczep autologiczny (
autograft
)-dawcą i biorcą jest ten sam
organizm
•
przeszczep izogeniczny (syngeniczny,
isograft
)-dawca i biorca są
identyczni genetycznie
•
przeszczep allogeniczny (homologiczny,
allograft
)-dawca i biorca
należą do tego samego gatunku , ale są odmienni genetycznie
•
przeszczep ksenogeniczny (heterologiczny,
xenograft
)-dawca i
biorca należą do innych gatunków
TERMINOLOGIA PRZESZCZEPÓW

Ze względu na miejsce przeszczepiania
wyróżnia się:
• przeszczep ortotropowy – wykonywany w
tę samą okolicę ciała, w której
anatomicznie narząd się znajduje
• przeszczep heterotropowy – wykonywany
w miejsce anatomicznie odmienne.
TERMINOLOGIA PRZESZCZEPÓW

• zespół groźnych dla życia objawów klinicznych
spowodowany obniżoną reaktywnością
immunologiczną dawcy
• najczęściej rozwija się po przeszczepach szpiku
• przyczyną choroby jest oddziaływanie
alloreaktywnych i dominujących limfocytów T
dawcy z komórkami biorcy (głównie komórkami
skóry, wątroby, przewodu pokarmowego)
• zapobieganie temu procesowi polega na
podawaniu leków immunosupresyjnych oraz
eliminowaniu ze szpiku kostnego dawcy
dojrzałych limfocytów T
CHOROBA PRZESZCZEP PRZECIW
GOSPODARZOWI (GvHD)
(Graft versus Host Disease)
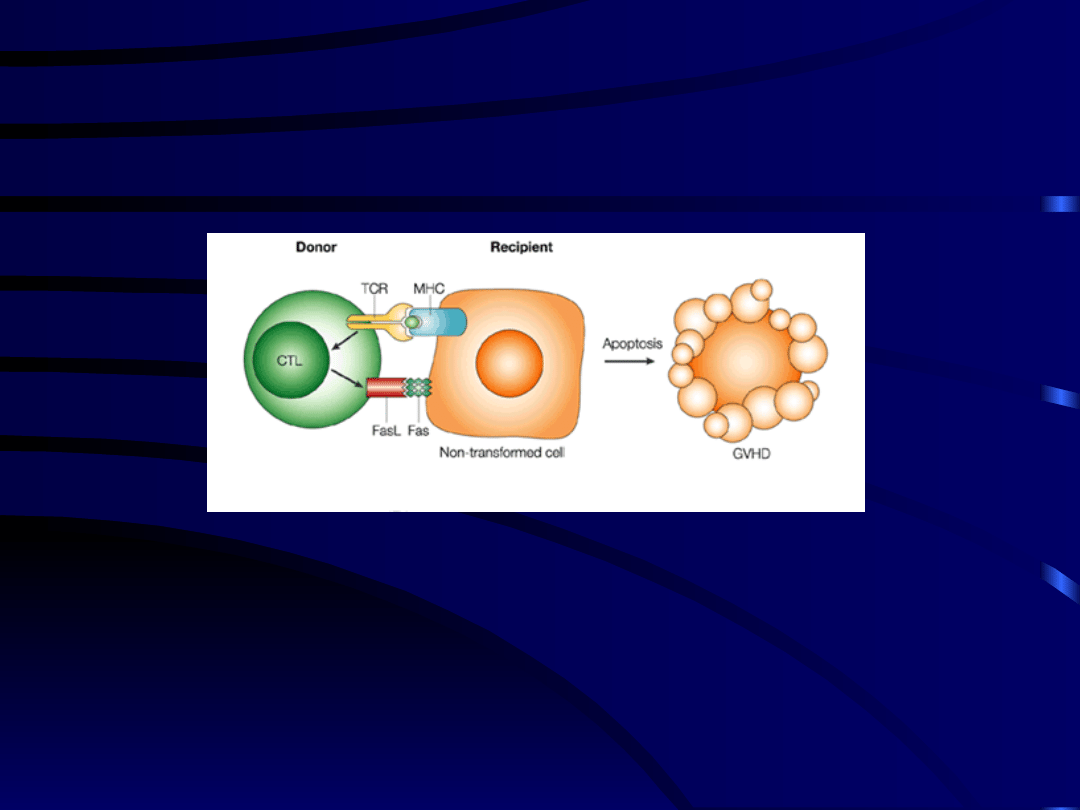
CHOROBA PRZESZCZEP PRZECIW
GOSPODARZOWI (GvHD)
(Graft versus Host Disease)

• niektóre antygeny HLA zwiększają ryzyko wystąpienia
pewnych chorób (badania statystyczne)
• asocjacje antygenów HLA z określonymi chorobami
tłumaczy się następująco:
- nasilanie lub osłabianie odpowiedzi immunologicznej
przez określone antygeny HLA
- antygeny HLA mogą pełnić rolę receptora dla danego
czynnika zakaźnego
- podobieństwo antygenów HLA do antygenów
bakteryjnych (tolerancja infekcji)
- współdziałanie z innymi genami warunkującymi
podatność na dana chorobę
ASOCJACJA NIEKTÓRYCH CHORÓB Z
ANTYGENAMI HLA

• zespół nadnerczowo-płciowy – HLA-B27
• zesztywniające zapalenie stawów kręgosłupa –
HLA-B27
• łuszczyca – HLA-Cw6
• celiakia – HLA-DR3
• choroba Gravesa-Basedowa – HLA-DR3
• cukrzyca typ I – HLA-DR3, HLA-DR4
• nużliwość mięsni – HLA-DR3, HLA-B8
• toczeń rumieniowaty – HLA-DR3
• SM – HLA-DR2
• RZS – HLA-DR4
ASOCJACJA NIEKTÓRYCH CHORÓB Z
ANTYGENAMI HLA

GENETYCZNE
PODSTAWY
ONKOGENEZY

NOWOTWÓR
Nowotworem nazywamy nieprawidłową tkankę,
która rozrasta się nadmiernie i w sposób
nieskoordynowany z sąsiadującymi tkankami.
Nadmierny rozrost spowodowany jest
niepohamowaną proliferacją komórek,
nieustającą nawet po wyeliminowaniu
czynnika, który ją wywołał.
Nowotwór nie jest więc tworem obcym
organizmowi, a tkanką własną ustroju. Rozwija
się wraz z nim, bez niego nie istnieje. Może
powstać w każdym okresie życia człowieka,
nawet w łonie matki.

Zaburzenia:
• Cyklu komórkowego
• Procesu apoptozy
• Interakcji międzykomórkowych
NOWOTWÓR
NOWOTWÓR

RODZAJE NOWOTWORÓW
•
NOWOTWORY ŁAGODNE-włókniak,
brodawczak, tłuszczak, gruczolak,
torbiel
epidermalna
• NOWOTWORY ZŁOŚLIWE-raki
(tkanka
nabłonkowa), mięsaki (tkanka
nienabłonkowa)
• NOWOTWORY MIEJSCOWO
ZŁOŚLIWE-
rak podstawnokomórkowy,
włókniak
powięziowy, guz mieszany ślinianek

CECHY NOWOTWORÓW
nowotwór łagodny
nowotwór złośliwy
SZYBKOŚĆ WZROSTU
powolny
szybki
TOREBKA
zwykle jest
nie ma
NACIEKANIE TKANEK
nie ma
jest
WRASTANIE DO NACZYŃ nie ma
jest
PRZERZUTY
nie ma
są
WZNOWY
nie ma
są
BUDOWA
HISTOLOGICZNA
zbliżona do tkanki
prawidłowej
różni się od tkanki
prawidłowej, wykazuje
cechy anaplazji

STANY PRZEDRAKOWE
Stan przedrakowy to taka zmiana chorobowa, z której
częściej niż w przypadku tkanek prawidłowych tego
samego narządu rozwija się nowotwór.
Znamy dużą liczbę takich patologii. Przykładem może
być polipowatość rodzinna jelita grubego, rogowacenie
starcze skóry, skóra żółta pergaminowa, przewlekły
zanikowy nieżyt żołądka, wrzodziejące zapalenie jelita
grubego, niektóre postacie nadżerki szyjki macicy,
zwyrodnienie gruczołowe sutka i wiele innych.
Oglądając pod mikroskopem preparaty histologiczne
wycinków, stwierdza się zawsze charakterystyczne dla
stanu przedrakowego cechy, polegające na
opóźnionym i nieprawidłowym różnicowaniu komórek.
Stanów przedrakowych w żadnym wypadku nie wolno
lekceważyć. Wymagają one odpowiedniego leczenia i
stałej kontroli lekarskiej.

RAK PRZEDINWAZYJNY
Jest to rozrost komórek, które mają cechy nowotworu
złośliwego, ograniczony tylko i wyłącznie do warstwy
nabłonka. Inne powszechnie używane nazwy to rak
śródnabłonkowy lub in situ (czyli: w pierwotnym
położeniu).
Nie jest możliwe rozróżnienie raka przedinwazyjnego
od stanu przedrakowego “na oko”, bez mikroskopu.
Dlatego wykonanie odpowiednich badań, nawet
nieprzyjemnych jak pobranie wycinka tkanki, jest
życiową koniecznością. Rak przedinwazyjny nie daje
przerzutów. Jest całkowicie wyleczalny. Natomiast
nieleczony w miarę upływu czasu przechodzi zawsze w
raka inwazyjnego, który cechuje się pełną złośliwością.

KLASYFIKACJA TNM
Klasyfikacja TNM jest łatwo zrozumiałym
systemem stosowanym do określenia
rozległości nowotworu w obrębie tkanek i
narządów. Składa się ona z trzech elementów:
•T (tumor) - guz w umiejscowieniu
pierwotnym
•N (nodulus) - ocena stanu węzłów chłonnych
•M (metastases) - przerzuty odległe.

KLASYFIKACJA TNM
Liczby dodawane do litery T oznaczają wielkość guza.
Liczby dodawane do litery N oznaczają stopień zajęcia
węzłów chłonnych.
W odniesieniu do litery M używa się dwóch oznaczeń:
M0 - brak przerzutów i M1 - odległe przerzuty.
Ze względu na uwarunkowania anatomiczne każdy
nowotwór złośliwy posiada swoją własną skalę TNM i tak
na przykład N2 w raku pęcherza nie oznacza tego
samego co N2 w raku sutka.
Wprowadzenie jednolitego sposobu opisywania
zaawansowania procesu nowotworowego,
akceptowanego na całym świecie, ułatwia komunikację
między lekarzami i prowadzenie badań naukowych.

ZMIANY CHROMOSOMOWE W
KOMÓRKACH NOWOTWOROWYCH
• P.C. Nowell i D.A. Hungerford rozpoczęli
w 1960
roku badania cytogenetyczne komórek
nowotworowych
• Najczęstsze aberracje chromosomowe w
komórkach nowotworowych to
duplikacje, delecje,
translokacje i poliploidie

ZMIANY CHROMOSOMOWE W
KOMÓRKACH NOWOTWOROWYCH

ETAPY TRANSFORMACJI
NOWOTWOROWEJ
•
INICJACJA
• PROMOCJA
• PROGRESJA
HIPOTEZA KNUDSONA

INICJACJA
Inicjacja jest to faza, w której czynnik
rakotwórczy, działając na zdrową komórkę,
powoduje zmianę w jej materiale
genetycznym, czyli mutację. Jeżeli
zaatakowana komórka ma zdolności do
podziałów, to wywołana mutacja się utrwala i
jest przekazywana następnym pokoleniom
komórek. Taka zmutowana komórka nazywa
się inaczej zainicjowaną.

PROMOCJA
Na etapie promocji zainicjowana komórka
przechodzi wiele kolejnych mutacji, aż staje się
typową komórką nowotworową. Jedną z
ważniejszych cech różnicujących komórkę
prawidłową od zainicjowanej jest to, że komórki
zainicjowane charakteryzują się zaburzonymi
zdolnościami przylegania do otaczających
komórek. Ta ich właściwość we wczesnym okresie
rozwoju nowotworu umożliwia im przekroczenie
naturalnych barier pomiędzy tkankami, a w
późniejszym może ułatwiać powstawanie
przerzutów. W tej fazie rozwoju zatrzymanie
procesu tworzenia nowotworu jest jeszcze
możliwe i tak też się dzieje w większości
przypadków.

PROGRESJA
Ostatnim etapem jest progresja. Dochodzi do
niej, gdy organizm z jakichś względów jest
osłabiony. Wtedy to następuje wzrost komórek
nowotworowych, który przeważnie przebiega
niepowstrzymanie i jest nieodwracalny. Dopiero
w tym okresie możliwe jest kliniczne
rozpoznanie choroby, ponieważ pojawiają się jej
pierwsze objawy.

CZYNNIKI KANCEROGENNE
• KARCYNOGENEZA FIZYCZNA-UVB,
UVA,
promieniowanie jonizujące
• KARCYNOGENEZA CHEMICZNA-związki
gentotoksyczne i epigenetyczne
• KARCYNOGENEZA BIOLOGICZNA-
wirusy
onkogenne (HPV 5, 8, 14, 16, EBV, HBV,
HCV,
HTLV-1, HHV8, Helicobacter pylori)

ROLA ONKOGENÓW I WIRUSÓW
ONKOGENNYCH W ONKOGENEZIE

ROLA ONKOGENÓW I WIRUSÓW
ONKOGENNYCH W ONKOGENEZIE
cyclin D1 +
cdk4/cdk6
p16(INK4
a)
p15(INK4
b)
p18(INK4
c)
pRb-E2F-DP
complex
cyclin D1-
cdk4/cdk6
complex
E2F-DP
pRb
phase S genes
promoters
+
P
P
P

ROLA ONKOGENÓW I WIRUSÓW
ONKOGENNYCH W ONKOGENEZIE
oncogenic
stimuli
p14(ARF)
hdm2-p14(ARF)
complex
p53
stabilization
DNA damage
p53
hdm
2
p53
p53
degradation
p21(Cip1
)
cell cycle
arrest
apoptosi
s
ub
ub
ub

ROLA ONKOGENÓW I
ANTYONKOGENÓW W
ONKOGENEZIE
Białko
regulatorowe
Mutacja/modyfikacja
genu
Nowotwory
p53
mutacje punktowe,
delecje
ponad połowa nowotworów występujących u człowieka
pRb
mutacje punktowe,
hipermetylacja
promotora
siatkówczak złośliwy, drobnokomórkowy rak płuca,
kostniakomięsak, rakowiak
p15(INK4b)
delecje homozygotyczne
hipermetylacja
promotora
czerniak
złośliwy,
rak
trzustki,
rak
szyjki
macicy,
kostniakomięsak, niedrobnokomórkowy rak płuca, nowotwory
układu chłonnego, glejaki
rak kolczystokomórkowy, chłoniak Burkitta, ostra białaczka
szpikowa,
ostra białaczka limfatyczna
p16(INK4a)
delecje homozygotyczne
mutacje punktowe
hipermetylacja
promotora
glejaki, międzybłoniak, rak nosogardła, ostra białaczka
limfatyczna, rak jajnika,
rak pęcherza moczowego, mięsak, chłoniak mózgu
rak dróg żółciowych, rak przełyku, czerniak złośliwy, rak
trzustki
ostra białaczka szpikowa, szpiczak mnogi, rak przełyku, rak
szyjki macicy, niedrobnokomórkowy rak płuca
p19(ARF)
delecje eksonu 1β
linie komórkowe czerniaka (SK-MEL-5, A2058)
p21(Cip1)
nadekspresja genu
osłabiona ekspresja genu
rak
wątrobowokomórkowy,
rak
kolczystokomórkowy,
niedrobnokomórkowy rak płuca
rak żołądka, rak jelita grubego, rak jajnika, rak przełyku,
niedrobnokomórkowy rak płuca

ROLA ONKOGENÓW I
ANTYONKOGENÓW W
ONKOGENEZIE
Białko
regulatorowe
Mutacja/modyfikacja
genu
Nowotwory
cyklina D1
amplifikacja genu
inwersja: inv(11)
(p15;q13)
translokacja: t(11;14)
(q13;q32)
drobnokomórkowy i niedrobnokomórkowy rak płuca, rak
pęcherza moczowego,
rak
kolczystokomórkowy,
rak
sutka,
rak
wątrobowokomórkowy, nowotwory układu pokarmowego,
szpiczak mnogi
gruczolak przytarczyc
chłoniaki wywodzące się z komórek B, przewlekła białaczka
limfatyczna, białaczka plazmocytowa
cyklina D2
nadekspresja genu
insercje wirusowe
(HTLV-1, EBV)
nowotwory jelita grubego, nowotwory jądra, rak żołądka
białaczka T-komórkowa dorosłych, chłoniak Burkitta
cyklina D3
nadekspresja genu
rak sutka, chłoniaki
cyklina E
amplifikacja genu
rak sutka, rak jelita grubego, rak żołądka
cdk4
amplifikacja genu
mutacje punktowe
kostniakomięsak, glejaki, rak sutka
czerniak złośliwy
mdm2
amplifikacja genu
kostniakomięsak, glejakomięsak, rak przełyku, rak żołądka

GENETYCZNE PREDYSPOZYCJE
DO CHOROBY NOWOTWOROWEJ
KLUCZ DIAGNOSTYCZNY LYNCHA:
• rozpoznanie nowotworu w młodym wieku
• nowotwory u krewnych pierszego stopnia
• dwa różne nowotwory u tego samego pacjenta
• występowanie nowotworów w co najmniej w
dwóch
pokoleniach
• autosomalny dominujący typ dziedziczenia
nowotworów

GENETYCZNE PREDYSPOZYCJE
DO CHOROBY NOWOTWOROWEJ
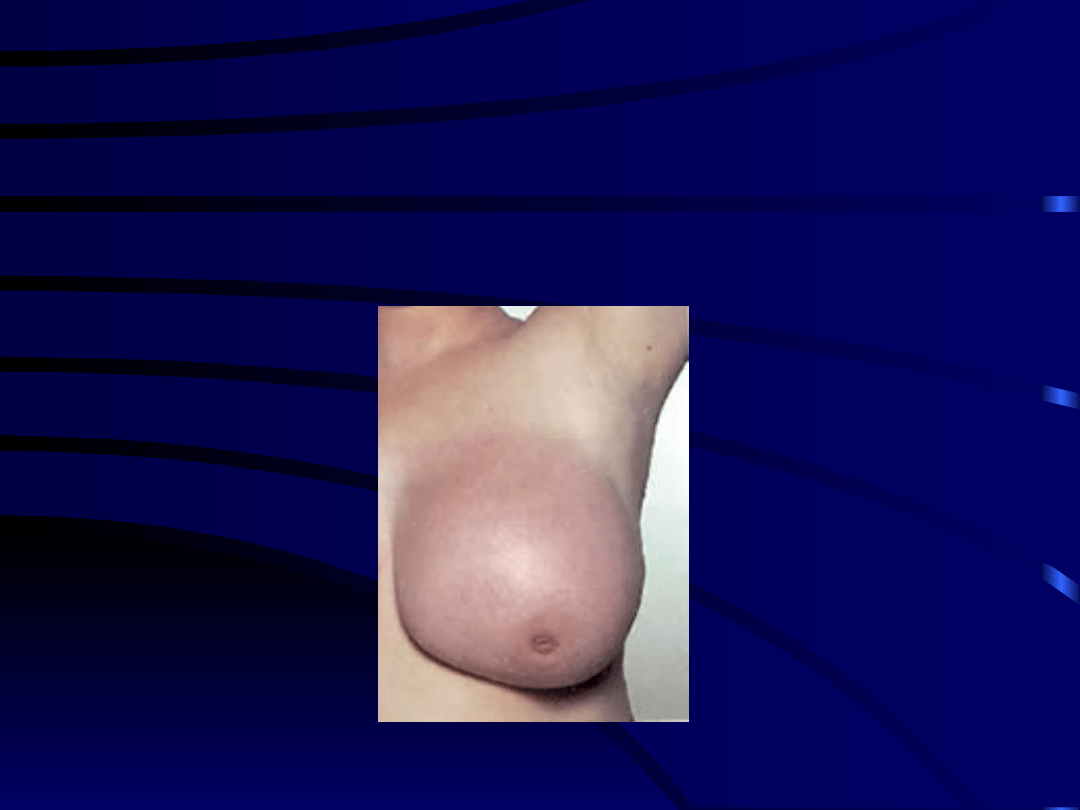
Rak sutka
Częste objawy:
• Guzek
• Zmiany brodawki (wciągnięcie,
uwypuklenie, zmiana koloru)
• Zmiany na skórze (wciągnięcie, zmiana
koloru,
nie gojące się owrzodzenia)
• Wydzielina z gruczołu (czasem
podbarwiona krwią)
• Powiększone węzły chłonne w dole
pachowym

Ryzyko zachorowania zwiększają:
• Rak sutka u matki lub siostry
• Otyłość
• Bezdzietność, nie karmienie piersią
• Wieloletnie stosowanie hormonalnych
środków
antykoncepcyjnych
• Wczesna pierwsza miesiączka
• Późna menopauza
GENETYCZNE PREDYSPOZYCJE DO
GENETYCZNE PREDYSPOZYCJE DO
CHOROBY NOWOTWOROWEJ
CHOROBY NOWOTWOROWEJ
Rak sutka
Rak sutka
GENETYCZNE PREDYSPOZYCJE
DO CHOROBY NOWOTWOROWEJ
Rak sutka

GENETYCZNE PREDYSPOZYCJE
DO CHOROBY NOWOTWOROWEJ
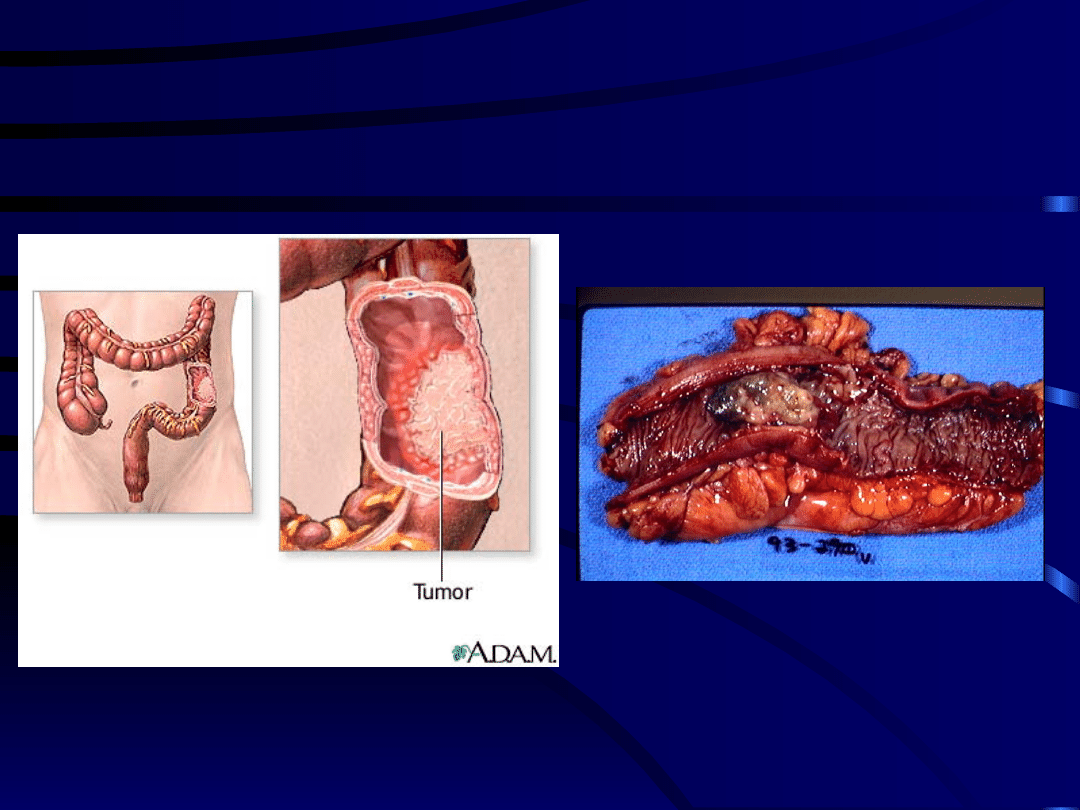
Rak jelita grubego
Częste objawy:
• Zmiana w rytmie wypróżnień (biegunki lub
zaparcia)
• Nieprawidłowe domieszki w stolcu (śluz,
krew)
• Bóle w jamie brzusznej
• Krwawienie z odbytnicy
• Niedokrwistość
• Utrata masy ciała

GENETYCZNE PREDYSPOZYCJE DO
GENETYCZNE PREDYSPOZYCJE DO
CHOROBY NOWOTWOROWEJ
CHOROBY NOWOTWOROWEJ
Rak jelita grubego
Rak jelita grubego
Ryzyko zachorowania zwiększają:
• Polipy gruczolakowate
• Rodzinna polipowatość okrężnicy
• Wrzodziejące zapalenie jelita grubego
• Choroba Leśniowskiego-Crohna
GENETYCZNE PREDYSPOZYCJE DO
GENETYCZNE PREDYSPOZYCJE DO
CHOROBY NOWOTWOROWEJ
CHOROBY NOWOTWOROWEJ
Rak jelita grubego
Rak jelita grubego

• Xeroderma pigmentosum (A do G,
XPV wariant)
• Zespół znamion atypowych
(FAMMM syndrome)
GENETYCZNE PREDYSPOZYCJE
DO CHOROBY NOWOTWOROWEJ
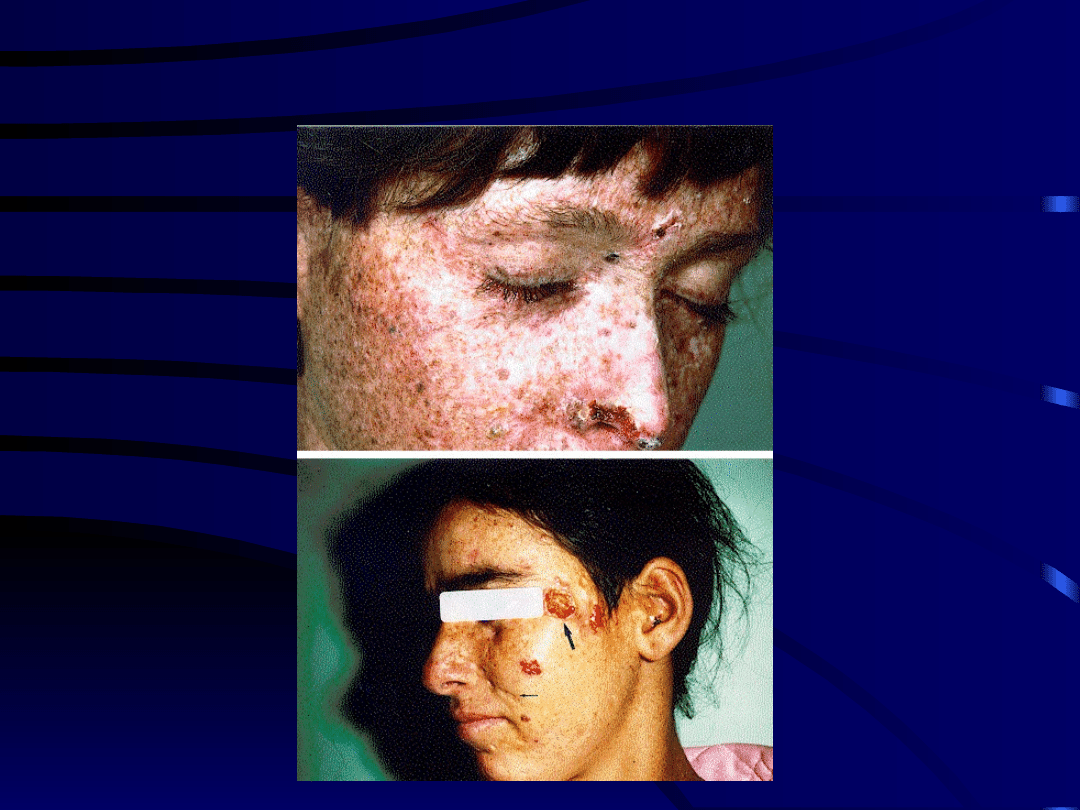
Xeroderma pigmentosum
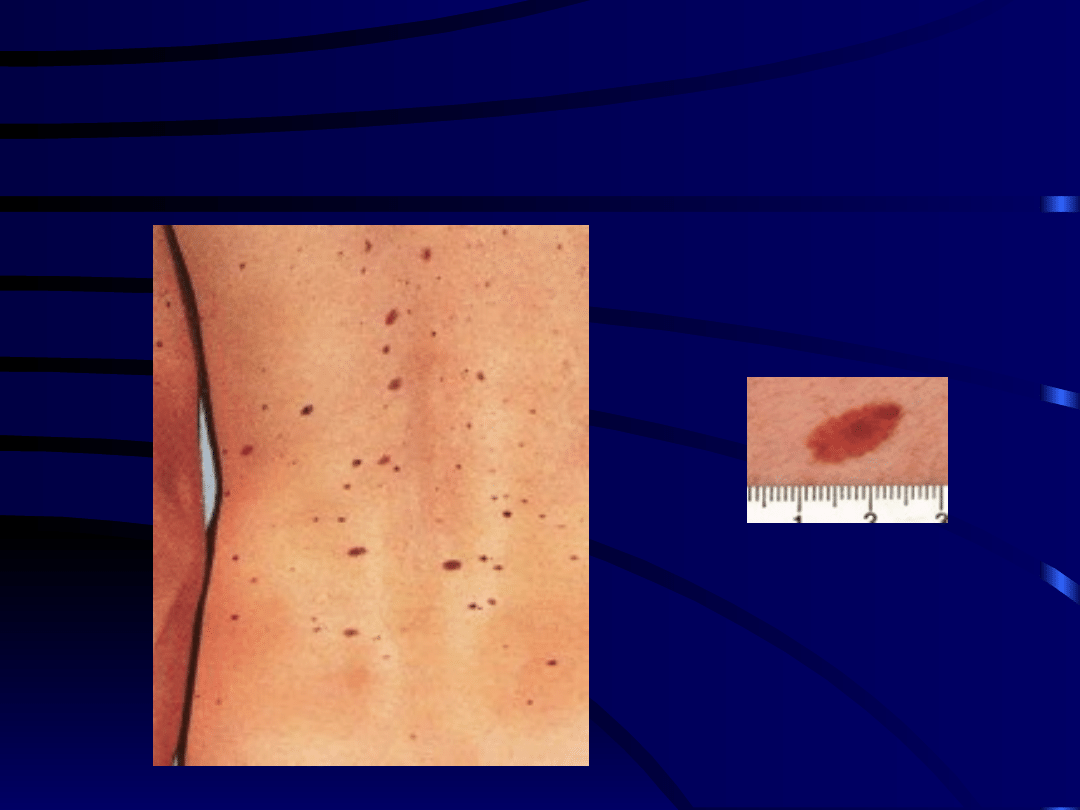
FAMMM syndrome

Name
Chromosome
Protein
Function
Importance
CMM1
1p36
unknown
unknown
not confirmed
CMM2
9p21
p16(INK4a)
antioncogene
confirmed
CMM3
12q14
CDK4
oncogene
only in 3 families with FAMMM
syndrome
CMM4
9p21
p14(ARF)
antioncogene
isolated exon 1β mutations in some
cases of melanoma-astrocytoma
syndrome
ROLA ONKOGENÓW I
ANTYONKOGENÓW W CZERNIAKU
RODZINNYM
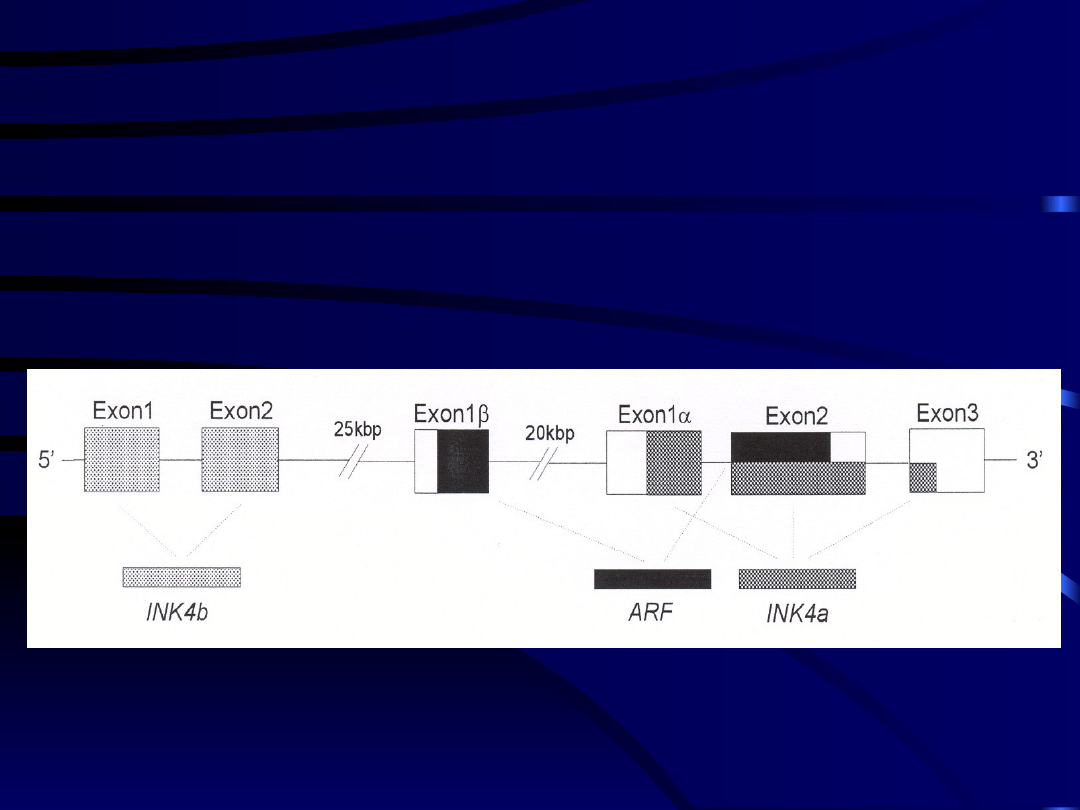
LOCUS INK4a/ARF
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
Wyszukiwarka
Podobne podstrony:
Antygeny zgodności tkankowej
ANTYGENY ZGODNOŚCI TKANKOWEJ
Ćw 05 Antygeny zgodności tkankowej Test mikrolimfocytotoksyczny
Antygeny zgodności tkankowej
Antygeny zgodności tkankowej
ANTYGENY ZGODNOSCI TKANKOWEJ I PROBLEMY TRANSPLANTOLOGII
Ag zgodnosci tkankowej przeszcz Nieznany
Metody oznaczania Ag zgodności tkankowej
notatki gołąb, 5. Główny układ zgodności tkankowej, Immunologia rozrodu
Główny układ zgodności tkankowej, materiały farmacja, Materiały 3 rok, mat 3 rok, Immuno
GŁÓWNY UKŁAD ZGODNO¦CI TKANKOWEJ MHC
GŁÓWNY UKŁAD ZGODNOŚCI TKANKOWEJ
Wyklad 6 Testy zgodnosci dopasowania PL
3 ogolny schemat replikacji i onkogeza DNA wirusowa
wyklad 6 Testy zgodnosci dopasowania PL
Fizjologia płynu tkankowego
więcej podobnych podstron