
Zaburzenia gospodarki
wodno-elektrolitowej
i kwasowo-zasadowej

Homeostaza
Izow
olem
ia
Izoton
ia
Izo
hy
dri
a
Izojo
nia

Homeostaza
Dla ustroju najważniejsze jest
zachowanie wolemii
DO
2
=Q x 1,3 x Hb x SaO
2
Wszystkie procesy zyciowe zachodzą
w środowisku wodnym

Regulacja wolemii
• Mechanizm autoregulacji nerek
(renina-angiotensyna)
• Mechanizm aldosteronowy
• Mechanizm ADH
• Mechanizm bezpośredniej lub
pośredniej regulacji czynności
nerki przez układ nerwowy

Angiotensyna II:
• powoduje skurcz naczyń obwodowych
• aktywuje układ współczulny
• w nerkach - zwiększa resorpcję zwrotną Na
• w nadnerczach - stymuluje sekrecję
aldosteronu
• w przysadce - stymuluje sekrecję ADH
• w oun - stymuluje ośrodek pragnienia
• Skutek: wzrost ECV i zwiększenie perfuzji
kłębków nerkowych

Bilans wodny
Pobór wody
• 1.woda spożywana:
• płyny
1500 ml
• woda z pokarmów
stałych
700 ml
• 2. woda
oksydacyjna
300ml
• Razem
2500ml
Utrata wody
1. z moczem
1500ml
2. perspiratio
insensibilis
• utrata przez płuca
300ml
• utrata przez skórę
600ml
3. z kałem
100ml
Razem
2500ml

Woda oksydacyjna
Woda oksydacyjna
W czasie spalania:
100 węglowodanów powstaje 60 ml wody oksydacyjnej
100g tłuszczów powstaje 110 ml wody oksydacyjnej
100g białek powstaje 44 ml wody oksydacyjnej
Tkanki
nieuwodnione
40-46%
Przestrzeń
śródnaczyniowa
5%
Rozmieszczenie wody
w poszczególnych
przestrzeniach wodnych
Woda całkowita
60%
Przestrzeń
pozakomórkowa
20%
Przestrzeń
śródkomórkowa
40%
Przestrzeń
pozakomórkowa
i pozanaczyniowa 15%
“Trzecia przestrzeń”
<2-3%

Objętość dobowa (w ml) oraz stężenie jonów
w wydalinach i wydzielinach ustrojowych
Ślina
1500
Sok żołądkowy
2500
Żółć
500
Sok trzustkowy
700
Sok jelitowy
3000
Kał
100

Perspiratio insensibilis = utrata wody bez elektrolitów
Utrata wody
Utrata przez skórę - 75%, przez płuca - 25%
Zwiększona utrata wody drogą parowania u chorych
gorączkujących i oparzonych.

Osmolalność płynów ustrojowych - ok. 290 mmol/kg H
2
O
Ustrój broni stałej osmolalności
płynów ustrojowych
Osmolalność osocza = 1,86 x [Na] + [glukoza/18] + [BUN/2,8]
Ciśnienie osmotyczne osocza = 1,86 x [Na] + [glukoza/18]
Każdy wzrost ciśnienia osmotycznego osocza powoduje
odwodnienie komórek. Błony komórkowe są przepuszczalne
dla wody.

Regulacja izotonii płynów
ustrojowych
• Mechanizm pragnienia
• Wytwarzanie wolnej wody na poziomie
nerek (ADH) -
mechanizm skuteczny przy
ciśnieniu osmotycznym<295mmol/kg H
2
O
•
Klirens osmotyczny
-
objętość wody
potrzebna do wydalenia substancji
osmotycznie czynnej w postaci
izoosmotycznego w stosunku do osocza moczu
Klirens wolnej wody
- C
H
2
O
= V - C osm
C osm = P osm
U osm x V

Wydzielanie ADH
Jest spowodowane odwodnieniem osmoreceptorów podwzgórza.
Hipernatremia wywołuje większe niż hiperglikemia
uwalnianie ADH
.
Hiperglikemia
Przemieszczenie wody z komórek
do przestrzeni pozakomórkowej
hiponatremia
ADH
poliuria
odwodnienie

Izohydria - ustrój dąży do stałego
stężenia jonów H+
pH = 7,35-7,45 - optymalne pH dla reakcji
zachodzących w komórkach
Cel:
= K
pCO
2
HCO
3

Ustrój dąży do stałego składu elektrolitowego
przestrzeni wodnych
Płyny ustrojowe są elektroobojętne,
czyli suma K
+
= suma A
-
w danym płynie.
Jest to możliwe dzięki właściwościom
półprzepuszczalnych błon komórkowych
i pomp błonowych
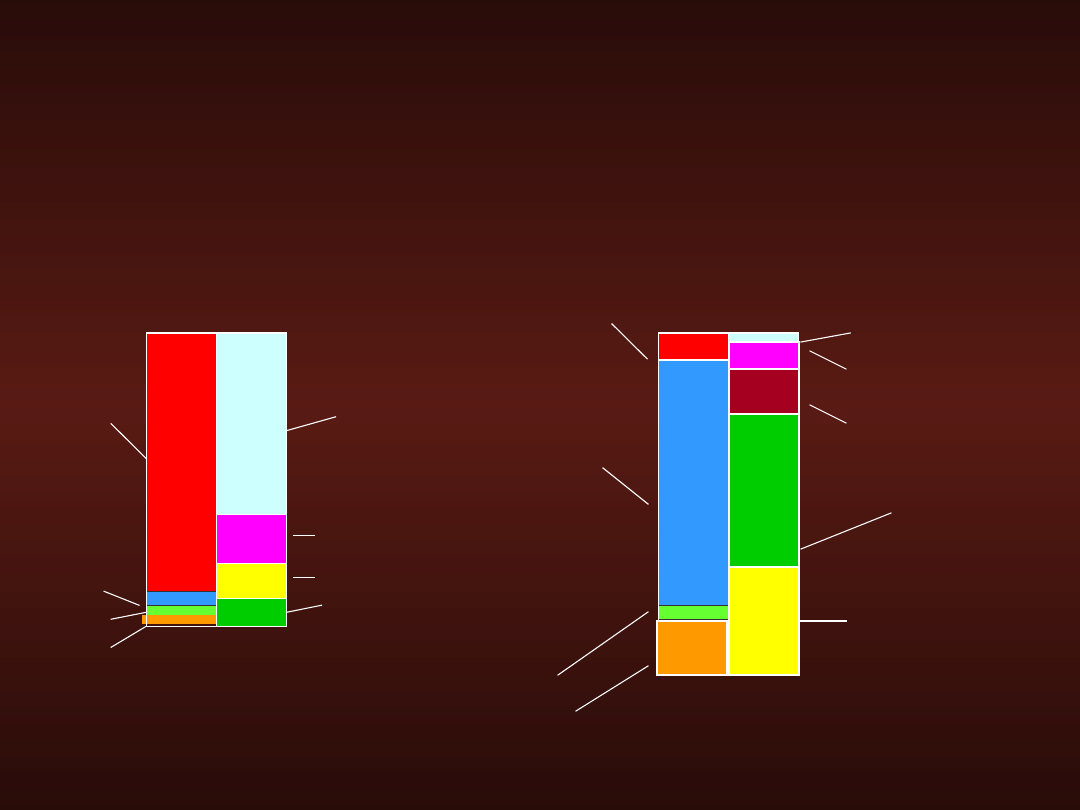
Izojonia a elektroobojętność
Osocze
K
+
= A
-
= 153 mEq/l
Płyn śródkomórkowy mięśnia
K
+
= A
-
= 198 mEq/l
Na=142
K = 4
Ca = 5
Mg = 2
Cl =
101
HCO3 = 26
Białczany = 16
Inne aniony = 10
Na=1
0
Ca = 2
Mg = 25
Cl = 3
HCO3 = 10
Białczany = 65
K = 160
Fosforany = 100
Siarczany = 20

Prowadzenie płynoterapii w
okresie pooperacyjnym
zależy od:
•
zapotrzebowania podstawowego
•
utraty śródoperacyjnej
•
wydzielania ADH
(należy przetaczać płyny
zawierające Na)

Dobowe zapotrzebowanie na wodę
Pierwsze 10 kg masy ciała 100 ml/kg
Następne 10 kg masy ciała 50 ml/kg
Na każdy następny kilogram 20 ml/kg
Przy założeniu, że: utrata poprzez parowanie
w warunkach fizjologicznych wynosi:
15 x masa ciała = ilość (w ml) wody utraconej
drogą perspiratio insensibilis

W przypadku gorączki należy dodać:
ok. 500 ml na każdy
o
C > 37
o
Chorym oparzonym należy dodać to, co tracą
przez uszkodzoną skórę:
utrata (ml/h) =
= (25 + powierzchnia oparzenia w %) x BSA (m
2
)
Chorym z niedrożnością należy uzupełnić
utratę wynikającą z przechodzenia wody
do “trzeciej przestrzeni”, uwzględniając
skład jonowy traconych płynów.

Najważniejsza jest wolemia.
W przypadku krwawienia z utratą krwi < 15 %
należy przetoczyć
czterokrotną
objętość utraty
w postaci krystaloidów i koloidów.
Płynoterapia nie jest celem sama w sobie.
Należy pamiętać o istnieniu obciążenia wstępnego serca,
którego wzrost tylko do pewnego momentu poprawia rzut serca.

Sód - miernik zaburzeń
równowagi wolnej wody
Stężenie tego jonu bardziej
zależy od całkowitej objętości
wody w ustroju (TBW) niż od
zasobów tego pierwiastka w
organizmie

Czy hipernatremia
(>145 mEq/l)
to rzeczywisty nadmiar
sodu?
Zawartość w ustroju
Na ECV
Na
Wolnej wody
1.
2.
3.

Hipernatremia z
odwodnieniem -
najczęstsza sytuacja
Wywiady:
• wymioty, biegunka
• niedostateczna
podaż płynów
• leki moczopędne
• współistniejąca
niewydolność nerek
Objawy subiektywne:
• wzmożone
pragnienie
• osłabienie
• brak apetytu
• apatia
• omdlenia
ortostatyczne

Hipernatremia z
odwodnieniem
Objawy kliniczne:
•
zmniejszenie masy ciała
•
suchość błon śluzowych
•
zmniejszone napięcie
skóry
•
zmniejszone napięcie
gałek ocznych
•
ortostatyczne zmiany
tętna i ciśnienia
•
tachykardia
“Objawy
laboratoryjne”
• zwiększona
osmolalność moczu
• zmniejszona diureza
• mocznika, białko
• Ht

Hipernatremia z
odwodnieniem
Zawsze dochodzi do odwodnienia komórek!
Najpierw należy uzupełnić utraconą objętość (płyny, osocze. krew),
a dopiero następnie wolną wodę.
m.c. x % TBW = TBW
prawidłowe Na+
x TBW= aktualna TBW
mierzone Na+
TBW - aktualna TBW = deficyt wody

Hipernatremia z
odwodnieniem
• 1/2 deficytu uzupełnia się w 12 h
(dłużej jeżeli hipernatremia trwa kilka dni)
•
Cały deficyt uzupełnia się w 48h.
Szybsze uzupełnianie może spowodować obrzęk mózgu
( uwaga na endogenne osmole!)
•
uzupełnia się 5% glukozą

Hipernatremia z
odwodnieniem
Moczówka prosta ( ADH) m.in. pacjenci po urazie głowy
• ośrodkowa
• nerkopochodna
ADH do nosa - 5-10j. co 4-6h.

Hipernatremia z
przewodnieniem - sytuacja
rzadsza
•
Niewłaściwe żywienie pozajelitowe
• Leczenie NaHCO
3
Leczenie: stymulacja diurezy

Czy hiponatremia
(<135 mEq/l)
to rzeczywisty niedobór
sodu?
Zawartość w ustroju
Na ECV
Na
Wolnej wody
1.
2.
3.

Hiponatremia z
przewodnieniem -
sytuacja stosunkowo rzadka
• zespół TUR
• Niewydolność serca,
• Niewydolność nerek (niektóre
typy),
• Niewydolność wątroby.
Występuje w następujących sytuacjach:

Hiponatremia z
prawidłową ECV-
sytuacja
częsta
Niebezpieczeństwo wiąże się z przewodnieniem
komórek
• Najczęściej problem ten dotyczy chorych
odwodnionych uzupełnianych płynami
niezawierającymi Na+
• lub pacjentów w okresie pooperacyjnym, którym
przetoczono płyny niezawierające Na+ w okresie
zwiększonej sekrecji ADH

Hiponatremia z
prawidłową lub
zwiększoną ECV
Leczenie:
Gdy nie ma objawów : stymulowanie diurezy
ograniczenie wolnej wody
(należy uzupełniać straty wynikające
z perspiratio insensibilis)
W przypadku wystąpienia objawów - drgawek, śpiączki
(Na <120): należy przetaczać 3% NaCl, uzupełnić K+

Hiponatremia z
prawidłową lub
zwiększoną ECV
Leczenie: ujemny bilans
m.c. x % TBW = TBW
aktualny
Na+
x TBW= oczekiwana TBW
wymagany Na+
TBW - oczekiwana TBW = wielkość ujemnego
bilansu

Hiponatremia z
odwodnieniem -
częsta
sytuacja
•
biegunka,
• cukrzyca,
• stosowanie leków moczopędnych,
• odwodnienie wyrównywane płynami
niezawierającymi Na
+
.

Hiponatremia z
odwodnieniem
Leczenie:
brak objawów:
wlew 0,9%NaCl
gdy są objawy:
uzupełnienie wyliczonego deficytu
w następującej kolejności:
1.
m.c.
x
(% TBW) = TBW
2. 125 - aktualny Na
+
= deficyt na 1litr TBW
3. Deficyt na 1litr TBW x TBW = deficyt do uzupełnienia

Hiponatremia z
odwodnieniem
Leczenie:
• 1/2 deficytu należy uzupełnić w 24h.
• Szybkie uzupełnienie grozi mielinolizą mostu.
• Deficyt należy uzupełniać 3% NaCl tak, aby pzyrost
stężenia Na
+
nie był szybszy niż 1-2 mEq / l /h.
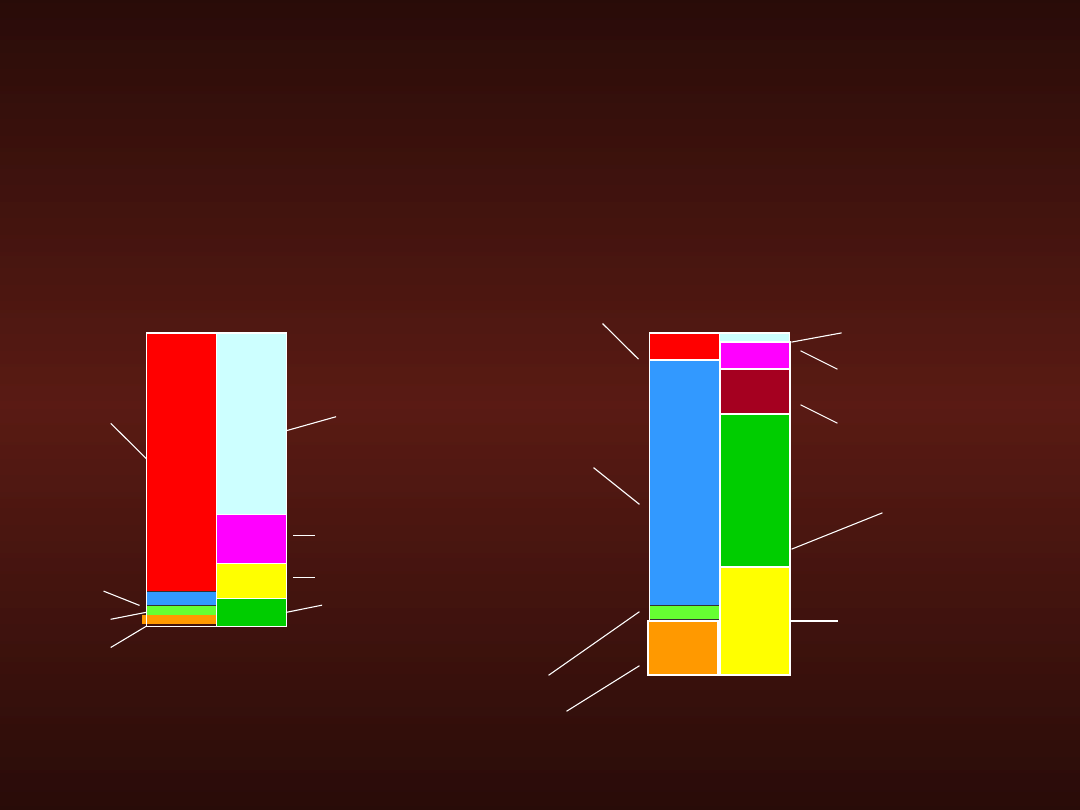
Potas - główny kation
wewnątrzkomórkowy
Na=142
K = 4
Ca = 5
Mg = 2
Cl =
101
HCO3 = 26
Białczany = 16
Inne aniony = 10
Osocze
Płyn śródkomórkowy
mięśnia
Na=1
0
Ca = 2
Mg = 25
Cl = 3
HCO3 = 10
Białczany = 65
K = 160
Fosforany = 100
Siarczany = 20

Hipokaliemia <3,5
mEq/l
Przyczyny:
• przesunięcie do wnętrza komórki
• niedobór

Hipokaliemia <3,5
mEq/l
H
+
H
+
K
+
Na
+
zasadowica

Hipokaliemia <3,5
mEq/l
Utrata:
• drogą przewodu pokarmowego (odsysanie treści
żołądkowej, wymioty)
• drogą nerek (rzeczywista utrata, leki
moczopędne)
Objawy hipokaliemii:
• osłabienie mięśni
• zaburzenia rytmu serca (skurcze dodatkowe),
migotanie komór

Hipokaliemia <3,5
mEq/l
Dobowa podaż potasu - 40-60 mEq
W przypadku niedoboru:
• uzupełnianie doustne
• uzupełnianie dożylne:
• powoli 10 mEq/h (ból, arytmie)
• do żyły obwodowej roztwory o stężeniu
< 40 mEq/l

Hipokaliemia <3,5
mEq/l
• Jeżeli poziom K+ w osoczu przy
prawidłowym pH
wynosi :
• 3,5 mEq/l - należy uzupełnić 80 mEq
• 3,0 mEq/l - należy uzupełnić 200 mEq
• 2,5 mEq/l - należy uzupełnić 500 mEq

Hiperkaliemia >5,2
mEq/l
Przyczyny:
• przesunięcie z komórek do
przestrzeni pozakomórkowej
• utrudnione wydzielanie przez nerki
• niewydolność nadnerczy

Hiperkaliemia >5,2
mEq/l
H
+
H
+
K
+
Na
+
• Kwasica
• uraz, hemoliza, krwawienie z przewodu pokarmowego
• niedobór insuliny

Hiperkaliemia >5,2
mEq/l
Objawy hiperkaliemii:
• osłabienie mięśni
• zaburzenia przewodnictwa, asystolia
Objawy zaczynają się pojawiać, gdy
stężenie potasu w surowicy wynosi >
6,5 mEq/l, zawsze są obecne >8
mEq/l

Hiperkaliemia >5,2
mEq/l
Leczenie:
1. zwiększanie progu błonowego -
10% glukonian Ca 10 ml iv. W ciągu 3 minut,
powtórzyć po 5 minutach, działa 30 minut
2. stymulacja serca
3. przesunięcie do komórek:
• 500 ml 20% glukozy + 10j insuliny w ciągu 1h
• 1-2 amp. NaHCO
3
- u części chorych
nieskuteczne, wiąże jony Ca

Hiperkaliemia >5,2
mEq/l
Leczenie c.d.:
4. zwiększenie usuwania potasu:
• zwiększenie wydalania potasu drogą nerek -
furosemid
• zwiększenie wydalania potasu drogą
przewodu pokarmowego poprzez wymianą
K
+
na Na
+
- sulfonowana żywica
polistyrenowa - Kayexylate - Resonium
p.o. 30g/50 ml sorbitolu
p.r. 50g/200 ml sorbitolu ( ma pozostać 1h)
• hemodializa

Pierwotne zaburzenie
• pCO
2
(kwasica
oddechowa)
• pCO
2
(zasadowica
oddechowa)
• HCO
3-
(kwasica
metaboliczna)
• HCO
3-
(zasadowica
metaboliczna)
Kompensacja
• HCO
3-
(zasadowica
metaboliczna)
• HCO
3-
(kwasica
metaboliczna)
• pCO
2
(zasadowica
oddechowa)
• pCO
2
(kwasica
oddechowa)
Cel:
= K
pCO
2
HCO
3

Gazometria krwi tętniczej:
• pH 7,35-7,45
• pO
2
90-100 mmHg
DO
2
=Q x 1,3 x Hb x
SaO
2
• pCO
2
35-45 mmHg
• HCO
3
22-26mEq/l
Jak odczytać wynik
gazometrii?

Jak odczytać wynik
gazometrii?
Zaburzenie jest pierwotnie
metaboliczne jeżeli:
• pH jest nieprawidłowe
• jeżeli
lub
pH to pCO
2
pH to pCO
2

L
Jak odczytać wynik
gazometrii?
Kwasica metaboliczna
• przewidywane pCO
2
= 1,5 x
HCO
3
+ 8
Zasadowica metaboliczna
• przewidywane pCO
2
= 0,7 x
HCO
3
+ 20

L
Jak odczytać wynik
gazometrii?
Zaburzenie ma charakter
oddechowy jeżeli:
• pH jest nieprawidłowe
• jeżeli
lub
pH to pCO
2
pH to pCO
2
Kwasica metaboliczna
Luka anionowa A
-
- K
+
= Na
+
- (Cl
-
+ HCO
3
-
) = 12 mEq/l
Kwasica z normalną
luką anionową
Kwasica ze zwiększoną
luką anionową
• biegunka
• kompensacja zasadowicy
oddechowej
• łagodna niewydolność nerek
• kwasica mleczanowa
• ciężka niewydolność nerek
• kwasica ketonowa
• zatrucia salicylanami, metanolem,
glikolem etylenowym

Kwasica mleczanowa -
przyczyny
• dług tlenowy
• wstrząs septyczny
• niewydolność wielonrządowa
Leczenie:
przyczynowe
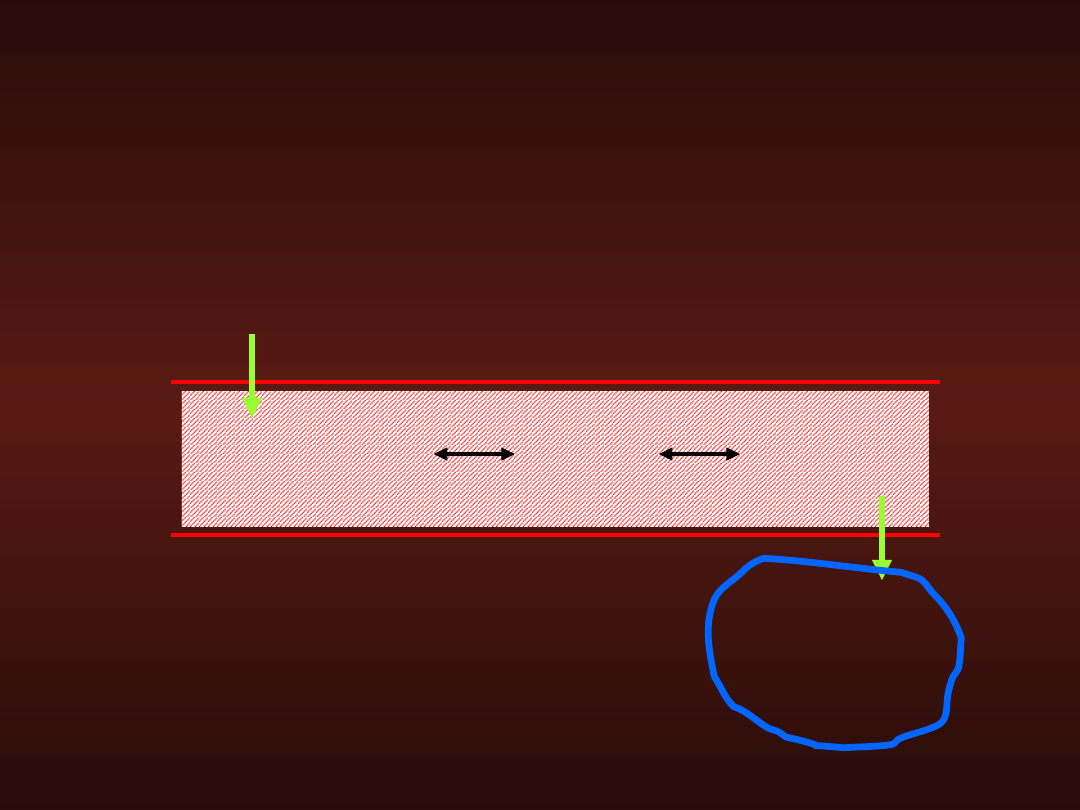
Kwasica metaboliczna a
leczenie
wodorowęglanami -
wady
H
+
H
+
H
+
+ HCO
3
-
H
2
CO
3
-
H
2
O
+
CO
2
Kwasica wewnątrzkomórkowa

Kwasica metaboliczna a
leczenie
wodorowęglanami -
wady
• hiperosmolarność
• wiązanie jonów Ca powodujące
zmniejszenie kurczliwości serca i
obniżenie RR
• nieskuteczność

Kwasica metaboliczna a
leczenie
wodorowęglanami
Wskazania do leczenia wodoroweglanami
• kwasica metaboliczna z pH < 7,2
• obniżenie RR pomimo wlewu katecholamin
Niedobór wodorowęglanów
0,4
x
m..c.
x
(żądane HCO
3
- aktualne
HCO
3
)
Podać połowę wyliczonego niedoboru w
postaci szybkiego wlewu, pozostałość
uzupełnić przez następne 6h.

Zasadowica metaboliczna
- najczęstsze przyczyny
Spowodowane utratą jonów Cl
-
• utrata soku żołądkowego
• leki moczopędne
Niezależne od Cl
-
• ECV

Dlaczego zasadowica jest
szkodliwa?
•
Zmniejsza dostarczanie tlenu
DO
2
=Q x 1,3 x Hb x SaO
2
• zmniejsza rzut serca
• przesuwa krzywą dysocjacji w lewo
(gorsze oddawanie tlenu w tkankach)
• zawsze powoduje kwasicę
wewnątrzkomórkową
• stymuluje glikolizę i
zwiększa
zapotrzebowanie na tlen

Zasadowica metaboliczna
Leczenie
:
•
Uzupełnianie chlorków
• deficyt Cl
-
0,4
x
m..c. (prawidłowe Cl
-
- aktualne Cl
-
)
• 1/2 deficytu należy podać przez 2-4h,
pozostały przez 24h
• uzupełnianie deficytu 0,9% NaCl (154
mEq/l), płynem żołądkowym
•
należy uzupełnić potas

Zasadowica metaboliczna
Leczenie ciężkiej zasadowicy:
• wlew do żyły centralnej 0,1N HCl
(100mEq/l H+)
• m..c.
X
0,5 (aktualne HCO
3
- mierzone
HCO
3
)
• prędkość wlewu 0,2 mEq/kg/h

Rola przewodu pokarmowego
w patogenezie zaburzeń
gospodarki wodno-elektrolitowej
i kwasowo-zasadowej
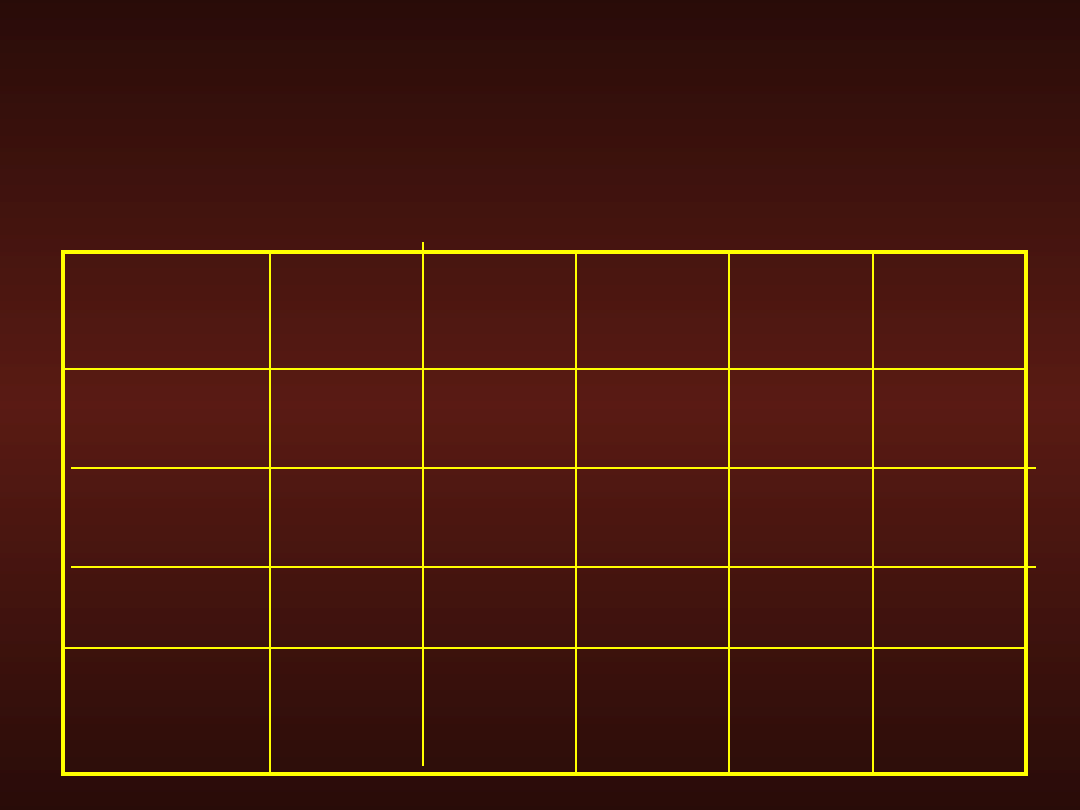
Objętość dobowa oraz stężenie poszczególnych
jonów w wydzielinach i wydalinach przewodu
pokarmowego
objętość
Na
K
Cl
HCO
3
ślina
sok
żołądkowy
żółć
sok
trzustkowy
1500
2500
500
700
10-15
20-90
130-155
110-150
15-20
5-15
4-8
3-10
10-40
20-150
80-110
40-90
2-10
-
25-40
70-110
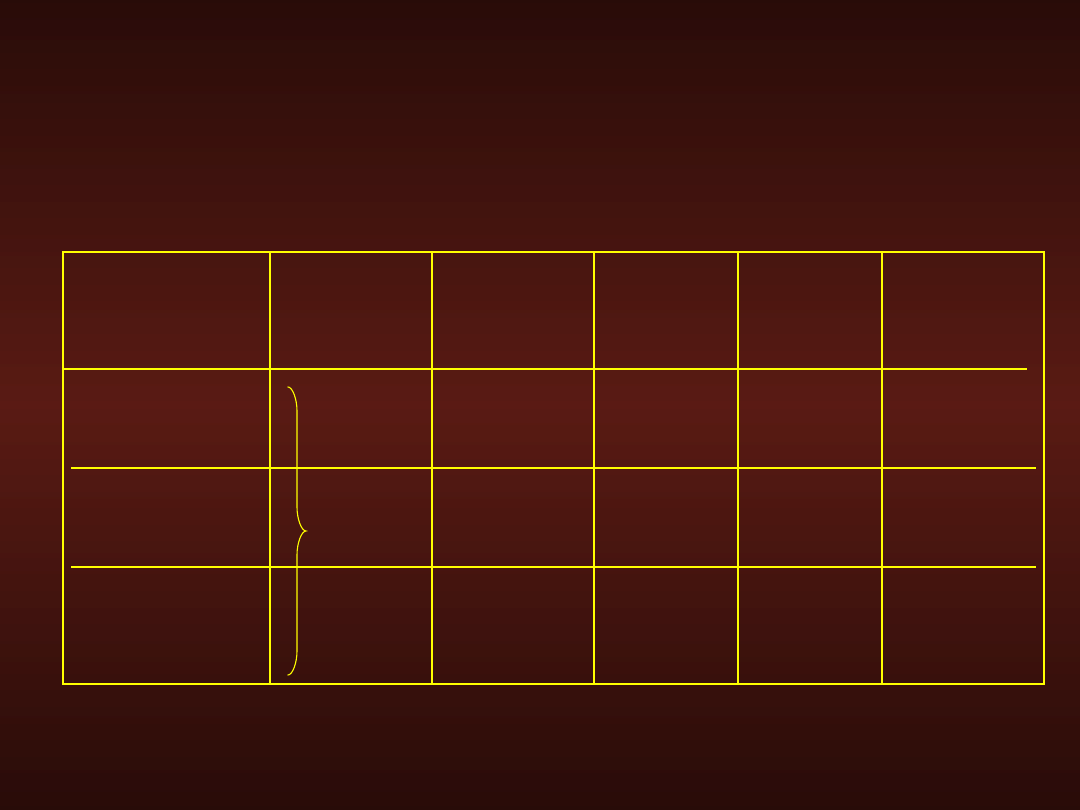
Objętość dobowa oraz stężenie poszczególnych
jonów w wydzielinach i wydalinach przewodu
pokarmowego
objętość
Na
K
Cl
HCO
3
Jelito czcze
Jelito kręte
Jelito grube
130-140
130-140
30-40
4
6
80-90
115-120
60-70
10-15
10-15
40-50
25-35
3 0
0
0
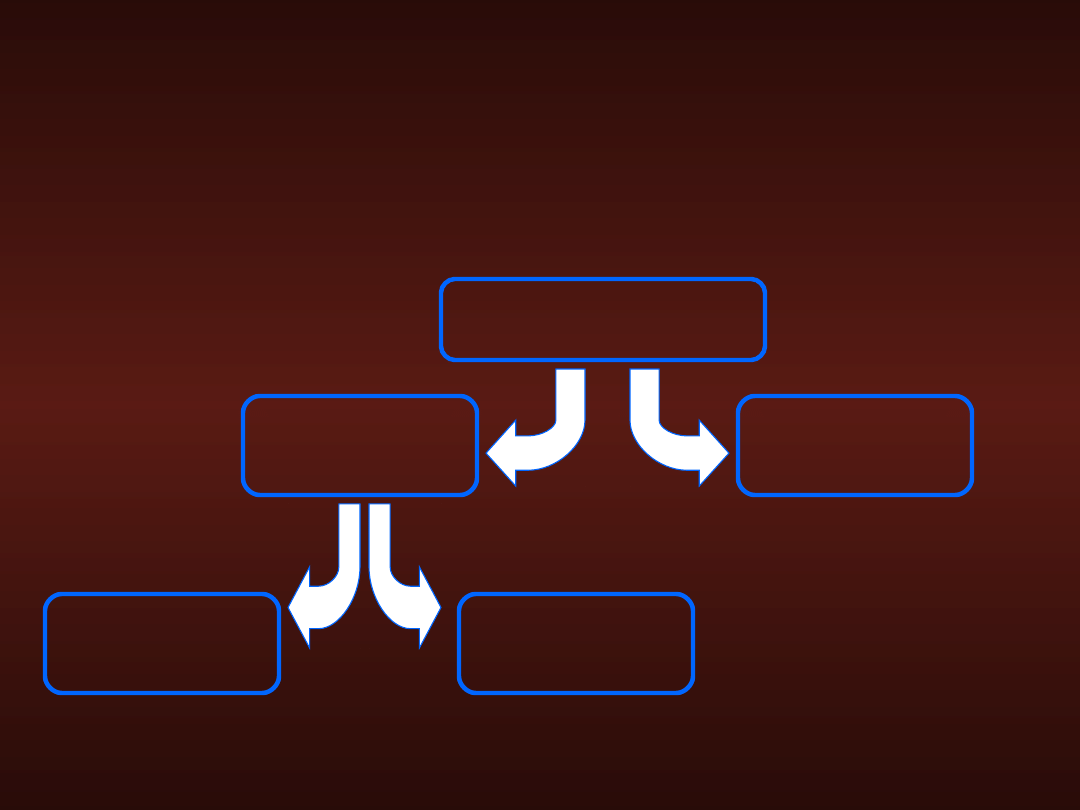
Wchłanianie w jelicie
Jelito czcze
2/3
Jelito kręte
1/3
Jelito cienkie
6/7
Wchłanianie wody
Jelito grube
1/7
Wchłanianie w jelicie
jelito
jelito
Jelito czcze
Jelito kręte
Na, Cl, K
z gradientem
osmotycznym
Na
H
HCO
3
Na
H
CO
2
H
2
O
H
2
CO
3
Na
H
HCO
3
Na
H
CO
2
H
2
O
H
2
CO
3
HCO
3
HCO
3
Cl
Cl
Objętość dobowa oraz stężenie poszczególnych
jonów w wydzielinach i wydalinach przewodu
pokarmowego
objętość
Na
K
Cl
HCO
3
Jelito czcze
Jelito kręte
Jelito grube
130-140
130-140
30-40
4
6
80-90
115-120
60-70
10-15
10-15
40-50
25-35
3 0
0
0

Wchłanianie w jelicie
Jelito grube
Na
Na
HCO
3
HCO
3
Cl
Cl
K
K
jelito
Objętość dobowa oraz stężenie poszczególnych
jonów w wydzielinach i wydalinach przewodu
pokarmowego
objętość
Na
K
Cl
HCO
3
Jelito czcze
Jelito kręte
Jelito grube
130-140
130-140
30-40
4
6
80-90
115-120
60-70
10-15
10-15
40-50
25-35
3 0
0
0

Wymioty
• zasadowica
• hipochloremia
• hipokaliemia
• hiponatremia
Biegunka
• kwasica
• hipokaliemia
• hiperchloremia
(utrata HCO
3
)
• hipernatremia

Mieszanka WHO
• Na - 90 mEq/l
• K - 20 mEq/l
• Cl - 80 mEq/l
• NaHCO
3
- 30 mEq/l
• glukoza - 111 mmol/l

Niedrożność
• Jelito czcze - utrata soku żołądkowego,
żółci, soku
trzustkowego,
zawartości jelita
• Jelito kręte - j.w.
Hipowolemia (utrata do „trzeciej
przestrzeni”, utrata Na, Cl, K, HCO
3

Niedrożność
Jelito grube
Ponieważ do okrężnicy dociera
zaledwie ok.500 ml treści,
niedrożność przez pewien czas
może nie wywoływać
poważniejszych zaburzeń.

Przetoki
•
Wysokie
- zasadowica,
hiponatremia
•
Wysokie bogate w żółć i sok
trzustkowy
- kwasica,
hiponatremia
•
Niskie
- kwasica, hipokaliemia

Lekceważąc zaburzenia wodno-elektrolitowe
i kwasowo-zasadowe sprawiamy,
że stan ogólny naszych pacjentów jest poważniejszy
niż by to mogło wynikać z ich choroby podstawowej.
Właściwe rozpoznanie zaburzeń jest
pomocne do wczesnego rozpoznania zarówno
powikłań jak i pogorszenia stanu chorego.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
Wyszukiwarka
Podobne podstrony:
Zaburzenia nerwicowe wyklad
Zaburzenia funkcji zwieraczy
Seminarium3 Inne zaburzenia genetyczne
Wstęp do psychopatologii zaburzenia osobowosci materiały
Zaburzenia rytmu serca
06 Psych zaburz z somatoformiczne i dysocjacyjne
zaburzenia zachowania t
Zabieg operacyjny zaburzenia homeostazy
Zaburzenia lękowe Neurobiologia lęku Terapia lęku
Zaburzenia widzenia obuocznego A Buzzeli 2007
W08 Patofizjologia zaburzeń gospodarki węglowodanowej
Zaburzenia ukł pozapiramidowego (1)
więcej podobnych podstron