
CZYNNIKI
KRWIOTWÓRCZE
CZYNNIKI KRWIOTWÓRCZE
GM-CSF
G-CSF
M-CSF
SCF
czynnik
komórek
macierzystyc
h
czynnik
stymulujący
tworzenie kolonii
granulocytów
czynnik
stymulujący
tworzenie kolonii
makrofagów
czynnik
stymulujący
tworzenie kolonii
granulocytów
i makrofagów
erytropoetyn
a
trombopoetyna
ligand
Flt3

CZYNNIK
KRWIOTWÓRCZ
Y
MIEJSCE
WYTWARZANIA
GŁÓWNA FUNKCJA
Erytropoetyna
nerki, wątroba
wytwarzanie erytrocytów
G-CSF
komórki endotelium,
fibroblasty, makrofagi
wytwarzanie neutrofili
Trombopoetyna
nerki, wątroba
wytwarzanie płytek krwi
M-CSF
fibroblasty, komórki
endotelium, makrofagi
wytwarzanie makrofagów i osteoklastów
SCF/ligand
receptora c-Kit
komórki zrębowe szpiku
komórki macierzyste, komórki progenitorowe
przeżycie/podział; różnicowanie komórek tucznych
Ligand Flt3
fibroblasty, kom. endotelium
b. wczesne komórki krwiotwórcze, czynnik
dojrzewania DCs
GM-CSF
limfocyty T, makrofagi,
komórki tuczne
wytwarzanie makrofagów i granulocytów, dojrzewanie
i aktywacja DCs
IL-3
limfocyty T, makrofagi
czynnik wzrostu komórek macierzystych i
progenitorowych linii mieloidalnej
IL-5
aktywowane limfocyty Th2
wytwarzanie eozynofilów
IL-6
aktywowane limfocyty T,
monocyty, fibroblasty,
komórki endotelium
stymulacja komórek progenitorowych, wytwarzanie
płytek krwi, wytwarzanie Ig w limfocytach B
IL-11
j.w.
pobudzenie komórek progenitorowych szpiku i
wytwarzania płytek krwi
IL-7
j.w.
przeżycie limfocytów T
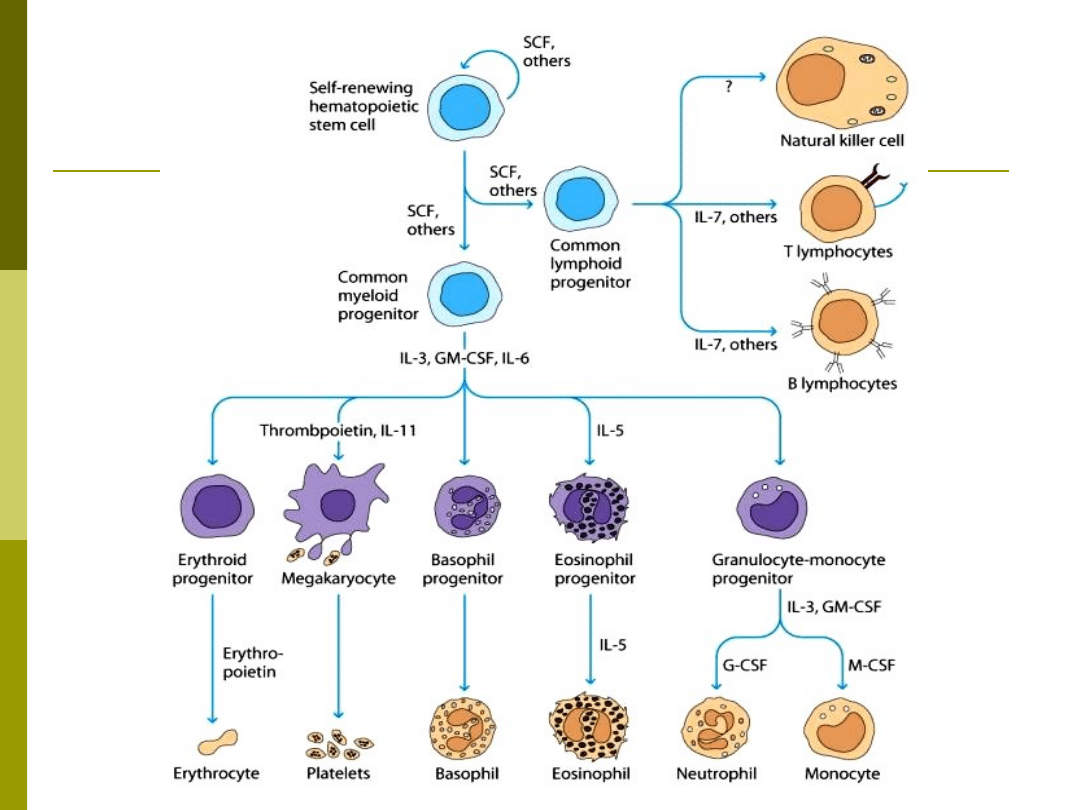
GM-CSF
Wpływ na komórki szeregu granulocytowo-
makrofagowego:
-zwiększa właściwości fagocytarne
-wzmaga wytwarzanie IL-1, IL-6, G-CSF, TNF
-zwiększa ekspresję cz. adhezyjnych
-zwiększa poziom receptorów dla fragmentów Fc
przeciwciał
Wpływ na funkcję dojrzałych limfocytów
-wzmaga cytotoksyczność komórek NK i LAK
GM-CSF i G-CSF
ZASTOSOWANIE KLINICZNE
GM-CSF: Leucomax, Leukine
G-CSF: filgrastim –Neupogen, lenograstim – Granocyte34,
pegfilgrastim – Neulasta
korekcja granulopenii po intensywnej chemioterapii
lub radioterapii
przyspieszenie regeneracji układu krwiotwórczego po
przeszczepieniu szpiku kostnego
mobilizacja komórek progenitorowych do krwi
obwodowej (autoprzeszczep)
leczenie zespołów mielodysplastycznych i cyklicznej
neutropenii
ERYTROPOETYNA
DZIAŁANIE:
pobudza erytropoezę
pobudza tworzenie płytek krwi
wpływa na wytwarzanie
przeciwciał przez komórki
plazmatyczne
wpływa na cytotoksyczność
komórek LAK
ZASTOSOWANIE KLINICZNE:
Eprex, Epogen, Procrit; Recormom
zmniejszenie niedokrwistości
w przebiegu niewydolności nerek
po chemioterapii nowotworów
po terapii AIDS z użyciem AZT
leczenie niedokrwistości w przebiegu
chorób przewlekłych, w zespołach
mielodysplastycznych
profilaktycznie u dawców krwi
zapobiegawczo przed planowanymi
operacjami chirurgicznymi, w
których przebiegu mogą utracić
znaczne ilości krwi
M-CSF
działa przede wszystkim na monocyty, makrofagi oraz ich
komórki progenitorowe
zwiększa ich właściwości żerne
stymuluje wytwarzanie cytokin TNF, IFN, IL-1, G-CSF
ZASTOSOWANIE KLINICZNE:
próby w leczeniu czerniaka oraz w przebiegu innych
nowotworów, a także w leczeniu grzybic narządowych
TROMBOPOEZA
IL-3
IL-6
IL-11 (stosowana w celu
korekcji trombocytopenii w
przebiegu niektórych chorób
lub po toksycznych terapiach)
Trombopoetyna
Trombopoetyna: zastosowania
kliniczne:
•
Chemioterapia guzów litych i białaczek
•
Radioterapia
•
Przeszczepianie szpiku
•
Niedokrwistość aplastyczna
•
Stany niewydolności hematopoezy
•
Transfuzjologia (magazynowanie
płytek, produkcja in vivo)
•
Zespoły mielodysplasyczne
•
Małopłytkowość w AIDS
•
Immunotrombocytopenia
•
Chirurgia serca
•
Chirurgia ogólna
SCF = ligand receptora c-Kit
wpływa na bardzo młode, multiotencjalne komórki macierzyste
krwiotworzenia
czynnik wzrostu komórek tucznych oraz melanocytów
aktywuje cytotoksyczność limfocytów
wykazuje działanie przeciwnowotworowe
Ligand Flt3 (Flt3L)

INTERFERONY
I – typu
α
- wytwarzana przez
aktywowane wirusem
leukocyty
β
- fibroblasty
κ
-keratynocyty
ω- leukocyty
II – typu
γ
-
wytwarzany przez:
• limfocyty T traktowane
antygenami, cytokinami lub
mitogenami,
• komórki NK pobudzone
cytokinami,
• komórki NKT
• aktywowane makrofagi /w
niewielkich ilościach/

INTERFERONY
IFN-α/β
IFN-γ
Lokalizacja
na
chromosomi
e
9
12
Pochodzenie wszystkie kom.
jądrzaste, głównie
fibroblasty, makrofagi,
kom. dendrytyzne
limfocyty Th1 i kom.
NK, limfocyty T CD8
+
i
γδ
Indukcja
przez
wirusy, inne cytokiny
(IL-1, TNF-α), niektóre
wewkomórkowe
bakterie i pierwotniaki
antygeny
Funkcje
aktywność
przeciwwirusowa,
zwiększa ekspresję
MHC klasy I, hamuje
proliferację komórek
aktywność
przeciwwirusowa,
zwiększa ekspresję
MHC klasy I i II,
aktywuje makrofagi
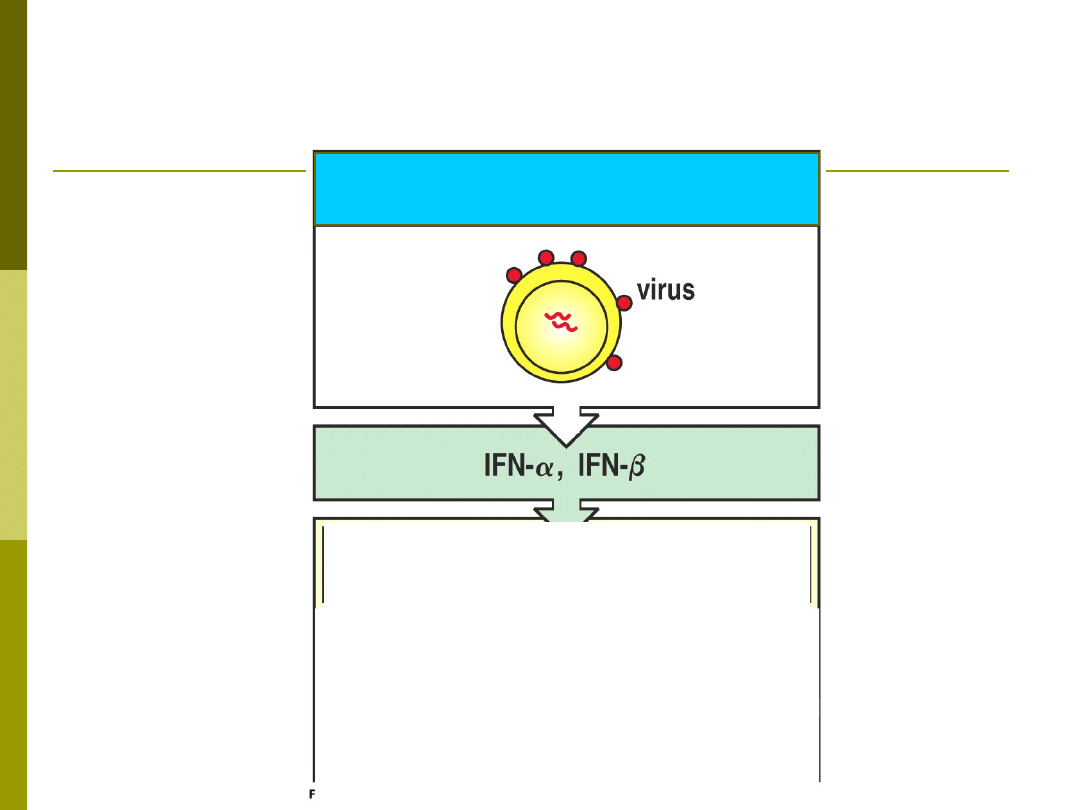
INTERFERON- i
INTERFERON-
Większość
komórek może
wytwarzać
IFN- i IFN-
w odpowiedzi
na zakażenie
wirusowe.
Zakażona wirusem komórka
gospodarza
indukuje oporność na
replikcję wirusa we wszystkich
komórkach
zwiększa ekspresję MHC I i
prezentację antygenu na
wszystkich komórkach
pobudza komórki NK do
zabijania komórek zakażonych
wirusem
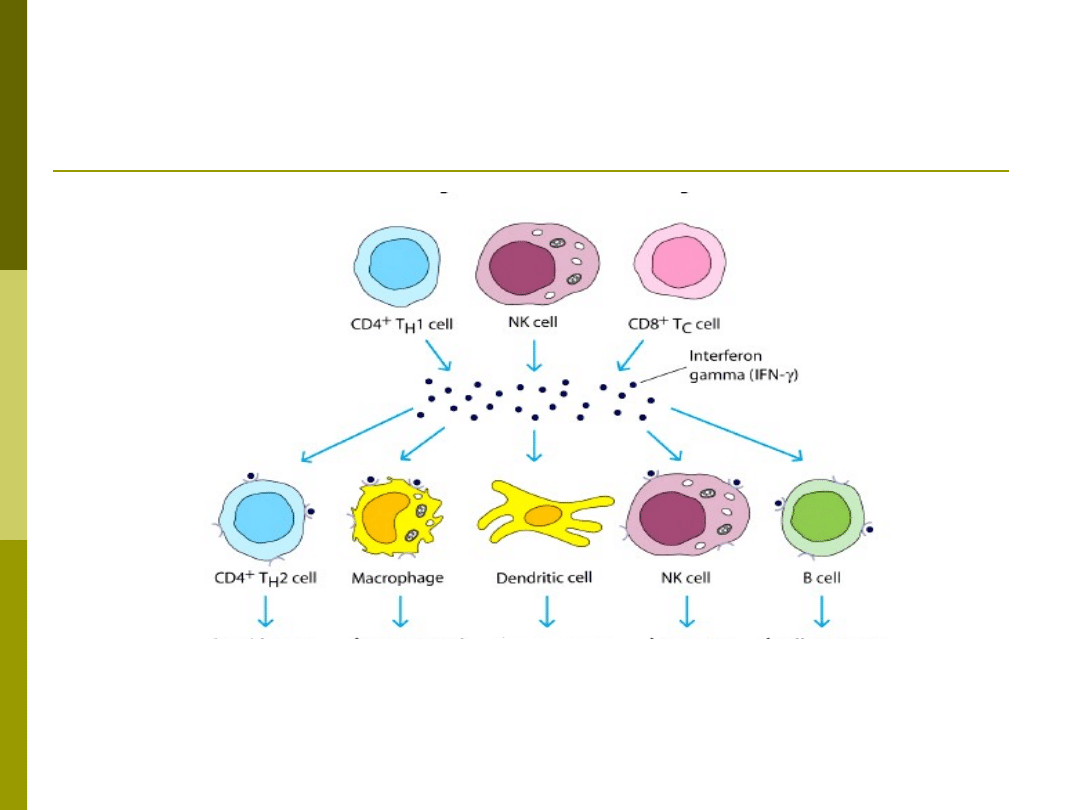
IFN- – silny aktywator
Proliferacj
a
Wytwarzan
ie IL-4 i IL-5
Ekspresja MHC
II
Aktywność
bakteriobójcza
Ekspres
ja
MHC II
Aktywnoś
ć
cytotoksyc
zna
Różnicowanie
Wytwarzanie
przeciwciał (
IgG2a;
IgE i IgG1)
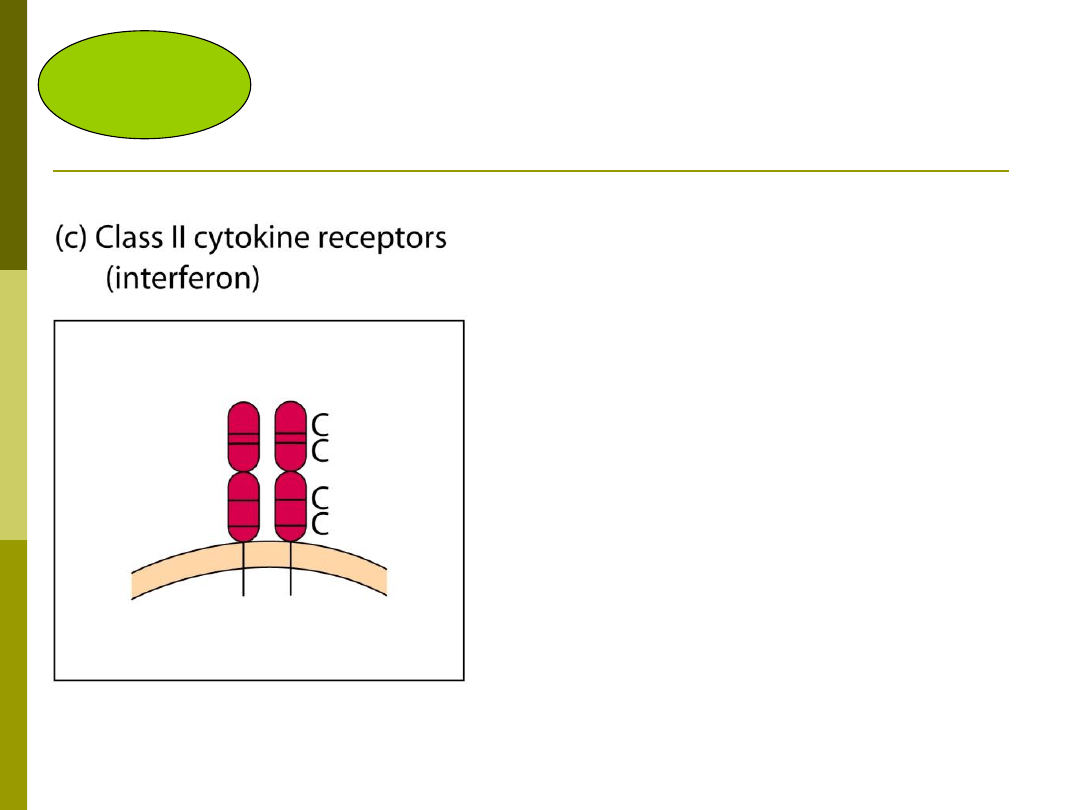
Receptory dla interferonów
•heterodimery
•dwie różne podjednostki
• interferony , i wiążą
się z tym samym
receptorem zbudowanym z
podjednostek IFNAR-1 i
IFNAR-2
•IFN-g wiąże się z
receptorem, w skład
którego wchodzą
podjednostki IFNGR-1 i
IFNGR-2
IFN
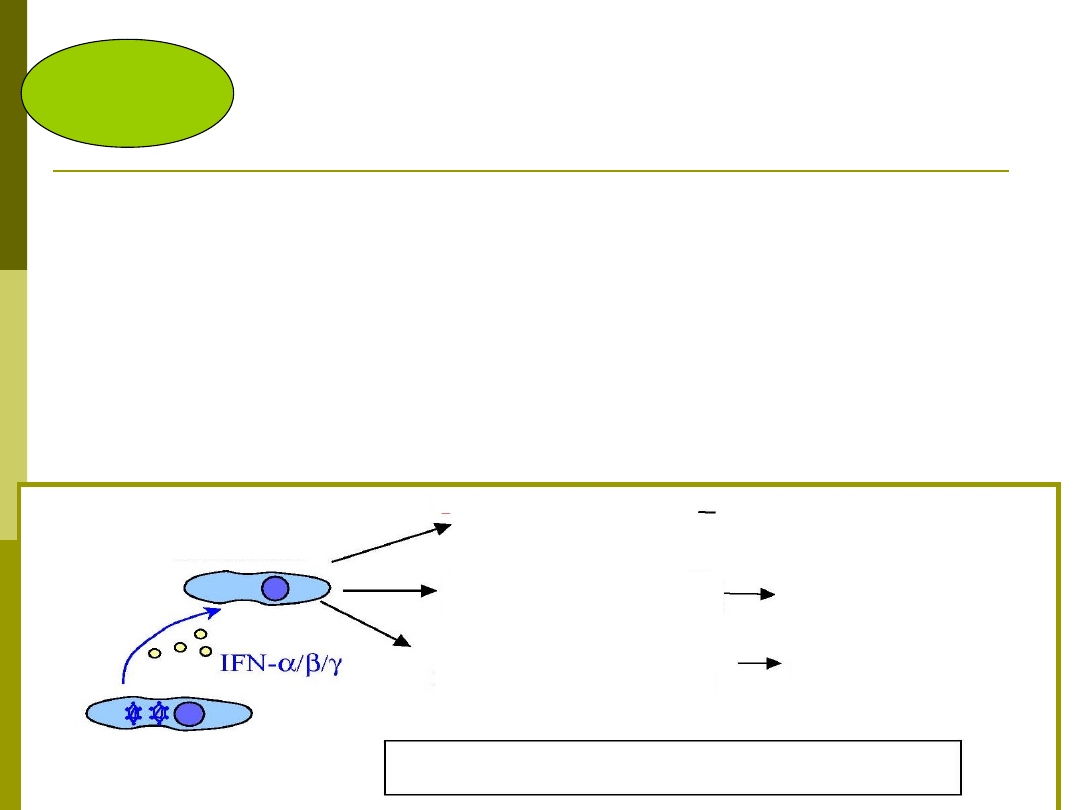
Działanie przeciwwirusowe
Interferony
nie wykazują bezpośredniego działania przeciwwirusowego,
oddziałują na komórki indukując w nich powstawanie czynników
przeciwwirusowych i „stanu gotowości przeciwwirusowej”:
syntezę
syntetazy oligoizoadenylanowej
powstanie oligonukleotydów
adenylanowych aktywujących RNazę L (w obecności dwuniciowego RNA)
ekspresję
deaminaz adenozynowych
dezaminacja adenozyny w obrębie
dwuniciowego RNA powstają inozyny
kinazę białkową R
autofosforylacja, fosforylacja podjednostki czynnika
inicjującego syntezę białka (kinaza R jest aktywna w obecności
dwuniciowego RNA, dlatego działa tylko w komórkach zakażonych przez
określone wirusy)
zakażona
komórka
zdrowa
komórka
zahamowanie szerzenia się wirusów
wirusowy RNA
- niefunkcjonalny
zahamowanie translacji
i syntezy białek wirusowych
rozkład wirusowego mRNA
oraz komórkowego
jednoniciowego RNA
syntetaza
oligoizoadenylan
owa
deaminazy
adenozynowe
kinaza białkowa R
IFN

Działanie przeciwwirusowe
Interferony nie wykazują bezpośredniego działania
przeciwwirusowego, ale oddziałują na inne komórki
indukując w nich powstawanie czynników
przeciwwirusowych i „stanu gotowości przeciwwirusowej”:
aktywują gen Mx, produkt tego genu hamuje drastycznie
replikację wirusa grypy i niektórych innych wirusów RNA
wzmagają aktywność komórek cytotoksycznych
(Tc, NK i K)
wzmagają aktywność cytotoksyczną i fagocytarną
makrofagów
IFN

Wpływ na układ
odpornościowy
cytotoksyczności :
limfocytów Tc, komórek K i
NK
ekspresji MHC (MHC klasy
I , MHC klasy II przez IFN-γ)
ekspresji niektórych
cząsteczek i receptorów
powierzchniowych np. CD80,
FcR
aktywacja makrofagów
fagocytozy
ekspresji innych cytokin:
IL-1, IL-6, TNF, IP10, MIG
IFN-γ najsilniej oddziałuje na
układ odpornościowy
Wpływ na proliferację
i różnicowanie komórek
inhibitory krwiotworzenia
(najsilniej
antyproliferacyjnie działa
IFN-γ)
IFN-γ podejrzewany o udział
w patogenezie
niedokrwistości aplastycznej
IFN

Działanie
przeciwnowotworowe
Działanie bezpośrednie:
Hamowanie proliferacji i pobudzanie
różnicowania komórek
nowotworowych
Modulują onkogeny komórkowe (C-
myc, c-fos, c-H ras) – wydłużenie
cyklu podziałowego
Oddziaływanie cytotoksyczne na
komórki nowotworowe
Działanie pośrednie:
Zwiększanie ekspresji
antygenów nowotworowych
Hamowanie powstawania naczyń
nowotworowych
Wpływ interferonów na układ
odpornościowy (aktywacja
cytotoksycznych mechanizmów
komórkowych, wzmożone
wytwarzanie cytokin o działaniu
przeciwnowotworowym np. TNF,
wywyołują lizę komórek
nowotworowych z udziałem
dopełniacza i na drodze ADCC)
IFN

Zastosowanie terapeutyczne
Przewlekła białaczka szpikowa
Białaczka włochatokomórkowa
T-komórkowy chłoniak skórny
Szpiczak mnogi (leczenie podtrzymujące u chorych, u których
uzyskano obiektywną remisję w wyniku chemioterapii
indukcyjnej)
Chłoniaki nieziarnicze o małym stopniu złośliwości prz.
pokarmowego
Mięsak Kaposiego w przebiegu AIDS
Czerniak złośliwy
Przewlekłe WZW B
Przewlekłe WZW C
Zaawansowane stadium raka nerki
Rakowiak z przerzutami do węzłów chłonnych lub do wątroby
oraz z "zespołem rakowiaka"
IFN-(Intron A, Roferon A, Alferon
N):
Wskazania ustalone:
IFN

Zastosowanie terapeutyczne
Rak pęcherza (podanie dopęcherzowe)
Rak jajnika (podanie dootrzewnowe)
Rak j. grubego
Neuroendokrynne nowotwory złośliwe
Nadpłytkowość
Czerwienica prawdziwa
Samoistna mielofibroza w fazie proliferacyjnej
Samoistna mieszana krioglobulinemia typu II
WZW D
AIDS (we wczesnych stadiach choroby w połączeniu z
azydotymidyną)
Zakażenia narządów płciowych HPV
Brodawczaki krtani
Zespół hipereozynofilowy
Układowa mastocytoza
Kłykciny kończyste
IFN-(Intron A, Roferon A, Alferon N):
Wskazania potencjalne:
IFN

Zastosowanie terapeutyczne
IFN- (Betaseron, Avonex, Rebif):
Stwardnienie rozsiane
IFN-(Imukin, Actimmune):
u dzieci z przewlekłą chorobą ziarniniakową
gruźlica
leiszmanioza trzewna
mononukleoza zakaźna
przewlekłe zakażenie wirusem Epstein-
Barra
rak nerki
rak jajników
RZS
IFN

Objawy uboczne
Podwyższona temp. ciała
Przyspieszona czynność serca
Bóle głowy
Bóle mięśniowe i kostne
Objawy ze strony ukł. pokarmowego
Objawy ze strony CUN
Zaburzenia funkcji nerek i krwiotworzenia
IFN
CHEMOKINY
Podobne strukturalnie do siebie cytokiny oddziałujące
chemotaktycznie, a często również aktywująco na różne
populacje leukocytów
Charakteryzują się małą masą cząsteczkową
Odgrywają kluczową rolę w:
Reakcjach zapalnych
Odporności przeciwzakaźnej
Krwiotworzeniu
Limfopoezie
Odpowiedzi przeciwnowotworowej
Odrzucaniu przeszczepów
Wytwarzane głównie przez monocyty i makrofagi
Prozapalne (indukowane)
– wytwarzane w trakcie reakcji
zapalnych
Limfoidalne (konstytutywne lub homeostatyczne)
– regulują
krążenie różnych populacji limfocytów, sterują migracją DCs
z tkanek obwodowych do obwodowych narządów
limfatycznych, uczestniczą w przemieszczaniu się
dojrzewających tymocytów do odpowiednich regionów grasicy
Ze względu na liczbę cystein oraz liczbę aminokwasów między
dwoma pierwszymi cysteinami wyróżniamy 4 podrodziny
C
(γ): limfotaktyna α i β
CC
(β) – oddziałują na limfocyty, monocyty, komórki
tuczne, eozynoile
CXC
(α) – oddziałują głównie na neutrofile i limfocyty
CX3C
(δ): fraktalkina (neurotaktyna)
CHEMOKINY
Wytwarzanie indukowane jest przez cytokiny
prozapalne: TNF, IL-1 oraz IFN- γ
Wydzielanie większości chemokin hamuje IL-10
(z wyjątkiem HCC-4) i TGF- β
Interferowanie z działaniem chemokin jest jednym
z częściej wykorzystywanych mechanizmów
obronnych drobnoustrojów
CHEMOKINY
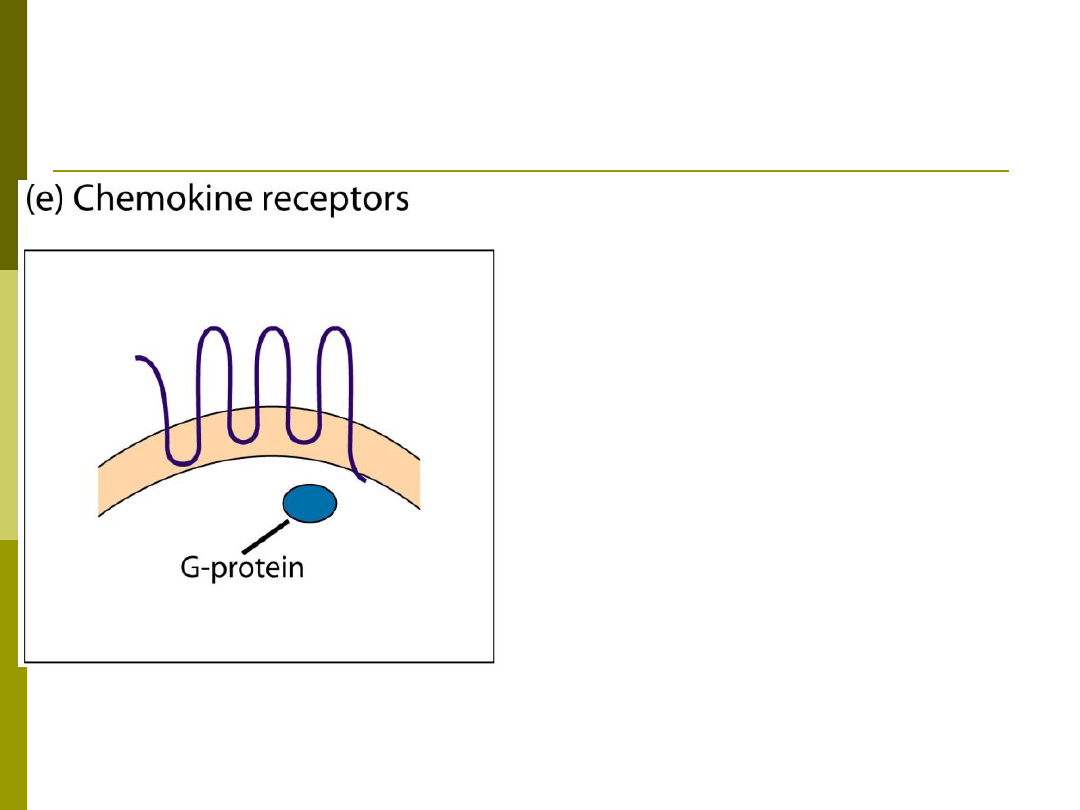
RECEPTORY DLA
CHEMOKIN
• Rodopsynopodobne receptory
związane z białkiem Gi,
przechodzące 7x przez błonę
komórkową
• Zidentyfikowano 20
receptorów dla chemokin
• jednym z mechanizmów
regulujących wrażliwość na
chemokiny jest
desensytyzacja ich
receptorów tzn. po
zadziałaniu chemokiny jej
receptor traci wrażliwość na
dalsze jego pobudzanie
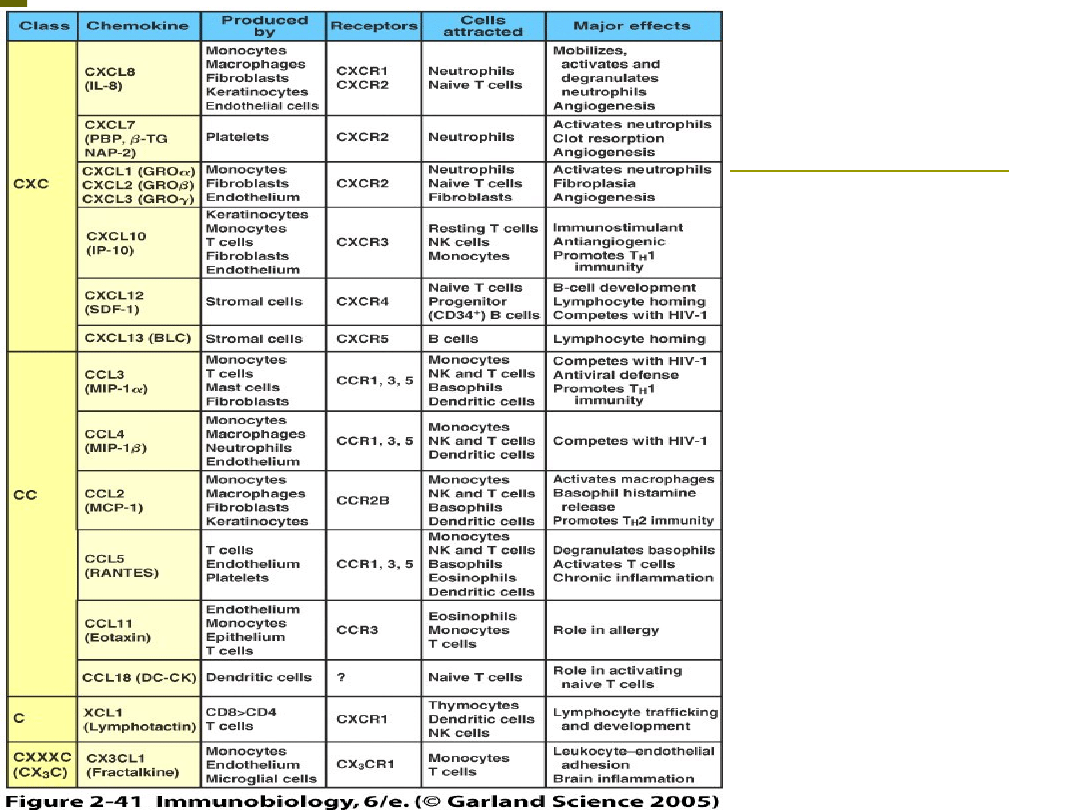
PMo anty-IL-8
-
łuszczyca, RZS i
inne choroby
zapalne
DZIAŁANIE CHEMOKIN
Mielopoeza i limfopoeza
MIP-1 i MIP-1 – różnicowanie
granulocytów i monocytów
SDF-1 – proliferacja prekursorów
limfocytów B
Aktywacja komórek
IL-8 – zwiększa fagocytozę i
bakteriobójcze właściwości
neutrofilów
MCP-1, MIP-1 - aktywują
monocyty
Eotaksyny, MIP-1 , RANTES –
aktywują eozynofile
MIP-1RANTES – proliferacja
limf. T, aktywują cytotoksyczność
Tc i NK, eozynofili do zmian
zapalnych w oskrzelach i płucach
Angiogeneza – IL-8, ENA-78, GCP-2,
GRO-, GRO-
Działanie antyangiogenne – PF4,
IP10, MIG
Odporność przeciwzakaźna
MIP-1udział w
odpowiedzi przeciw wirusowi
grypy
MIP-1RANTES, SDF-1 –
hamują infekcję komórek
przez wirus HIV
Odrzucanie przeszczepów
Formowanie nacieków
zapalnych w wielu chorobach
autoimmunizacyjnych
IL-8, MCP-1, MIP-1, MIP-2 –
RZS
Patogeneza chorób alergicznych
Eotaksyna, RANTES, MCP-2,
MCP-3, MCP-4 i MIP-1 -
chemotaksja
NADRODZINA CZĄSTECZEK CZYNNIKA
MARTWICY NOWOTWORU
TNF
i
limotoksyny
Tumor necrosis
factor
LIGHT
FasL
TRAIL
TNF-related
apoptosis
inducing
ligand
TRENCE
TNF related
activation-
induced
cytokine (ligand
osteoprotegryny
)
TNF I LIMFOTOKSYNY
Wyróżniamy:
TNF-α (TNF)
TNF- β (limfotoksyna α)
LT- β
TNF wytwarzany jest przede wszystkim przez monocyty i
makrofagi, natomiast źródłem zarówno TNF jak i LT-α są
limfocyty
Najsilniejszym bodźcem do wytwarzania TNF jest LPS ścian
bakteryjnych (w mniejszym stopniu GM-CSF, M-CSF oraz sam
TNF)
Istnieją 2 typy receptorów:
TNFR1 (p55, CD120α)-wszystkie kom. jądrzaste
TNFR2 (p75, CD120β)- leukocyty, kom. śródbłonka
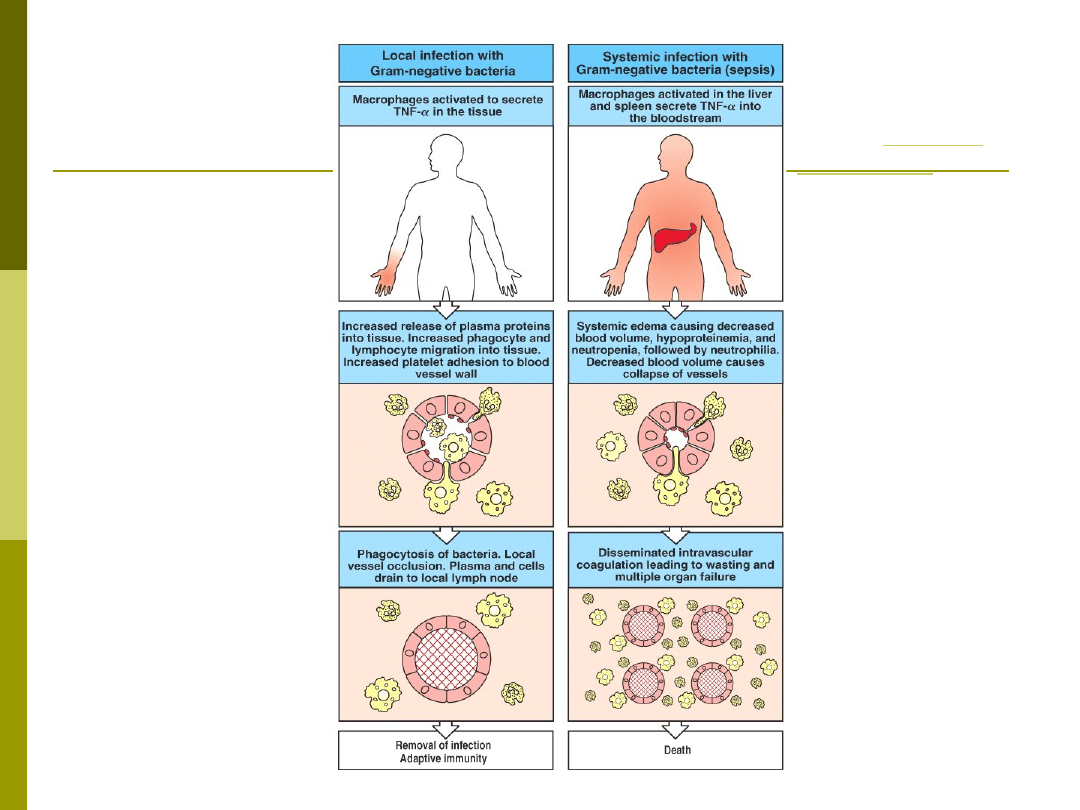
Układowo,
wysokie dawki
TNF
wstrząs
septyczny,
niewydolność
wielu narządów,
śmierć
W stanach
przewlekłych
długotrwałe
wydzielanie TNF
zubożenie tkanki
tłuszczowej w
zapasy lipidów
kacheksja
Miejscowo, TNF
zapalenie.
Patogenna rola TNF
w schorzeniach
autoimmunizacyjnyc
h, w odrzucaniu
przeszczepów, w
reakcji przeszczep
przeciw
gospodarzowi, w
AIDS
TNF odpowiedzialny
częściowo za
insulinooporność w
cukrzycy,
powstawanie zmian
miażdżycowych,
zapalenie trzustki,
alkoholowe
uszkodzenie wątroby
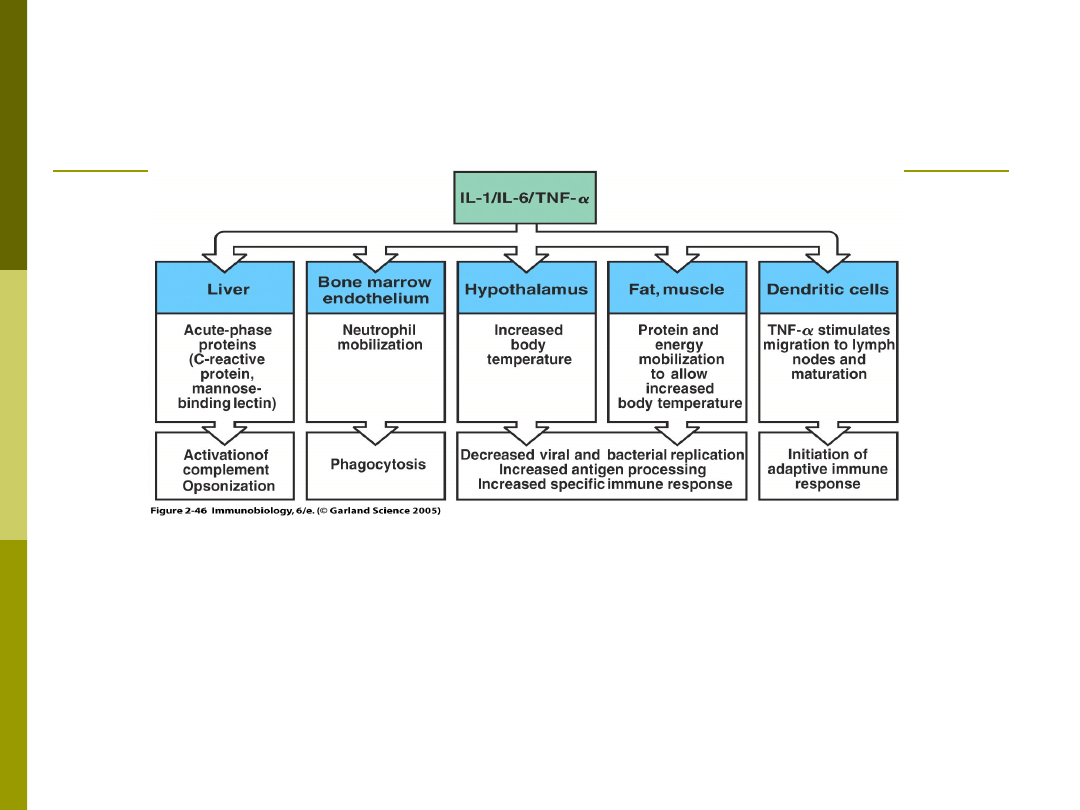
TNF A UKŁAD
ODPORNOŚCIOWY
Główna cytokina odpowiedzi zapalnej i immunologicznej
Wraz z IL-6 wzmaga proliferację i różnicowanie limfocytów B
Wraz z IL-2 i IL-6 wzmaga proliferację i różnicowanie limfocytów T
Wraz z IL-2 stymuluje cytotoksyczność monocytów, makrofagów, komórek NK
oraz powstawanie komórek LAK i limfocytów Tc
Na monocyty i makrofagi oddziałuje w sposób endo-,
para- i autokrynowy
działanie chemotaktycznie na monocyty i neutrofile
Aktywuje neutrofile, zwiększając ich właściwości
fagocytarne, bakteriobójcze i cytotoksyczne oraz
przyspiesza ich uwalnianie ze szpiku
Aktywuje cytotoksyczność eozynofilów wobec
pierwotniaków
Indukuje uwalnianie:
z makrofagów: IL-1, IL-6, GM-CSF, G-CSF, M-CSF,
PDGF, NGF, EGF, PAF, IFN- β, prostaglandyn i
leukotrienów
z limfocytów IFN-γ
Indukuje ekspresje MHC I oraz MHC II (wraz z IFN-γ)
TNF a UKŁAD
ODPORNOŚCIOWY
DZIAŁANIE
PRZECIWNOWOTWOROWE TNF
Działa bezpośrednio na kom. nowotworowe
indukuje apoptozę
hamuje proliferację
indukuje różnicowanie
Indukuje zmiany w naczyniach krwionośnych nowotworu
Pobudza odpowiedź immunologiczną przeciwnowotworową
ZASTOSOWANIE KLINICZNE
INHIBITORÓW TNF
Przeciwciała przeciw (TNF-α)
Infliximab
(Remicade) – chimeryzowane, mysio-ludzkie
przeciwciało monklonalne klasy IgG 1
Etanercept
(Enbrel) – białko fuzyjne, składające się z
pozakomórkowej części ludzkiego receptora TNFp75
powiązanego z częścią Fc ludzkiej IgG 1
Adalimumab
(D2E7) – ludzkie przeciwciało
monklonalne, wytworzone metodą inżynierii
genetycznej (lek zarejestrowany w Stanach
Zjednoczonych i krajach Europy Zachodniej)
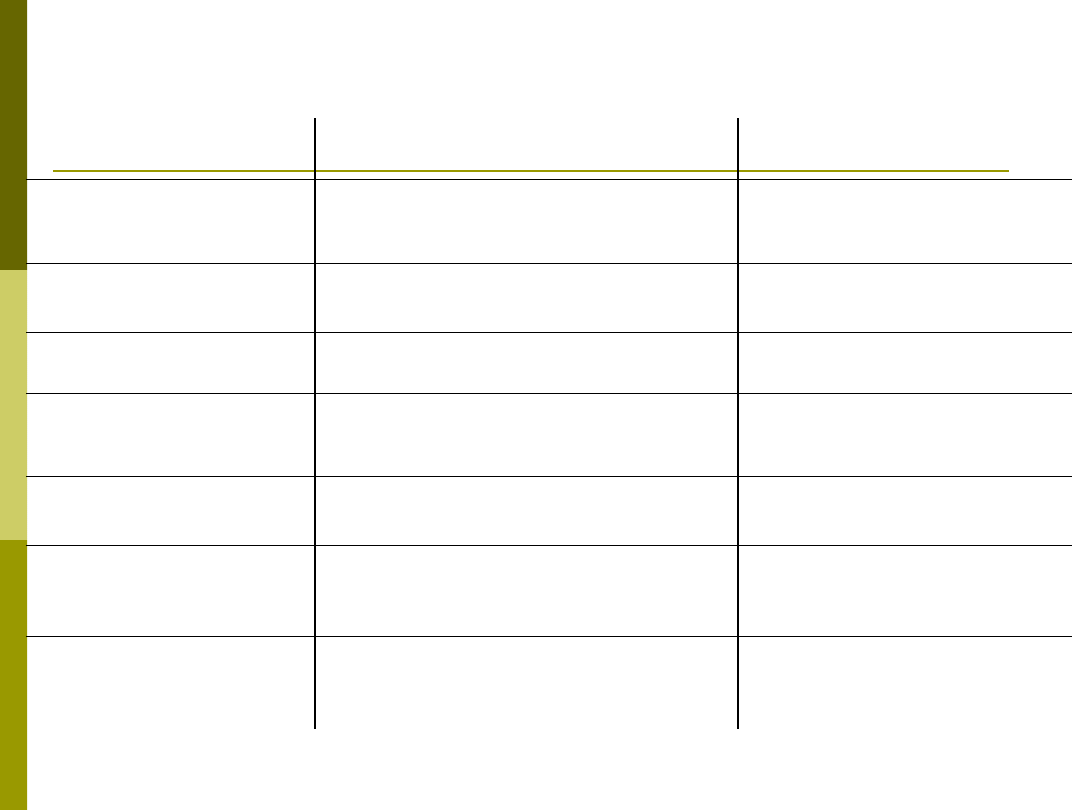
Infliximab i etanercept - różnice w budowie i mechanizmie
działania
Infliximab
(Remicade)
Etanercept
(Enbrel)
Charakterystyka
molekularna
Chimeryzowane mysio-ludzkie
monoklonalne przeciwciało IgG1
(ludzka część stała; mysia region
zmienny)
Białko fuzyjne; ligand
wiążący TNFRp75 kd
powiązany z częścią FcIgG1
Waga molekularna
~ 149 kd
~ 150 kd
Okres półtrwania
9 dni
4 dni
Mechanizm działania
Neutralizuje biologiczną aktywność
TNF-α; wiążąc rozpuszczalny
(monomery i trimery) i związany z
błoną komórkową TNF-α
Wiąże 2 cząsteczki TNF
działając jako "fałszywy"
receptor (decoy)
Zdolność wiązania TNF-β
(limfotoksyna)
nie
tak
Liza komórek zdolnych do
sekrecji TNF-α
(obwodowych monocytów,
makrofagów, neutrofili)
tak
nie
Indukcja apoptozy
(monocytów krwi
obwodowej i limfocytów w
lamina propria)
tak
nie
Wskazania
do
leczenia
Infliximabem
i
Etanerceptem
Infliximab (Remicade)
Etanercept (Enbrel)
•
Choroba Crohna (CD)
Postać aktywna, oporna
na inne terapie; przetoki
w CD
•
RZS, aktywne, oporne na
leczenie Mtx
(terapia skojarzona z
Mtx)
•
zesztywniające zapalenie
stawów kręgosłupa
(ZZSK)
•
RZS, aktywne
Terapia skojarzona z
Mtx
Monoterapia we
wczesnym RZS
•
Młodzieńcze idiopatyczne
zapalenie stawów
aktywne, postać
wielostawowa
•
Łuszczycowe zapalenie
stawów, aktywne
•
zesztywniające zapalenie
stawów kręgosłupa
(ZZSK)
Próby kliniczne:
różne postacie zapalenia naczyń, choroba Stilla u
dorosłych, zespół Sjögrena, zapalenie wątroby typu C, zapalenie
błony naczyniowej oka, zapalenie wielomięśniowe i skórno-
mięśniowe, SLE i stwardnienie rozsiane
DZIAŁANIA NIEPOŻĄDANE
Infekcje (górnych dróg
oddechowych, zapalenie oskrzeli,
zapalenie pęcherza, infekcje
skórne)
Ciężkie infekcje (zapalenie płuc,
zapalenie tkanki łącznej,
infekcyjne zapalenie stawu,
posocznica)
Trombocytopenia
Anemia
Leukopenia
Pancytopenia
Niedokrwistość aplastyczna
Reakcje alergiczne
Powstawanie autoprzeciwciał
Ciężkie reakcje
alergiczne/anafilaktyczne (w tym
obrzęk naczynioruchowy, skurcz
oskrzeli)
Drgawki
Rzadkie przypadki demielinizacji
OUN
Świąd
Pokrzywka
Reakcje w miejscu wstrzyknięcia
Gorączka
Przypadki zaostrzenia
zastoinowej niewydolności serca
Podostry skórny toczeń
rumieniowaty
Toczeń rumieniowaty przewlekły
Zaspół toczniopodobny
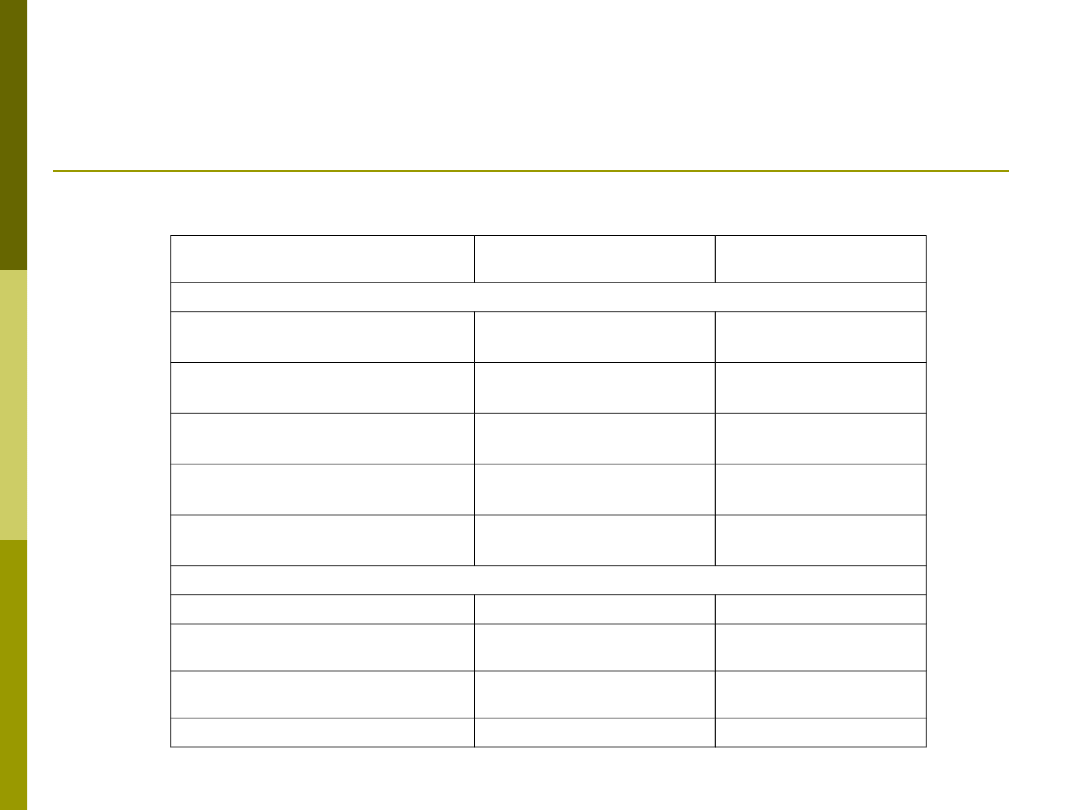
Ciężkie objawy niepożądane i autoprzeciwciała u chorych
leczonych infliximabem i etanerceptem
Objawy niepożądane
Infliximab
(Remicade)
Etanercept
(Enbrel)
CIĘŻKIE INFEKCJE
Mycobacterium tuberculosis (19)
(dane z 11 mies. 2001r.)
117/100 tys lecz./rok
16/100 tys. lecz./rok
Histoplasma capsulatum (21)
(dane z 7 mies. 2001r.)
16/100 tys.lecz./rok
1/100 tys. lecz./rok
Listeria monocytogenes (30)
(dane z 2002r.)
8/82 tys. lecz./rok
b.d.*
Zespół demielinizacyjny (24)
(dane z 2001r.)
2/100 tys. lecz./rok
18/100 tys. lecz./rok
Zespoły limfoproliferacyjne (5)
(dane z 19 mies. 2000 i 2001r.)
7/100 tys. lecz./rok
19/100 tys. lecz./rok
AUTOPRZECIWCIAŁA
ANA (28)
20-80%
11%
dsDNA (6, 28) (w klasach IgM i
IgA)
11-21%
13%
P-ciała antykardiolipidowe
(ACLA)(1,8,10)
13,5%
17%
HACA (antychimeryczne)(1,28)
8,5%
3%
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
Wyszukiwarka
Podobne podstrony:
CZYNNIKI KRWIOTWÓRCZEost
biochemia III, Czynniki warunkujące aktywność enzymów
CZYNNIKI KRWIOTWÓRCZE, Uczelnia, imunny
biochemia III;], Czynniki warunkujące aktywność enzymów
Misztal, Styka (red ) Stare i nowe struktury społeczne w Polsce Tom III Czynniki miastotwórcze st
Działanie czynników środowiskowych(1), 1.Lekarski, III rok, Patofizjologia, Materiały ŚUM
III wykład czynniki zagrożenia w laboratorium, Analityka Medyczna UMB, III, Analityka Ogólna, Wykład
Krwiotwórczy 2(1), STOMATOLOGIA, III ROK, Patomorfologia
Psychologiczne czynniki mające znaczenie w relacji pacjent - personel medyczny, studia ratownictwo,
Substytucja czynników produkcji wykład III, Ekonomika
Czynniki ryzyka nowotworu jądra, Pielęgniarstwo licencjat cm umk, III rok, Geriatria i pielęgniarstw
Czynniki wplywajace na zdrowie czlowieka 2, Studia, Turystyka i rekreacja, semestr III, Wychowanie z
Czynniki zjadliwosci gronkowca, Szkoła, III rok, interna głównie ''P
Czynniki fizyczne WORD, medycyna, III rok, patofizjologia
CZYNNIKI FIZYCZNE ODDZIALUJACE NA USTROJ WORD, medycyna, III rok, patofizjologia
czynniki leczące w psychoterapii część III opracowanie
Działanie czynników środowiskowych(1), 1.Lekarski, III rok, Patofizjologia, Materiały ŚUM
więcej podobnych podstron