
CZYNNIKI
KRWIOTWÓRCZE
CZYNNIKI KRWIOTWÓRCZE
GM-CSF
G-CSF
M-CSF
SCF
czynnik
komórek
macierzystyc
h
czynnik
stymulujący
tworzenie kolonii
granulocytów
czynnik
stymulujący
tworzenie kolonii
makrofagów
czynnik
stymulujący
tworzenie kolonii
granulocytów
i makrofagów
erytropoety
na
trombopoetyn
a
ligand
Flt3
CZYNNIK
KRWIOTWÓRC
ZY
MIEJSCE
WYTWARZANIA
GŁÓWNA FUNKCJA
Erytropoetyna
nerki, wątroba
wytwarzanie erytrocytów
G-CSF
komórki endotelium,
fibroblasty, makrofagi
wytwarzanie neutrofili
Trombopoetyna
nerki, wątroba
wytwarzanie płytek krwi
M-CSF
fibroblasty, komórki
endotelium, makrofagi
wytwarzanie makrofagów i osteoklastów
SCF/ligand
receptora c-Kit
komórki zrębowe szpiku
komórki macierzyste, komórki progenitorowe
przeżycie/podział; różnicowanie komórek
tucznych
Ligand Flt3
fibroblasty, kom.
endotelium
b. wczesne komórki krwiotwórcze, czynnik
dojrzewania DCs
GM-CSF
limfocyty T, makrofagi,
komórki tuczne
wytwarzanie makrofagów i granulocytów,
dojrzewanie i aktywacja DCs
IL-3
limfocyty T, makrofagi
czynnik wzrostu komórek macierzystych i
progenitorowych linii mieloidalnej
IL-5
aktywowane limfocyty
Th2
wytwarzanie eozynofilów
IL-6
aktywowane limfocyty T,
monocyty, fibroblasty,
komórki endotelium
stymulacja komórek progenitorowych,
wytwarzanie płytek krwi, wytwarzanie Ig w
limfocytach B
IL-11
j.w.
pobudzenie komórek progenitorowych szpiku i
wytwarzania płytek krwi
IL-7
j.w.
przeżycie limfocytówT
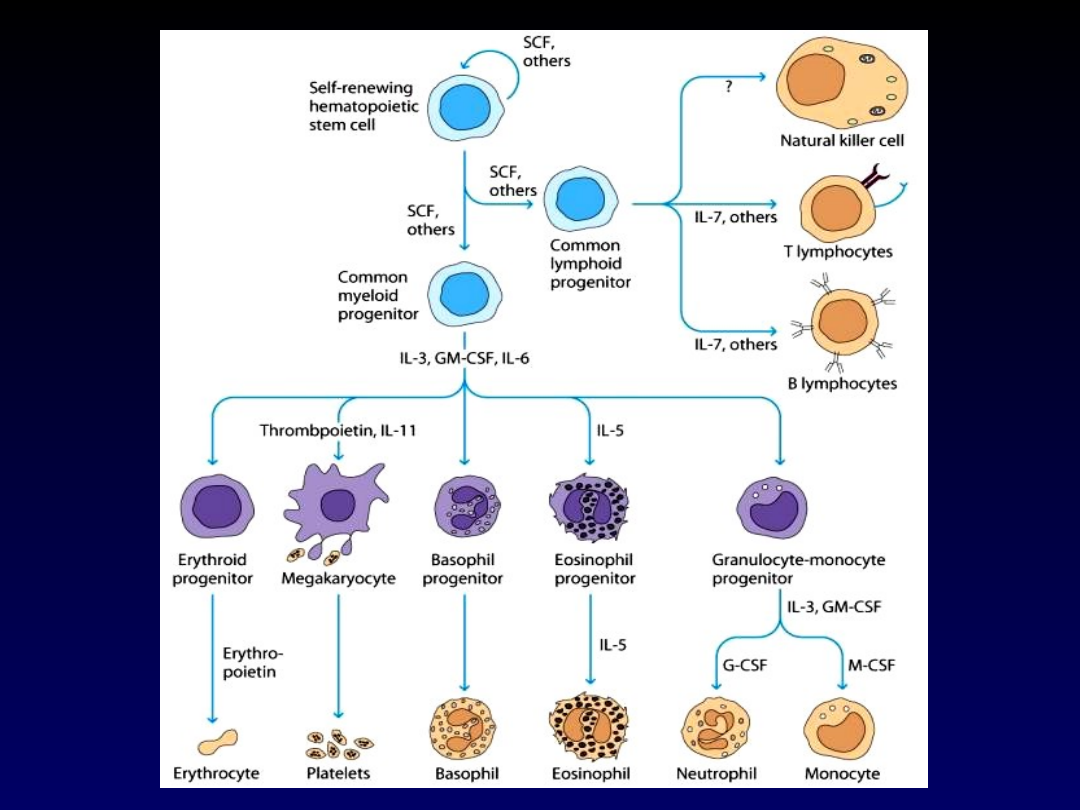

GM-CSF
• Wpływ na komórki szeregu granulocytowo-
makrofagowego:
-zwiększa właściwości fagocytarne
-wzmaga wytwarzanie IL-1, IL-6, G-CSF, TNF
-zwiększa ekspresję cz. adhezyjnych
-zwiększa poziom receptorów dla fragmentów
Fc przeciwciał
• Wpływ na funkcję dojrzałych limfocytów
-wzmaga cytotoksyczność komórek NK i LAK

GM-CSF i G-CSF
ZASTOSOWANIE KLINICZNE
GM-CSF: Leucomax, Leukine
G-CSF: filgrastim –Neupogen, lenograstim – Granocyte34,
pegfilgrastim – Neulasta
• korekcja granulopenii po intensywnej chemioterapii
lub radioterapii
• przyspieszenie regeneracji układu krwiotwórczego po
przeszczepieniu szpiku kostnego
• mobilizacja komórek progenitorowych do krwi
obwodowej (autoprzeszczep)
• leczenie zespołów mielodysplastycznych i cyklicznej
neutropenii

ERYTROPOETYNA
DZIAŁANIE:
• pobudza erytropoezę
• pobudza tworzenie płytek
krwi
• wpływa na wytwarzanie
przeciwciał przez komórki
plazmatyczne
• wpływa na cytotoksyczność
komórek LAK
ZASTOSOWANIE KLINICZNE:
Eprex, Epogen, Procrit; Recormom
• zmniejszenie niedokrwistości
– w przebiegu niewydolności nerek
– po chemioterapii nowotworów
– po terapii AIDS z użyciem AZT
• leczenie niedokrwistości w przebiegu
chorób przewlekłych, w zespołach
mielodysplastycznych
• profilaktycznie u dawców krwi
• zapobiegawczo przed planowanymi
operacjami chirurgicznymi, w
których przebiegu mogą utracić
znaczne ilości krwi

M-CSF
• działa przede wszystkim na monocyty, makrofagi
oraz ich komórki progenitorowe
• zwiększa ich właściwości żerne
• stymuluje wytwarzanie cytokin TNF, IFN, IL-1, G-
CSF
ZASTOSOWANIE KLINICZNE:
• próby w leczeniu czerniaka oraz w przebiegu
innych nowotworów, a także w leczeniu grzybic
narządowych

TROMBOPOEZA
• IL-3
• IL-6
• IL-11 (stosowana w celu
korekcji trombocytopenii w
przebiegu niektórych
chorób lub po toksycznych
terapiach)
• Trombopoetyna
Trombopoetyna: zastosowania
kliniczne:
• Chemioterapia guzów litych i białaczek
• Radioterapia
• Przeszczepianie szpiku
• Niedokrwistość aplastyczna
• Stany niewydolności hematopoezy
• Transfuzjologia (magazynowanie
płytek, produkcja in vivo)
• Zespoły mielodysplasyczne
• Małopłytkowość w AIDS
• Immunotrombocytopenia
• Chirurgia serca
• Chirurgia ogólna

SCF = ligand receptora c-Kit
• wpływa na bardzo młode, multiotencjalne komórki
macierzyste krwiotworzenia
• czynnik wzrostu komórek tucznych oraz melanocytów
• aktywuje cytotoksyczność limfocytów
• wykazuje działanie przeciwnowotworowe
Ligand Flt3 (Flt3L)

INTERFERONY
I – typu
α
- wytwarzana przez
aktywowane wirusem
leukocyty
β
- fibroblasty
κ
-keratynocyty
ω
II – typu
γ
- wytwarzany przez
limfocyty T traktowane
antygenami, cytokinami lub
mitogenami, przez komórki
NK pobudzone cytokinami,
przez komórki NKT oraz w
niewielkich ilościach przez
aktywowane makrofagi
INTERFERONY
IFN-α/β
IFN-γ
Lokalizacja
na
chromosomie
9
12
Pochodzenie
wszystkie kom. jądrzaste,
głównie fibroblasty,
makrofagi, kom.
dendrytyzne
limfocyty Th1 i kom. NK,
limfocyty T CD8
+
i γδ
Indukcja
przez
wirusy, inne cytokiny (IL-
1, TNF-α), niektóre
wewkomórkowe bakterie i
pierwotniaki
antygeny
Funkcje
aktywność
przeciwwirusowa,
zwiększa ekspresję MHC
klasy I, hamuje
proliferację komórek
aktywność
przeciwwirusowa,
zwiększa ekspresję MHC
klasy I i II, aktywuje
makrofagi
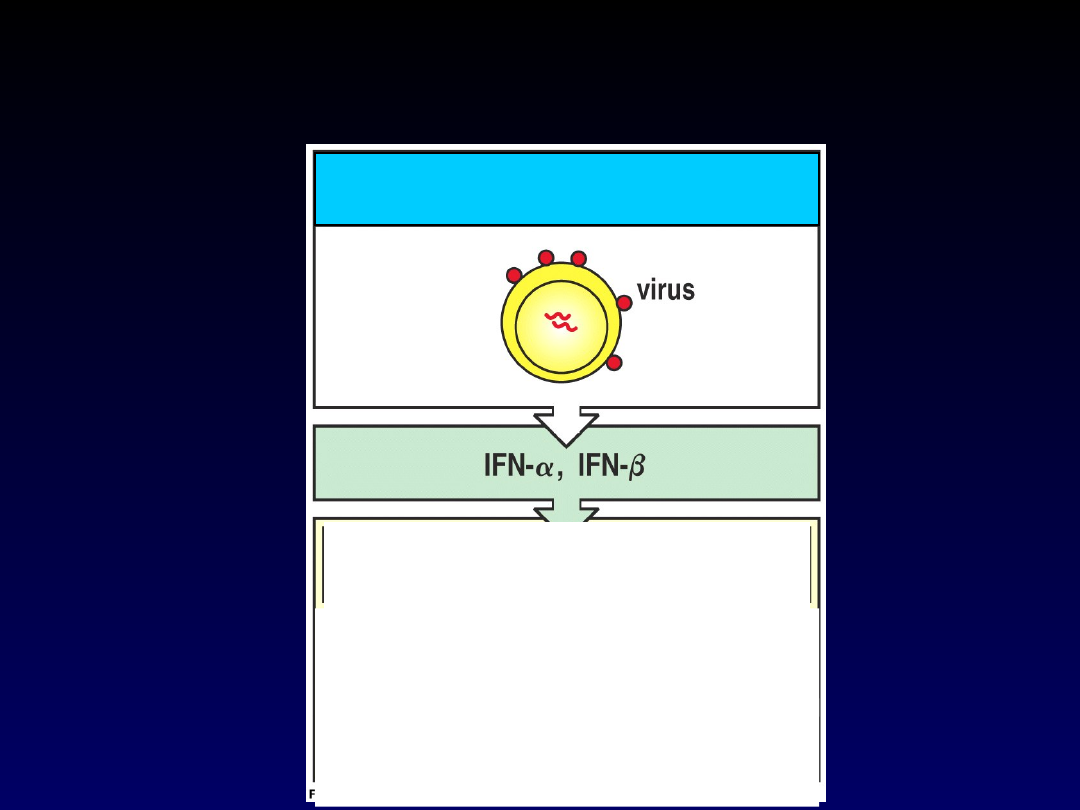
INTERFERON- i
INTERFERON-
Większość
komórek może
wytwarzać IFN-
i IFN- w
odpowiedzi na
zakażenie
wirusowe.
Zakażona wirusem komórka
gospodarza
indukuje oporność na
replikcję wirusa we wszystkich
komórkach
zwiększa ekspresję MHC I i
prezentację antygenu na
wszystkich komórkach
pobudza komórki NK do
zabijania komórek zakażonych
wirusem
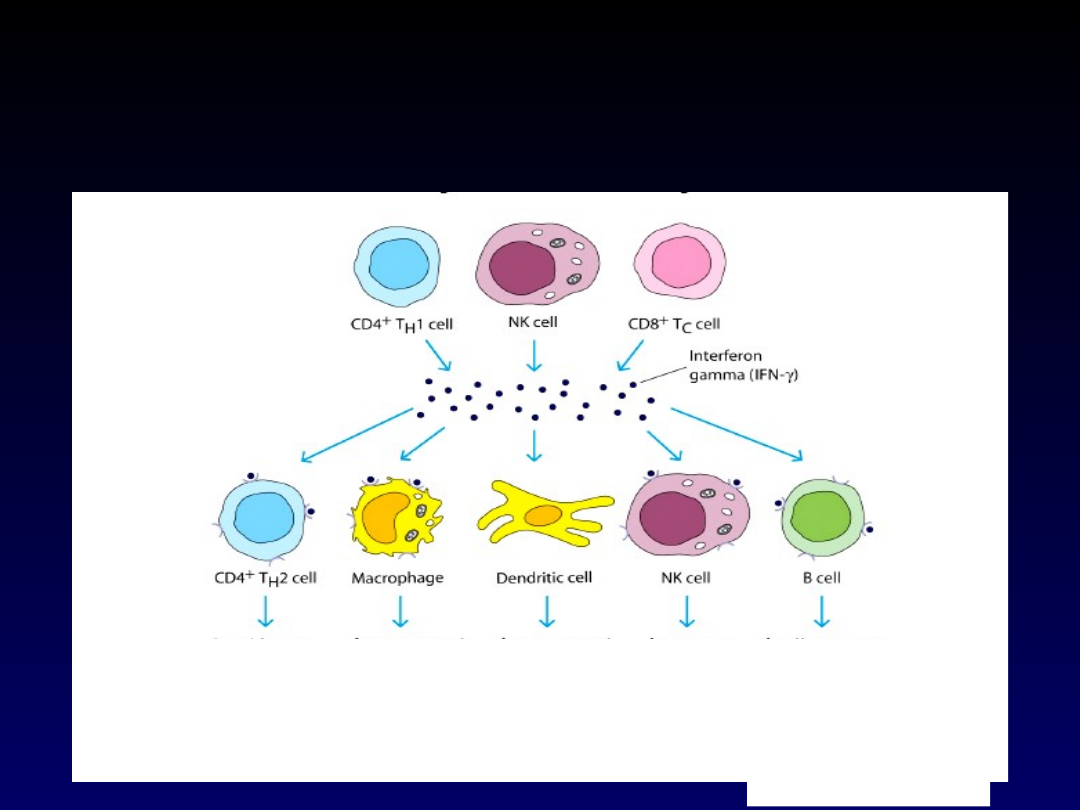
IFN- – silny aktywator
Proliferacj
a
Wytwarzan
ie IL-4 i IL-5
Ekspresja MHC
II
Aktywność
bakteriobójcza
Ekspres
ja
MHC II
Aktywnoś
ć
cytotoksyc
zna
Różnicowanie
Wytwarzanie
przeciwciał (
IgG2a;
IgE i IgG1)
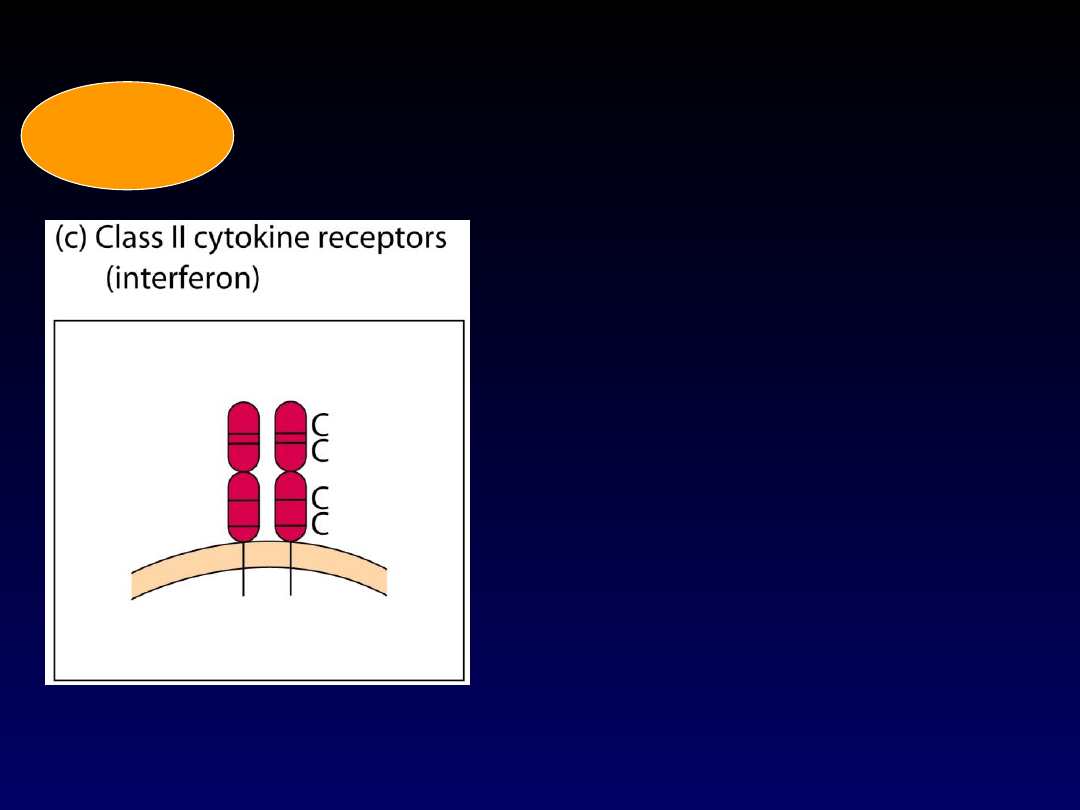
Receptory dla interferonów
•heterodimery
•dwie różne podjednostki
• interferony , i wiążą
się z tym samym
receptorem zbudowanym z
podjednostek IFNAR-1 i
IFNAR-2
•IFN-g wiąże się z
receptorem, w skład
którego wchodzą
podjednostki IFNGR-1 i
IFNGR-2
IFN
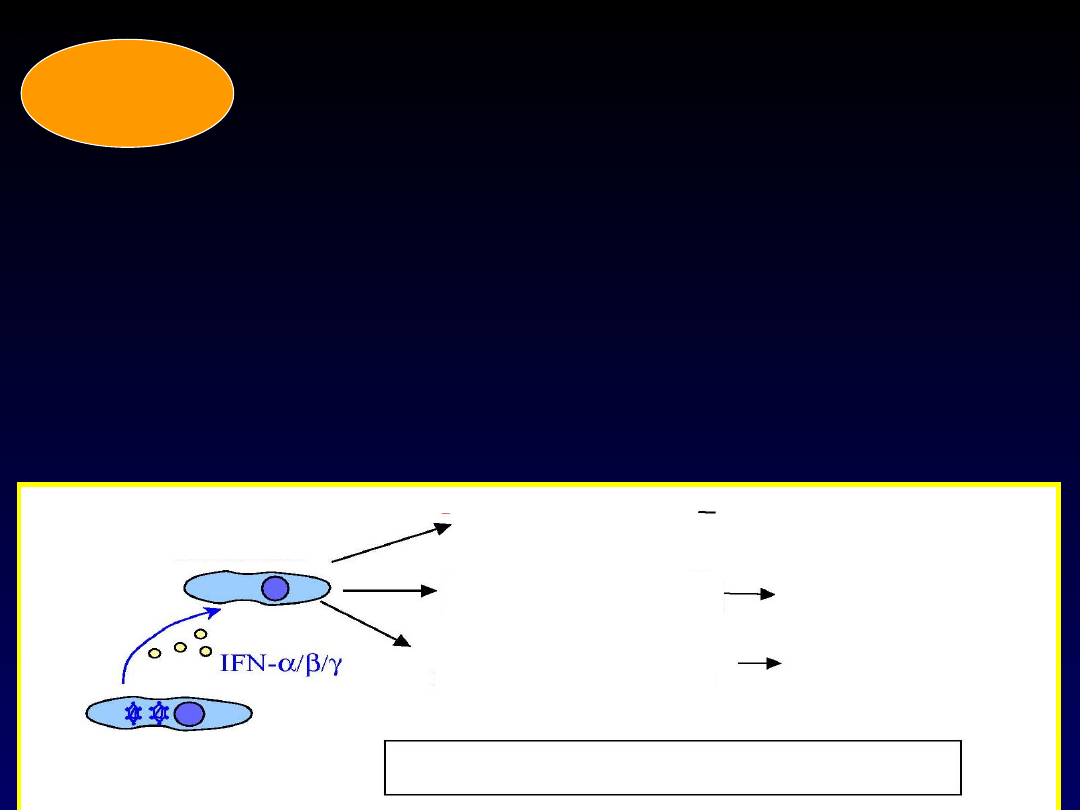
Działanie przeciwwirusowe
Interferony
nie wykazują bezpośredniego działania przeciwwirusowego, oddziałują
na komórki indukując w nich powstawanie czynników przeciwwirusowych i „stanu
gotowości przeciwwirusowej”:
syntezę
syntetazy oligoizoadenylanowej
powstanie oligonukleotydów
adenylanowych aktywujących RNazę L (w obecności dwuniciowego RNA)
ekspresję
deaminaz adenozynowych
dezaminacja adenozyny w obrębie
dwuniciowego RNA powstają inozyny
kinazę białkową R
autofosforylacja, fosforylacja podjednostki czynnika
inicjującego syntezę białka (kinaza R jest aktywna w obecności dwuniciowego
RNA, dlatego działa tylko w komórkach zakażonych przez określone wirusy)
zakażona
komórka
zdrowa
komórka
zahamowanie szerzenia się wirusów
wirusowy RNA
- niefunkcjonalny
zahamowanie translacji
i syntezy białek wirusowych
rozkład wirusowego mRNA
oraz komórkowego
jednoniciowego RNA
syntetaza
oligoizoadenylan
owa
deaminazy
adenozynowe
kinaza białkowa R
IFN

Działanie przeciwwirusowe
Interferony nie wykazują bezpośredniego działania
przeciwwirusowego, ale oddziałują na inne komórki
indukując w nich powstawanie czynników
przeciwwirusowych i „stanu gotowości przeciwwirusowej”:
– aktywują gen Mx, produkt tego genu hamuje drastycznie
replikację wirusa grypy i niektórych innych wirusów RNA
– wzmagają aktywność komórek cytotoksycznych
(Tc, NK i K)
– wzmagają aktywność cytotoksyczną i fagocytarną
makrofagów
IFN

Wpływ na układ odpornościowy
cytotoksyczności :
limfocytów Tc, komórek K i
NK
ekspresji MHC (MHC klasy
I , MHC klasy II przez IFN-γ)
ekspresji niektórych
cząsteczek i receptorów
powierzchniowych np. CD80,
FcR
• aktywacja makrofagów
fagocytozy
ekspresji innych cytokin:
IL-1, IL-6, TNF, IP10, MIG
• IFN-γ najsilniej oddziałuje na
układ odpornościowy
Wpływ na proliferację
i różnicowanie komórek
• inhibitory
krwiotworzenia
(najsilniej
antyproliferacyjnie działa
IFN-γ)
• IFN-γ podejrzewany o
udział w patogenezie
niedokrwistości
aplastycznej
IFN

Działanie
przeciwnowotworowe
Działanie bezpośrednie:
• Hamowanie proliferacji i
pobudzanie różnicowania
komórek nowotworowych
• Modulują onkogeny komórkowe
(C-myc, c-fos, c-H ras) –
wydłużenie cyklu podziałowego
• Oddziaływanie cytotoksyczne na
komórki nowotworowe
Działanie pośrednie:
• Zwiększanie ekspresji
antygenów nowotworowych
• Hamowanie powstawania naczyń
nowotworowych
• Wpływ interferonów na układ
odpornościowy (aktywacja
cytotoksycznych mechanizmów
komórkowych, wzmożone
wytwarzanie cytokin o działaniu
przeciwnowotworowym np. TNF,
wywyołują lizę komórek
nowotworowych z udziałem
dopełniacza i na drodze ADCC)
IFN

Zastosowanie terapeutyczne
• Przewlekła białaczka szpikowa
• Białaczka włochatokomórkowa
• T-komórkowy chłoniak skórny
• Szpiczak mnogi (leczenie podtrzymujące u chorych, u których
uzyskano obiektywną remisję w wyniku chemioterapii indukcyjnej)
• Chłoniaki nieziarnicze o małym stopniu złośliwości prz.
pokarmowego
• Mięsak Kaposiego w przebiegu AIDS
• Czerniak złośliwy
• Przewlekłe WZW B
• Przewlekłe WZW C
• Zaawansowane stadium raka nerki
• Rakowiak z przerzutami do węzłów chłonnych lub do wątroby oraz
z "zespołem rakowiaka"
IFN-(Intron A, Roferon A, Alferon
N):
Wskazania ustalone:
IFN

Zastosowanie terapeutyczne
• Rak pęcherza (podanie dopęcherzowe)
• Rak jajnika (podanie dootrzewnowe)
• Rak j. grubego
• Neuroendokrynne nowotwory złośliwe
• Nadpłytkowość
• Czerwienica prawdziwa
• Samoistna mielofibroza w fazie proliferacyjnej
• Samoistna mieszana krioglobulinemia typu II
• WZW D
• AIDS (we wczesnych stadiach choroby w połączeniu z
azydotymidyną)
• Zakażenia narządów płciowych HPV
• Brodawczaki krtani
• Zespół hipereozynofilowy
• Układowa mastocytoza
• Kłykciny kończyste
IFN-(Intron A, Roferon A, Alferon N):
Wskazania potencjalne:
IFN

Zastosowanie terapeutyczne
IFN- (Betaseron, Avonex, Rebif):
• Stwardnienie rozsiane
IFN-(Imukin, Actimmune):
• u dzieci z przewlekłą chorobą ziarniniakową
• AZS
• gruźlica
• leiszmanioza trzewna
• mononukleoza zakaźna
• przewlekłe zakażenie wirusem Epstein-
Barra
• rak nerki
• rak jajników
• RZS
IFN

Objawy uboczne
• Podwyższona temp. ciała
• Przyspieszona czynność serca
• Bóle głowy
• Bóle mięśniowe i kostne
• Objawy ze strony ukł. pokarmowego
• Objawy ze strony CUN
• Zaburzenia funkcji nerek i krwiotworzenia
IFN

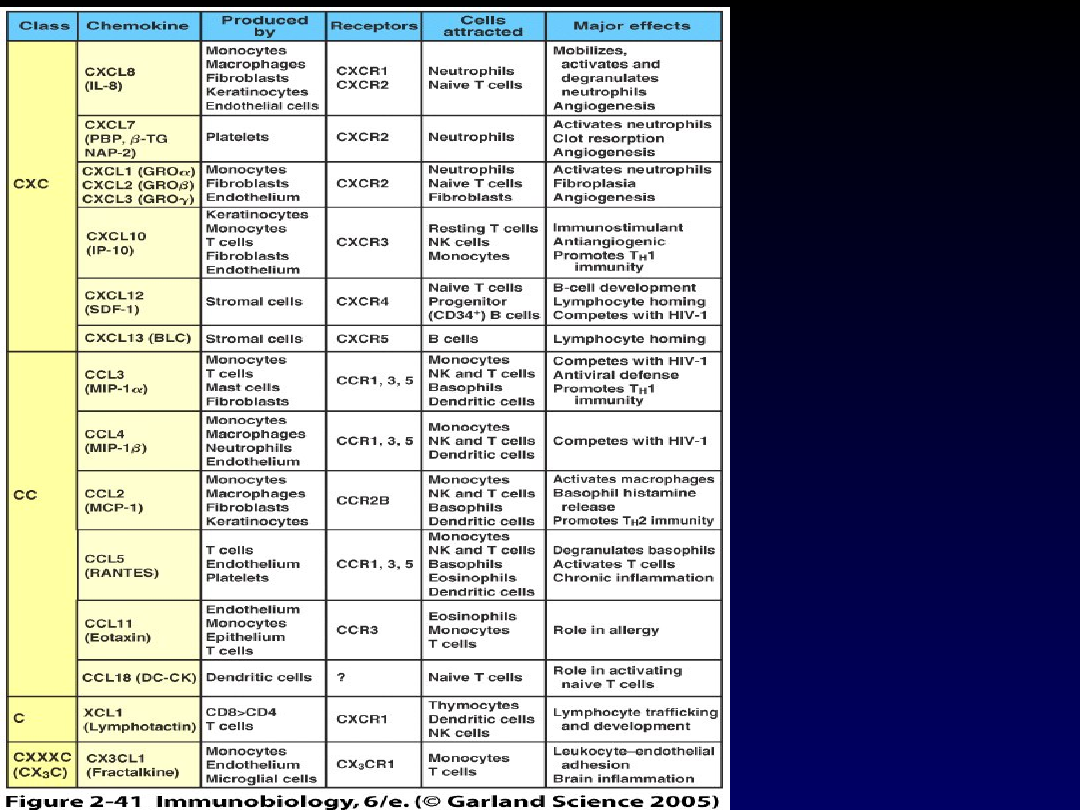
CHEMOKINY
• Podobne strukturalnie do siebie cytokiny oddziałujące
chemotaktycznie, a często również aktywująco na różne
populacje leukocytów
• Charakteryzują się małą masą cząsteczkową
• Odgrywają kluczową rolę w:
– Reakcjach zapalnych
– Odporności przeciwzakaźnej
– Krwiotworzeniu
– Limfopoezie
– Odpowiedzi przeciwnowotworowej
– Odrzucaniu przeszczepów
• Wytwarzane głównie przez monocyty i makrofagi

Prozapalne (indukowane)
– wytwarzane w trakcie reakcji
zapalnych
Limfoidalne (konstytutywne lub homeostatyczne)
– regulują
krążenie różnych populacji limfocytów, sterują migracją DCs
z tkanek obwodowych do obwodowych narządów
limfatycznych, uczestniczą w przemieszczaniu się
dojrzewających tymocytów do odpowiednich regionów grasicy
• Ze względu na liczbę cystein oraz liczbę aminokwasów między
dwoma pierwszymi cysteinami wyróżniamy 4 podrodziny
– C
(γ): limfotaktyna α i β
– CC
(β) – oddziałują na limfocyty, monocyty, komórki
tuczne, eozynoile
– CXC
(α) – oddziałują głównie na neutrofile i limfocyty
– CX3C
(δ): fraktalkina (neurotaktyna)
CHEMOKINY

• Wytwarzanie indukowane jest przez
cytokiny prozapalne: TNF, IL-1 oraz IFN-
γ
• Wydzielanie większości chemokin hamuje
IL-10 (z wyjątkiem HCC-4) i TGF- β
• Interferowanie z działaniem chemokin
jest jednym z częściej wykorzystywanych
mechanizmów obronnych drobnoustrojów
CHEMOKINY
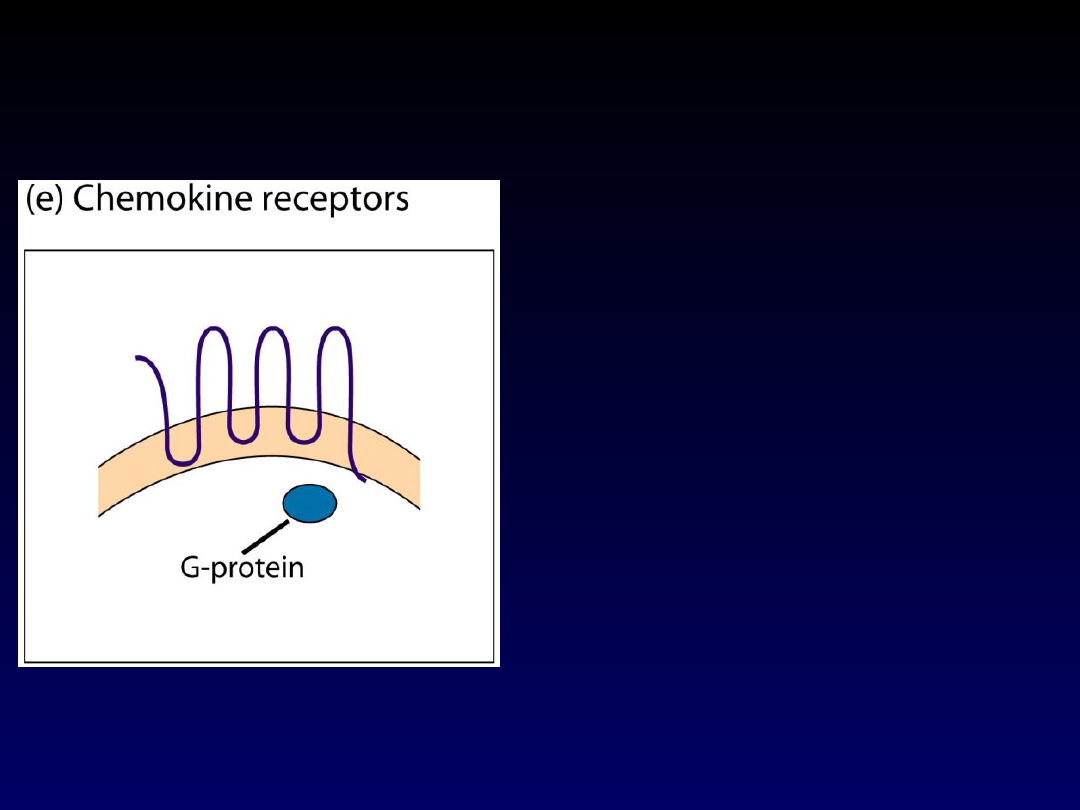
RECEPTORY DLA
CHEMOKIN
• Rodopsynopodobne receptory
związane z białkiem Gi,
przechodzące 7x przez błonę
komórkową
• Zidentyfikowano 20
receptorów dla chemokin
• jednym z mechanizmów
regulujących wrażliwość na
chemokiny jest
desensytyzacja ich
receptorów tzn. po
zadziałaniu chemokiny jej
receptor traci wrażliwość na
dalsze jego pobudzanie
PMo anty-IL-8
-
łuszczyca, RZS i
inne choroby
zapalne

DZIAŁANIE CHEMOKIN
Mielopoeza i limfopoeza
• MIP-1 i MIP-1 – różnicowanie
granulocytów i monocytów
• SDF-1 – proliferacja prekursorów
limfocytów B
Aktywacja komórek
• IL-8 – zwiększa fagocytozę i
bakteriobójcze właściwości
neutrofilów
• MCP-1, MIP-1 - aktywują
monocyty
• Eotaksyny, MIP-1 , RANTES –
aktywują eozynofile
• MIP-1RANTES – proliferacja
limf. T, aktywują cytotoksyczność
Tc i NK, eozynofili do zmian
zapalnych w oskrzelach i płucach
Angiogeneza
– IL-8, ENA-78, GCP-2,
GRO-, GRO-
Działanie antyangiogenne
– PF4,
IP10, MIG
Odporność przeciwzakaźna
• MIP-1udział w
odpowiedzi przeciw wirusowi
grypy
• MIP-1RANTES, SDF-1 –
hamują infekcję komórek
przez wirus HIV
Odrzucanie przeszczepów
Formowanie nacieków
zapalnych w wielu chorobach
autoimmunizacyjnych
• IL-8, MCP-1, MIP-1, MIP-2 –
RZS
Patogeneza chorób alergicznych
• Eotaksyna, RANTES, MCP-2,
MCP-3, MCP-4 i MIP-1 -
chemotaksja
NADRODZINA CZĄSTECZEK
CZYNNIKA MARTWICY
NOWOTWORU
TNF i
limotoksy
ny
Tumor
necrosis
factor
LIGHT
FasL
TRAI
L
TNF-related
apoptosis
inducing
ligand
TRENCE
TNF related
activation-
induced
cytokine
(ligand
osteoprotegr
yny)

TNF I LIMFOTOKSYNY
•
Wyróżniamy:
– TNF-α (TNF)
– TNF- β (limfotoksyna α)
– LT- β
• TNF wytwarzany jest przede wszystkim przez monocyty i
makrofagi, natomiast źródłem zarówno TNF jak i LT-α są
limfocyty
• Najsilniejszym bodźcem do wytwarzania TNF jest LPS
ścian bakteryjnych (w mniejszym stopniu GM-CSF, M-CSF
oraz sam TNF)
• Istnieją 2 typy receptorów:
– TNFR1 (p55, CD120α)-wszystkie kom. jądrzaste
– TNFR2 (p75, CD120β)- leukocyty, kom. śródbłonka
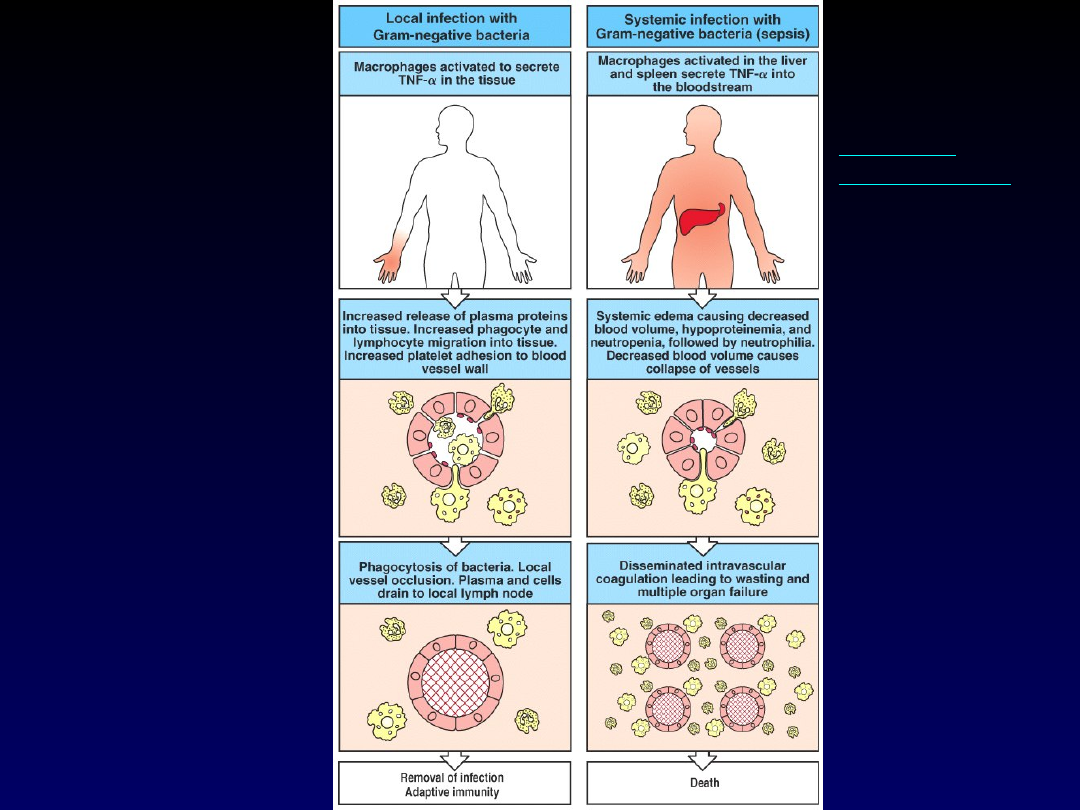
Układowo,
wysokie dawki
TNF mogą
doprowadzić do
wstrząsu
septycznego,
niewydolności
wielu narządów i
śmierci.
W stanach
przewlekłych
długotrwałe
wydzielanie TNF
wywołuje
zubożenie tk.
tłuszczowej w
zapasy lipidów i
prowadzi do
kacheksji.
Miejscowo, TNFa
może powodować
zapalenie.
Patogenna rola TNF
w schorzeniach
autoimmunizacyjnyc
h, w odrzucaniu
przeszczepów, w
reakcji przeszczep
przeciw
gospodarzowi, w
AIDS.
TNF odpowiedzialny
częściowo za
insulinooporność w
cukrzycy,
powstawanie zmian
miażdżycowych,
zapalenie trzustki,
alkoholowe
uszkodzenie wątroby
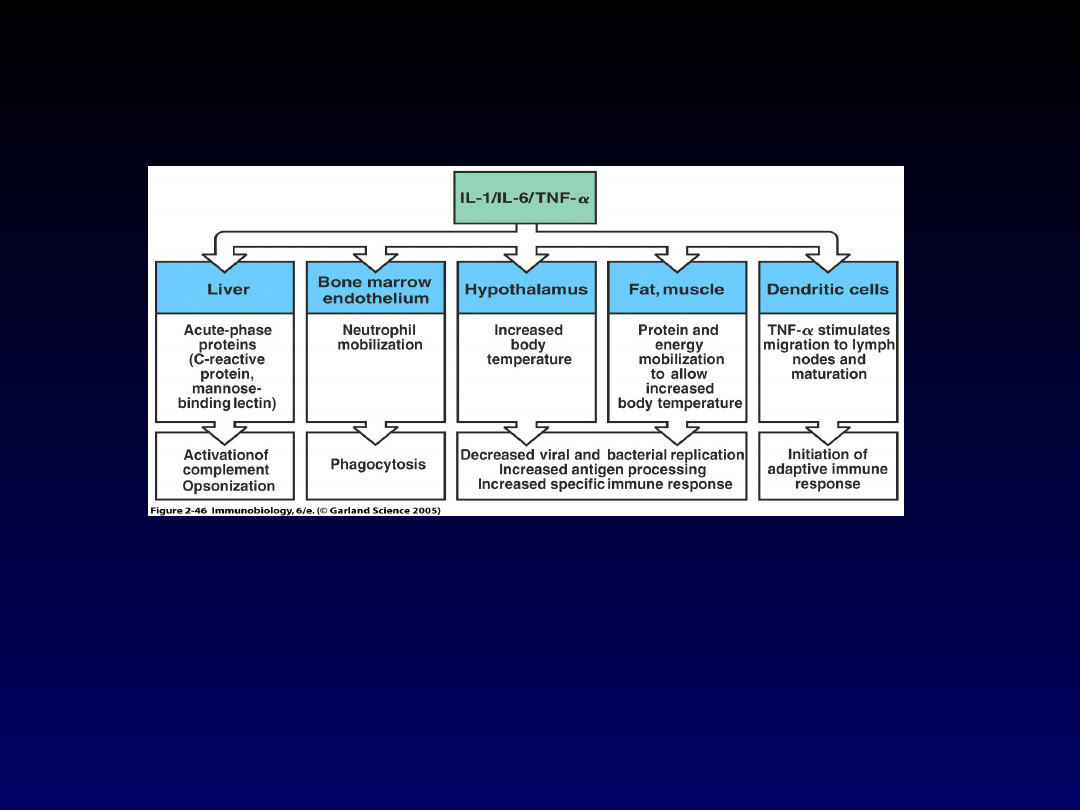
TNF A UKŁAD
ODPORNOŚCIOWY
• Główna cytokina odpowiedzi zapalnej i immunologicznej
• Wraz z IL-6 wzmaga proliferację i różnicowanie limfocytów B
• Wraz z IL-2 i IL-6 wzmaga proliferację i różnicowanie limfocytów T
• Wraz z IL-2 stymuluje cytotoksyczność monocytów, makrofagów,
komórek NK oraz powstawanie komórek LAK i limfocytów Tc

• Na monocyty i makrofagi oddziałuje w sposób endo-, para- i
autokrynowy
• działanie chemotaktycznie na monocyty i neutrofile
• Aktywuje neutrofile, zwiększając ich właściwości
fagocytarne, bakteriobójcze i cytotoksyczne oraz przyspiesza
ich uwalnianie ze szpiku
• Aktywuje cytotoksyczność eozynofilów wobec pierwotniaków
• Indukuje uwalnianie:
– z makrofagów: IL-1, IL-6, GM-CSF, G-CSF, M-CSF, PDGF,
NGF, EGF, PAF, IFN- β, prostaglandyn i leukotrienów
– z limfocytów IFN-γ
• Indukuje ekspresje MHC I oraz MHC II (wraz z IFN-γ)
TNF A UKŁAD
ODPORNOŚCIOWY

DZIAŁANIE
PRZECIWNOWOTWOROWE TNF
• Działa bezpośrednio na kom. nowotworowe
– indukuje apoptozę
– hamuje proliferację
– indukuje różnicowanie
• Indukuje zmiany w naczyniach krwionośnych
nowotworu
• Pobudza odpowiedź immunologiczną
przeciwnowotworową

ZASTOSOWANIE KLINICZNE
INHIBITORÓW TNF
Przeciwciała przeciw (TNF-α)
• Infliximab
(Remicade) – chimeryzowane, mysio-ludzkie
przeciwciało monklonalne klasy IgG 1
• Etanercept
(Enbrel) – białko fuzyjne, składające się z
pozakomórkowej części ludzkiego receptora TNFp75
powiązanego z częścią Fc ludzkiej IgG 1
• Adalimumab
(D2E7) – ludzkie przeciwciało
monklonalne, wytworzone metodą inżynierii
genetycznej (lek zarejestrowany w Stanach
Zjednoczonych i krajach Europy Zachodniej)
Infliximab i etanercept - różnice w budowie i mechanizmie
działania
Infliximab
(Remicade)
Etanercept
(Enbrel)
Charakterystyka
molekularna
Chimeryzowane mysio-ludzkie
monoklonalne przeciwciało IgG1
(ludzka część stała; mysia region
zmienny)
Białko fuzyjne; ligand
wiążący TNFRp75 kd
powiązany z częścią
FcIgG1
Waga molekularna
~ 149 kd
~ 150 kd
Okres półtrwania
9 dni
4 dni
Mechanizm działania
Neutralizuje biologiczną
aktywność TNF-α; wiążąc
rozpuszczalny (monomery i
trimery) i związany z błoną
komórkową TNF-α
Wiąże 2 cząsteczki TNF
działając jako "fałszywy"
receptor (decoy)
Zdolność wiązania
TNF-β (limfotoksyna)
nie
tak
Liza komórek zdolnych
do sekrecji TNF-α
(obwodowych
monocytów,
makrofagów,
neutrofili)
tak
nie
Indukcja apoptozy
(monocytów krwi
obwodowej i
limfocytów w lamina
propria)
tak
nie

Wskazania do leczenia Infliximabem i Etanerceptem
Infliximab (Remicade)
Etanercept (Enbrel)
• Choroba Crohna (CD)
Postać aktywna, oporna
na inne terapie; przetoki
w CD
• RZS, aktywne, oporne na
leczenie Mtx
(terapia skojarzona z
Mtx)
• zesztywniające zapalenie
stawów kręgosłupa
(ZZSK)
• RZS, aktywne
•Terapia skojarzona z
Mtx
•Monoterapia we
wczesnym RZS
• Młodzieńcze idiopatyczne
zapalenie stawów
aktywne, postać
wielostawowa
• Łuszczycowe zapalenie
stawów, aktywne
• zesztywniające zapalenie
stawów kręgosłupa
(ZZSK)
Próby kliniczne:
różne postacie zapalenia naczyń, choroba Stilla u
dorosłych, zespół Sjögrena, zapalenie wątroby typu C, zapalenie
błony naczyniowej oka, zapalenie wielomięśniowe i skórno-
mięśniowe, SLE i stwardnienie rozsiane

DZIAŁANIA NIEPOŻĄDANE
• Infekcje (górnych dróg
oddechowych, zapalenie
oskrzeli, zapalenie pęcherza,
infekcje skórne)
• Ciężkie infekcje (zapalenie
płuc, zapalenie tkanki
łącznej, infekcyjne zapalenie
stawu, posocznica)
• Trombocytopenia
• Anemia
• Leukopenia
• Pancytopenia
• Niedokrwistość aplastyczna
• Reakcje alergiczne
• Powstawanie autoprzeciwciał
• Ciężkie reakcje
alergiczne/anafilaktyczne (w
tym obrzęk naczynioruchowy,
skurcz oskrzeli)
• Drgawki
• Rzadkie przypadki
demielinizacji OUN
• Świąd
• Pokrzywka
• Reakcje w miejscu
wstrzyknięcia
• Gorączka
• Przypadki zaostrzenia
zastoinowej niewydolności
serca
• Podostry skórny toczeń
rumieniowaty
• Toczeń rumieniowaty
przewlekły
• Zaspół toczniopodobny
Ciężkie objawy niepożądane i autoprzeciwciała u
chorych leczonych infliximabem i etanerceptem
Objawy niepożądane
Infliximab
(Remicade)
Etanercept
(Enbrel)
CIĘŻKIE INFEKCJE
Mycobacterium tuberculosis
(19)
(dane z 11 mies. 2001r.)
117/100 tys lecz./rok
16/100 tys. lecz./rok
Histoplasma capsulatum (21)
(dane z 7 mies. 2001r.)
16/100 tys.lecz./rok
1/100 tys. lecz./rok
Listeria monocytogenes (30)
(dane z 2002r.)
8/82 tys. lecz./rok
b.d.*
Zespół demielinizacyjny (24)
(dane z 2001r.)
2/100 tys. lecz./rok
18/100 tys. lecz./rok
Zespoły limfoproliferacyjne
(5)
(dane z 19 mies. 2000 i
2001r.)
7/100 tys. lecz./rok
19/100 tys. lecz./rok
AUTOPRZECIWCIAŁA
ANA (28)
20-80%
11%
dsDNA (6, 28) (w klasach IgM
i IgA)
11-21%
13%
P-ciała antykardiolipidowe
(ACLA)(1,8,10)
13,5%
17%
HACA (antychimeryczne)
(1,28)
8,5%
3%
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
Wyszukiwarka
Podobne podstrony:
CZYNNIKI KRWIOTWÓRCZE, Uczelnia, imunny
III CZYNNIKI KRWIOTWÓRCZEost
Czynnik środowiskowy, a czynnik ekologiczny
Analiza czynnikowa II
epidemiologia, czynniki ryzyka rola pielegniarki rak piersi szkola, nauczyciel
czynniki wpływające na zmeczenie psychiczne w pracy
Czynniki szkodliwe II(1)
CZYNNIKI ROZWOJU 2
Czynniki chemiczne w środowisku pracy prezentacja
CZYNNIKI BIOLOGICZNE
(2,3) Działania nieporządane, toksytczne leków Metabolizm, czynniki wpływające na działanie substanc
Czynniki ryzyka choroby niedokrwiennej serca cz
Czynniki konkurencyjnosci organizaci publicznych Wyklad V
Ergonomia w Transporcie Chemiczne czynniki pracy materiały pędne i smary
więcej podobnych podstron