
CHOROBY WIRUSOWE I
BAKTERYJNE
PRZEWODU
ODDECHOWEGO U
BYDŁA

Syndrom oddechowy bydła - BRDC
(Bovine Respiratory Disease
Complex)
• in. gorączka załadunkowa, choroba z
zatłoczenia czy też bronchopneumonia
• wieloczynnikowa etiologia
• charakter sezonowy (jesień, zima)
• najbardziej podatne cielęta

ETIOLOGIA
• wirusowa
– bydlęcy syncytialny wirus oddechowy (BRSV),
– bydlęcy wirus parainfluenzy typu 3 (PI3)
– bydlęcy herpeswirus typ 1 (BHV-1) (IBR/IPV)
– enterowirus bydła
– adenowirus , reowirus, rinowirus, koronawirus
bydła
– wirus wirusowej biegunki bydła i choroby błon
śluzowych (BVD/MD)

• bakteryjna
– Mannheimia haemolytica
– Pasteurella multocida
– Mycoplasma bovis
– Arcanobacterium pyogenes
– Chlamydophila pecorum
– Histophilus somni i in.

• Pasożytnicza
– Dictyocaulus viviparus

• czynniki niezakaźne
– pojemność oddechowa płuc cielęcia
– długość okrywy włosowej, rzutująca na
termoizolację
– temperatura, wilgotność, ruch
powietrza
– stres, nadmierne zagęszczenie
– transport
– zabiegi profilaktyczne i lecznicze
– odsadzanie

Objawy:
• wzrost ciepłoty wewnętrznej do 40°C -
42.2°C
• nieznaczna osowiałość
• spadek spożycia paszy
• duszność wydechowa
• wzrost częstości oddechów
• kaszel
• obfity wypływ z nosa i worka
spojówkowego

Objawy cd.:
• charakterystyczna postawa z
wyciągniętą do przodu głową oraz
podciągniętymi powłokami brzusznymi
• najczęściej rozwarta jama ustna z dużą
ilością piany
• w końcowym stadium – w ok.
grzbietowej oraz mostka - obrzęki
tkanki podskórnej, szeleszczące przy
mocniejszym dotyku

Zmiany
anatomopatologiczne
• obrzęk i rozedma płuc
• brak spoistości tkanki płucnej
• wybroczyny pod opłucną płucną
• występowanie błon szklistych w
pęcherzykach płucnych
• zgrubienie przegród międzypęcherzykowych
połączone z ich nacieczeniem
• zanik nabłonka wyścielającego pęcherzyki
płucne

Obraz makroskopowy płuc uzyskanych od
cieląt
z klinicznymi objawami syndromu
oddechowego
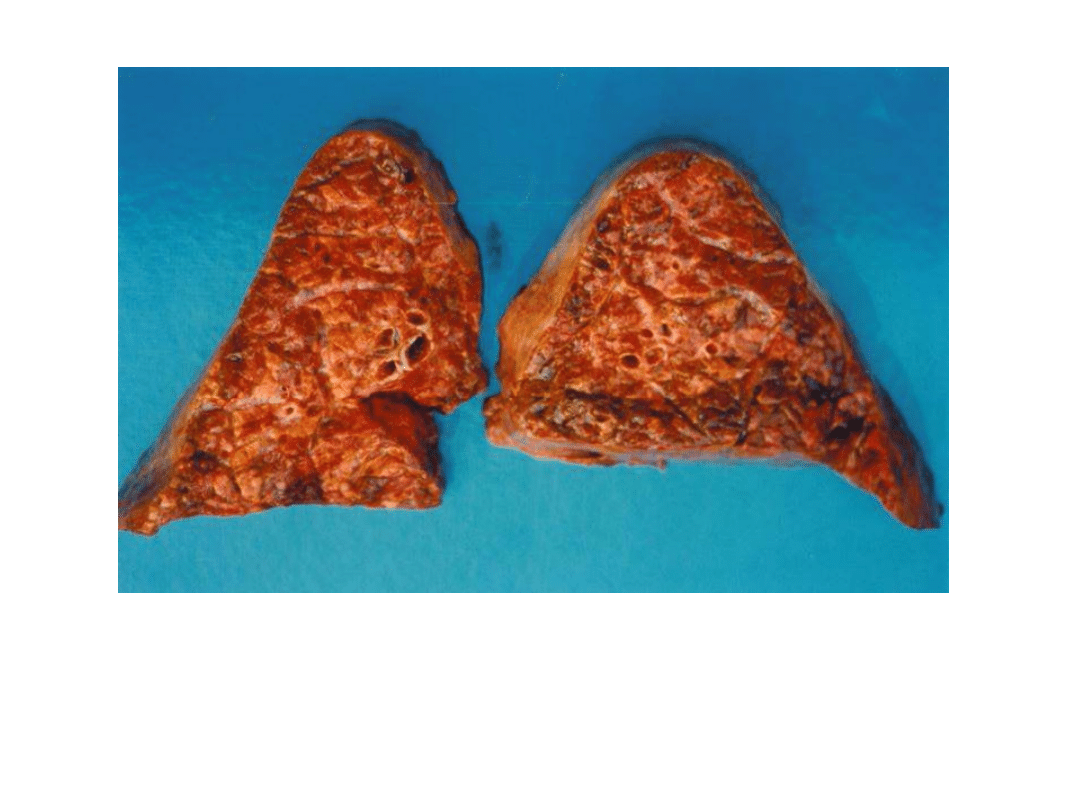
Powierzchnia przekroju płuc cielęcia z
klinicznymi objawami syndromu
oddechowego

ROZPOZNANIE
• badania kliniczne, laboratoryjne i
sekcyjne (najlepsze efekty daje
połączenie wszystkich)

Badanie kliniczne
• zapis ilości i rodzaju oddechów
• badanie temperatury rektalnej
• obserwacja objawów klinicznych
• objawy kliniczne i zmiany
patologiczne w układzie
oddechowym są mało
patognomiczne

Badanie laboratoryjne
• przeprowadzane z prób pobranych
przyżyciowo od chorych zwierząt lub
podczas badania sekcyjnego
• próby pobierane od kilku zwierząt
W zależności od czynnika:

Wirusy
• izolacja wirusa, wykrycie antygenu
(barwienie, wykrycie kwasów
nukleinowych)
– wymazy z nosa, płyn z płukania płuc, wycinki
tkanki płucnej
• przeciwciała - próba neutralizacji wirusa,
ELISA
– podwójne próby surowicy
• badanie histopatologiczne
– próby z płuc

Bakterie
• hodowla
– płyn z płukania płuc, wycinki tkanki
płucnej
• badanie histopatologiczne
– próby z płuc

Leczenie
• antybiotyki + niesterydowe leki
przeciwzapalne
– wczesne rozpoczęcie leczenia
– antybiotyk musi osiągać w tkance
płucnej stężenia hamujące namnażanie
się głównych patogenów bakteryjnych
jeszcze przed rozwojem
nieodwracalnych uszkodzeń tkanek

Stosowane antybiotyki:
• florfenikol
• tylmikozyna
• tulatromycyna
• ceftiofur
• danofloksacyna
• enrofloksacyna
• cefquinon
• marbofloksacyna
• oksytetracyklina

Stosowane NLPZ:
• fluniksyna
• karprofen
• ketoprofen
• meloksikam
• kwas tolfenamowy

Zapobieganie
• ograniczenie stresu
• zapewnienie odpowiedniej ilości siary
• unikanie mokrej ściółki, przeciągu i
nadmiernego zagęszczenia
• kontrola sanitarna i kwarantanna
młodych zw.

Szczepienia
• szczepionki poliwalentne, żywe i
inaktywowane
– Bovilis Bovipast RSP zawiera BRSV, PI3 i
Mannheimia haemolytica

Programy szczepień
• cielęta posiadające przeciwciała
matczyne powyżej 2 tyg. życia
• cielęta bez przeciwciał matczynych od 4
miesiąca życia
• stado podstawowe
– 5 ml s.c. dwukrotnie w odstępie 4 tygodni
– szczepienie przypominające – pojedyncza
dawka ok. 2 tyg. przed przewidywanym
okresem zwiększonego zagrożenia (transport,
wprowadzenie do stada, zmiana utrzymania)

Wpływ zespołu oddechowego na
sektor produkcji bydła mięsnego
• uważany jest za zasadniczą przyczynę strat
ekonomicznych w sektorze bydła mięsnego
• w Europie roczne straty powodowane przez
zespół oddechowy wynoszą w przeliczeniu
na jedno cielę rasy mlecznej od
45 do 55
Euro
, a
117.5 Euro
w przeliczeniu na cielę
rasy mięsnej
• wzrost zachorowalności = wzrost kosztów
ponoszonych na leczenie

Enzootyczna
bronchopneumonia cieląt
• zakaźna i zaraźliwa, najczęściej o
podostrym lub przewlekłym przebiegu
• jest przyczyną największych strat wśród
młodych osobników
• obejmuje niekiedy ponad 90% zwierząt
w stadzie
• lokalny, enzootyczny charakter
• nasila się wraz ze wzrostem koncentracji
cieląt

Wirus syncytialny układu
oddechowego bydła (BRSV)
• zaliczany do pneumowirusów
(Paramyxoviridae)
• namnaża się w urzęsionych komórkach
nabłonka oddechowego i
pneumocytach typu II
• duża zmienność antygenowa -
podgrupy A, B, AB
• bydło zakażone BRSV – bardziej
zarażone na wtórne infekcje bakteryjne

Rozprzestrzenianie się wirusa
• w stadach bydła mlecznego (bliski kontakt
zwierząt) –
3 – 10 dni
• przy
pastwiskowym systemie utrzymania –
kilka tyg. – kilka miesięcy
zanim obejmie
stado
• gdy stado w pełni wrażliwe, wprowadzenie
BRSV =>
– 60-80 do 100% zakażonych
– 20-50% wykaże obj. kliniczne
– 10-20% ginie (zwłaszcza przy powikłaniach
bakt.)

• na zakażenie podatne najbardziej
cielęta, zwłaszcza ras mięsnych
• niepowikłane zakażenie BRSV
praktycznie nigdy nie przebiega w
postaci przewlekłej
• u cieląt zakażonych latentnie
podczas porodu objawy kliniczne
zauważane „z opóźnieniem”

Wyróżnia się dwie, klinicznie różne
postacie infekcji BRSV:
• wczesny zespół BRSV
– u cieląt, które od wiosny (II-IV) do lata są
cielętami ssącymi (przy matce)
– choruje niewiele sztuk
– kaszel, gorączka, wypływ z nosa
– niewiele przypadków śmiertelnych

• późny zespół BRSV
– ujawnia się od 3 tyg. do trzech mies. po
odsadzeniu
– silny, suchy kaszel, wypływ z nosa i oczu
– łatwy do przeoczenia ponieważ
zwierzęta zachowują się normalnie
– pierwsze upadki mogą sugerować
problem

Charakterystyczne zmiany
• histologicznie obecne są
wielojądrowe syncytia komórkowe w
pogrubiałej ścianie oskrzelików i
pęcherzyków płucnych oraz w ich
świetle
• syncytia mogą wypełniać
śródplazmatyczne, eozynofilowe
ciałka wtrętowe

Rozpoznanie
• izolacja wirusa, wykrycie antygenu:
– test immunofluorescencji bezpośredniej DIF
– PCR
• próby:
– wymaz z gardła lub nosa ( w materiale tym
BRSV obecny jest od 2-3 do 8-10 dnia od
zakażenia)
– popłuczyny z tchawicy i płuc
– zamrożone wycinki zmienionych chorobowo
płuc

• badania serologiczne
– test seroneutralizacji
– ELISA
– test immunofluorescencji pośredniej
– do oceny serokonwersji bada się
surowice pochodzące od tych samych
zwierząt w ostrej fazie choroby i w 15
dni – 3 tyg. później
• zwykle obserwowany jest 4 – 16 krotny
wzrost miana

Stosowanie szczepionek przeciw
BRSV może się wiązać z pewnym
ryzykiem, dlatego decyzja o
wprowadzeniu szczepień powinna
być uzależniona od statusu stada i
realnego zagrożenia BRSV.

Wirus parainfluenzy 3 (PI3V)
• rodzina Paramyxoviridae
• szeroko rozpowszechniony u bydła i
innych przeżuwaczy
• groźny dla niezabezpieczonych,
niechronionych przez przeciwciała
siarowe cieląt i niekiedy dla młodych i
dorosłych zwierząt, które mają
dziedziczny poziom przeciwciał
przeciw PI3V

• odgrywa podrzędną rolę w
wywoływaniu poronień u bydła
• we wczesnej fazie zakażenia antygeny
wirusowe wykryć można w próbkach
wymazu z nosa, śluzie tchawiczym,
zmienionych chorobowo tkankach za
pomocą:
– hodowli komórkowych (efekt cytopatyczny)
– IF

Adenowirusy bydlęce (BAV
1-9)
• 10 grup antygenowych
• 2 podgrupy serologiczne (I – BAV 1, 2, 3,
9, 10; II – 4, 5, 6, 7, 8)
• występowaniu zakażenia sprzyja
niedostateczna siarowa ochrona,
czynniki środowiskowe, inne zakażenia
• gdy objawy dotyczą także ukł.
pokarmowego i dochodzi do rozwoju
pneumoenteritis obserwuje się wyższą
śmiertelność

• na całym świecie występują
bezobjawowe zakażenia
adenowirusowe w związku z czym
pojawiają się u zwierząt zapalenia
wielostawowe, poronienia i
zaburzenia płodności

• histopatologicznie widoczne są
typowe dla infekcji adenowirusowych
wtręty wewnątrzkomórkowe
• wirusy można wykryć w wysięku z
nosa, kale i punktatach ze stawów a
pośmiertnie w tkance płucnej

Reowirusy
• rodzina Reoviridae
• szeroko rozpowszechnione u bydła
• 9 rodzajów, w tym 3 serotypy
patogenne (wszystkie trzy obecne u
bydła)
• ich zakaźność w zakresie pH 2.2 – 8.0
• rezerwuarem mogą być kuczmany (jako
mechaniczni przenosiciele lub wektory)

• brak objawów zakażenie lub niezauważalne
• wykazano jednak serokonwersję i
narastanie mian przeciwciał swoistych dla
reowirusów u 26% zwierząt w badanej
populacji
• wirus widoczny jako
wewnątrzcytoplazmatyczne twory w
aparacie Golgiego
• w okresie wiremii wirusa można wykazać w
wydzielinie z nosa i worka spojówkowego

• reowirusy wykazują tropizm do
małżowin nosowych, tchawicy, płuc,
migdałków i śródpiersiowych węzłów
chłonnych
• diagnostyka obejmuje badanie PCR,
hodowlane, badanie par surowic,
odczyn zahamowania hemaglutynacji
oraz test seroneutralizacji
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
Wyszukiwarka
Podobne podstrony:
choroby wirus i bakter ukł odd Bo
choroby wirus i bakter ukł odd Bo
Interna Ch ukł odd dolne dr odd
cw 4 patologia ukl odd
Zmiany w ukł odd w przebiegu układowych chorób tkanki łącznej, INTERNA, reumatologia
chor ukł krąż PPT
piel slajdy1 ukl odd id 357119 Nieznany
kardiologia i ch ukł odd
piel slajdy1 ukl odd
wykład 15 (13 03 2013) stymulacja ukł odd u dzieci z MPD
APD 9 ukł synchroniczne
PA2 4 podstawy ukł sekw
Zaburzenia ukł pozapiramidowego (1)
ukł kostny KD
1 bo
Stres a ukł krąż Sałabun Sękowska
Obw ukł nerw
więcej podobnych podstron