
SKŁADNIKI
MIKROSTRUKTURALNE
STOPÓW ŻELAZA
WYKŁAD IV

ROZTWORY STAŁE
•
Żelazo występuje w dwóch odmianach
alotropowych:
▫do temperatury 912°C
▫oraz od temperatury 1394°C do temp.
topnienia 1538°C
•
Struktura krystaliczna żelaza jest regularna
przestrzennie centrowana (RPC, C12, A2)
•
Żelazo o takiej strukturze krystalicznej: to
żelazo α
•
Roztwory na osnowie żelaza α są nazywane
ferrytem i często oznaczane α

ROZTWORY STAŁE c.d.
•
W
zakresie
temp.912-1394°C
struktura
krystaliczna żelaza jest regularna ściennie
centrowana (RSC, CF4, A1)
•
Roztwory na osnowie żelaza o takiej strukturze
krystalicznej to: austenit i oznaczane γ, zaś
żelazo jest nazywane żelazem γ
•
W stopach żelaza zarówno w przypadku ferrytu
i austenitu występują dwa rodzaje roztworów:
▫ roztworów międzywęzłowe
▫ roztwory substytucyjne

STRUKTURA KRYSTALICZNA Fe
(żelaza)- WYMIARY LUK W
STRUKTURACH ŻELAZA
Struktura
krystaliczna
Fe
Rodzaj luki
Promień luki
Wyrażony przez
ułamek
promienia atomu
Fe
pm
RSC, cF4, A1
Oktaedryczna
0,414
52,6
Tetraedryczna
0,225
28,6
RPC, cI2, A2
Oktaedryczna
0,155
19,2
tetraedryczna
0,291
36,1
Promienie atomowe żelaza i pierwiastków tworzących z żelazem
roztwory międzywęzłowe są następujące: Fe-α-124pm, Fe-γ-
127pm, C-77pm, N-71 pm, B- 97 pm, H- 46 pm i O – 60 pm

ROZTWORY MIĘDZYWĘZŁOWE I
SUBSTYTUCYJNE
•
Pierwiastki takie jak: C, N, B, H i O tworzą z
żelazem α jak i γ roztwory międzywęzłowe
•
Roztwory substytucyjne tworzą pozostałe
pierwiastki jeżeli są rozpuszczalne w żelazie
•
Ułożenie atomów w strukturze krystalicznej
żelaza α jest luźniejsze niż w strukturze
krystalicznej żelaza γ
•
Stosunek objętości atomów do objętości w jakiej
się one znajdują nazywamy stopniem wypełnienia
przestrzeni przez atomy:
▫ w żelazie α=0,68
▫ w żelazie γ-0,74

RÓŻNICE W GĘSTOŚCI UŁOŻENIA
ATOMÓW W AUSTENICIE I
FERRYCIE
•
Powoduje, ze podczas przemiany żelaza γ o
większej gęstości w żelazo α o gęstości
mniejszej, wzrost objętości o ok. 1%
•
Ze względu na gęstsze ułożenie atomów w
austenicie niż w ferrycie- szybkość dyfuzji w
austenicie jest mniejsza niż w ferrycie w tej
samej temperaturze
•
Dla przykładu: współczynnik samodyfuzji
żelaza w Fe-α jest około 10
2
razy większy niż w
Fe-γ
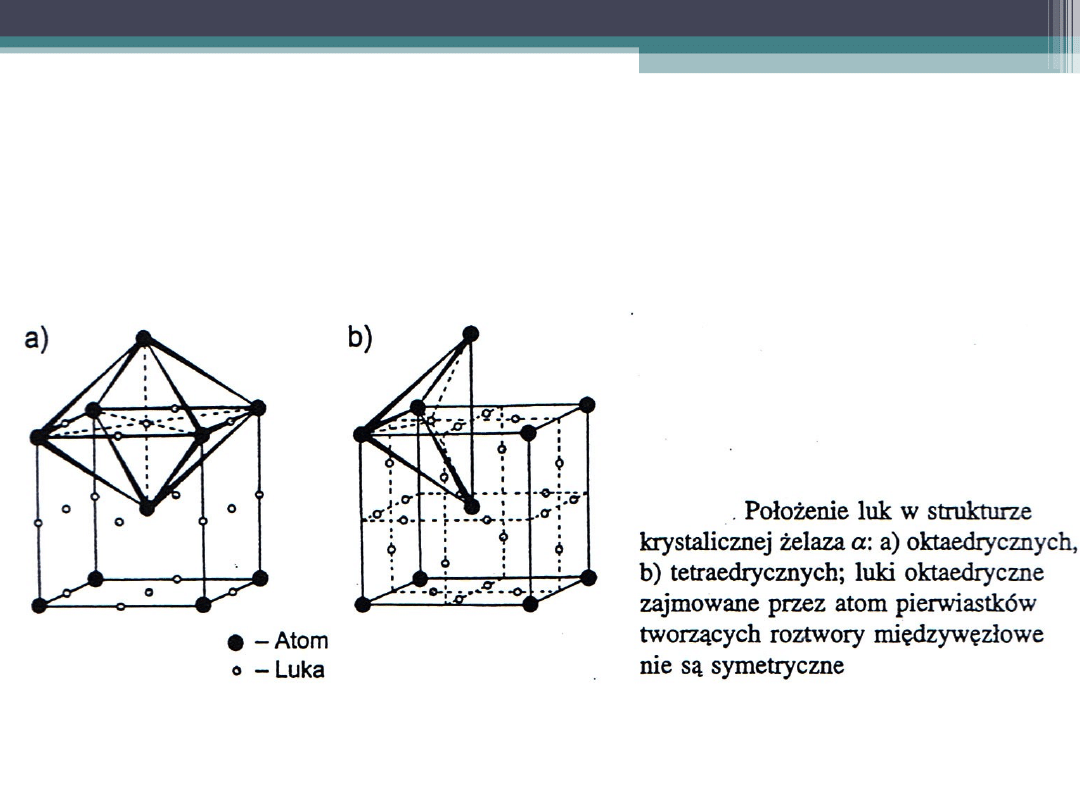
POŁOŻENIE LUK W KOMÓRKACH
ELEMENTARNYCH ŻELAZA α
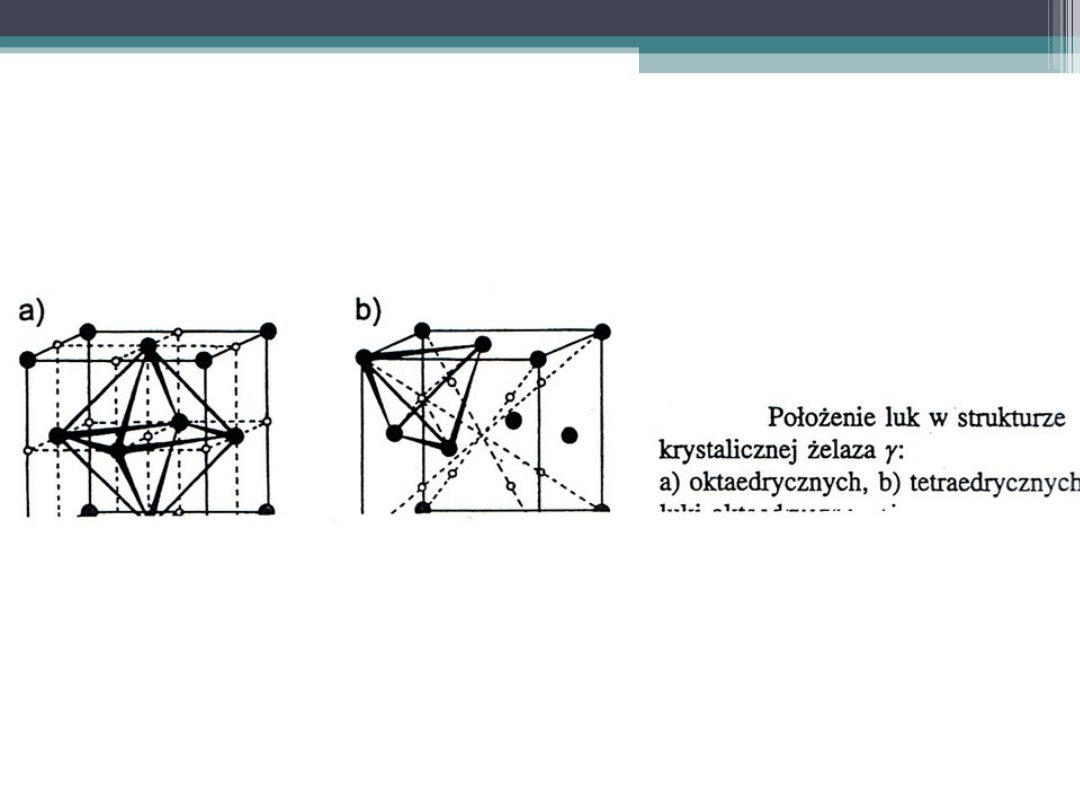
POŁOŻENIE LUK W KOMÓRKACH
ELEMENTARNYCH ŻELAZA γ

WNIOSKI
•
W obu rodzajach struktur krystalicznych żelaza
atomy pierwiastków tworzących roztwory
międzywęzłowe zajmują luki oktaedryczne
•
W żelazie γ luki oktaedryczne są symetryczne
(znajdujące się w nich atomy akładnika
rozpuszczonego powodują jedynie zmianę
objętości komórki)
•
W żelazie α luki oktaedryczne nie są
symetryczne (luka jest w jednym kierunku
znacznie mniejsza niż w dwóch pozostałych)

WNIOSKI c.d.:
•
Austenit stabilny w wysokiej temperaturze
charakteryzuje się względnie dużą
rozpuszczalnością węgla
•
Ferryt stabilny w niskiej i wysokiej
temperaturze charakteryzuje się znacznie
mniejszą rozpuszczalnością atomów
międzywęzłowych (ze względu na mniejsze
luki oktaedryczne między atomami żelaza w
strukturze krystalicznej ferrytu)
•
W temperaturze przemiany eutektoidalnej
(727°C) rozpuszczalność węgla w austenicie
jest 35 razy większa niż w ferrycie

WNIOSKI c.d.:
•
Duża różnica w rozpuszczalności oraz duże
zniekształcenie struktury krystalicznej RPC przez
atomy międzywęzłowe ma bardzo duże znaczenie
praktyczne
•
Podczas chłodzenia austenitu z temperatury jego
stabilności do temperatury, w której przestaje być
stabilny, tworzy się mechanizmem dyfuzyjnym
(ferryt staje się ubogi w węgiel oraz węgliki)
•
Znaczne różnice w rozpuszczalności węgla w
ferrycie i w austenicie oraz bardzo duże
umocnienie w roztworze ferrytu atomami węgla
są wykorzystane do zwiększenia wytrzymałości
stali przez obróbkę cieplną

DZIĘKUJĘ ZA
UWAGĘ
Document Outline
Wyszukiwarka
Podobne podstrony:
BADANIA MIKROSKOPOWE STOPÓW ŻELAZA żeliwa pw plock
Badanie mikrostruktury stopów żelaza
Mikrostruktura stopów żelaza
BADANIA MIKROSKOPOWE STOPÓW ŻELAZA żeliwa pw plock
Ferryt jako składnik strukturalny stopów technicznych na osnowie żelaza ma zwykle budowę
wyklad IV
Prezentacja wykłady I IV
Wykład IV Model Portera
E Tezy pedagogiki Marii Montessori Ped przedszk wykład IV
WYKŁAD IV(1)
WYkład IV 4
Wykład IV Ubezpieczenia dla przedsiębiorstw
Ogolnotech dla Bio I WYKLAD IV
więcej podobnych podstron