
wybrane zagadnienia z diagnostyki
koagulologicznej
Jadwiga Hartwich

Diagnostyka laboratoryjna w hemostazie
Pod red. Prof. Jastrzębskiej
OINPHARMA Warszawa2009
Biblioteka diagnosty laboratoryjnego
MERCK Manual
Podręcznik diagnostyki i terapii, IIIwydanie polskie,
Elsevier, Urban&partner Wrocław 2006.

Czynniki krzepnięcia
• Czynnik I fibrynogen
• Czynnik II protrombina
• Czynnik III tromboplastyna tkankowa TF, cz.
tkankowy
• Czynnik IV jony wapnia
• Czynnik V proakcerelyna
• Czynnik VII prokonwertyna
• Czynnik VIII antyhemofilowy (kofaktor
aktywacji X)
• Czynnik IX przeciwhemofilowy B, czynnik
Christmas
• Czynnik X Stuarta -Prowera
• Czynnik XI przeciwhemofilowy C
• Czynnik XII czynnik kontaktu (Hagemana)
start u.wewnątrzpochodnego
• Czynnik XIII stabilizujący fibrynę,
fibrynoligaza, Laki-Lorand

Kompleks białka C i S tworzy tzw.
aktywowane białko C (ang.:
Activated Protein C; APC). Inicjatorem procesu aktywacji
jest trombina (T), która łączy się z glikoproteiną śródbłonka
–
trombomoduliną
(TM).
Dopiero
kompleks
trombina/trombomodulina uczynnia białko C
APC jest “języczkiem u wagi” między układem krzepnięcia i
fibrynolizy. APC unieczynnia czynniki Va i VIIIa (hamowanie
krzepnięcia), natomiast aktywuje fibrynolizę poprzez
nasilenie wytwarzania plazminy drogą unieczynniania
inhibitora aktywatorów plazminogenu (PAI-1)
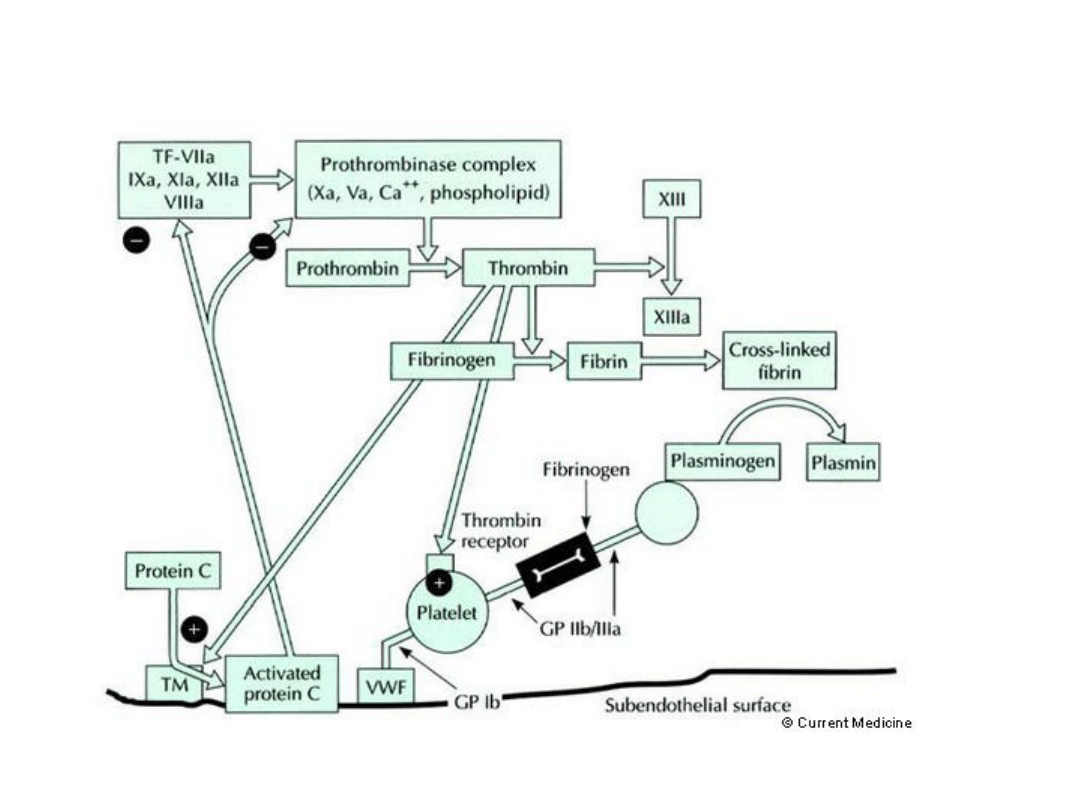
układ krzepnięcia – na
nowo
ocena układu osoczowego:
• PT
• APTT
• TT
• czas reptylazowy
(niezależny od heparyny/hirudyny)
• KCT
• czas diluted Russel Viper Venom Time
(aktywacja IX, X)
• czas batroxobinowy (Bothrops atrox)
(fibrynopeptyd A)
• czas ekarynowy ECT (Echis carinatus
ThrmeizoThr, hirudin anticoag. in HIT)
ocena markerów aktywacji:
• fragmenty protrombiny 1+2 (F 1+2)
• kompleksy trombina - antytrombina III
(TAT)
• monomery fibryny
• fibrynopeptydy A i B
• D-dimery
ocena poszczególnych
czynników
krzepnięcia:
• aktywność
• stężenie
inhibitory układu osoczowego:
• antytrombina III
• białko C
• białko S
• inhibitory patologiczne
układ osoczowy
testy koagulologiczne
ocena płytek:
• ilość
• objętość
• PDW (wskaźnik anizocytozy płytek)
ocena czynników płytkowych:
• czynnik płytkowy 3 (PF3)
• czynnik płytkowy 4 (PF4)
• -tromboglobulina
funkcja płytek:
• czas krwawienia
• retencja (adhezja)
• agregacja
• stopień retrakcji skrzepu
ocena globalna
• globalna aktywność fibrynolityczna
• czas lizy euglobulin
• czas trombinowy
• czas reptylazowy (batroxobinowy)
• pojemność fibrynolityczna po stazie żylnej
ocena poszczególnych czynników
fibrynolizy:
• plazminogen
• t-PA
markery fibrynolizy:
• kompleksy plazmina-a2-antyplazmina (PAP)
• produkty degradacji fibrynogenu i fibryny
inhibitory fibrynolizy:
• a2-antyplazmina
• inhibitor aktywatorów plazmiinogenu (PAI)
• C1-inhibitor
płytki
fibrynoliza
testy koagulologiczne

wspólna nazwa grupy produktów degradacji fibryny połączonych
wiązaniem kowalencyjnym przez cz. XIIIa
D-dimery
nieprawidłowe wyniki D-dimerów stwierdza się w:
• zakrzepicy żył głębokich
• DIC
• zakrzepicy tętniczej
• zatorowości płucnej
ponadto monitorowanie D-dimerów stosuje się w:
• terapii trombolitycznej
• nowotworach (rak jajnika)
• powikłanym zawale serca
• choroby nerek
testy koagulologiczne

Pochodne
dihydroksykumaryny
(np.
warfaryna
i
acenokumarol) lub fenylinandionu, które wchodzą w skład
antykoagulantów doustnych, są antymetabolitami
witaminy K.
Podczas leczenia tymi środkami białko C, białko S oraz
czynniki II, VII, IX, X nie ulegają obróbce
posttranslacyjnej
(czyli
gamma-karboksylacji
N
końcowych reszt glutaminowych) w wątrobie i tym
samym nie wykazują normalnej aktywności w hemostazie
(mimo, że mierzone jako antygeny mogą wykazywać swój
prawidłowy poziom w osoczu).
Najprostszym i najczęściej stosowanym oznaczeniem w
kontroli leczenia antykoagulantami doustnymi jest czas
protrombinowy (PT) i jego pochodne współczynniki.
• historycznie najbardziej wiarygodny i najczęściej używany
test kliniczny monitorujący leczenie antykoagulantami
ograniczenia:
– duża ilość odczynników do jego wykonywania na rynku o
różnej czułości na zmniejszone ilości czynników krzepnięcia
zależnych od wit. K
– aktualna koncepcja leczenia przeciwkrzepliwego mówi o
niskiej jego “intensywności”
– powyższe problemy rozwiązane przy pomocy zastosowania
INR (International Normalized Ratio)
monitorowanie leczenia antykoagulantami doustnymi
testy koagulologiczne
czas protrombinowy PT
J Clin Path 1985; 38:133-134; WHO Tech Rep
J Clin Path 1985; 38:133-134; WHO Tech Rep
Ser. #687 983.
Ser. #687 983.
• matematyczna “korekta” współczynnika
protrombinowego do różnic w czułości poszczególnych
tromboplastyn
• jest oparty na tromboplastynach refeeerencyjnych o
ustalonej czułości i zastosowaniu
• INR jest współczynnikiem protrombinowym, który
uzyskanoby stosując referencyjną tromboplastynę
• pozwala na standaryzację wyników pomiędzy
laboratoriami oraz pozwala na porównanie
współczynników protrombinowych
monitorowanie leczenia antykoagulantami doustnymi
testy koagulologiczne
INR

(
(
)
)
PT pacjenta (s)
PT pacjenta (s)
średni normalny PT (s)
średni normalny PT (s)
INR =
INR =
ISI
ISI
INR = International
Normalized Ratio
ISI = International
Sensitivity Index
monitorowanie leczenia antykoagulantami doustnymi
testy koagulologiczne
INR
monitorowanie leczenia heparyną
testy koagulologiczne
dostępne metody monitorowania
1. testy niespecyficzne
• APTT
• TT
• ACT
2. oznaczenie specyficznego
hamowanie aktywności IIa oraz Xa
• chronometryczne (aktywność koagulacyjna)
• amidolityczne (aktywność enzymatyczna)

Heparyna to kofaktor jednego z najważniejszych naturalnych
inhibitorów kaskady krzepnięcia – antytrombiny (AT).
Najpowszechniej stosowanym sposobem monitorowania leczenia
heparyną niefrakcjonowaną jest oznaczanie czasu częściowej
tromboplastyny
po
aktywacji
(aPTT)
(jeśli
użytym
aktywatorem krzepnięcia jest kaolin, to określa się go czasem
kaolinowo-kefalinowym)
Heparyny frakcjonowane
Są to cząsteczki o średniej masie 3200-6500. Skrócenie
łańcucha polisacharydowego (zwłaszcza poniżej 18 reszt
cukrowcowych) powoduje większe powinowactwo tych heparyn
do cz. Xa, natomiast znacznie mniejsze działanie inaktywujące
trombinę (cz IIa) (brak sekwencji pentasacharydowej – kofaktora
AT ). Stąd nie można monitorować działania tych leków za
pomocą aPTT, a zmiany aPTT, TT czy czasu krzepnięcia
występują dopiero przy bardzo wysokich stężeniach heparyn
frakcjonowanych we krwi.

monitorowanie leczenia heparyną
testy koagulologiczne
ACT
(activated clotting time)
czas krzepnięcia po aktywacji
czas krzepnięcia krwi pełnej w probówce zawierającej celit bądź związki
metali dwuwartościowych (aktywator czynnika XII) w temperaturze 37C.
zastosowanie:
kardiologia interwencyjna
zwłaszcza przy zastosowaniu inhibitorów
Gp IIb/IIIa (abciximab)
operacje z krążeniem pozaustrojowym
dializa
afereza
neutralizacja działania heparyny
protaminą
norma < 120 s
zakres terapeutyczny ok.
300 s
zalety:
szybkość i prostota wykonania
standaryzacja
terapia przeciwzakrzepowa
inhibitory glikoproteiny IIb/IIIa
przeciwciała:
abciximab
chimera Fab c7E3 hamująca specyficznie płytkowy receptor sekwencji
RGD obecnej na fibrynogenie (łańcuch A i ), vWF, fibronektynie
zastosowanie kliniczne:
udowodnione zmniejszenie powikłań i śmiertelności
po interwencjach endowaskularnych w kardiologii (badania EPIC)
analogi peptydowe i nie-peptydowe RGD:
eptifibatide
heptapeptyd o mniejszym powinowactwie do GpIIb/IIIa od abciximabu
tirofiban
analogi niepeptydowe o krótszym okresie półtrwania
xemilofiban
orofiban
zastosowanie kliniczne:
udowodnione zmniejszenie powikłań i śmiertelności w niestabilnej dusznicy bolesnej
bez konieczności interwencji (badania PRISM, PURSUIT)
brak efektu w PTCA, zwiększenie śmiertelności w grupie badanej (badania EXCITE, OPUS)
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
Wyszukiwarka
Podobne podstrony:
Wybrane zagadnienia z diagnostyki pedagogicznej - ściąga (ćwiczenia), Resocjalizacja, wybrane zagadn
Wybrane zagadnienia diagnostyki chorób układu żylnego, Z innych uczelni CHIRURGIA
Wybrane zagadnienia diagnostyki chorób układu żylnego
Wybrane zagadnienia prawa Pedagika Specjalna 2 ppt
2 Wybrane zagadnienia statyki plynowid 19736 ppt
2 Wybrane zagadnienia statyki płynówid 19729 ppt
Podstawowe badania w diagnostyce chorób układu moczowego oraz wybrane choroby układu moczowego ppt
2 Wybrane zagadnienia statyki płynów 4id 19733 ppt
pedagogika resocjalizacyjna Wybrane zagadnienia teoretyczne, diagnostyczne i metodyczne
2 Wybrane Zagadnienia Statyki Płynów 5id 19734 ppt
Podstawy teoretyczne oraz wybrane zagadnienia z zakresu diagnozy zaburzeń integracji sensoryczne(1)
WYBRANE SCHORZENIA DIAGNOSTYKA ppt
Wybrane zagadnienia prawa Pedagika Specjalna 2 ppt
05 Badanie diagnostyczneid 5649 ppt
Wybrane zagadnienia prawa3
Wakcynologia – wybrane zagadnienia
więcej podobnych podstron