
Dylewski Paweł
Gajowski Robert

Izomerazy to enzymy przekształcające
cząsteczkę w jej izomer, czyli zmieniające
układ atomów w cząsteczce
Nie dodają one, ani nie odcinają żadnych
atomów. Jedynie zmieniają ich układ w
cząsteczce
Przenoszone mogą być zarówno pojedyncze
atomy jak i ich całe grupy.
Ogólna reakcja: AB -> BA

Izomeraza glukozowa należy do klasy
izomeraz (EC 5), jest intramolekularną
oksydoreduktazą (EC 5.3) i konwertuje
aldozy i ketozy (EC 5.3.1), oraz jest piąta w
swojej klasie.
EC 5.3.1.5
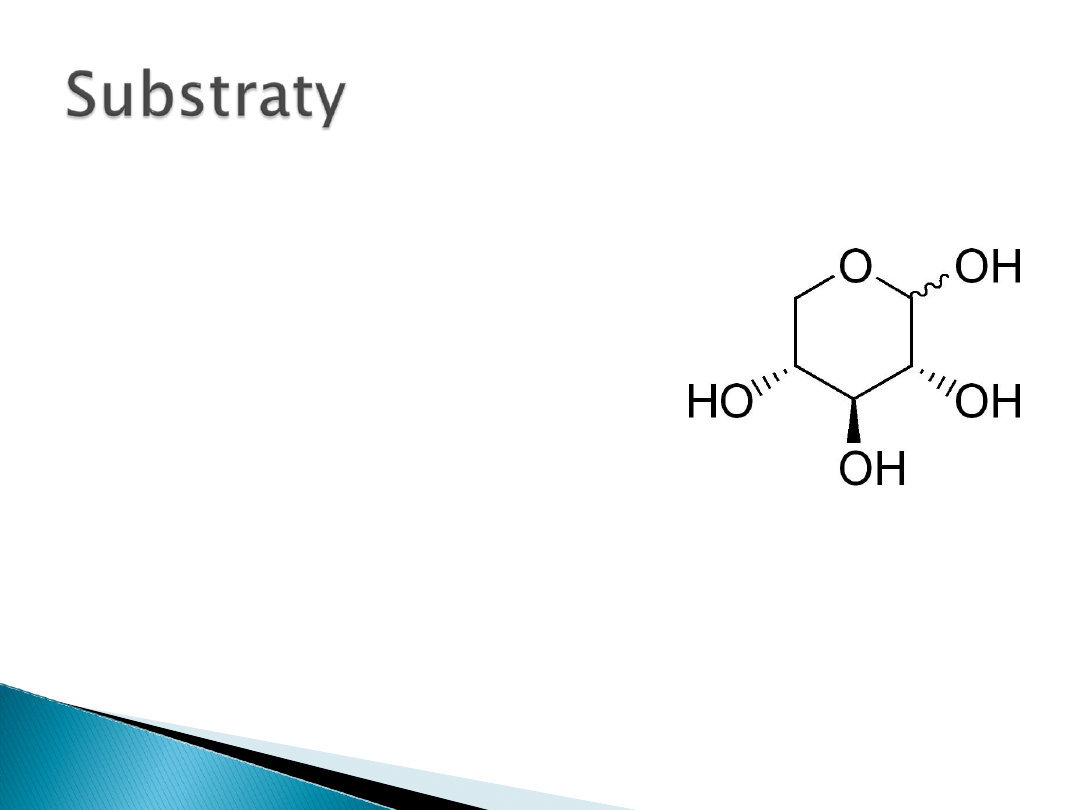
Izomeryzowane substancje:
Glukoza do fruktozy
Fruktoza do glukozy
Ksyloza do ksylulozy
Ksyloza - węglowodan, monosacharyd
wchodzący w skład hemiceluloz w postaci
ksylanów.

D-ksylozo izomeraza
D-ksylozo ketoizomeraza
D-ksylozo ketol-izomeraza
Nazwa systematyczna: D-ksylozo aldozo-
ketozo-izomeraza
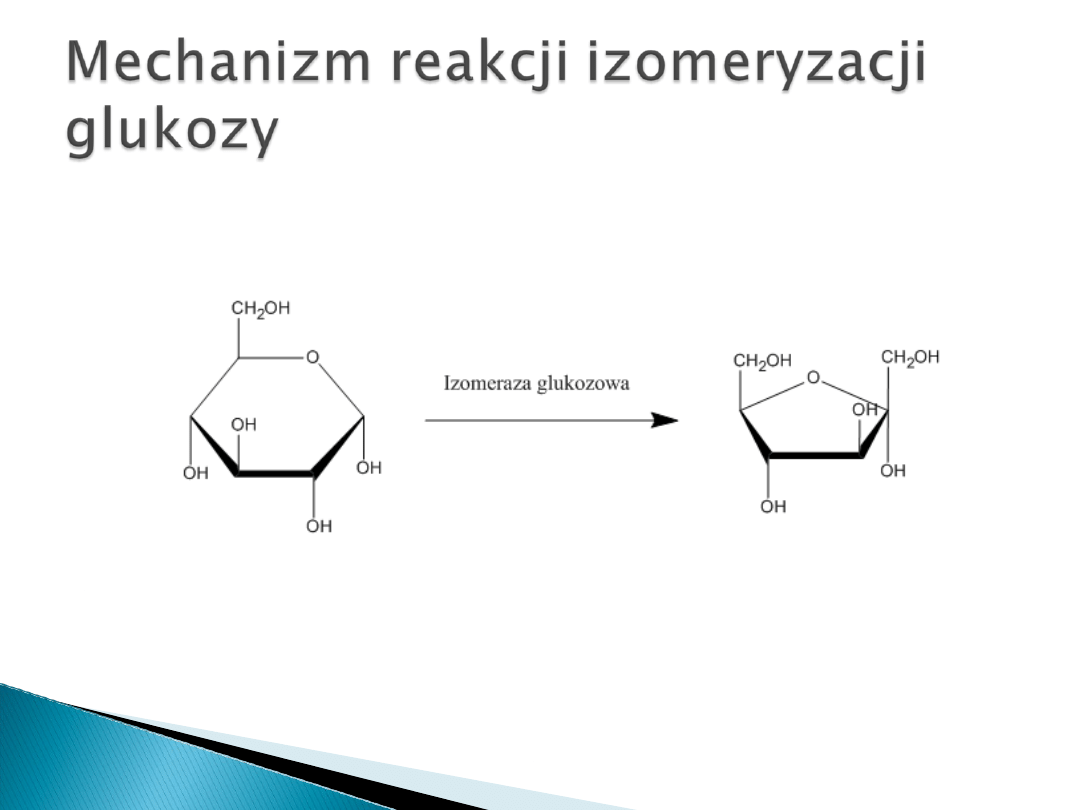

Mikroorganizmy:
Streptomyces sp. (np. actinoplanes)
Lactobacillus sp. (np. L. brevis)
Bacillus sp. (np. B. coagulans)
Paracolobactrum sp.
Clostridium sp. (np. C. thermosulfurogenes)

Źródło bakterii :
gorące źródła w
parku narodowym
Yellowstone
Enzym: termostabilna
izomeraza
glukozowa

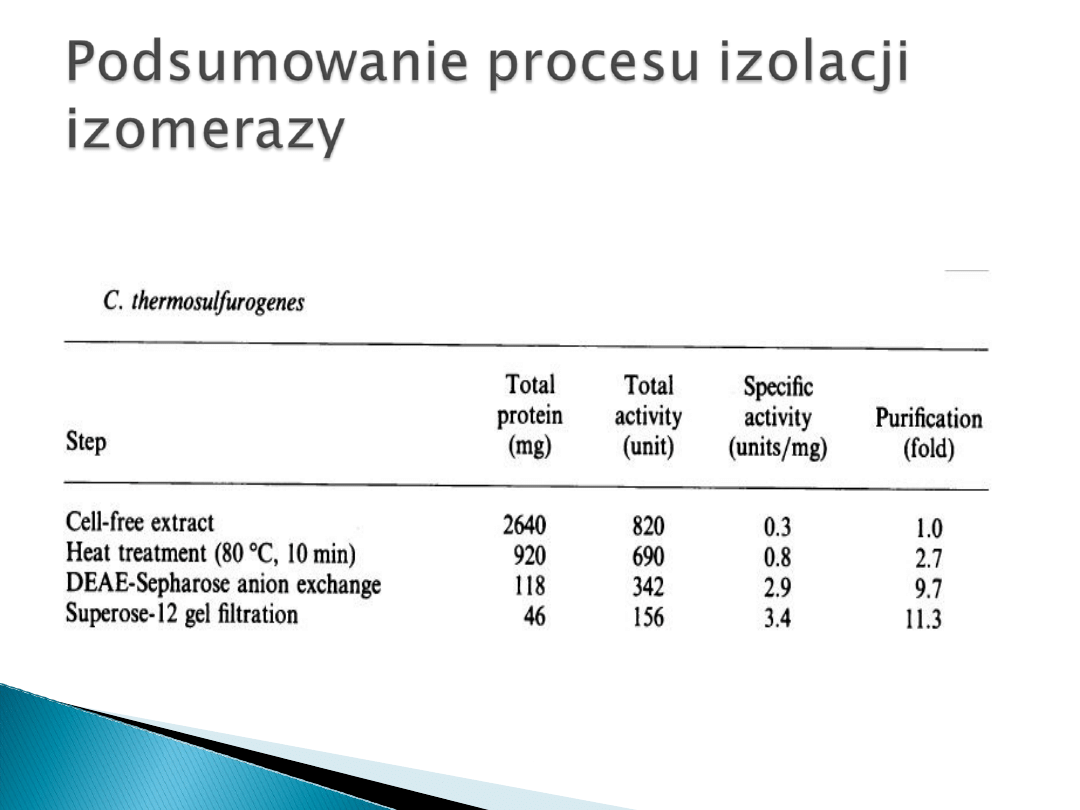
Etapy:
Przygotowanie ekstraktu komórkowego
Ogrzewanie
Frakcjonowanie
Chromatografia kolumnowa
Całość przeprowadzamy w warunkach
tlenowych i 4
oC

50g komórek zawieszamy w 200ml 50 mM
buforu Mops
(3-morfolinopropanosulfonowy), 10mM
MgSO
4
, 1 mM CoCl
2
Dezintegracja prasą Francuską przy 124MPa
Odwirowanie przy 12000g, 20 min.
Zebranie supernatantu

Ogrzewanie supernatantu w termobloku, w
temperaturze 80
o
C
Ochłodzenie do 4
o
C
Odwirowanie przy 12000g przez 20 min

Dodanie stałego siarczanu amonu do
ogrzewanego ekstraktu w celu uzyskania
65% saturacji
Wytrącający się osad usunięto przez
odwirowanie 20000g przez 30 min.
Dodano kolejną porcję siarczanu, 85%
saturacja
Zebrano osad, zawieszono w buforze Mops i
dializowano przez noc w tym samym
buforze

Użyte złoże: DEAE-Sepharose CL-6B
Bufor Mops
Gradient chlorku sodu (0-0.5 M) do
przemywania
Następnie dokonano:
Ultrafiltracji
Filtracji żelowej

SDS-Page
Ogniskowanie izoelektryczne
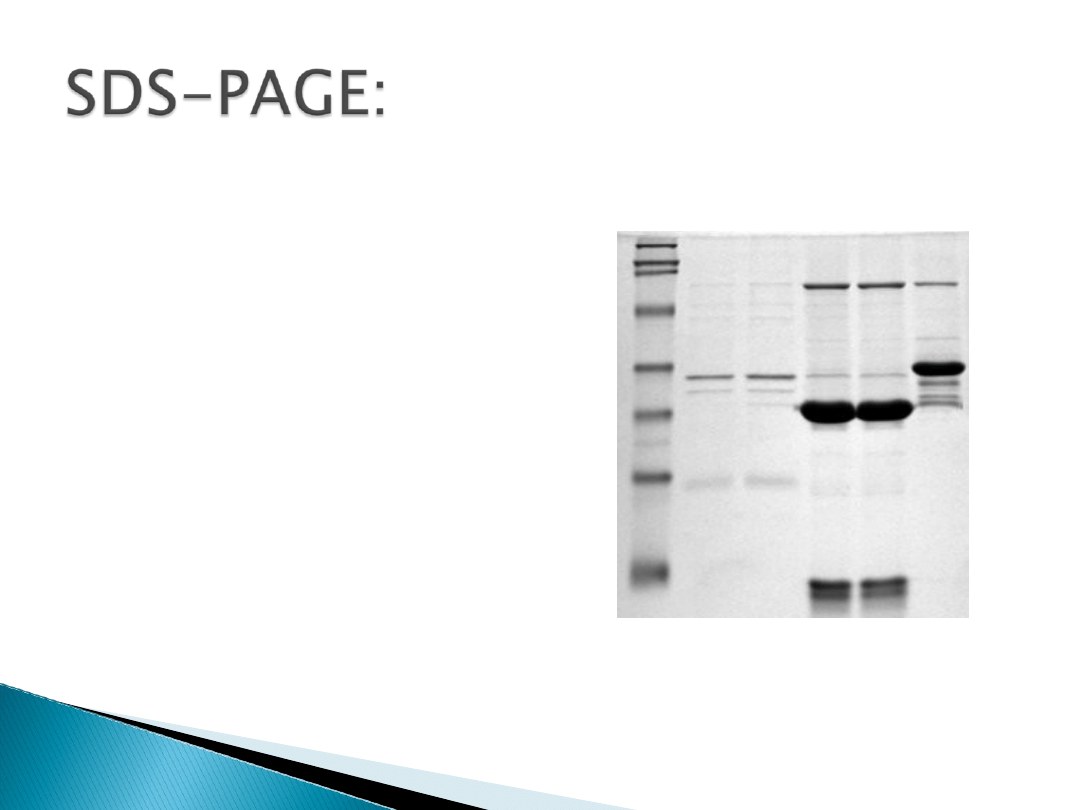
Elektroforeza w żelu
denaturującym
pozwala na rozdział
cząstek pod
względem wielkości.
Uzyskanie
pojedynczego paska
świadczy o czystości
produktu.

Pozwala na rozdział
białek ze względu
na ich punkt
izoelektryczny.
Otrzymanie
pojedynczego paska
świadczy o
czystości produktu.

1ml mieszaniny reakcyjnej (0.8 M-glukoza,
10 mM-MgSO
4
, 1 mM-CoCI
2
i preparat
enzymatyczny w buforze 100 mM-Mops)
inkubowano w temp. 65
o
C przez 30 min.
Po tym czasie dodano 1ml 0.5M HClO
4
dla
zatrzymania reakcji
Do pomiaru glukozy wykożystano
amperometryczny czujnik enzymatyczny

Stałe te uzyskano z wykresu Lineweavera-
Burka
Jest to funkcja 1/rs=f(1/Cs), gdzie Cs to
stężenie substratu, a rs to zmiana tego
stężenia w czasie
Pomiarów dokonano w 65
o
C, dla 3 różnych
substratów
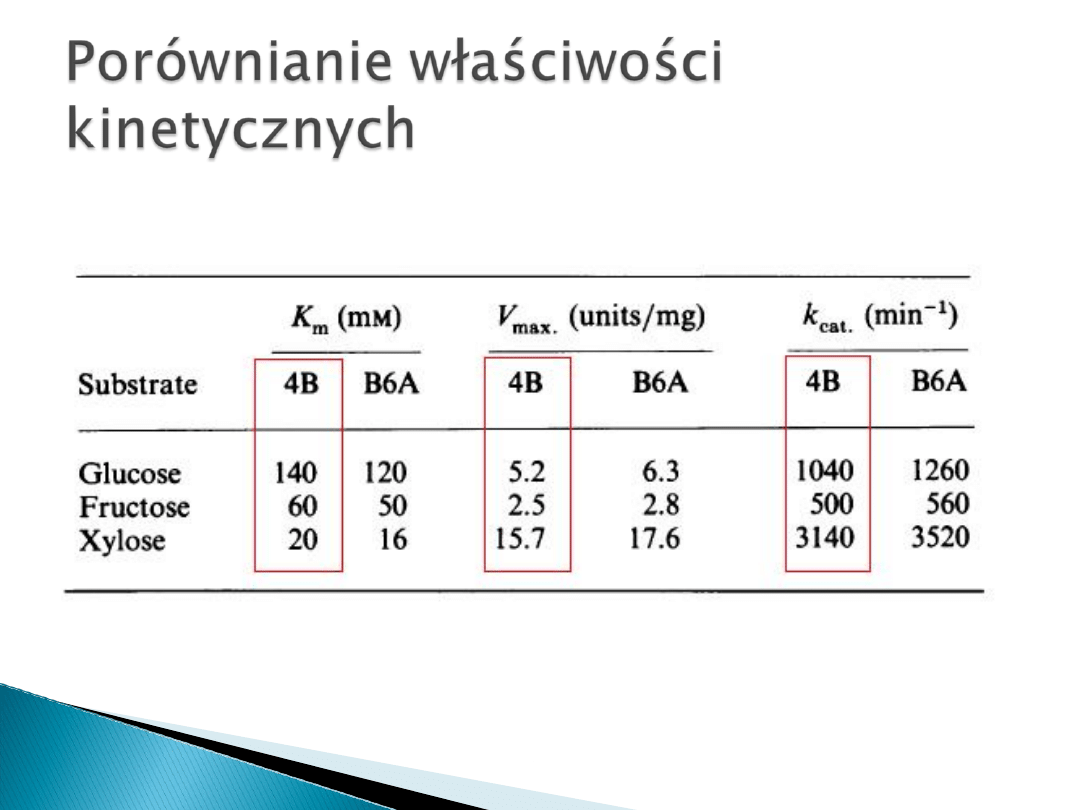

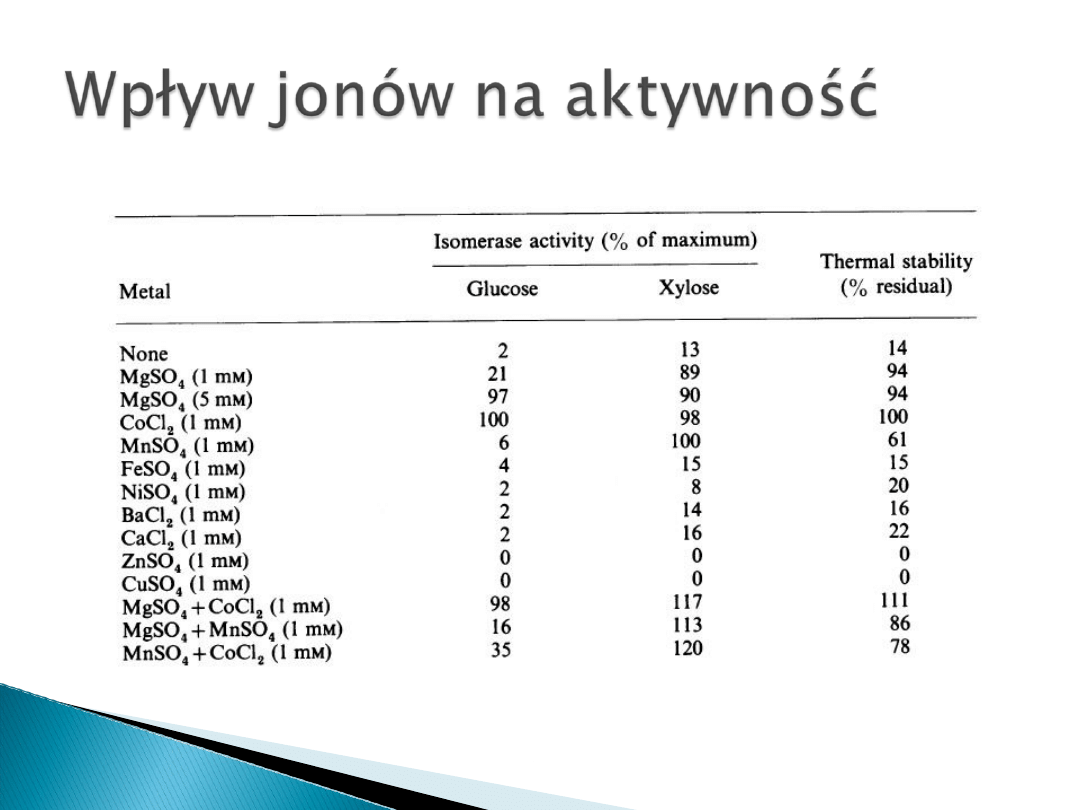
Na izomeryzację glukozy:
Do aktywności wymagane są jony Co
2+
albo
Mg
2+
Na izomeryzację ksylozy:
Do aktywności wymagane są jony Mn
2+
(1mM), Co
2+
(1 mM) albo Mg
2+
(1 mM)

Zarówno na izomeryzację glukozy jak i
ksylozy inhibicyjny wpływ mają jony Zn
2+
i
Cu
2+
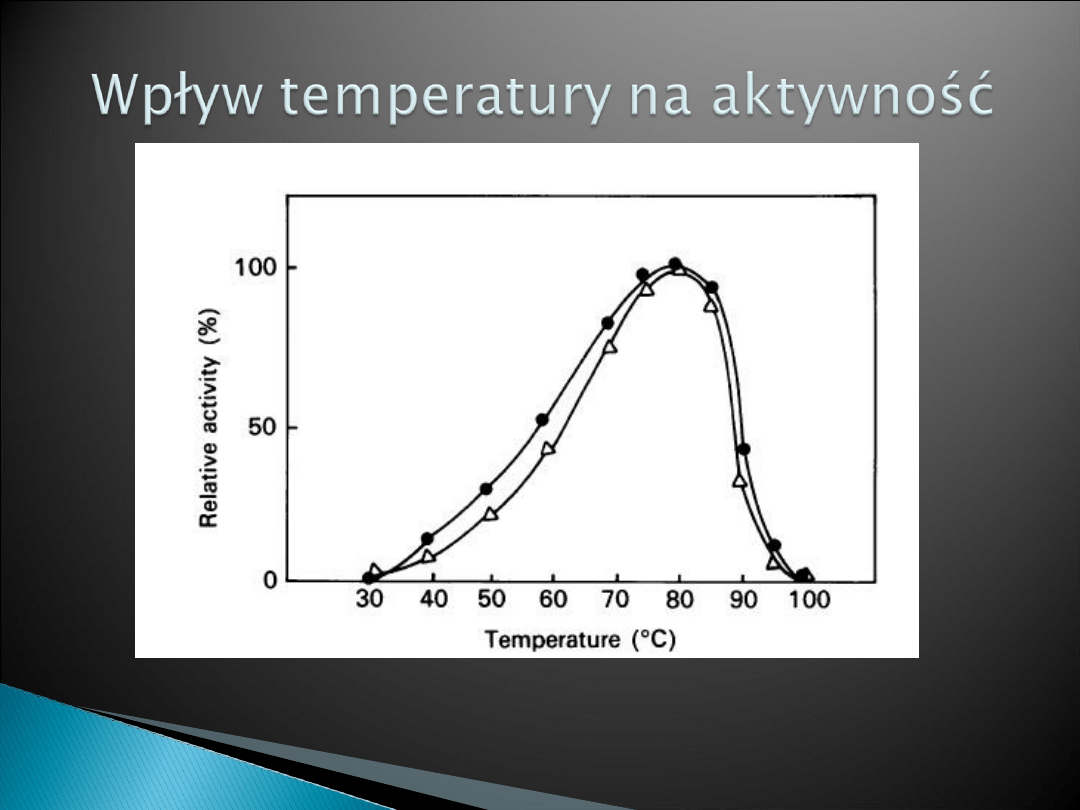
Kropka to C.thermosulfurogenes
100% aktywności = 7.1 U/mg
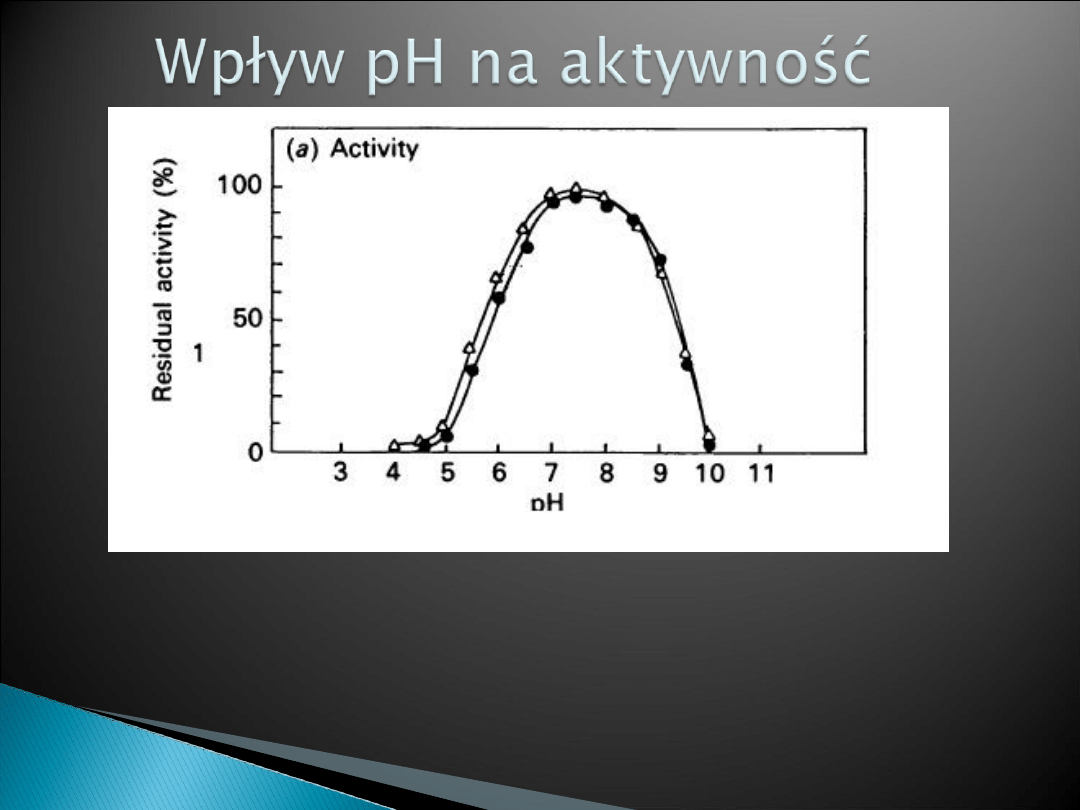
Kropka to C.thermosulfurogenes
100% aktywności = 4.5 U/mg
użyto buforów: glicyloglicynowego(pH 3.0-4.5) i
Mops
(pH 6.5 – 8.6)
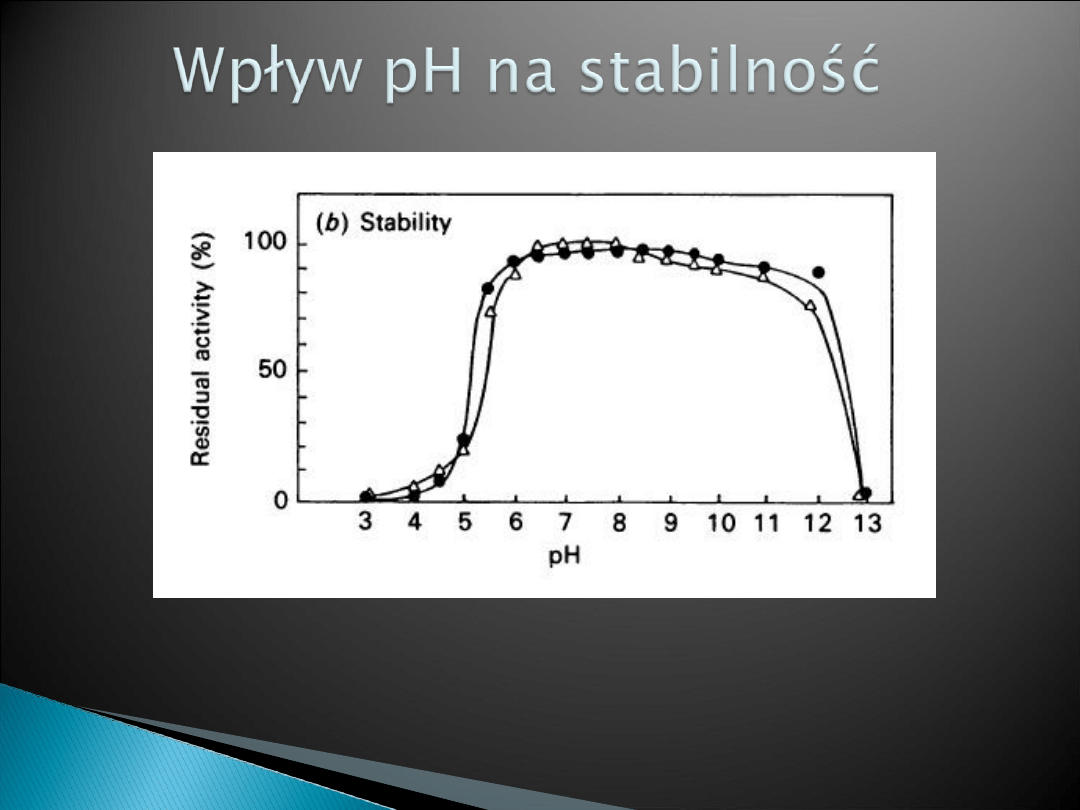
Kropka to C.thermosulfurogenes


Przemysł spożywczy – produkcja syropu
glukozowego zawierającego fruktoze
Wykożystanie: lody,ciasta, napoje, słodycze

Przemysł gorzelniczy:
Ksyluloza – źródło
węgla dla
fermentujących
drożdży
Proces SFIX -
Jednoczesna
Fermentacja i
Izomeryzacja Ksylozy.

Źródła internetowe
Internetowe bazy danych(NC-IUBMB,BRENDA)
Purification and characterization of
thermostable glucose isomerase from
Clostridium thermosulfurogenes and
Thermoanaerobacter strain B6A, Chanyong
LEE, J. Gregory ZEIKUS, Biochem. J. (1991)
273, 565-571
CHEMIA BIOORGANICZNA P. Kafarski B.
Lejczak
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
Wyszukiwarka
Podobne podstrony:
Wyznaczanie stałych równania kinetycznego reakcji izomeryzacji D – glukozy do D fruktozyx
Bryjak, inżynieria bioreaktorów L, reakcja izomeryzacji D glukozy do D fruktozy teoria
Izomeraza sprawko, [3] Izomeraza glukozowa
bioreaktory sprawko cegła, inżynieria bioreaktorów lab, [3] Izomeraza glukozowa, nie moje
instrukcja reaktory przepływowe-izomeraza[2011], [3] Izomeraza glukozowa
Wyznaczanie stałych równania kinetycznego reakcji izomeryzacji D – glukozy do D fruktozy(1)
izomeria optyczna
izomeria zwiazkow organicznych
Filtracja,resorpcja zwrotna i wydalanie glukozy z moczem
Syrop glukozowo fruktozowy
Izomeria związków organicznych
Izomeria(1)
Transportery glukozy, Ratownicto Medyczne, BIOCHEMIA
Izomeryzacja ostateczna wersja
Cukrzyca i inne zaburzenia przemiany glukozy
Izomeria 4 id 221207 Nieznany
Izomeria konformacyjna
glukoza polarymetria
więcej podobnych podstron