
22.06.21
1
Zaburzenia gospodarki
kwasowo – zasadowej
rozpoznawanie i leczenie.

22.06.21
2
Organizm ludzki utrzymuje w warunkach
fizjologicznych stałe stężenie jonów H
+
we krwi
( izohydria ) wynoszące 35-45 mml/l
( pH =7.45 –7.35 ), pomimo stałej generacj H
+
dzięki obecności 2 pozakomórkowych i 2
śródkomórkowych układów buforowych.
W przestrzeni wodnej pozakomórkowej
są to
układy buforowe – wodorowęglanowy i
białczanowy.
W przestrzeni wodnej śródkomórkowej
są to
układy buforowe – fosforanowy i
hemoglobinianowy.

22.06.21
3
Układy buforowe ustroju ludzkiego.
Wodorowęglanowy.
Białczanowy.
Hemoglobinianowy.
Fosforanowy.

22.06.21
4
Układ buforowy wodorowęglanowy.
łatwość usuwania przez płuca produktu
odwodnienia kwasu węglowego (CO
2
)
reakcja przebiega w układzie otwartym
– szybkie usuwanie (CO
2
) drogą płuc
sprawia ,że stanowi on najważniejszy
układ buforowy płynu
pozakomórkowego zapewniając
izohydrię

22.06.21
5
Układ buforowy fosforanowy.
główny układ buforowy
wewnątrzkomórkowy
w warunkach wzmożonego powstawania
jonów H
+
fosforan
dwuzasadowy( Na
2
HPO
4
) wiążąc jeden
jon H
+
przekształca się w fosforan
jednozasadowy (NaH
2
PO
4
)
fosforan jednozasadowy ulega wydaleniu
przez nerki

22.06.21
6
Układ białczanowy
.
Stanowią go w roztworze kwaśnym
grupy zasadowe a w roztworze
zasadowym grupy fenolowe
aminokwasów białek
Stanowią ważny
wewnątrzkomórkowy układ
buforowy

22.06.21
7
Układ hemoglobinianowy
jest najważniejszym układem
buforującym wśród białek ( Hg
stanowi ¾ całego białka krwi

22.06.21
8
Pojęcia podstawowe.
Odczyn roztworu – pH.
Według teorii Bronsteda kwasem nazywamy
cząsteczki, które mają zdolność oddawania
jonów H
+
czyli są dostawcami protonów a
zasadami substancje, które przyłączają jony H
+
czyli są ich biorcami.
NH
3
+ H
+
NH
4
(zasada )
HCO
3
+ H
+
H
2
0 + C0
2
( zasada )

22.06.21
9
pH = - log ( H
+
)
Krytyka pojęcia pH roztworu:
-wartość stężenia jonów H
+
w skali pH odzwierciedla skalę logarytmiczną
spadek pH z 7.7 do 7.4 powoduje wzrost stężenia
H
+
z 20 d0 40 nmol/l
spadek pH z 7.4 d0 7.1 wzrost stężenia H
+
z 40
do 80 nmol/l

22.06.21
10
Równanie Hendersona _ Hasselbacha.
pH = pK + log HCO
3
-
H
2
C03
pH = 6.1 + log HC0
3
pC0
2
x0.03
Gdzie pC0
2
=mmHg
komponenta
metaboliczna
komponenta
oddechowa

22.06.21
11
Normy.
pH 7.36 – 7.44
pC0
2
33-44 mmHg
stand. HCO
3
22-26 mmol/l
BE +/- 2 mmol/l
p0
2
75 – 100 mmHg

22.06.21
12
pH -
największą przydatność kliniczną ma
pomiar pH krwi tętniczej lub arterializowanej krwi
włośniczkowej
stand. HCO
3
– oznacza stężenie wodorowęglanów
w osoczu uzyskanym z krwi całkowicie
utlenowanej i wysyconej dwutlenkiem wegla prz
ciś. cząstkowym 40 mmHg w tem. 37
o
C
BE – nadmiar zasad
, określa tę ilość kwaśności
lub zasadowości miareczkowej jaką uzyskuje się
miareczkując roztwór do pH = 7.40 prz pCO
2
40
mmHg w tem. 37
o
C.
Jeżeli BE jest ujemne oznacza to nadmiar
kwasów nielotnych lub deficyt zasad.

22.06.21
13
Pojęcie luki anionowej.
Zgodnie z prawem elektroobojętności plynów
ustrojowych suma ładunków dodatnich w płynach
ustrojowych musi równać sumie ładunków
ujemnych. ( stęż kationów = stęż anionów ).
Norma 12 mEql +/- 4
LA =( Na
+
) – ( Cl
-
+ HCO
3
) .
Zwiększenie luki aninowej:
- zmniejszenia stężenia sumy kationów
( hipomagnezemia, hipokalcemia, hipokalemia)
-zwiększenia sumy anionów (kwasy –
acetooctowy, beta- hydroksymasłowy, mlekowy,
fosforowy i siarkowy: w zatruciach salicylanami,
paraldehydem, metanolem, glikolem etylenowym
)

22.06.21
14
Zmniejszenie luki anionowej.
-zwiększenie sumy kationów ( hiperkalemia,
hiperkalcemia, hipermagnezemia , gammapatie
monoklonalne IgG )
- zmniejszenie sumy anionów ( w
hipoalbuminemii )

22.06.21
15
Kationy mEq/l
Aniony mEq/l
K 4.5
Ca 5.0
Mg 1.5
Bialka 15
Fosforany 2
Siarczany 1
Kwasy
organiczne 5
Razem 11
mEq/l
Rzem 23 mEq/l
Stężenia kationów i anionów tworzących
lukę aninowa
.

22.06.21
16
Kliniczna wartość oznaczania luki anionowej.
Kwasica metaboliczna.
Z normalna luka aninową Ze zwiększoną luka
aninową
Z hiperchloremia ;
kwasica wywołana
biegunką, kwasica
kanalikowa
nerkowa,
nadczynność
przytarczyc,
diuramid, z
rozcieńczenia 0.9 %
NaCl
Z prawidł lub
zmniejsz stęż Cl –z
rozcień płyn
bezelektrolitowymi
Kw. endogenne:
ketonowe(cukrzycowa,
głodowa,
poalkoholowa),mleczan
owa, mocznicowa,
śpiączka cukrzyc.
Hipermolarna
Kw egzogenne:glikol
etylenowy, metanol,
salicylanu, kw.
mrówkowy i szczawiowy

22.06.21
17
Rola nerki w gospodarce kwasowo – zasadowej.
Rola nerek w gospodarce wydz.H
+
polega na:
- resorpcji zwrotnej wodorowęglanów
przesączonych w kłębuszkach nerkowych
( zachodzi dzięki wydzielaniu H
+
z kanalików
proksymalnych.
NaHC0
3
+ H
+
H
2
C0
3
+ Na
+
H
2
0 + CO
2
Na
+ ( do nerki )

22.06.21
18
- Regeneracja wodorowęglanów w procesie
wytwarzania kwaśności miareczkowej i
amoniogenezy
Kwaśność
miareczkowa.
Na
2
HP0
4
H
+
NaH
2
P0
4
+
Na
( do nerki )
Amoniogeneza.
NH
3,
H
+
,
NaCl
św. kanalika
Komórka
kanali.
mocz
Na
+
NH
4
Cl

22.06.21
19
Podział zaburzeń równowagi kwasowo-
zasadowej.
Wyróżniamy :
1. Zaburzenia oddechowe.
2. Zaburzenia metaboliczne.
3. Zaburzenia mieszane.
22.06.21
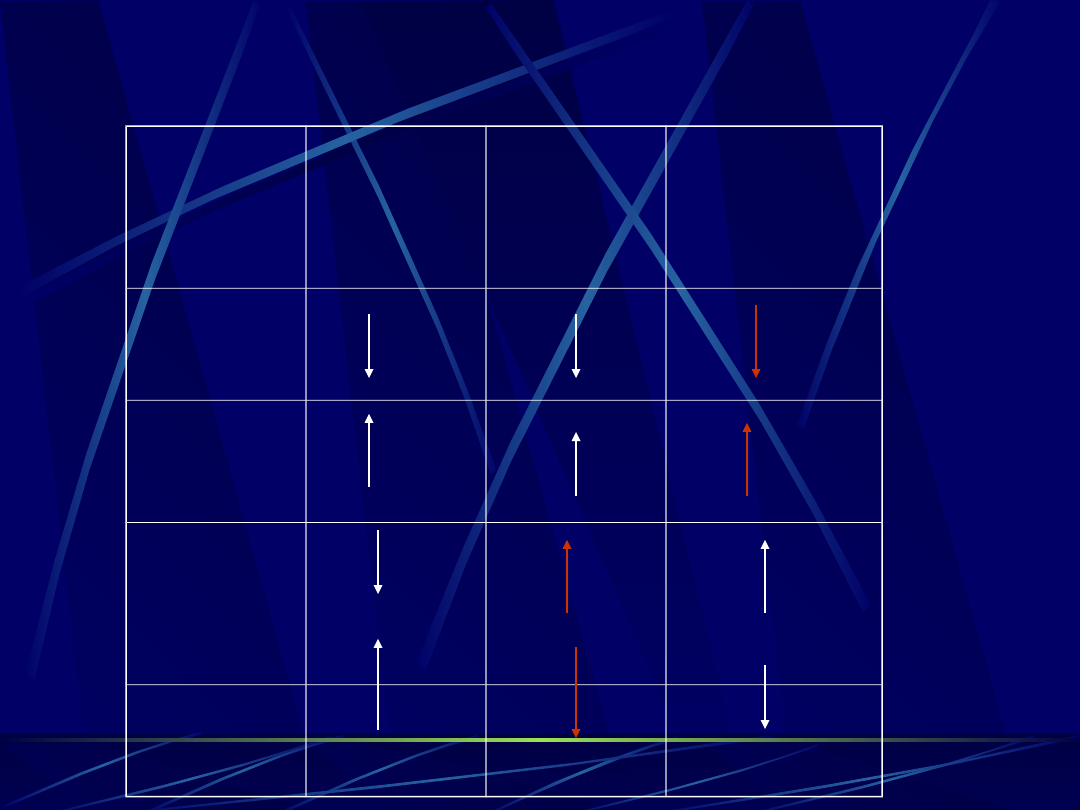
20
Rodzaj
zaburz
enia
pH
pCO
2
HCO
3
Kw.
Metab.
Zas.
Metab
Kw.
Oddec
h
Zas.
oddech
Zaburzenia równowagi kwasowo –
zasadowej .

22.06.21
21
Kwasica oddechowa.
Kwasica oddechowa ostra
– jest następstwem
retencji CO
2
wywołanej porażeniem nerwowej
regulacji oddychania(uszkodzenie pnia mózgu w
czasie niewłaściwie leczonej hiponatriemii,
porażenia ośrodka oddechowego lekami
_morfina, barbiturany, status epilepticus,
uszkodzenie górnego odcinka rdzenia
kręgowego, zespół Guillain- Barre, miasthenia
gravis,złamanie żeber, zapalenie płuc,odma
opłucnowa, obrzęk płuc,niedodma, ostra
niewydolność serca, choroba górska.

22.06.21
22
Obraz kliniczny.
Klinicznie –
dopiero gdy hipowentylacja
spowoduje hipoksemię i sinicę.
Objawy mózgowe- bóle głowy, senność, drżenie
mięśni, obrzęk tarczy n.II, zaburzenia
świadomości ( maska guza mózgu ).
Niebezpieczeństwo - zaburzenia rytmu serca,
migotanie komór.
Leczenie ;
1. Przyczynowe ( leczenie zapaleń , środki
wykrztuśne,)
2. W stanach zagrożenian życia – intubacji i
tracheostomia
3. P/wskazane –środki nasenne, narkotyczne.
4. Tlenoterapia – mieszanki 3-5 % C0
2
+
95 % 0
2
.

22.06.21
23
Kwasica oddechowa przewlekł
– jest
zaburzeniem rownowagi kwasowo- zasadowej
spowodowanym wzrostem ciśnienia
cząsteczkowego C0
2
krwi. Powyższe objawy są
wywołane depresją nerowej regulacji
oddychania, przewlekłymi chorobami kości,
mięśni,płuc, opłucnej orez serca.
Kliniczne –
dominują objawy choroby
podstawowej oraz niewydolności
oddechowej( sinica, hipoksemia, hiperkapnia,
cechy przeciążenia PK).
Leczenia przyczynowe i tlenoterapia.

22.06.21
24
Zasadowica odechowa
jest to zaburzenie równowagi
kwasowozasadowej, w którym dochodzi do
pierwotnego zmniejszenia pC0
2
uwarunkowanego
hiperwentylacja . Ma najczęściej charakter ostry.
Przyczyny-
silne bodźce nerwowe ( bóle, nerwica,
urazy zimno ), uszkodzenie lub drażnienie OUN
przez neo, gorączka, toksyny bakteryjne, leki
( teofilina, salicylany, przewlekła hipoksji
( niewydolność serca).
Obraz kliniczny
– bogaty symptomatologia
neurologiczno –psychiatryczna, zaburznia
świadomości, parestezje, tężyczka,
Leczenie;
1 Przyczynowe
2. Podawanie tlenu z domieszką 5-10% C0
2
–
ostrożnie
3.Leki – barbiturany i morfina

22.06.21
25
Kwasica cukrzycowa ketonowa.
Jest wynikiem bezwzględnego lub względnego
niedoboru insuliny, będącego przyczyną spadku
utylizacji glukozy , zwiększenia lipolizy,
powstawania ciał ketonowych oraz
hiperkatabolizmu białkowego. Określenia kwasica
ketonowa należy używać wówczas, kiedy oprócz
obecności ciał ketonowych w moczu we krwi
stwierdza się pH < 7.30 i stężenie HCO
3
poniżej
15 mmol/l.
Przyczyny:
bezwzględny lub względny niedobór insuliny,
nadmierna praca fizyczna, infekcje bakteryjne i
wirusowe, sters fizyczny lub jako pierwszy objaw
nie rozpoznanej cukrzycy.

22.06.21
26
Obraz kliniczny.
Postępujące osłabienie,brak łaknienia, silne
pragnienie, senność, objawy maski „ostrego
brzucha”, oddech kwasiczy Kussmaula,
odwodnienie , zapach acetonu z ust,
tachykardia, wstrząs, w ciężkiej kwasicy –
głeboka śpiączka i nie reaguje na żadne bodźce
Badania laboratoryjne;
glikemia> 600 mg%, ketonemia i ketonuria,
spadek pH, pCO
2
i HCO
3
mierny wzrost BUN,
hiponatriemia i hiperkaliemia,

22.06.21
27
Leczenia:
Kontrola diurezy, oznaczanie glikiemii co 1 h,
gazometrii co 2 h
Postępowanie:
0.9 NaCl% lub 0.45 % Na Cl 6 l w ciągu 6 h
następnie podawać NaCl 0.9 % z 5 % glukozą +
8 j Actrapid
HM ( po odstawieniu pompy z insuliną)
Insulina 10-20 j Actrapid HM iv ( bolus ), iv im
Insulina w pompie 5-10 j /h gdy glikiemia<250
mg% odstawiamy pompę z insulioną , insulina
wg profilu,
gdy K < 5.5 mmol/l KCl iv 15 mmol/h przez 6 h
a następnie 7 mmol/l przez koleje 18 h

22.06.21
28
gdy pH < 7.1 i v 40 ml 8.4 % NaHCO
3
do chwili wzrostu pH do wymienionej wartości
nie więcej niż 100 ml /d
NaHCO
3
= MC (kg ) x X 0.4 X ( 24 – st HCO
3
)=
w razie hipofosfatemii < 0.7 mmol/l
suplementacja fosforanów.

22.06.21
29
Kwasica nerkowa.
Kwasica przewlekła.
Jest spowodowana zmniejszeniem się masy
czynnego miąższu nerkowego czego objawem
jest kwasica metaboliczna z hipokalcemia i
hiperfosfatemią , zwiększona luka anionowa.
Leczenie
przewlekłej kwasicy moczniocowej
stanowi fragment leczenia PNN, nie wymaga
żadnego leczenia farmakologicznego do chwili
zmniejszenia stężenia HCO
3
poniżej 14 mmol/l
lub pH < 7.20

22.06.21
30
Kwasica nerkowa ostra.
Jest ostrą niewydolnością nerek jest to nagłe
ustanie funkcji hemostatycznej, wydalniczej i
endokrynnej.

22.06.21
31
Obraz kliniczny.
W dużym stopniu zależy od postaci o.n.n. i
czynnika wywołującego.
Obraz na podstawie o.n.n.n.
Przebieg 2 fazowy:
- okres skąpomoczu (10-14 dni )
- okres wielomoczu ( 7 -10 dni )

22.06.21
32
Okres skąpomoczu.
Kliniczne:
obraz ostrego zatrucia mocznicowego ( bóle
glowy , psychozy , depresja, wymioty,
nudności,biegunka, objawy skazy
krwotocznej,oddech Kussmaula, cechy płuca
nawodnionego.
Laboratoryjnie:
kwasica metaboliczna,,wzrost kreatyniny,
mocznika, hiperkalemia, hiponatriemia,
hipokalcemia i hipomagnezemia
Okres wielomoczu;
w początkowym okresie parametry biochemiczne
mocznicy mogą ulec krótkotrwałemu wzrostowi,
normalizacji Na i K w surowicy.

22.06.21
33
Skapomocz lub bezmocz.
o.n.n pozanerkowa.
o.n.n przednerkowa
o.n.n nerkowa
Określić rodzaj przeszkody
Określić przyczynę hipoperfuzji
nerek.
Ustalić czy przyczyna uwarunkowana
jest zmianami zapalnymi czy niezapal
nymi

22.06.21
34
Leczenie kwasicy
gdy NaHCO
3
< 15 mml/l
wyrównywanie zaburzeń gospodarki wodnej i
jonowej

22.06.21
35
Zasadowica metaboliczna.
Jest to stan charakteryzujący się ujemnym
bilansem jonów wodorowych i zwiekszenie
stężenia wodorowęglanów.
Przyczyny;
zasadowica substrakcyjna - wymioty,biegunki,
utrata z moczem
zasadowica addycyjna – cytrynian sodu, mleczan
sodu, węglan wapnia
zasadowica z powodu niedoboru potasu –
hiperaldosteronizm, zespół złego wchłaniania,
utrata z moczem, niedobór magnezu.

22.06.21
36
Objawy kliniczne:
z powodu hipokaliozy objawy z OUN
( psychozy, depresje, stany lękowe)
zanik odruchów ścięgnistych, skurcza dodatkowe
mięśnia sercowego, objawy niedrożności
porażennej jelit, odwodnienie izotoniczne.
Leczenie:
wyrównywanie niedoborów elektrolitowych i
wody, postępowaniem z wyboru jest podawanie
0.9 % NaCl z KCl
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
Wyszukiwarka
Podobne podstrony:
Gospodarka kwasowo zasadowa
Zaburzenia gospodarki kwasowo zasadowej
ZABURZENIA GOSPODARKI KWASOWO ZASADOWEJ ppt
Zaburzenia Gospodarki Kwasowo-Zasadowej, MEDYCYNA, Biochemia
Gospodarka kwasowo-zasadowa, Studia - materiały, Fizjologia
6 Zaburzenia gospodarki kwasowo zasadowej
Gospodarka kwasowo zasadowa 2007 ppt
Patologia gospodarka kwasowo zasadowa organizmu
Zaburzenia gospodarki kwasowo zasadowej 1(1)
Podstawowe mechanizmy w regulacji gospodarki kwasowo zasadowej
(4871) gospodarka kwasowo zasadowa
10 GOSPODARKA WODNO ELEKTROLITOWA I RÓWNOWAGA KWASOWO ZASADOWAid 10549 ppt
więcej podobnych podstron