
Jagoda Przybysz
gr. V

Katabolizm zasad
purynowych
Produkty degradacji kwasów nukleinowych, a
więc nukleotydy, nukleozydy lub wolne zasady
azotowe , przez układ krążenia przedostają się
do wątroby.
Niektóre zasady purynowe, np. adenina, mogą
być wykorzystane ponownie do syntezy kw.
nukleinowych, ale tylko przez niektóre komórki.
Inne puryny podlegają przekształceniom
prowadzącym do wytworzenia kwasu
moczowego.

Katabolizm zasad
purynowych
Kwas moczowy jest ostatecznym metabolitem
przemiany puryn, wydalanym z organizmu, u
ludzi, małp człekokształtnych, gadów i ptaków.
U innych zwierząt ulega on przekształceniu w
alantoinę lub kw. alantoinowy, a u gatunków
zajmujących niższe miejsca w systematyce –
rozkłada się na mocznik i kw. glioksalowy.
Katabolizm zasad
purynowych
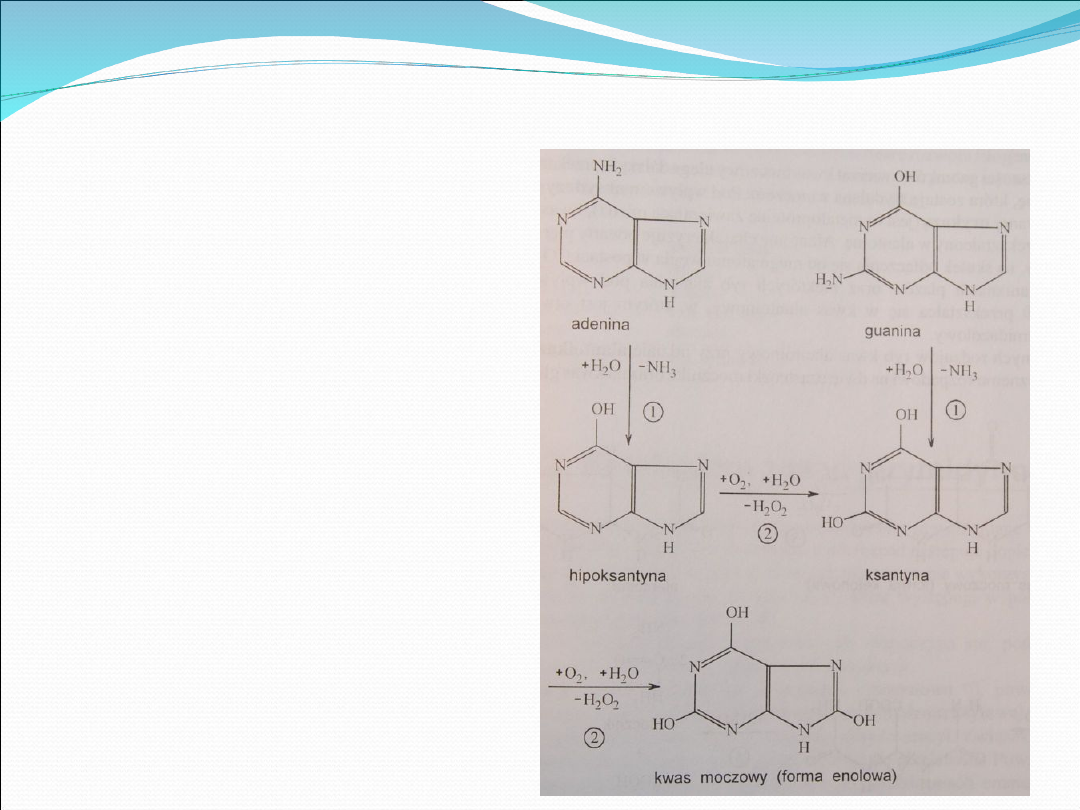
Katabolizm zasad
purynowych, zawierających
grupy aminowe,
rozpoczyna się od reakcji
deaminacji, katalizowanych
przez odpowiednie
deaminazy (1).
W wyniku deaminacji z
adeniny powstaje
hipoksantyna, a z guaniny-
ksantyna.
Obydwa te związki pod
wpływem oksydazy
ksantynowej (2) ulegają
utlenieniu do kw.
moczowego.
Katabolizm zasad
purynowych
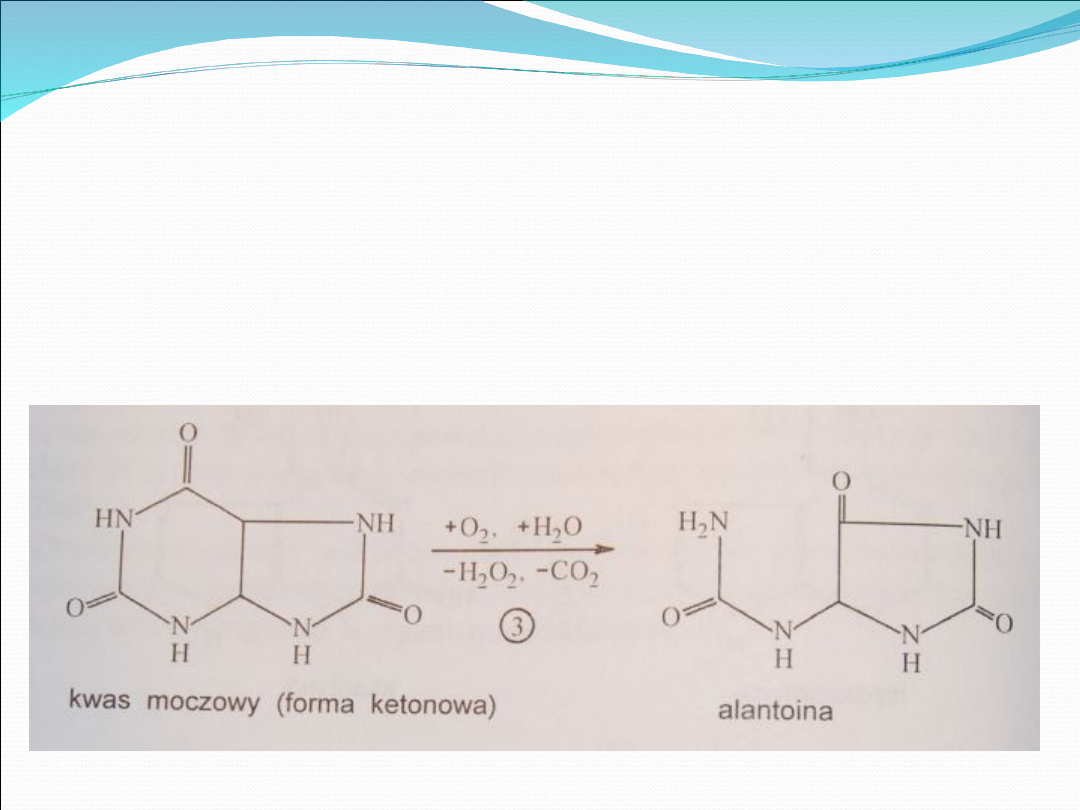
U większości gatunków zwierząt kw. moczowy
pod wpływem oksydazy moczanowej, zwanej
urykazą (3), zostaje przekształcony w
alantoinę.
Katabolizm zasad
purynowych
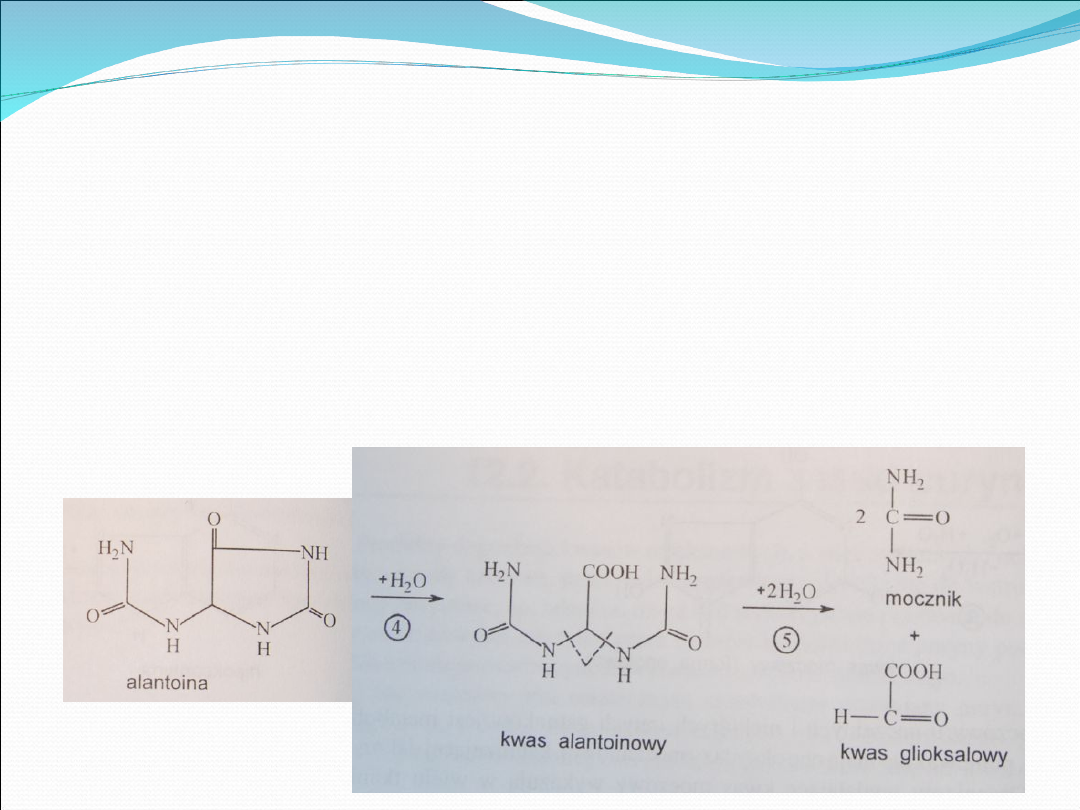
W organizmach płazów i niektórych ryb alantoina pod
wpływem alantoinazy (4) przekształca się w kw.
alantoinowy.
U pewnych rodzajów ryb kw. alantoinowy przy udziale
alantoikazy (5) ulega hydrolitycznemu rozpadowi na
2 cząst. mocznika i na kw. glioksalowy
Katabolizm zasad
purynowych
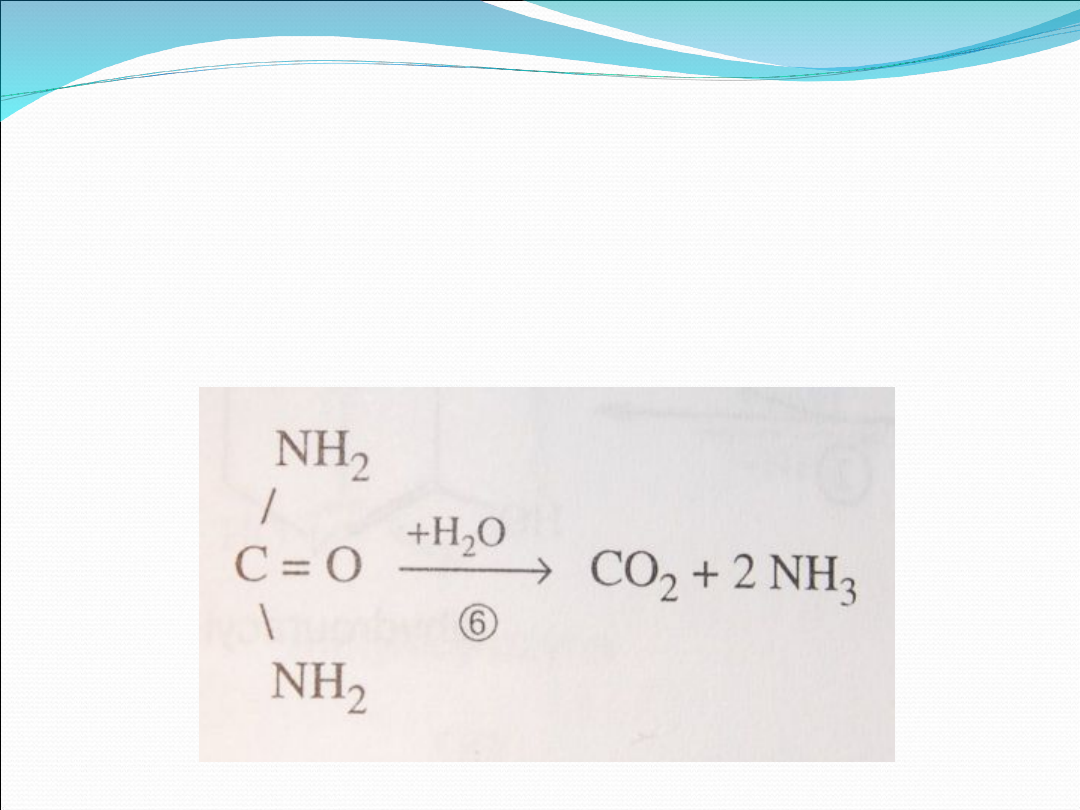
U zwierząt bezkręgowych następuje
degradacja mocznika za pomocą ureazy(6)
do amoniaku i dwutlenku węgla.

Katabolizm zasad
pirymidynowych
Zasady pirymidynowe mogą być w
organizmie ponownie wykorzystane do
syntezy kw. nukleinowych, ale jedynie te,
które występują w połączeniach
nukleozydowych lub nukleotydowych.
Katabolizm wolnych zasad pirymidynowych
rozpoczyna się również od procesów
deaminacji.
Katabolizm zasad
pirymidynowych
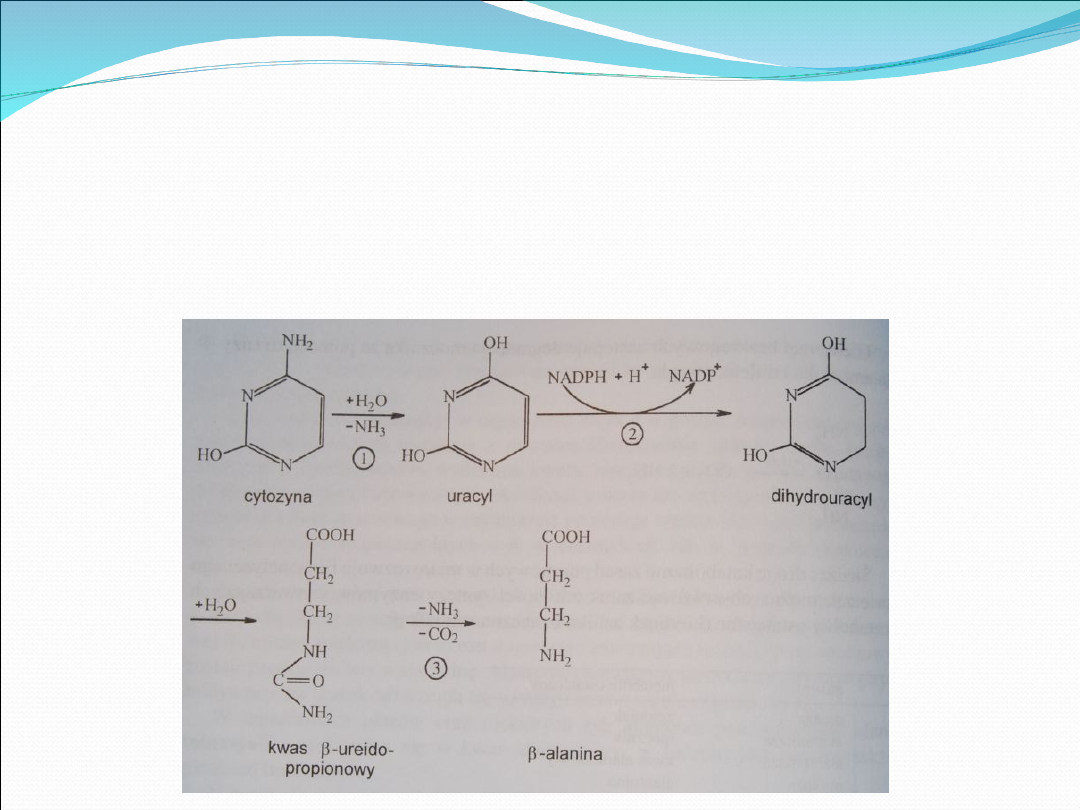
Deaminację cytozyny katalizuje deaminaza cytozynowa (1), powodując jej przejście w
uracyl.
Pod wpływem dehydrogenazy dihydrouracylowej (2), współdziałającej ze
zredukowanym NADP, powstaje dihydrouracyl.
Związek ten ulega przemianom (rozerwanie pierścienia), powstaje kw. β-
ureidopropionowy.
Z niego, po deaminacji i dekarboksylacji przy udziale ureidopropionazy (3), powstaje β-
alanina.
Katabolizm zasad
pirymidynowych
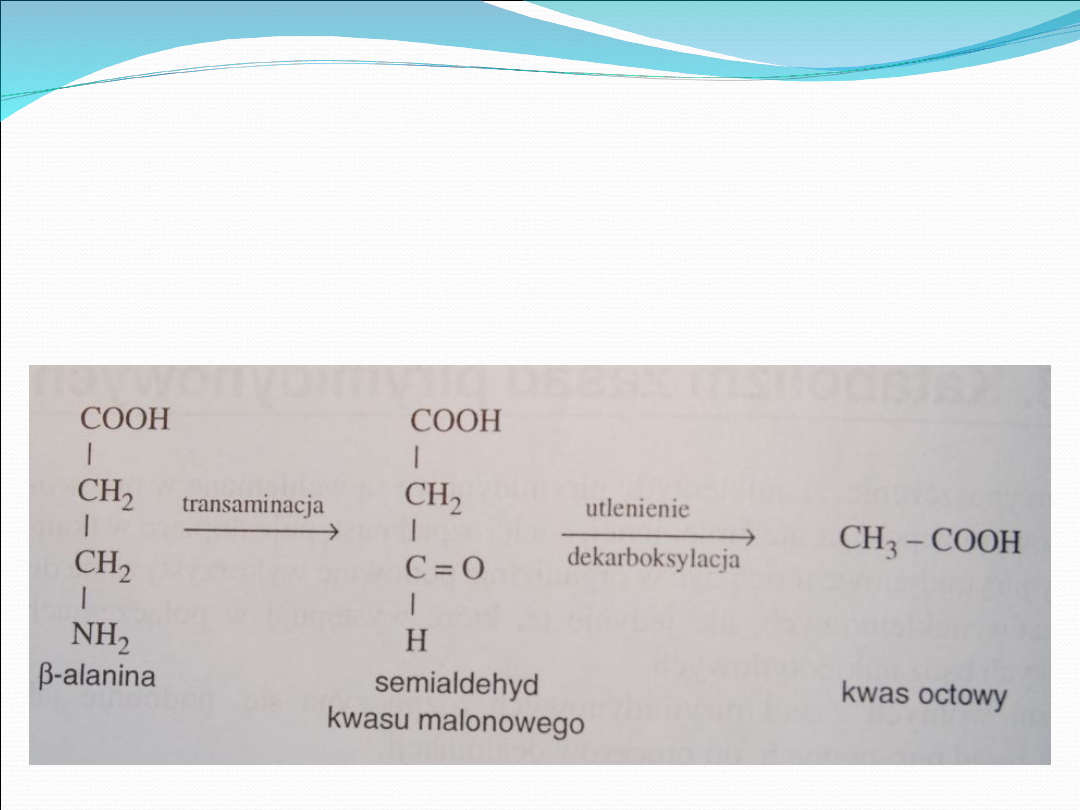
β-alanina w wyniku transaminacji przekształca się
w semialdehyd kwasu malonowego, który ulega
utlenieniu oraz dekarboksylacji, skutkiem czego
powstaje z niego kwas octowy.
Katabolizm zasad
pirymidynowych
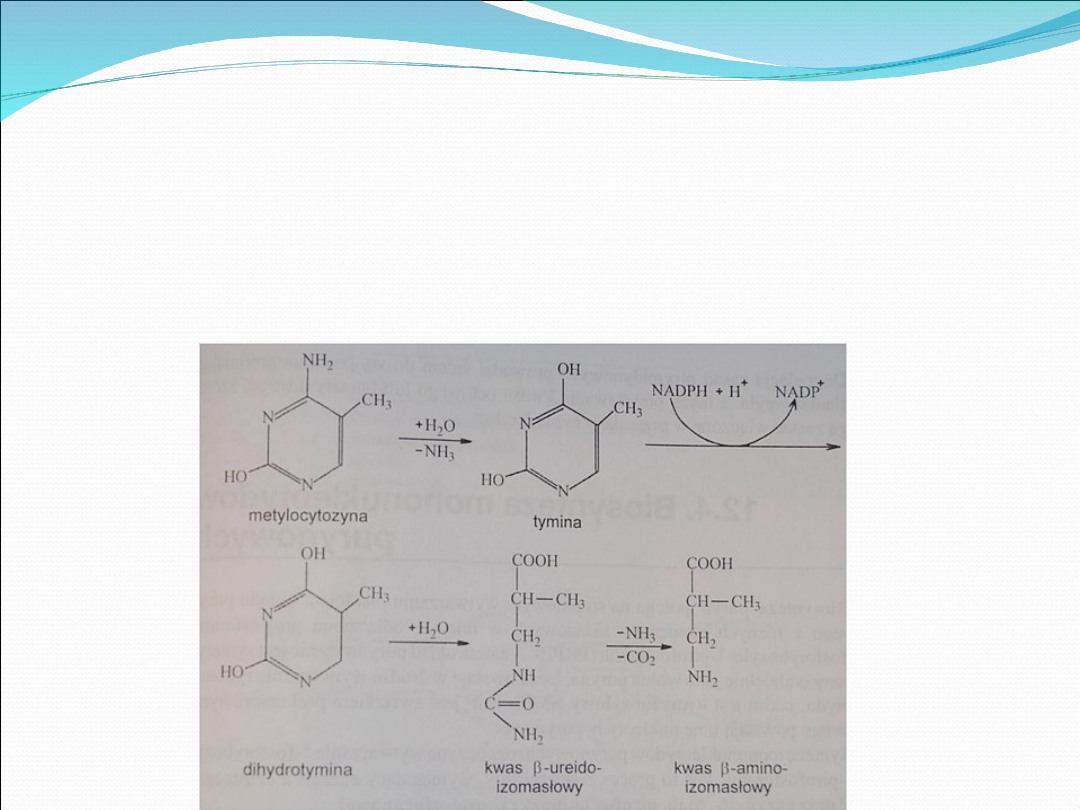
Podobnie przebiega katabolizm metylocytozyny.
Pod wpływem deaminazy powstaje z niej tymina, a po enzymatycznym
uwodorowaniu przez zredukowany NADP zostaje wytworzona dihydrotymina.
Następnie dochodzi do rozerwania pierścienia, w efekcie czego powstaje kwas β-
ureidoizomasłowy.
W reakcjach deaminacji i dekarboksylacji kwas ten przechodzi w kwas β-
aminoizomasłowy.

Katabolizm zasad
pirymidynowych
Dalsze przekształcenia kw. β-aminoizomasłowego prowadzą przez
transaminację do semialdehydu metylomalonowego
Związek ten następnie może ulec utlenieniu do kw. metylomalonowego i w
reakcji izomeryzacji przejść w kw. bursztynowy
Inna droga przemiany semialdehydu metylomalonowego polega na jego
utlenieniu i dekarboksylacji do kw. propionowego.

Katabolizm zasad
pirymidynowych
Degradacja zasad pirymidynowych prowadzi zatem
do wydzielania amoniaku i dwutlenku węgla, a także
powstawania kw. octowego lub bursztynowego, które
mogą zostać włączone w przemiany cyklu Krebsa.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
Wyszukiwarka
Podobne podstrony:
Katabolizm zasad purynowych i pirymidynowych
Wykład katabolizm azotu aminokwasów
11b Azotowanie i nawęglanie (PPTminimizer)id 13076 ppt
Znajomosc zasad udzielania pierwszej pomocy
20 Stosowanie zasad projektowan Nieznany (2)
46 zasad zdrowego rozsadku(1)
metodyka katabolozm
Podstawowe informacje na temat zasad przylaczenia farm wiatrowych
115 USTAWA o szczeg zasad p Nieznany (2)
10 ZASAD ZDROWEGO ZYWIENIAid 11 Nieznany
40 zasad email marketingu
11 niezmiennych zasad skutecznego dzialania
02 Przestrzeganie przepisów prawa i zasad ekonomiki
36 USTAWA o szczegolnych zasad Nieznany (2)
Azotowce id 74705 Nieznany (2)
02 Stosowanie przepisów prawa i zasad ekonomiki
więcej podobnych podstron