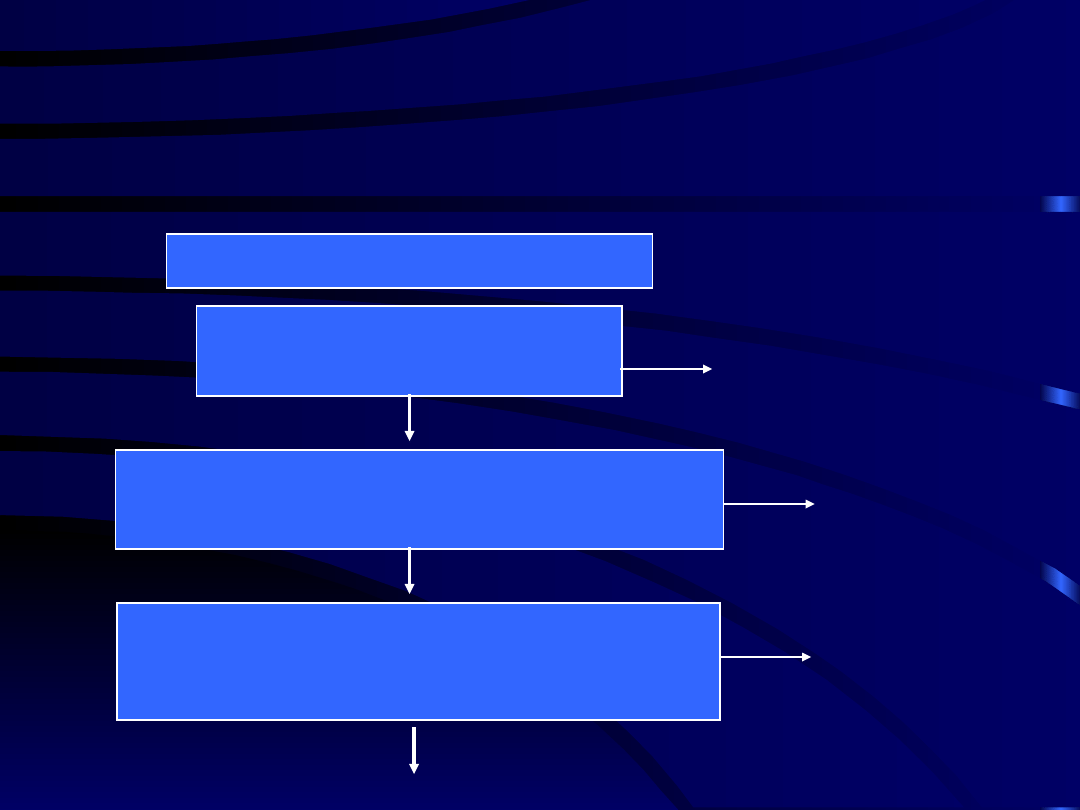
Leczenie farmakologiczne
bólu przewlekłego
Kliniczna ocena chorego
NLPZ, Paracetamol
+ leki adjuwantowe
kontynuacja
(-)
(+)
(-)
Słabe opioidy + proste analgetyki
+ leki adjuwantowe
kontynuacja
(+)
Silne opioidy + proste analgetyki
+ leki adjuwantowe
(+)
kontynuacja
(-)
Skieruj do specjalisty

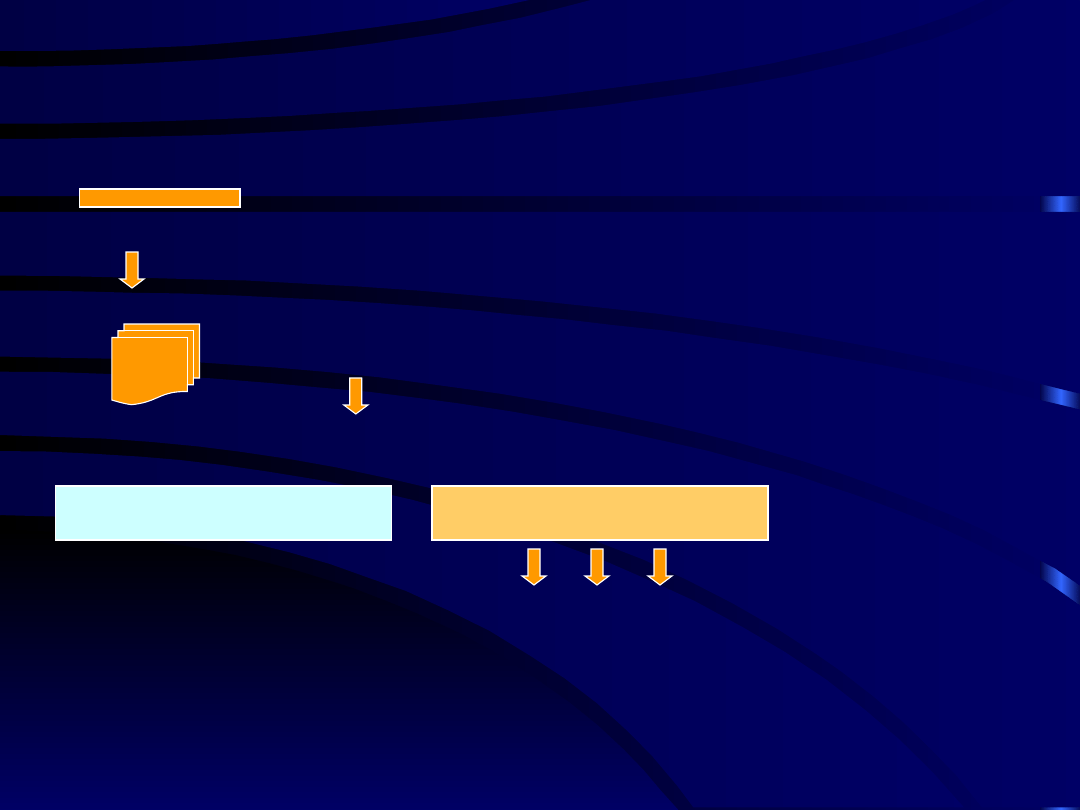
FARMAKOTERAPIA:
ustalenie
skutecznej kombinacji
leków - testy
farmakologiczne
Wielokierunkowe leczenie bólu przewlekłego
TENS, EAK
mobilizacja zstępujących
mechanizmów kontroli bólu
TERAPIA
PSYCHOLOGICZNA
modulowanie „pamięci bólowej”
W wybranych przypadkach
BLOKADY I NEUROLIZY
ZABIEGI NEUROCHIRURGICZNE
• Dekompresja
• Neurodestrukcja
• Neurostymulacja
REHABILITACJA
dążenie do uzyskania
samowystarczalności
poprawa jakości życia
Aktywność
cyklooksygenazy
Fosfolipidy błony komórkowej
Fosfolipaza A
Kwas arachidonowy
Syntaza prostaglandynowa PGHS
c
cyklooksygenaza
peroksydaza
Nadtlenek - PGG2
PGH2
Modulator stanu zapalnego
Prostacyklina
PGI2
Tromboksan
TXA2
Prostaglandyny
PGE2, PGD2, PGF2

COX-1 i COX -2
COX 1
•
główny enzym
konstytutywny
•
produkcja
prostanoidów:
śluzówka żołądka
komórki nerek
płytki krwi
śródbłonek naczyniowy
Prostanoidy spełniają
rolę cytoprotekcyjną
COX 2
• główny enzym
indukowany
• produkcja prostanoidów:
pod wpływem endotoksyny,
cytokin prozapalnych.
Prostaglandyny powodują
objawy zapalenia: ból
wzrost przepuszczalności
naczyń, gorączkę

Klasyfikacja NLPZ
Nazwa grupy
Nazwa leku
COX-1/COX-2
1. Klasyczne NLPZ
np: indometacyna, ibuprofen
0,5 - 3
2. Preferencyjne
inhibitory COX-2
meloksykam, nimesulid
10- 20
3. Wybiórcze
inhibitory COX-2
rofekosyb, celekosyb 150 -250

Potencjalne możliwości
zastosowania wybiórczych
inhibitorów COX-2
1
. Przeciwzapalne w chorobach reumatologicznych
2. Przeciwbólowe w bólu ostrym i przewlekłym
3. Przeciwgorączkowe
4. Prewencja raka jelita grubego i innych nowotworów
5. Prewencja choroby Alzheimera
6. Leczenie zagrażającego porodu

NLPZ - Działania
niepożądane
OUN:
zawroty głowy
upośledzenie słuchu
Reakcje alergiczne - astma
idukowana aspiryną
Przewód pokarmowy:
objawy dyspeptyczne
bóle
nudności, wymioty
nadżerki, krwawienia
Nerki:
upośledzenie filtracji
kłębkowej
Układ krwiotwórczy:
trombocytopenia
niedokrwistość
agranulocytoza aplastyczna

NLPZ - Działania
niepożądane
Wskaźnik śmiertelności
dla wszystkich chorych przyjmujących NLPZ 0,22%
Groźne powikłania po 3-miesięcznym stosowaniu 1 - 2%
Groźne powikłania po rocznym stosowaniu
2 - 5%
Częstość występowania dyspepsji
10 - 20%
Objawy dyspeptyczne nie stanowią ostrzeżenia
przed wystąpieniem groźnych powikłań !

Paracetamol - ośrodkowy mechanizm
działania
1. Może oddziaływać na zstępujący układ antynocyceptywny
(działanie analgetyczne było znacznie słabsze po uszkodzeniu
serotoninergicznych dróg opuszkowo-rdzeniowych przez
5,7-dihydroksytryptaminę)
2. Hamowania syntazy NO i następowej produkcji tlenku azotu
(antynocyceptywne działanie jest odwracane poprzez podanie naturalnego
substratu syntazy tlenku azotu L-argininy)
3. Działanie na izoformy COX-2, które wrażliwe są
na paracetamol
4. Hamowanie produkcji wolnych rodników
(pośrednie oddziaływanie na zmniejszenie aktywności
ośrodkowej cyklooksygenazy)
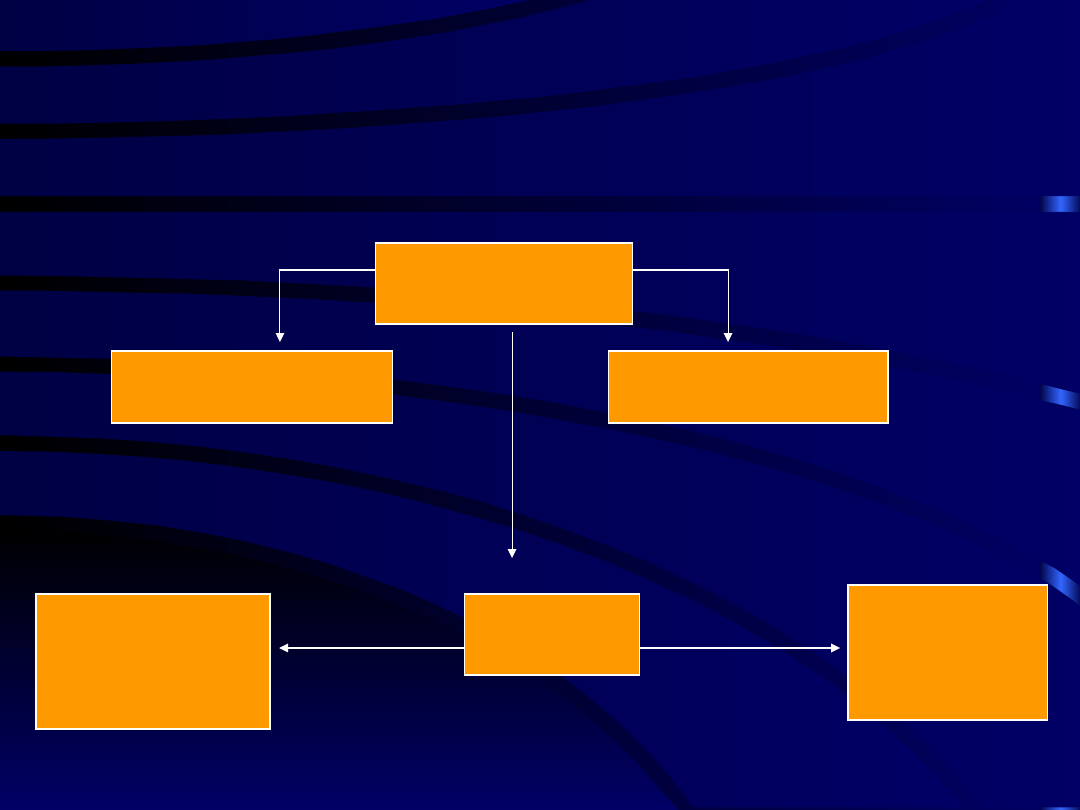
Paracetamol
- objawy niepożądane
Paracetamol
Siarczan P
Glukuronid P
NAPQI
P 450
GlutationSprzężenie
z cysteiną
Brak
glutationu
Uszkodzenie
wątroby
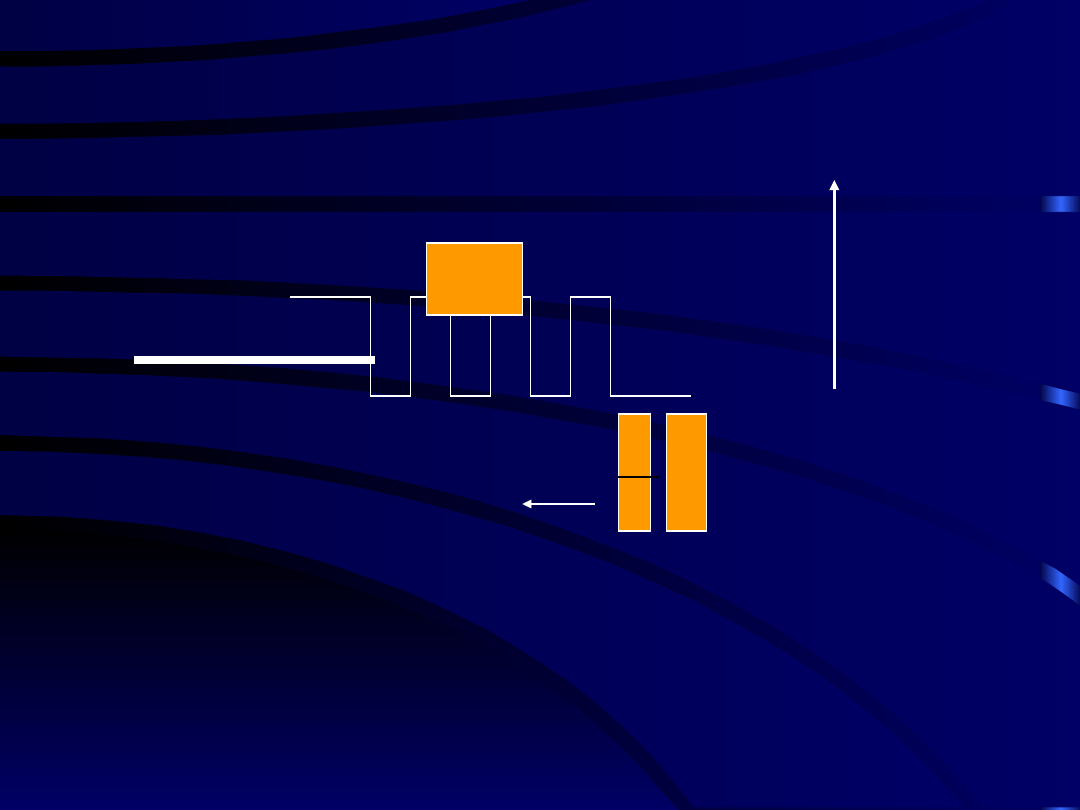
Molekularny mechanizm
działania opioidów
Ag
Błona komórkowa
N
C
GTP
- guanozynotrisfosforan
Hydroliza
GTP
Hiperpolaryzacja komórki:
Zamknięcie kanałów Ca
++
VSCC-N
Otwarcie kanałów K
Zmniejszenie uwalniania
neurotransmitera
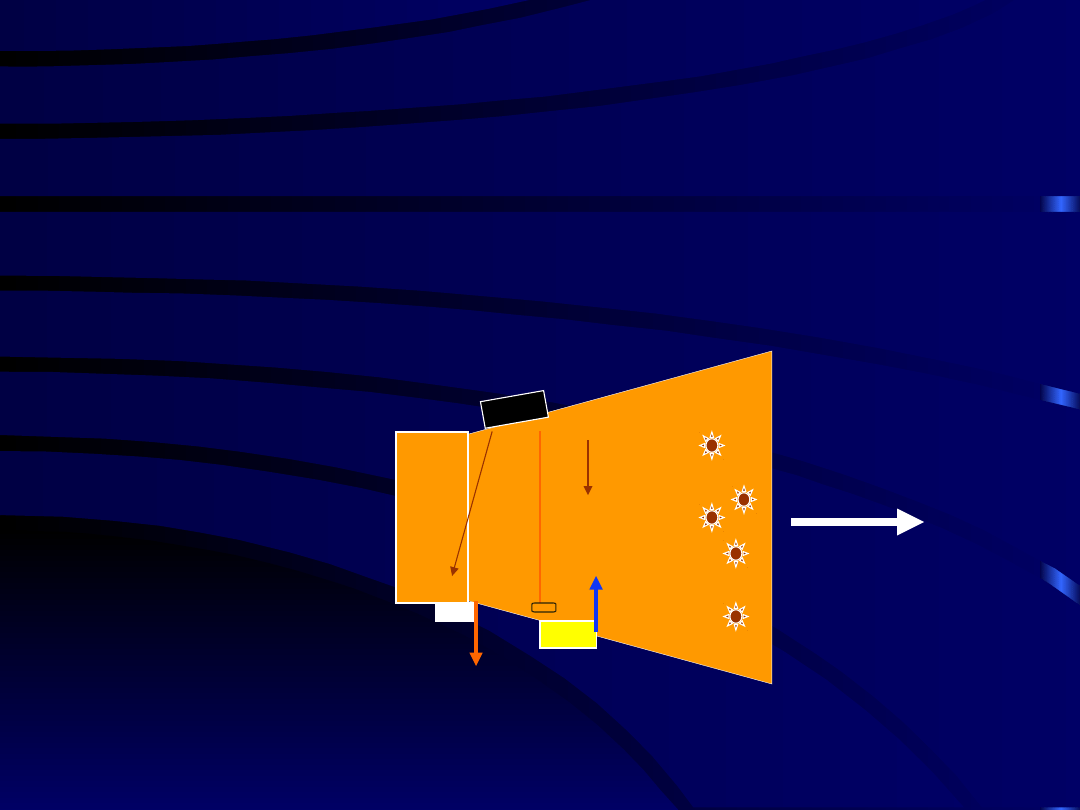
Molekularny mechanizm
działania opioidów
2a. K
+
2b. Ca
+
1. cAMP
Osłabienie
neurotransmisji
3.
4.
1. Zmniejszenie cAMP
2 a. Otwarcie kanałów K
2 b. Zamknięcie kanałów Ca
3. Zmniejszenie
uwalniania
neuroprzekaźnika
4. Analgezja

Optymalizacja leczenia
opioidami
- kierunki badań klinicznych
• Nowe leki
• Alternatywne drogi stosowania
• Leczenie objawów niepożądanych
• Wzmocnienie analgezji opiodowej
• Wzmocnienie działania endogennych
systemów opioidowych

Optymalizacja leczenia
opioidami
- nowe leki
• Fentanyl
• Alfentanyl
• Sufentanyl
• Remifentanyl
• Mirfentanyl
• Trefentanyl
• Fentanyl
przezskórny
• Tramadol
Sear JW. Brit J Anaesth 1998

Optymalizacja leczenia
opioidami - alternatywne
drogi podawania
Doustna, doodbytnicza, podskórna, donosowa,
wziewna, przezskórna, okołordzeniowa,
Naśluzówkowa
wskazania:
premedykacja
ból pooperacyjny
u dzieci
Stosowane leki:
fentanyl
sufentanyl
petydyna
Wziewna
wskazania:
duszność
tolerancja ruchu
ból pooperacyjny
Stosowane leki:
fentanyl
morfina
kodeina
Przezskórna
wskazania:
ból nowotworowy
ból neuropatyczny
Stosowane leki:
fentanyl

Optymalizacja leczenia
opioidami - wzmocnienie siły
działania
1. Leki znieczulenia miejscowego (zo, pp)
2. Leki przeciwdepresyjne
3. Klonidyna
4. Antagoniści NMDA
5. Antagoniści receptorów CCK-B, NK, BK

Wzmocnienie działania
endogennych systemów
opioidowych
Bardziej fizjologiczną analgezję można uzyskać poprzez
przedłużenie czasu działania naturalnych petydów opioidowych
Enkefaliny - peptydy szybko metabolizowane przez enzymy:
NEP (neutral endopeptidase) i APN (aminopetidase)
Obydwa enzymy należą do rodziny metalopeptydaz)
Mieszanina NEP/APN: działanie synergistyczne,
komplementarne
Inhibitory metaloproteaz: Kelatorfan, RB-38A, RB-101
Noble F. and Roques BP. IASP Press 1997

Kierunki leczenia bólu neuropatycznego
• Leczenie schorzenia podstawowego
(cukrzyca, półpasiec, zapobieganie powstawania
przetrwałego bólu pooperacyjnego, pourazowego)
• Zmniejszenie stopnia natężenia doznań bólowych
• Leczenie niekorzystnych objawów towarzyszących
• Leczenie psychologiczne: strategie radzenia sobie

Leczenie farmakologiczne
bólu neuropatycznego
Metoda prób i błędów:
podawanie kolejno
leków o uznanej
skuteczności działania
aż do uzyskania
ulgi w dolegliwościach
Testy farmakologiczne:
ustalenie skutecznie
działających leków lub
ich kombinacji poprzez
podanie dożylne z
placebo.
Pośrednie ustalenie
mechanizmu powstawania
bólu

Testy analizy
farmakologicznej
Stosowane substancje
mechanizm działania
Opioidy
receptory opioidowe
Tramadol
receptory opioidowe,
układ NA i 5-HTergiczny
Lidokaina
patologiczne miejsca pobudzeń
w zakresie I neuronu
Propacetamol
ośrodkowy (NOS?, COX?,5- HT?)
Ketamina
receptory NMDA
Fentolamina
receptory alfa adrenergiczne
Ketoprofen
obwodowy i ośrodkowy - COX-2
Ponadto mogą być zastosowane barbiturany (amytal sodu)
czy agonista receptorów alfa 2 – Kloniodyna

Leki skutecznie działające w
bólu neuropatycznym
• (EBM) Ustalenie skuteczności w oparciu
o kontrolowane badania randomizowane
• NNT - (number needed to treat) - liczba
pacjentów, którym trzeba podawać dany
lek aby u jednego z nich uzyskać poprawę
tj. zmniejszyć ból w określonym stopniu
np. o 50%, przy przedziale ufności 95%

NNT
A. Liczba chorych u których
uzyskano zmniejszenie bólu
o 50% po podaniu leku
B. Liczba wszystkich chorych
u których podano badany
lek
C. Liczba chorych u których
uzyskano zmniejszenie bólu
o 50% po podaniu placebo
D. Liczba wszystkich chorych
u których podano placebo
1
A/B - C/D
20/40 - 4/40
NNT - lidokaina
=
2,5
1
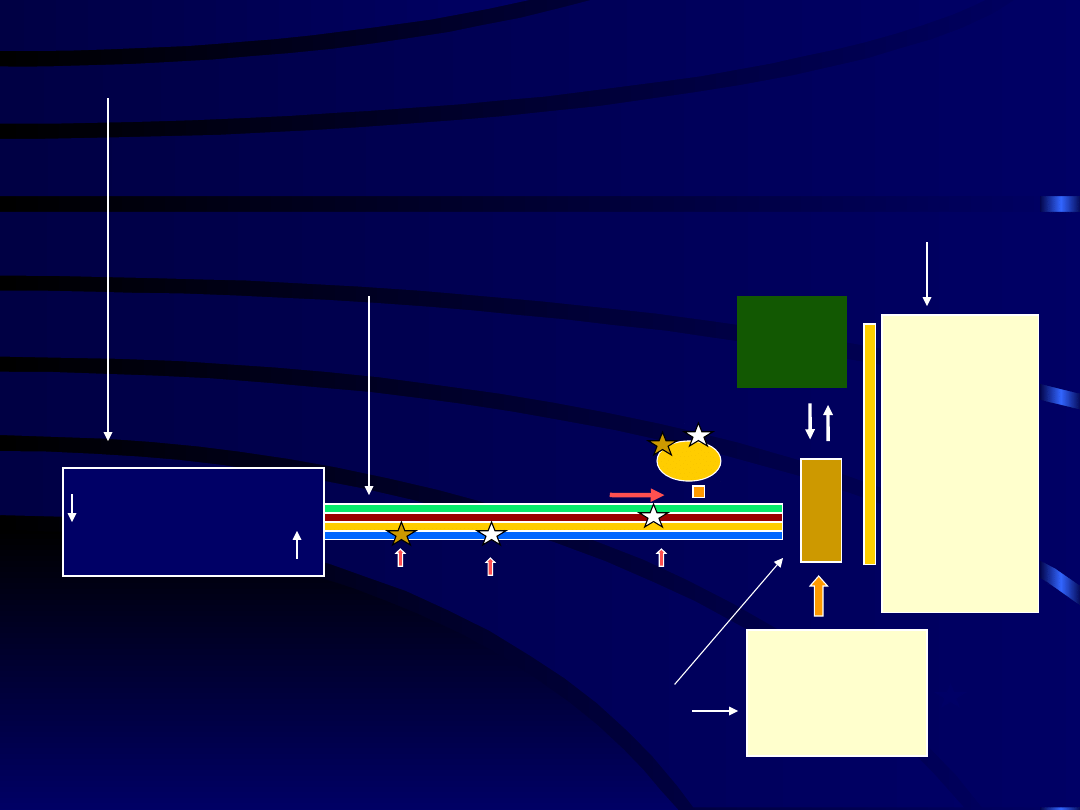
Leki modyfikujące proces transdukcji
DRG
RT
Kanały Na
TTX -R
Kanały Ca
VSCCs
efapsy
Sensytyzacja
Facilitacja
Aktywność
samoistna
Osłabienie
zstępujących
mechanizmów
kontroli:
GABA
Opioidy
CCK -B
Wzgórze
Kora
Patologiczne
unerwienie
współczulne
próg pobudliwości
śpiące receptory
Leki modyfikujące
proces transmisji
Leki modyfikujące proces modulacji
Leki wzmacniające zstępujące
mechanizmy kontroli

Transdukcja- obniżenie progu
pobudliwości
Bodźce
mechaniczne
ATP, GDNF
Receptory
purynergiczne
P2X3
Bodźce
termiczne
Waniloidy
H
+
, Na
+
, Ca
++
Receptory
waniloidowe
VR1
Bodźce
chemiczne
H
+
Receptory ASIC
VR1, MDEG
(mammalian degenertaion)
D E P O L A R Y Z A C J A

Możliwości oddziaływania na
proces transdukcji
Kortykosteroidy -
nieaktywne
Inhibitory COX-2 -
brak badań kontrolowanych
Kapsaicyna
NNT 3,5 - 5,9
Rekombinowany NGF -
brak badań kontrolowanych
Opioidy -
brak badań kontrolowanych
LA -
brak badań kontrolowanych

Kapsaicyna
Alkaloid z owoców papryki
Usuwa neuroprzekaźnik SP z nerwów czuciowych
Inaktywuje receptory VR 1
Zastosowana miejscowo w postaci kremu wywoływała
znamienny efekt w 3 z 5 badań w neuropatii cukrzycowej
NNT - 2,5 - 4,9, łącznie 5,9
Stosowana również w neuralgii popółpaścowej NNT - 5,3
Po uszkodzeniu nerwu - NNT - 3,5
Sindrup SH; Jensen TS. Ból 2000

Działanie miejscowe - powierzchniowo
na zakończenia nerwowe
Działanie ogólne - stężenie we krwi
wynosi 0,13 mcg/mL
Plaster zawierający
665 mg lidokainy
stosowany w leczeniu
neuralgii popółpaścowej
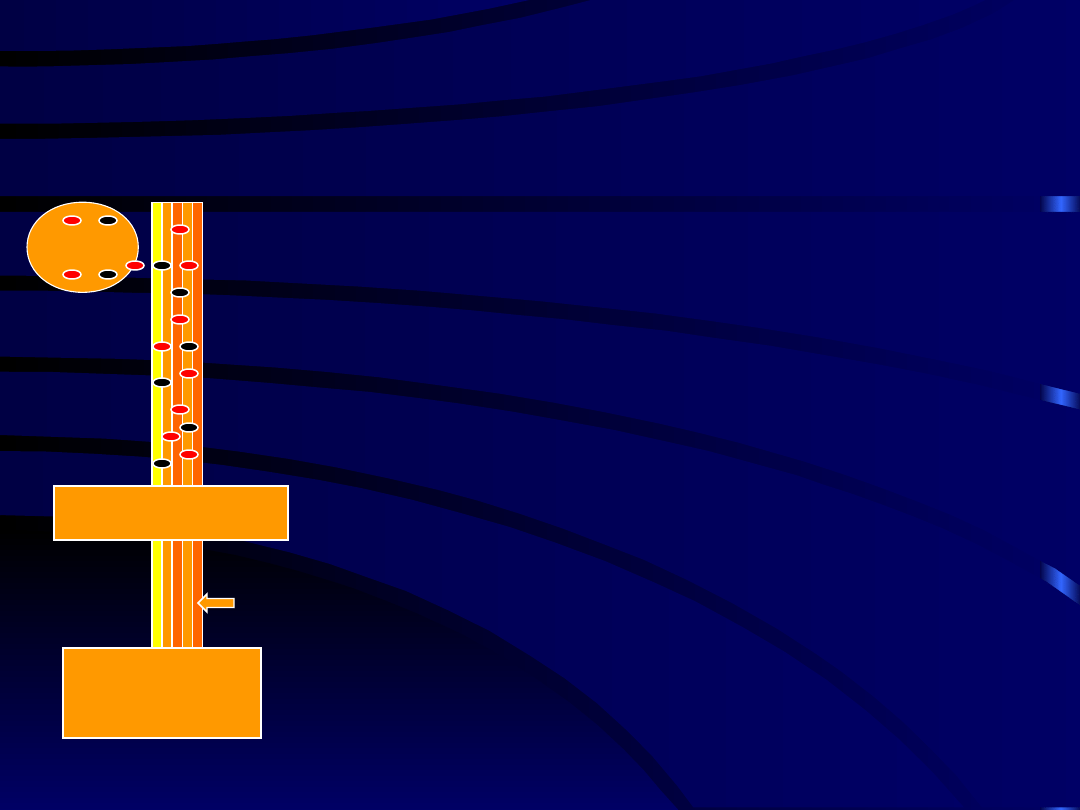
A-alpha
A-beta
A-gamma
A-delta
B
C
DRG
Uraz nerwu
Narząd
docelowy
- Patologiczne połączenia
pomiędzy
włóknami A, B i C - efapsy
Uszkodzenie nerwu prowadzi do zaawansowanych zmian
w ekspresji neuropeptydów i ich receptorów.
Powstaje nowy fenotyp w odniesieniu do tych molekuł.
Degeneracja
Możliwości modyfikacji patologicznie zmienionej
transmisji neuronalnej
- Ektopowe rozruszniki nerwu:
patologiczne kanały
Na (TTX-R),
kanały Ca (VSCCs),
syntetyzowane w DRG
- Zakłócenie śródaksonalnego transportu
(rola cytokin, NGF, komórek Schwanna)
- Synteza i transport śródaksonalny
nowych receptorów (adrenergiczne,
opioidowe)

Możliwości oddziaływania na proces
transmisji po uszkodzeniu nerwu
Ektopowe rozruszniki nerwu:
Lidokaina
NNT 2,5
Meksyletyna
NNT 10,
Fenytoina
NNT 2,6
Karbamazepina
NNT 3,3,
2
-
Guanetydyna, Fentolamina
-
nieaktywne ?
Cytokiny
-Leki antycytokinowe
:
brak badań kontrolowanych
(
kortykosteroidy, talidomid, pentoksyfilina, cyklosporyna)
,,
-
opioidy
obwodowo -
brak badań kontrolowanych

Leki przeciwdrgawkowe
Leki blokujące patologiczne kanały sodowe:
Lidokaina, Meksyletyna, Tokainid
Karbamazepina, Fenytoina, Topiramat, Lamotrigina
Leki o innym mechanizmie działania:
Lamotrigina
Gabapentin
Kwas walproinowy
Klonazepam

Lidokaina
Mechanizm działania po podaniu dożylnym:
selektywna blokada kanałów sodowych TTX-r,
zlokalizowanych w ogniskach patologicznych pobudzeń.
Miejsce działania:
nerwiak, ektopowe rozruszniki nerwu, zwój rdzeniowy.
Dawkowanie:
Wolny wlew (9 mg/min) dożylny 3 - 5mg/kg lidokainy
2 - 3 razy tygodniowo.
doustnie Meksyletyna (Mexitil) 400 - 600mg/24 godz.
Leki przeciwdrgawkowe
Stosowane w leczeniu bólów neuropatycznych.
Hamują samoistne pobudzenia we włóknach nerwowych
Karbamazepina (Amizepin, Tegretol), Fenytoina,
Kwas valproinowy, Klonazepam
Dawka
wstępna = 100 mg, dawka maksymalna = 1800 mg
Objawy niepożądane:
Uszkodzenie
szpiku kostnego
Senność
Zaburzenia
dyspeptyczne
Spowolnienie
myślenia
Ataksja
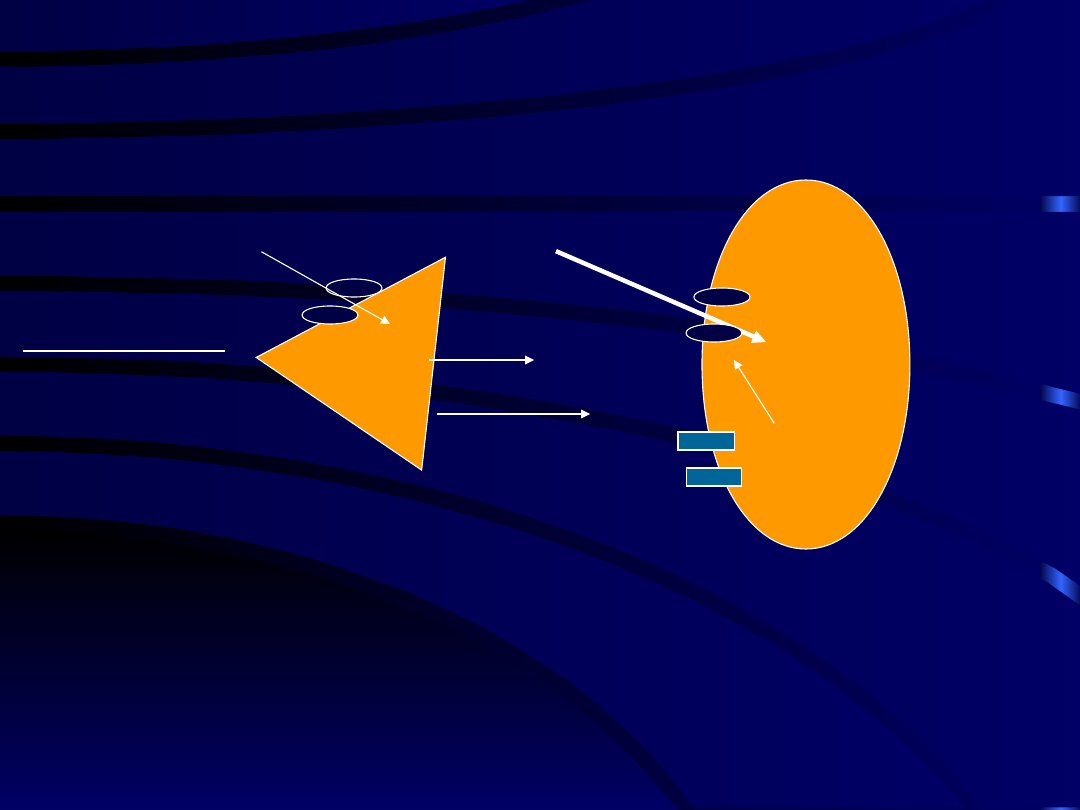
Gabapentyna
Ca
++
VGCC
GBP?
NMDA
VGCC
Glutaminiany
SP, CGRP
GBP?
GPB - działanie
na podjednostkę
2
VGCC
Pośredni wzrost stężenia GABA
- zablokowanie dekarboksylazy
glutaminianowej

Gabapentyna
Zastosowanie - ból neuropatyczny:
Neuralgia popółpaścowa - skuteczność 33% / 8% placebo
Neuropatia cukrzycowa - skuteczność 39% / 22% placebo
Dawki do 3600 mg/dobę
Objawy niepożądane: ataksja, senność, zawroty głowy
Rowbotham MC et al. IASP PRESS 2000

Lamotrigina
Mechanizm działania:
1. blokada kanałów sodowych TTX-r,
zlokalizowanych w ogniskach patologicznych
pobudzeń
2. Zmniejszenie uwalniania EAA
Zastosowanie - ból neuropatyczny
Dawki - 200 mg/dobę
Rowbotham MC et al. IASP PRESS 2000
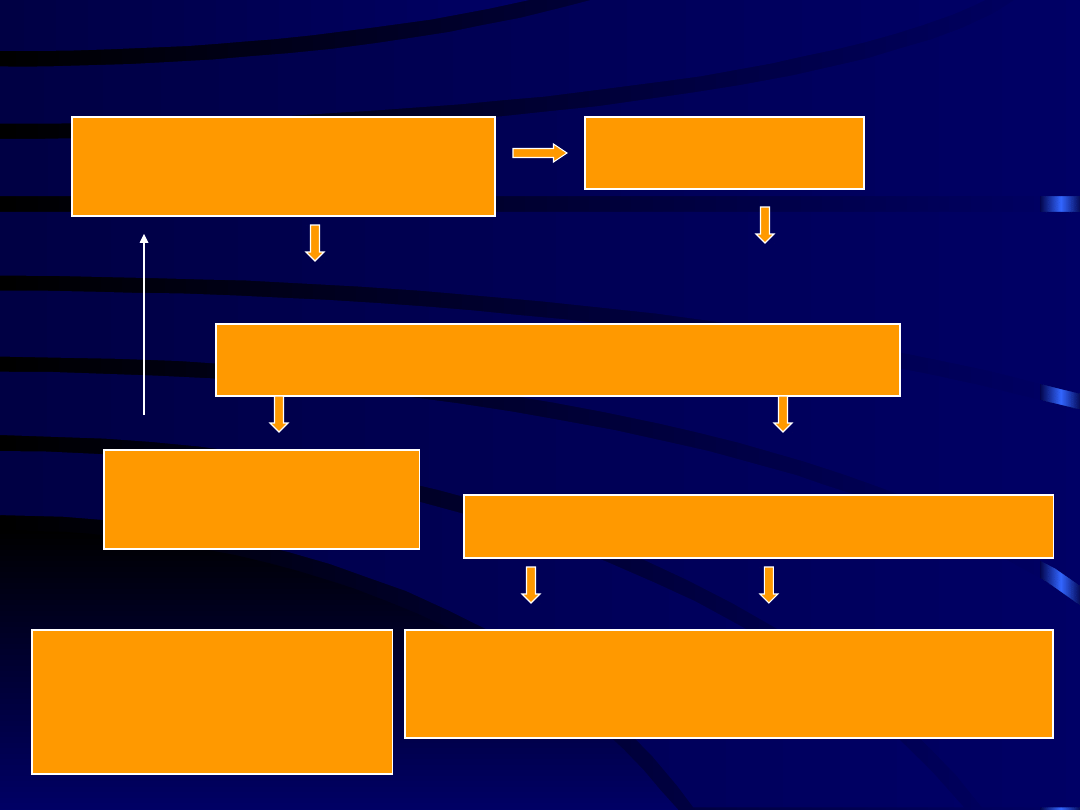
Sensytyzacja ośrodkowa - proces modulacji
Pobudzenie receptorów
błon komórkowych
Depolaryzacja
cAMP cGMP IP
3
Ca
++
„Drugi układ sygnałów”
PKA, PKC, CaCM
Fosforylacja kinaz białkowych
Produkcja NO,
Prostanoidów
EAA
Zmian przewodności kanałów jonowych
RECEPTOR NMDA !
Ekspresje genowe:
cFos, Jun
Docelowych
„Trzeci układ sygnałów”

Leki wpływające na proces
modulacji - RT rdzenia
kręgowego
Antagoniści receptora NMDA
Dekstrometorfan
NNT - 1,9 neuropatia cukrzycowa
bez efektu w neuralgii popółpaścowej (Sindrup Ból 201)
Ketamina, Memantyna
brak badań kontrolowanych
Inhibitory syntazy NO
Paracetamol ?
Inhibitory kinazy białkowej C - gnangliozydy
Antagoniści receptora NK - toksyczne neuropeptydy

Leki wpływające na
zstępujące mechanizmy
kontroli bólu
Receptory:
MOR
GABA
alfa2/5HT
adenozynowe
nAchR
Ca-N
CCK
kainowe
Opiaty
Gabapentyna
Heterocykliczne leki przeciwdepresyjne
Klonidyna
Adenozyna
Neostygmina
Conotoxin
Proglumid

Leki przeciwdepresyjne (LPD)
Mechanizm działania:
zwiększenie stężenia monoamin (NA, 5 HT) poprzez
zahamowanie ich fizjologicznej inaktywacji na poziomie
synapsy i opóźnienia wchłaniania zwrotnego.
Monoaminy działają w rogach tylnych rdzenia
i układzie zstępującej antynocycepcji.
TLPD działają przeciwdepresyjnie i wzmagają działanie
stosowanych opioidów.
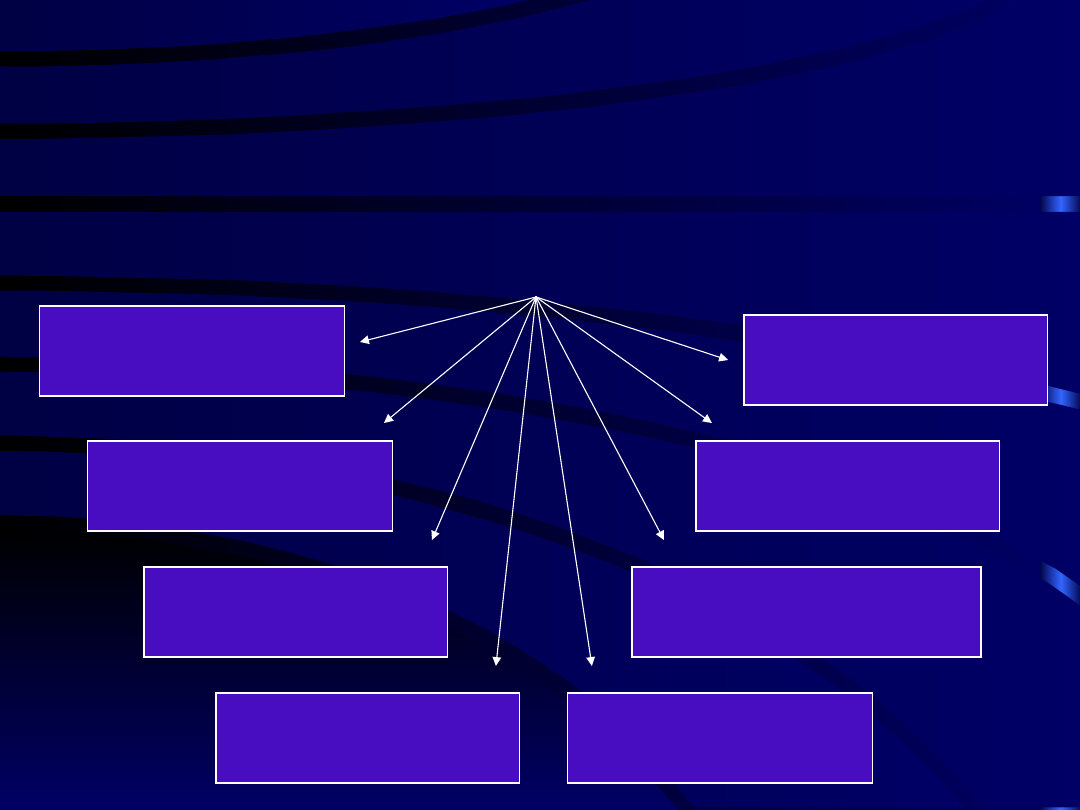
Amitryptylina, Imipramina,
Doxepina
Objawy niepożądane:
Dawka wstępna = 10 mg dawka maksymalnie użyteczna 75 mg/24 godz.
Suchość w ustach
Tachykardia
(50% leczonych)
Retencja moczu
Zaparcia
Napady jaskry
Senność
Zmęczenie
Ogólna niesprawność

Leki przeciwdepresyjne
wszystkie typy- NNT 3,0
NNT
• Nieselektywne inhibitory wychwytu NA i 5-HT (TLPD)
2,4
• Selektywne inhibitory wychwytu NA i 5-HT (SNRI)
- wenlafaksyna
brak badań kontrolowanych
• Inhibitory wychwytu NA (NRI)
3,4
• Selektywne inhibitory wychwytu 5-HT (SSRI)
6,7
- fluoksetyna, fluwoksamina, paroksetyna, sertralina,
citalopram
• Leki zwiększające wychwyt 5-HT
brak badań kontrolowanych
• Leki wpływające na receptory neuronów NA i 5-HT
- mianseryna, mirtazopina
brak badań kontrolowanych

Dlaczego przewlekły ból
neuropatyczny jest zazwyczaj oporny
na wszelkie formy leczenia?
2. Trwałe uszkodzenie neuronów
1. Złożona patogeneza
3. Nieznane jeszcze mechanizmy
powstawania

4. W wielu zespołach bólowych występuje ból mieszany:
zapalny, niezapalny, zależny od układu współczulnego
Dellemijn P. Pain 1999, Attal N., 2001
Złożona patogeneza
1. Każdy rodzaj bólu neuropatycznego ma inny
mechanizm powstawania
2. Różnice dotyczą indywidualnych pacjentów
z podobnym zespołem bólowym
3. W różnym okresie trwania bólu mechanizm
może być inny

Trwałe uszkodzenie neuronów
Uszkodzenie nerwu prowadzi do ekspresji i transkrypcji genów,
produkcji patologicznych drobin białek i trwałe obniżenie progu
pobudliwości neuronów, z możliwością (tak jak w padaczce)
samoistnych wyładowań.
Perspektywy skutecznego leczenia?
Techniki inżynierii genetycznej?
Nieznany mechanizm powstawania
Spinal cord glia: new players in pain
Wattkins L.R et al., Pain 93, 2001
Pobudzenie komórek gleju, uwalnianie cytokin prozapalnych
mogą być odpowiedzialne za powstawanie i podtrzymywanie
zespołu bólu przewlekłego.
Okołordzeniowe stosowanie leków antycytokinowych?

Metody leczenia
anestezjologiczne/chirurgi
czne
Blokady
Neurolizy
Termolezja, Kriolezja
Stymulacja rdzenia kręgowego
Zabiegi operacyjne rekonstrukcyjne
Zabiegi neurodestrukcyjne

Ciągłe znieczulenie
podpajęczynówkowe
•
Niepowodzenie
leczenia doustnego
•
Przewidywany czas
przeżycia > 3 mies.
•
Prawidłowe krążenie
płynu mózgowo-
rdzeniowego
• Uczulenie na opioidy
• Infekcja w miejscu
implantacji
• zaburzenia
krzepnięcia
• upośledzenie
krążenia p.m.r

Ciągłe znieczulenie
podpajęczynówkowe
• Stała infuzja leków
• Minimalne dawki
• Długi czas do
kolejnego
napełnienia
zbiornika
• Pacjent nie jest
narażony na częste
wstrzyknięcia
• Implantacja
trudniejsza
technicznie
• Problemy
techniczne z
cewnikiem i pompą
• Infekcja
• Przeciekanie płynu
m.r.

Nieopioidowe analgetyki
podpajęczynówkowo
• Klonidyna
• Neostygmina
• Midazolam
• Baklofen
• SNX 111
• Somatosrtatyn
a
• Amitryptylina
• R-PIA
• Kalcitonina
• Ketamina
• CPP
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
Wyszukiwarka
Podobne podstrony:
SEMINARIUM ból przewlekły, Anestezjologia
Ból przewlekły dylematy diagnostyczne i lecznicze
Przewlekły ból męskich narządów płciowych
analiza niepelnospr kobiet z przewlek bol dolnego odcinka kregos
Przewlekły ból miednicy mniejszej
Przewlekły ból miednicy
Przewlekła niewydolność nerek (2) 2
Studenci biegunka przewlekła'
Przewlekła NIEWYDOLNOŚĆ NEREK1
Dzien 2 Skutki przewlekłegostres
Przewlekłe zapalenie trzustki
więcej podobnych podstron