

Rodzaj syntetyzowanej pochodnej zależy
od kwasu tłuszczowego
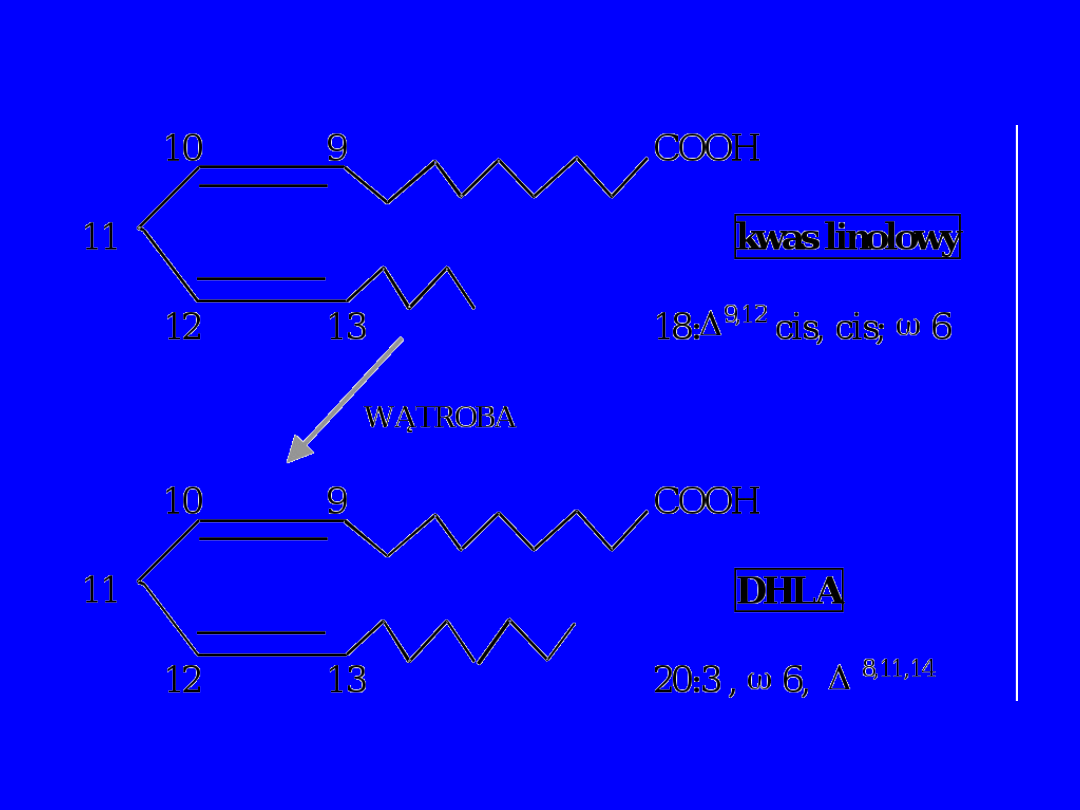
Główny składnik PUFA
kwas
linolowy
(18:
9,12
cis, cis; 6), który w
wątrobie ulega przemianie do kwasu
dihomo--
linolenowego
(20:3 , 6,
DHLA
,
8,11,14
) i
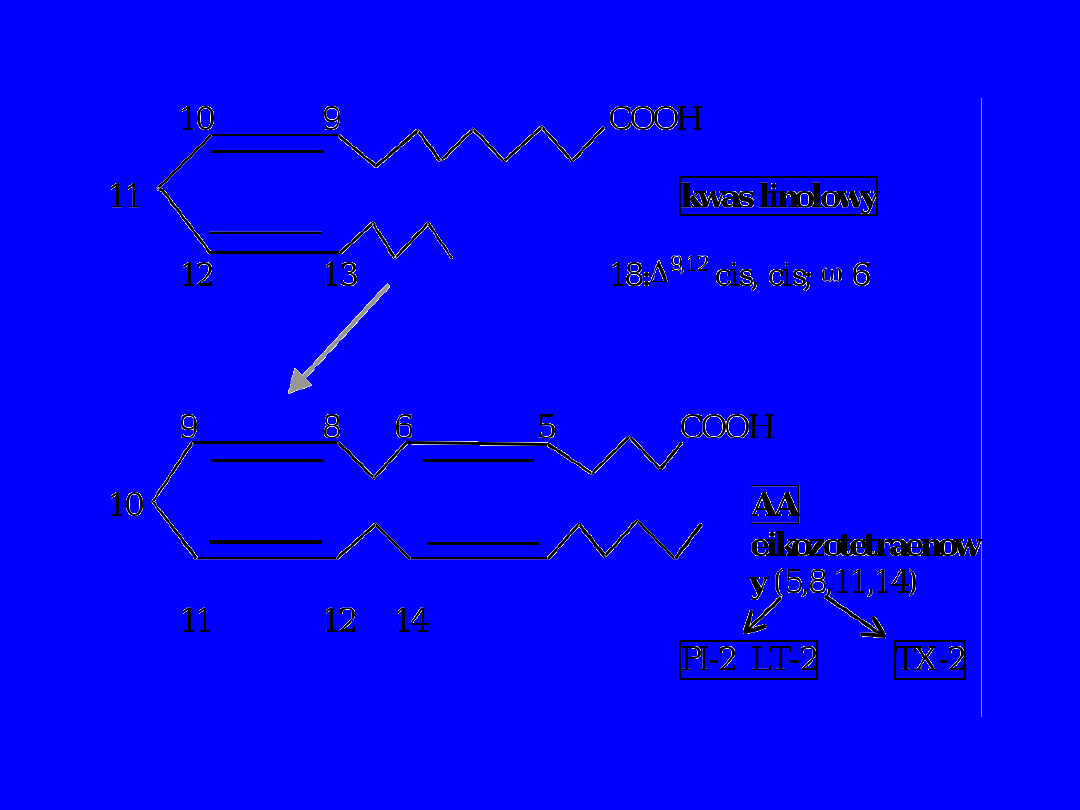
kwasu
arachidonowego
(20:4, 6,
AA,
5,8,11,14
)
Z DHLA tworzą się prostaglandyny
monoenowe
– PGE
1
Z AA tworzą się prostaglandyny
dienowe
– PGF
2
,
PGF
2
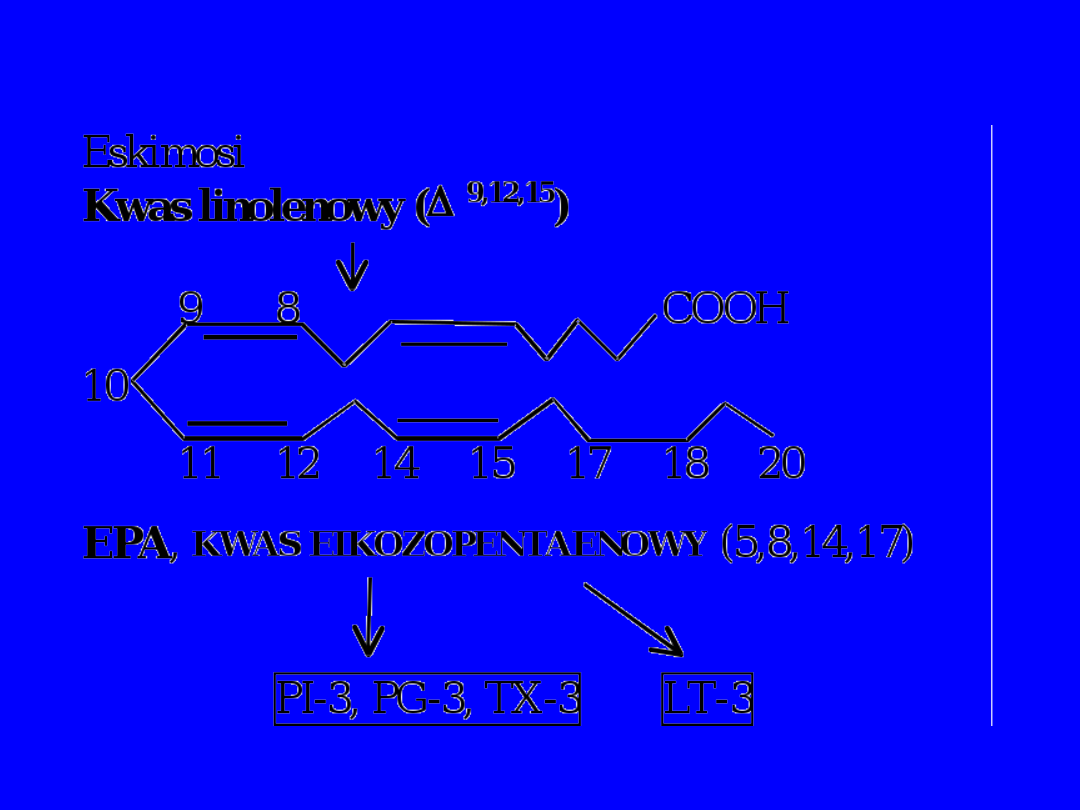
U eskimosów możliwość tworzenia prostaglandyn
trienowych
PROSTANOIDY
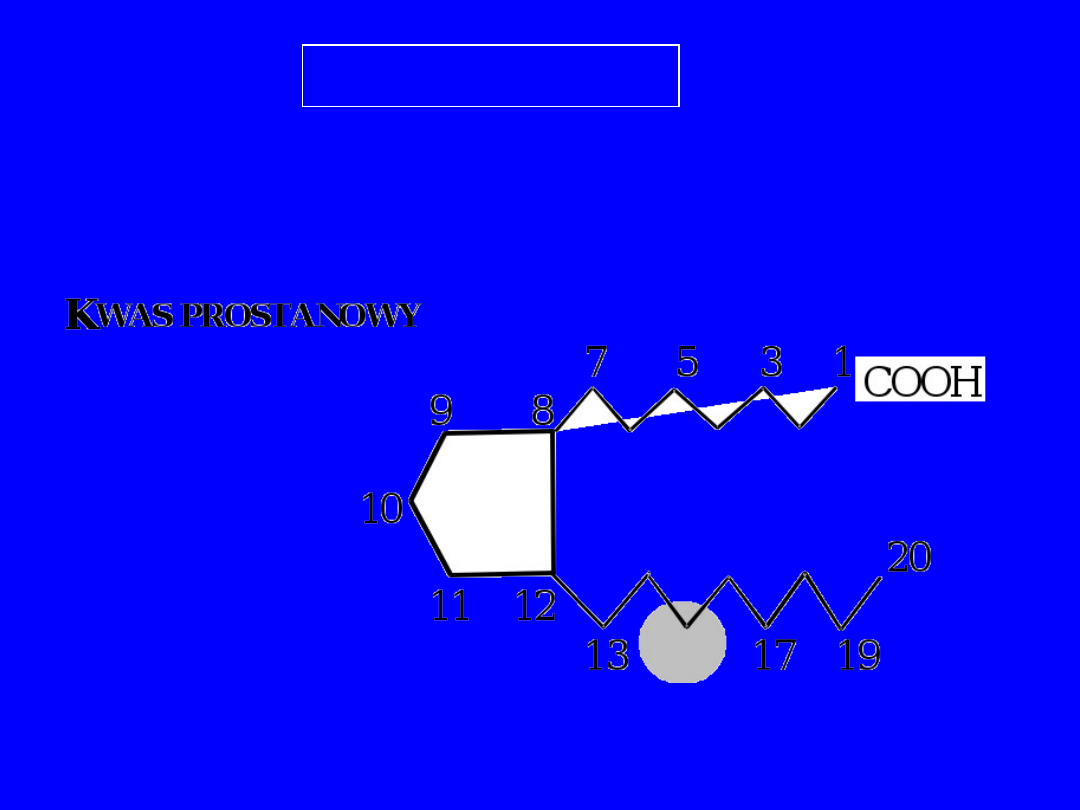
prostata, kwas prostanowy
eikozanoidy, dwudziestaki

PROSTANOIDY
SUBSTRATY
(A)
Kwas eikozatrienowy 20:3 , 6, DHLA,
8,11,14
kwas dihomo -
linolenowy
(B)
Kwas eikozatetraenowy 20:4, 6, AA,
5,8,11,14
(C) kwas eikozapentaenowy 20:5, 3, EPA,
5,8,11,14,17
Kwasy te wywodzą się z kwasów:
1. kwas linolowy 18:
9,12
cis, cis
6 (A,B)
2. kwas -linolenowy 18:
9,12,15
cis, cis, cis
3 (C)
3. kwas -linolenowy
18:
6,9,12
cis, cis, ci
s 6 A(B)
Kwasy ABC są substratami
prostaglandyn
A - monoenowych
np. PGE
1
B - dienowych
PGE
2
C - trienowych
PGE
3

Kwas
arachidonowy
AA;
eikozotetraenowy; NNKT; wit.F; omega6; roślinny;
4
Funkcja
powstawanie eikozanoidów
wtórny przekaźnik
Uwięziony w fosfolipidach błonowych w pozycji 2
glicerolu
Fosfolipaza A
2
- enzym błonowy; aktywność
konstytucyjna i indukowana
Fosfolipazy A
1
. A
2
, C i G - efektory
pośrednie w
działaniu hormonów
może go uwalniać także fosfolipaza C i D;
w wyniku działania fosfolipazy (C) powstają
diacyloglicerol;
fosfolipazy (D) kwas fosfatydowy – następnie
lipazy odcinają AA

Należy do tzw.
LSM
- lipid second mesenger
;
działają one nie tylko w komórce ale dyfundują
przez błonę i parakrynnie działają na drugą
komórkę
AA jako wtórny przekaźnik
OUN
kwas glutaminowy jako neurotransmiter
receptor NMDA pobudzenie wnikanie Ca
2+
aktywacja
fosfolipazy A
2
powstaje
AA opuszcza szczelinę ,
wnika do
synaptycznej receptory dla AA
uwalnianie kwasu glutaminowego ; sprzężenie
zwrotne
kwas glutaminowy w aspekcie pamięci świeżej
i uczenia się
Poza OUN - AA jako przekaźnik - nie
wiadomo
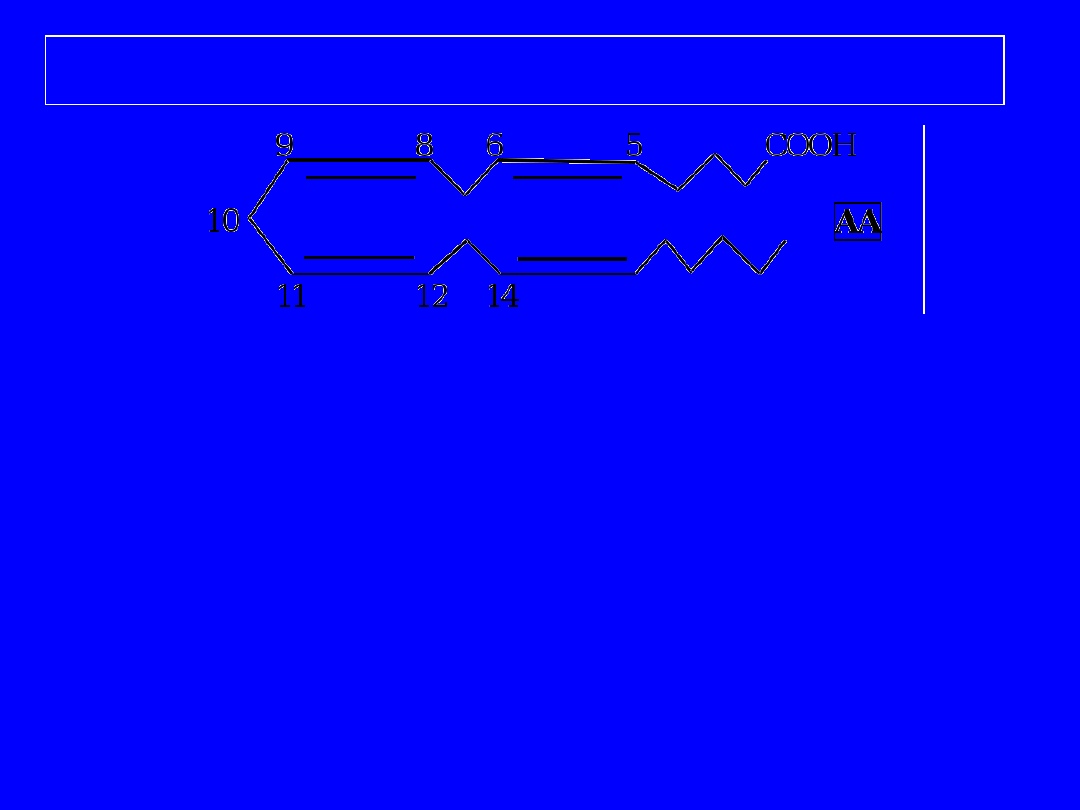
Przemiana kwasu arachidonowego
;
1.
CYKLOOKSYGENAZA
(C
OX
)
2.
LIPOOKSYGENAZA
(L
OX
)
3.
MONOOKSYGENAZY
zależne od cyt P450;
droga
epooksygenazowa; powstaje
kwas 5,6-epoksy-
arachidonowy - modulator
uwalniania somatostatyny z podwzgórza
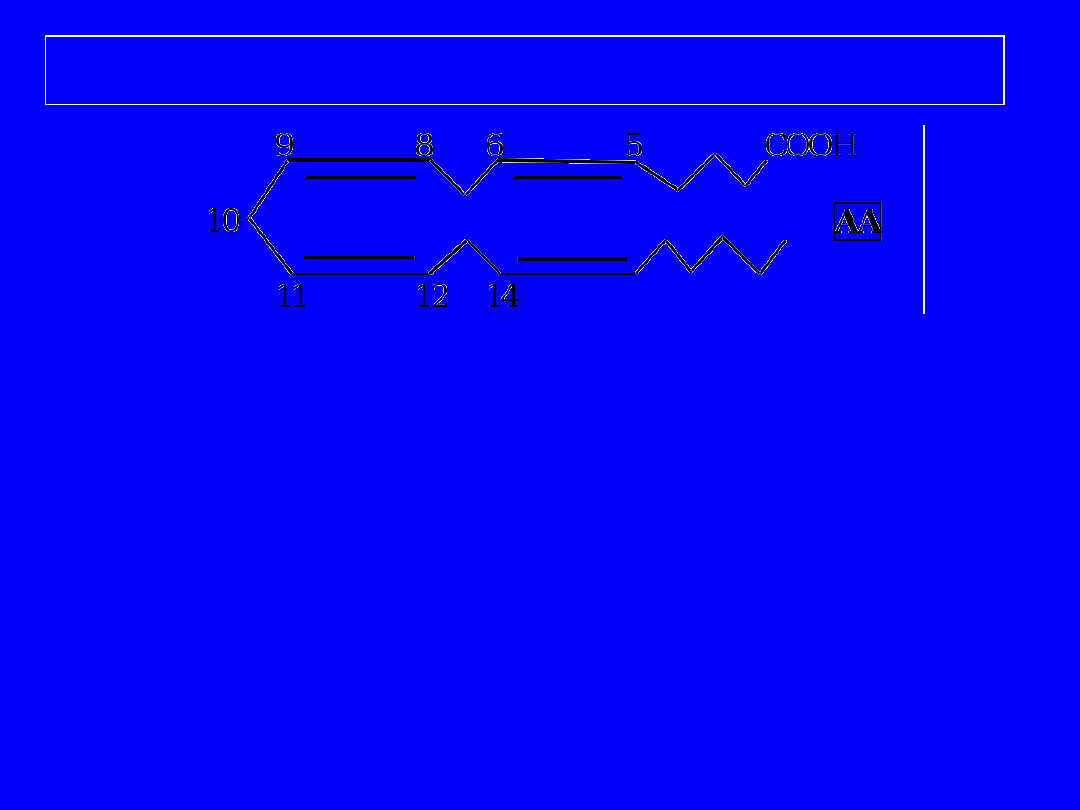
Przemiana kwasu arachidonowego
;
przekształcanie zaczyna się od
LIPOOKSYGENACJI;
przyłączenia O
2
;
lipooksygenaza
;
oksydoreduktaza kwas
tłuszczowy : tlen
; L
OX
pod wpływem L
OX
przesunięcie wiązania
podwójnego;
powstaje układ sprzężony
oraz grupa hydronadtlenkowa -
OOH
przy
odpowiednim atomie C :5,11,12,15
produkty utlenienia:
HPETE - kwas
hydroperoksyeikozatetraenowy
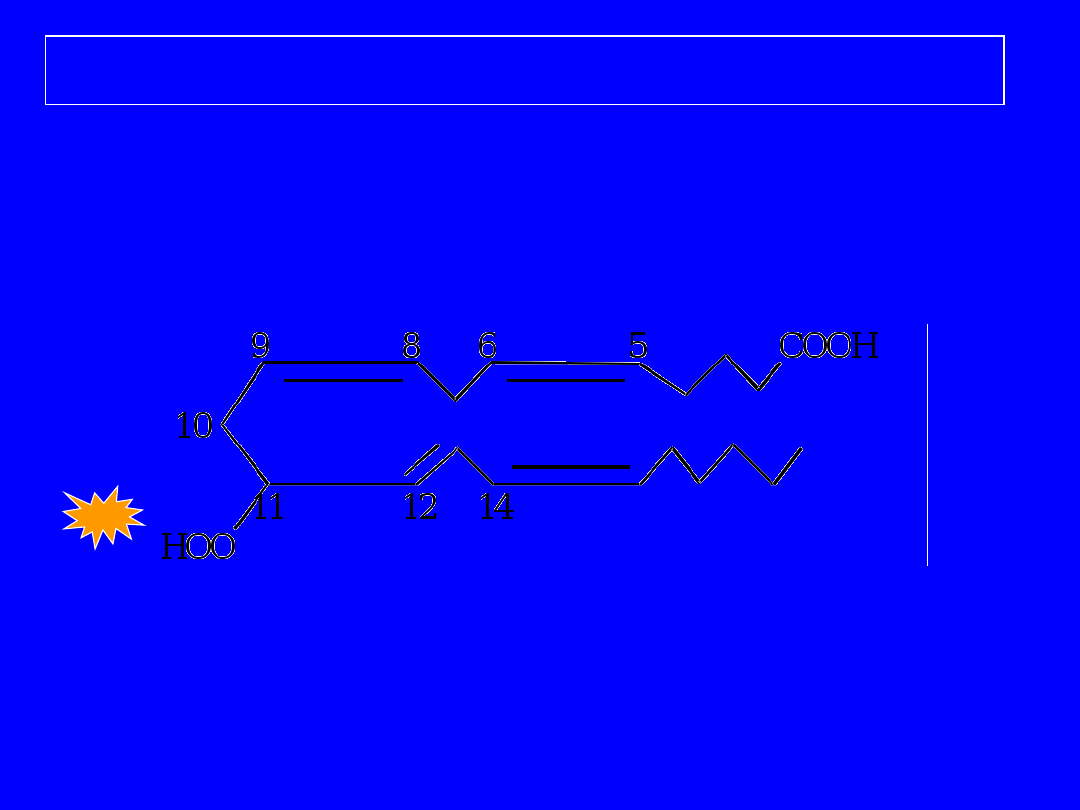
Przemiana kwasu arachidonowego
;
11L
OX
11-HPETE
- substancja macierzysta
dla
prostaglandyn
, tromboksanów,
prostacyklin; także
silny inhibitor
cyklooksygenazy
11-HPETE
nieenzymatycznie ulega
przekształceniu w odpowiedni
hydroksykwas
czyli
11-HETE
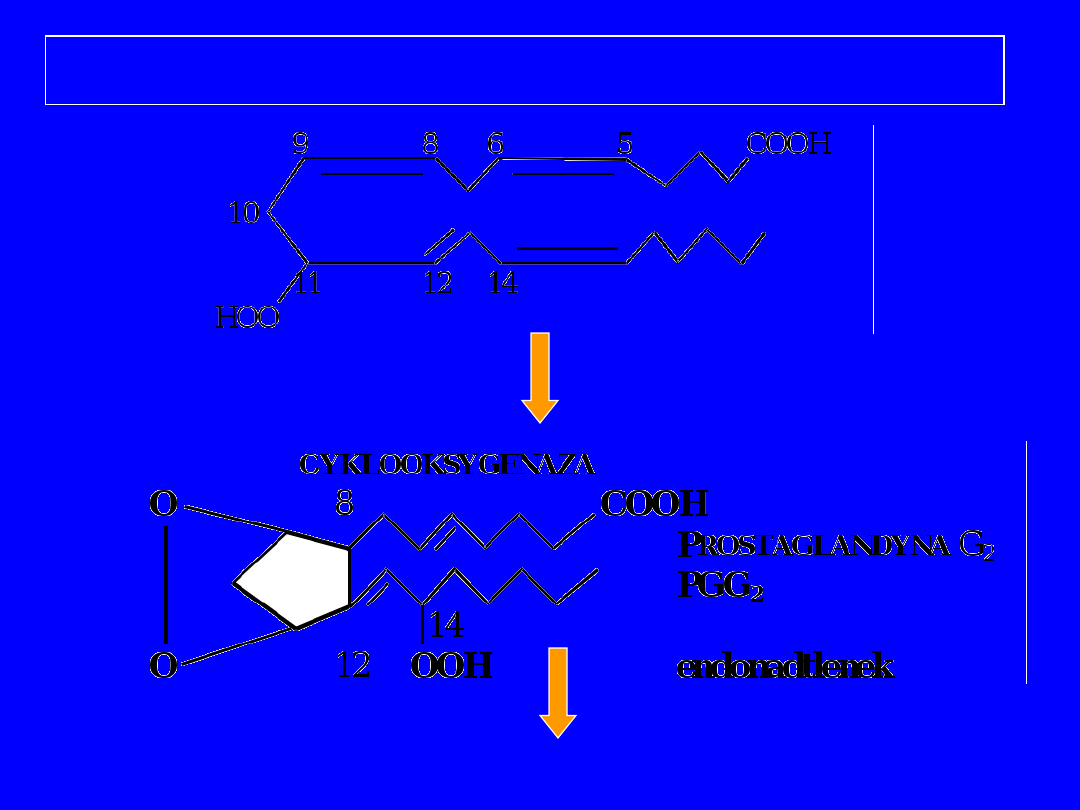
Przemiana kwasu arachidonowego
;
11-HPETE
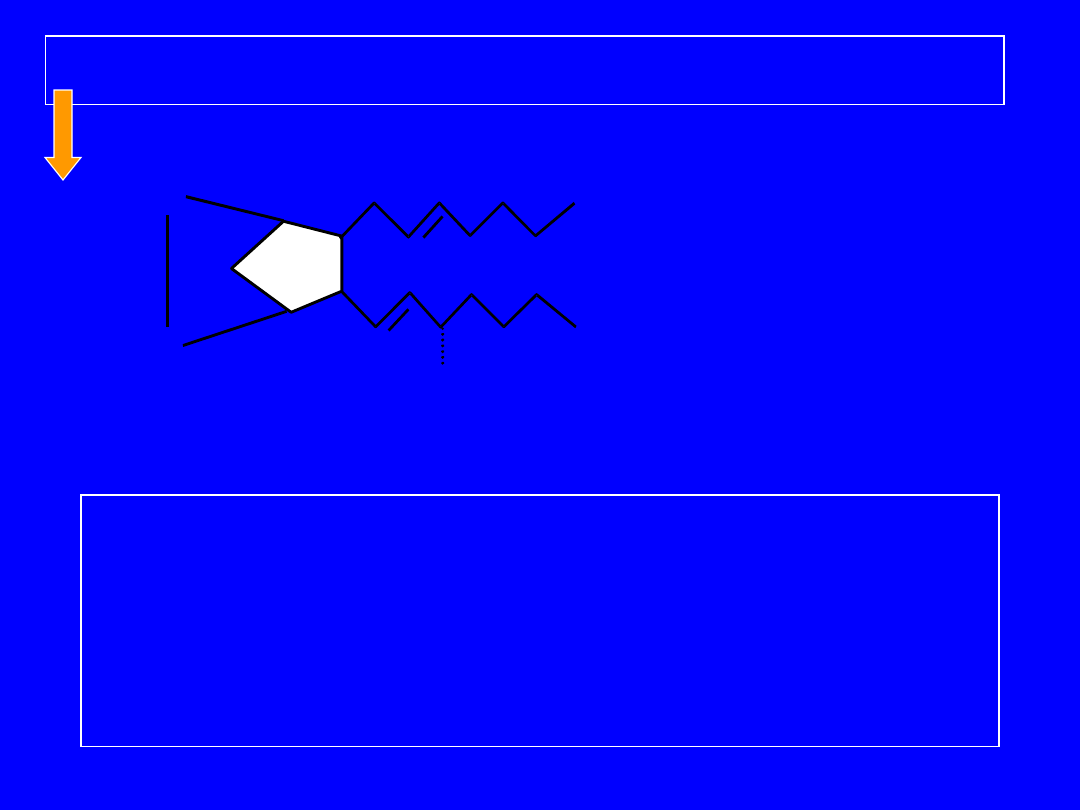
Przemiana kwasu arachidonowego
;
P
EROKSYDAZA
O
8
COOH
P
ROSTAGLANDYNA
H
2
PGH
2
12
ulega przekształceniu do
O
15
PGD, PGE, i PGF
OH
TX
PGI
Synteza prostaglandyn z AA
.Oksygenacja pomiędzy C9 i C11 oraz C15
.Odwodorowanie przy C8 i C11
.Wytworzenie wiązania między C8 i C12
.Izomeryzacja C=C z C14 na C13
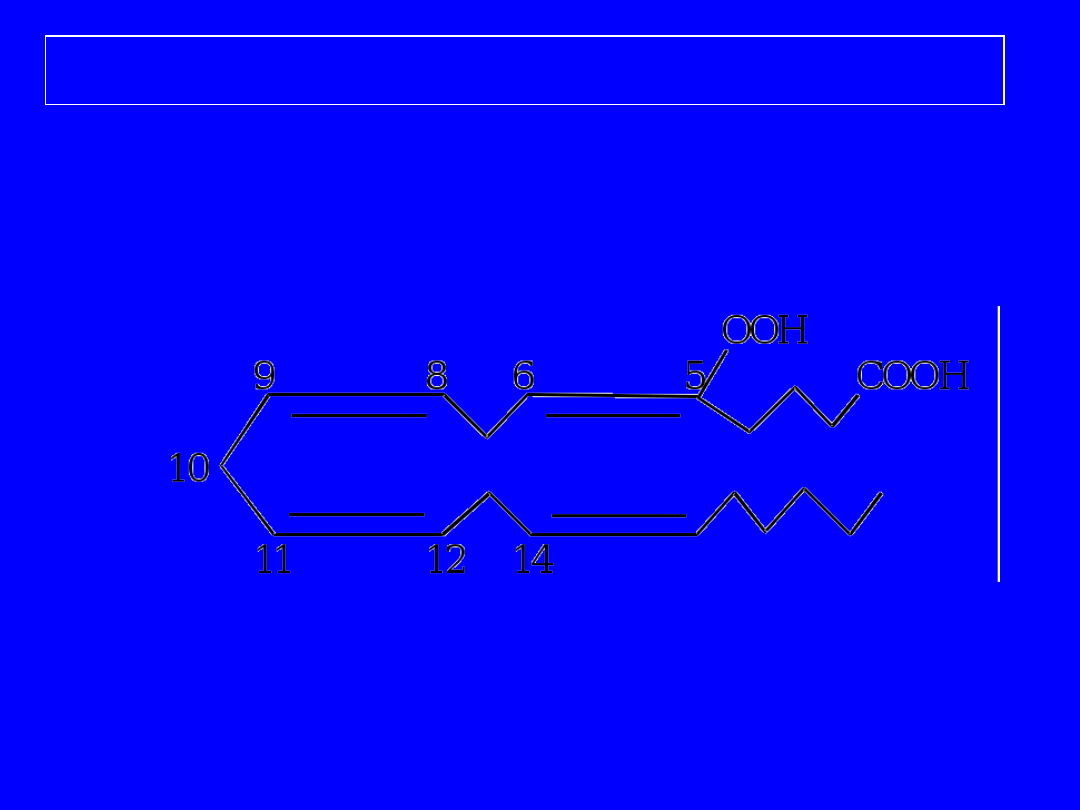
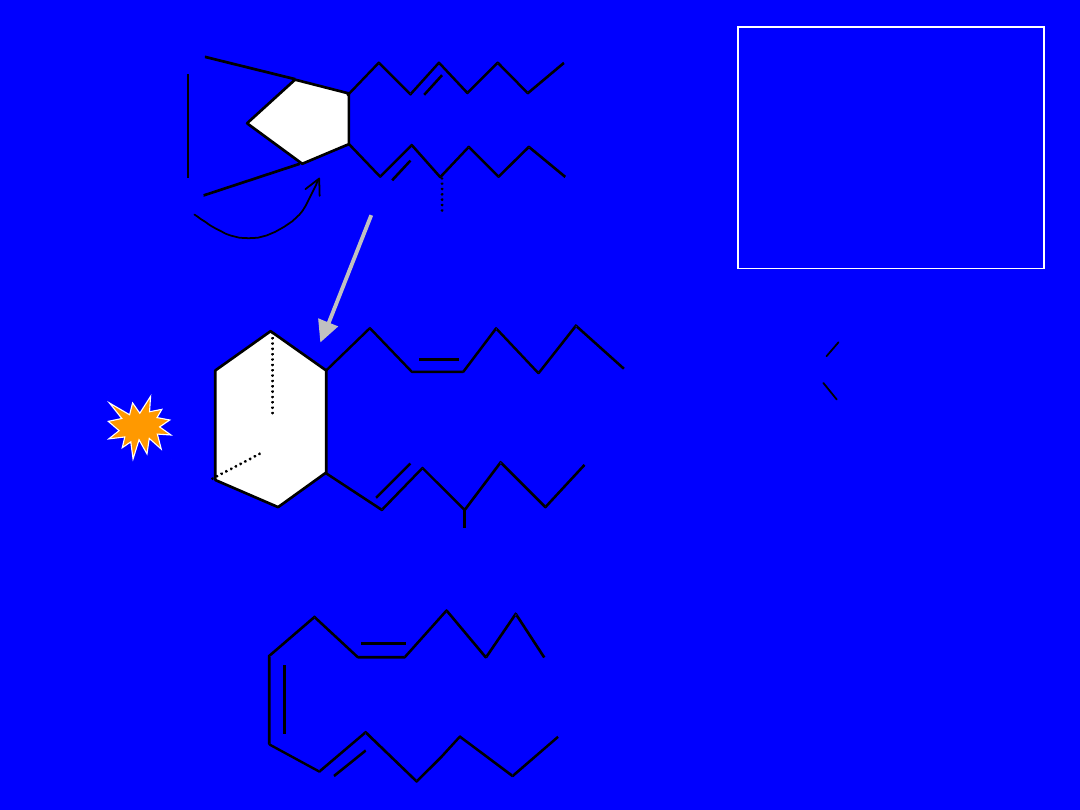
Przemiana kwasu arachidonowego
;
.
5L
OX
5-HPETE
sprzęganie z peptydami
leukotrieny
(leukocyty, komórki
tuczne)
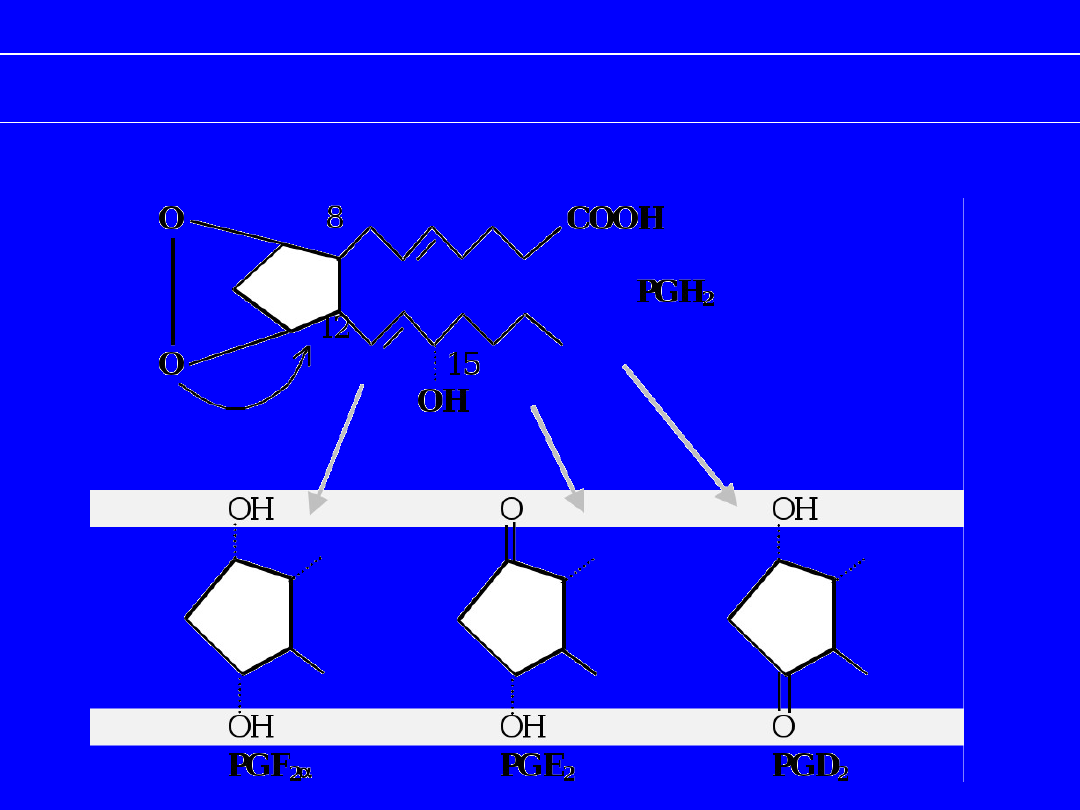
PGH
2
jako substrat do syntezy PGD, PGE i PGF
Powstawanie
PGD i PGE–
izomeryzacja
PGF –
redukcja

NOMENKLATURA PROSTAGLANDYN
Grupy A, B, C, D, E w zależności od
podstawienia
pierścienia
pięcioczłonowego –
cyklopentanowego
Nawa PG uwzględnia obecność w cząsteczce
grupy –OH przy C-15 o konfiguracji lub
Wiązanie podwójne oznacza się indeksem w
nazwie
literowej; 3 serie; od ilości
C=C przy górnym lub
dolnym łańcuchu
Np. PGA
1
; prostaglandyna A
1
; oznacza
obecność
pierścienia A – grupa
OH przy C-15 oraz wiązanie
podwójne
13-14 w pozycji trans (a ....OH; pod
płaszczyzną
Cyfra 2 oznacza obecność 2 wiązań
podwójnych 13-14
trans; 5-6 cis
Cyfra 3 oznacza obecność 3 wiązań
podwójnych
17-16 cis
PGF2 “” podaje położenie grupy OH przy
C-9

Struktura i synteza tromboksanu
Płytki krwi
Tx – budowa
nieprostaglandynowa
2 PGH2 1TxA
2
+ 1 MDA +
17C(OH)
Powstawanie TxA hamuje
imidiazol
i jego
pochodne, kwas nikotynowy
O
8
COOH
PGH
2
12
O
15
OH
9
CHO
10
COOH
CH
2
CHO
O
dialdehyd
11
12
15
malonowy
OH
9
COOH
+
C17
12
10
O
Struktura
i synteza
tromboks
anu

Synteza i struktura prostacyklin
Ściana naczyń -
PGI
Z PGH
2
– rozerwanie układu nadtlenkowego
Połączenie z C-6 z utworzeniem pierścienia
furanowego
Synteza PGI
2
zachodzi w
śródbłonku
naczyniowym, a jej
działanie jest skierowane
na płytki krwi
Zapobiega zlepianiu się płytek krwi
Czas półtrwania około 3 min., potem jest
przekształcana do
6-ketoprostaglandyny F
1
(6-keto-PGF1) nieaktywnej biologicznie.
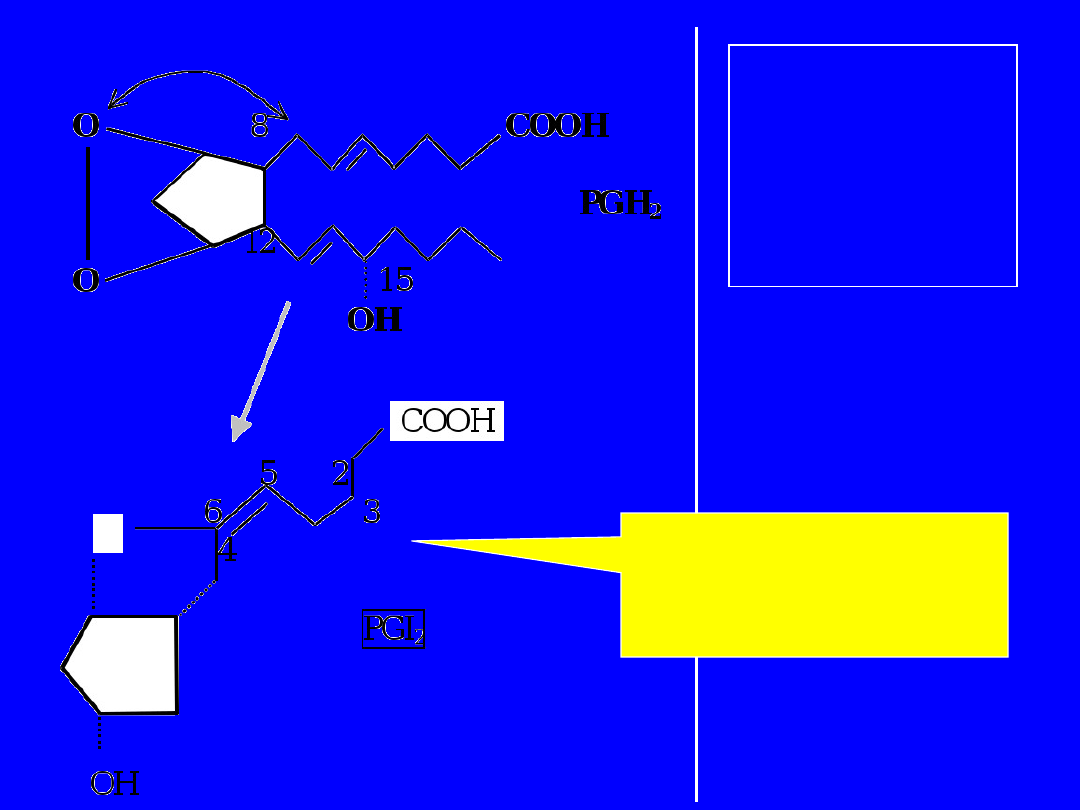
Synteza i
struktura
prostacyk
lin
O
Z PGH
2
– rozerwanie
układu nadtlenkowego
Połączenie z C-6 z utworzeniem
pierścienia furanowego
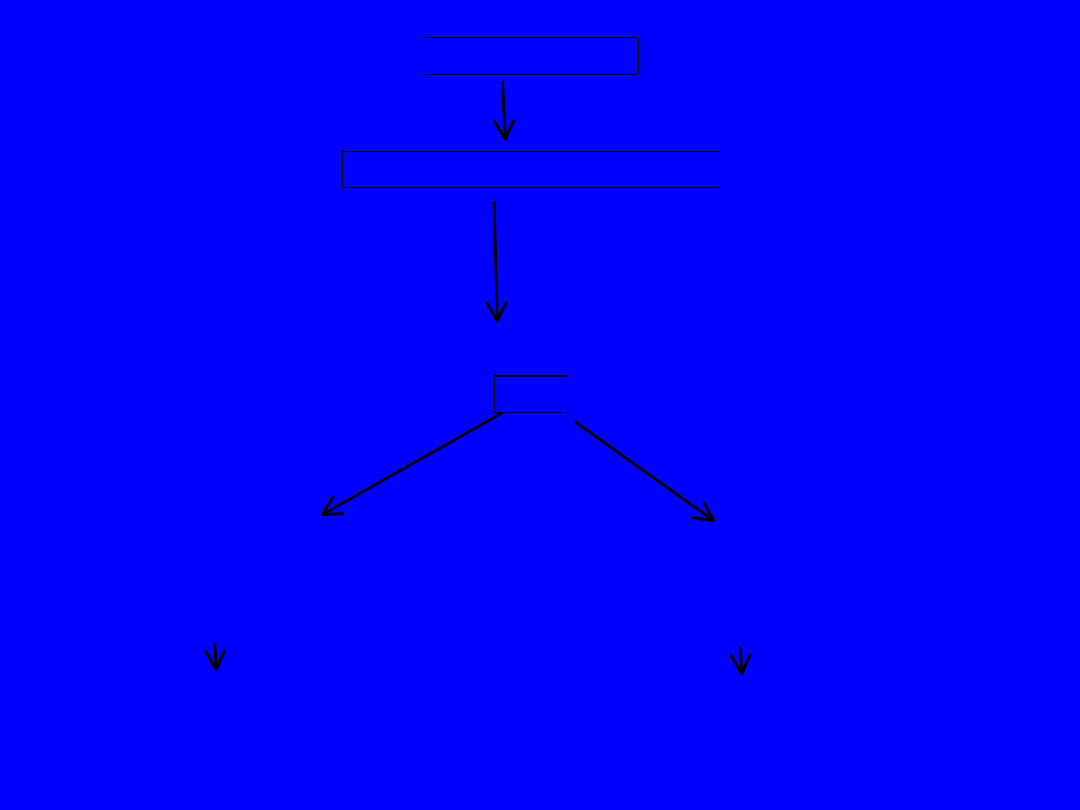
FOSFOLIPIDY
Glikokortykosterydy
Fosfolipaza
A
2
Np. hydrokortyzon
KWAS ARACHIDONOWY
15-hydro-peroksy
cyklooksygenaza
arachidonowy
aspiryna
o inne niesterydowe
HPETE
leki przeciwzapalne
N
ADTLENKI PROSTAGLANDYN
PGH
2
T
ĘTNICE
P
ŁYTKI KRWI
P
ROSTACYKLINA
TROMBOKSAN
A
2
PGI
2
TxA
2
t
0,5
= 3 min
t
0,5
= 32 sek
6-ketoprostaglandyna F
1
tromboksan B
2
6-keto-PGF
1
TxB2
LEUKOTRIENY
SYNTEZA
.
Powstają z AA pochodzącego z dwuwarstwy
fosfolipidowej
tworzącej
błonę
okołojądrową
.
Zadziałanie bodźca (np. alergenu) aktywowana
jest kinaza tyrozynowa, co uruchamia kaskadę
przemian
katalizowaną przez
fosfolipazę C
Powstają przekaźniki II rzędu: diacyloglicerol
(DAG) i 1,4,5-
trifosforan inozytolu (IP3).
IP3
uwalnia jony Ca
2+
z magazynów
wewnątrzkomórkowych
a
DAG
pobudza
kinazę
białkową
fosforylującą różne
białka w
komórce.
LEUKOTRIENY
SYNTEZA
.
Aktywowana jest (między innymi)
fosfolipaza
A2
, która
przemieszcza się w okolicę
otoczki jądrowej i uwalnia z błon kwas
archidonowy, który jest substratem dla 5-
lipooksygenazy
AA jest także substratem dla cyklooksygenazy,
katalizującej
cykl przemian do tromboksanów
i prostaglandyn, ale dla
niej substratem jest
AA z
fosfolipidów błony
komórkowej a
dla lipooksygenazy z błony jądrowej
.
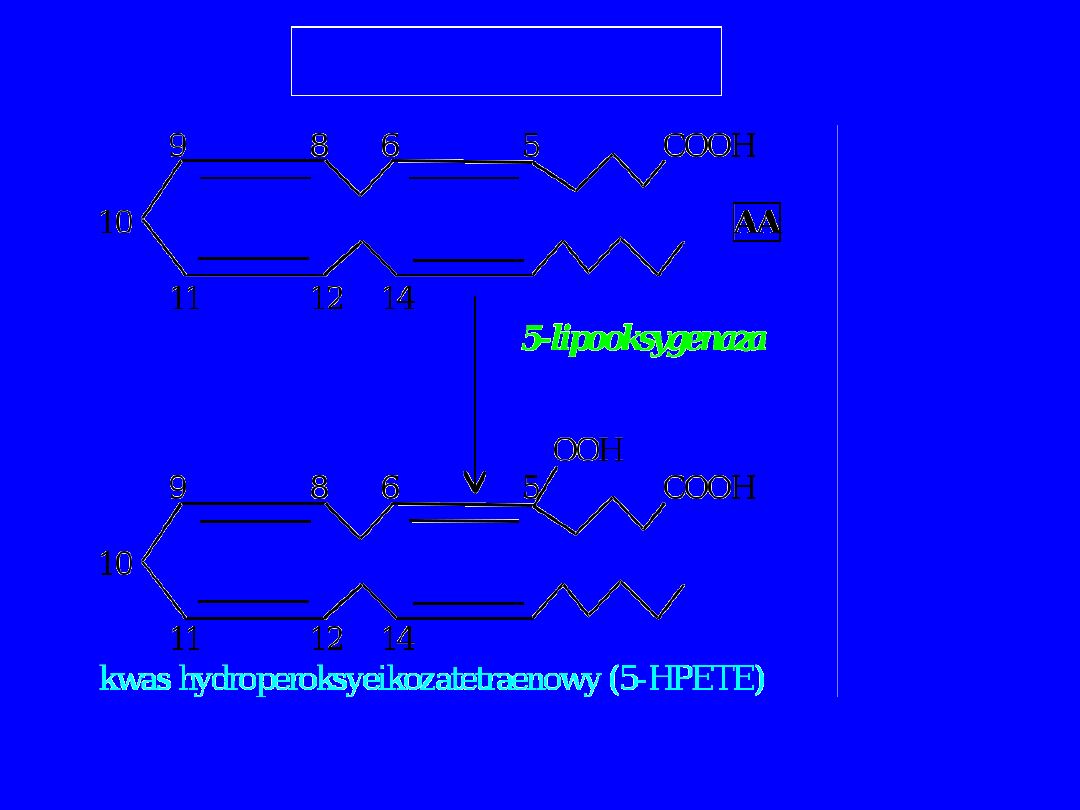
5-lipooksygenaza
działa wyłącznie w
kompleksie z
integralnym białkiem błony
jądrowej
FLAP
(5-
lipooksygenase
activating protein) w obecności jonów
Ca
2+
i
ATP.
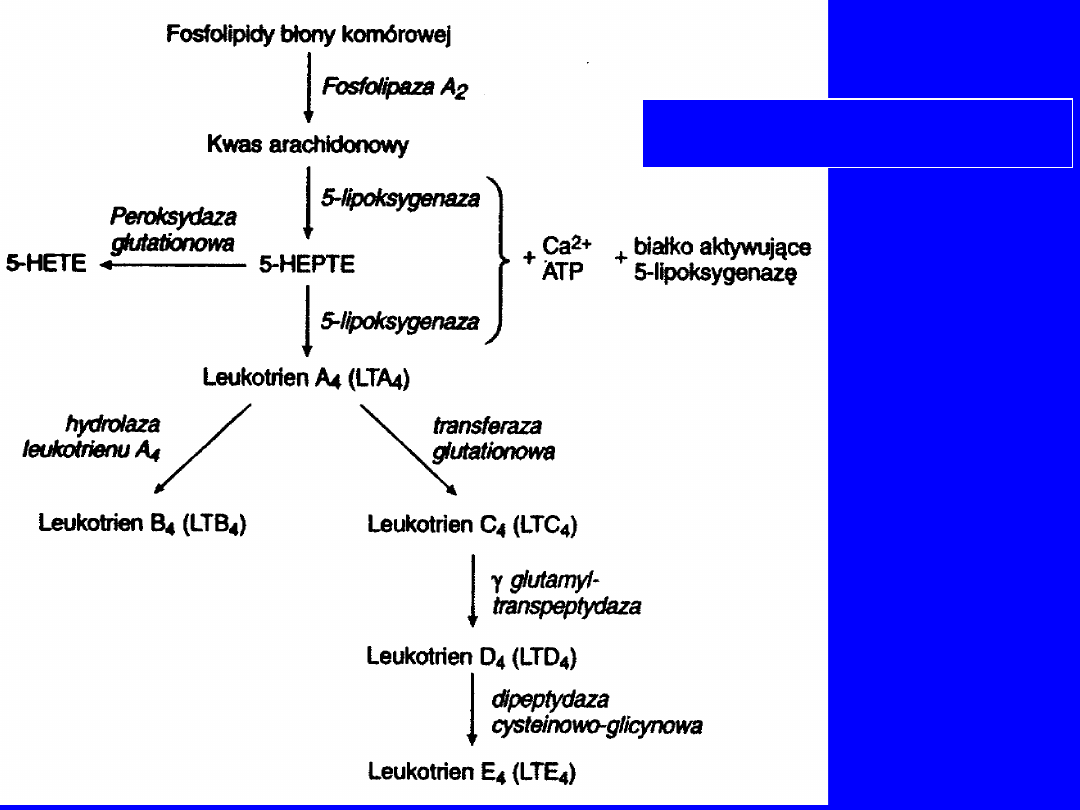
LEUKOTRIENY
SYNTEZA
.
Kompleks ten utlenia AA do nietrwałego kwasu
5-
hydroksyperoksy-eikozotetraenowego
(5-HPETE)
5-HPETE po wpływem
peroksydazy
glutationowej
ulega przemianie do kwasu 5-
hydroksyeikozatetraenowego (5-
HETE) lub pod
wpływem 5-lipooksygenazy do
leukotrienu
A
4
(LTA
4
).
Do LTA4
transferaza
glutationowa
przyłącza
glutation i powstaje leukotrien C4 (LTC4)
LTC4 wytwarzany jest w komórkach
efektorowych
zapalenia: komórkach
tucznych i granulocytach
zasadochłonnych i kwasochłonnych.
LEUKOTRIENY
SYNTEZA
.
LTC4 jest transportowany przez swoisty
receptor
transbłonowy poza
komórkę, gdzie pod wpływem
GGTP
powstaje leukotrien D4
W wyniku działania
dipeptydaz
cysteinylo
-
glicynowych
LTD4 ulega przemianie do
E4 (LTE4)
W granulocytach obojętnochłonnych i
makrofagach płucnych hydrolaza leukotrienu A4
wytwarza leukotrien B4
(LTB4)
LEUKOTRIENY
SYNTEZA
.
Powstają 2 grupy leukotrienów, różniące się
miejscem syntezy, receptorami i działaniem
.
Leukotrieny
cysteinylowe
– (C, D i E)
wytwarzane głównie
w granulocytach
kwasochłonnych i komórkach
tucznych;
receptorami są Cys-LT
4
(o wysokim
powinowactwie) iCys-LT
2
(niskim)
Druga grupa to
LTB
4
syntetyzowany w
aktywowanych
granulocytach
obojętnochłonnych i zasadochłonnych,
monocytach, makrofagach.
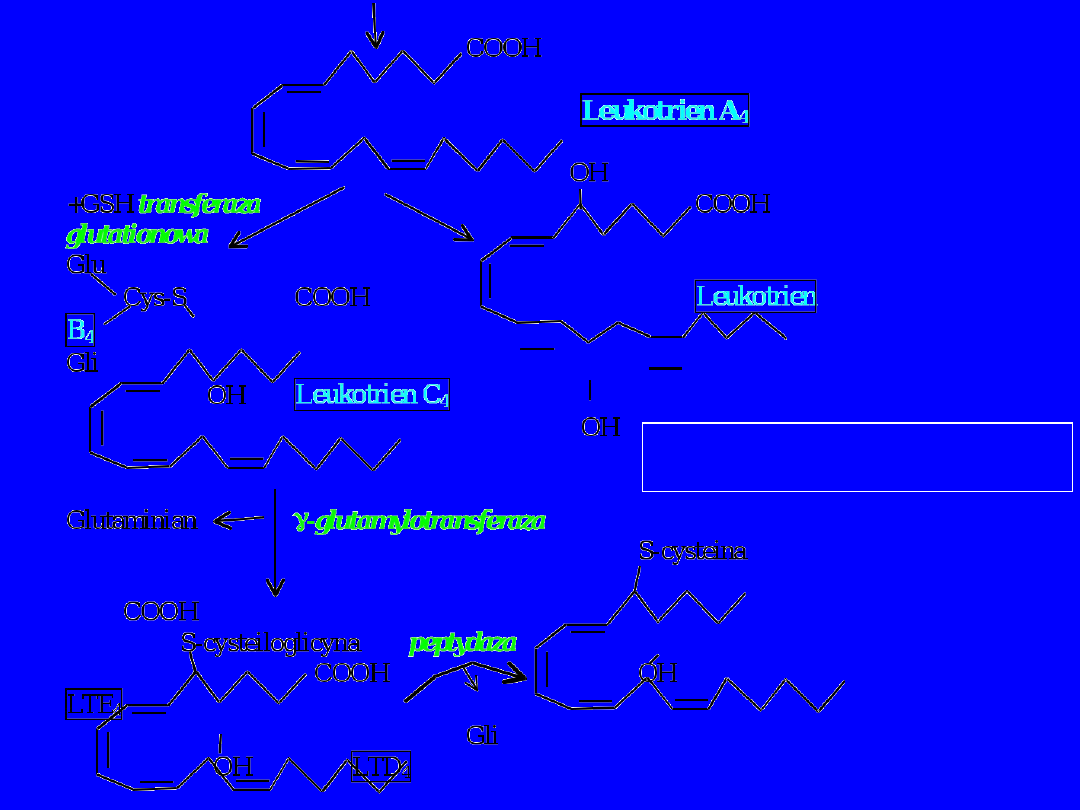
LEUKOTRIENY
5-HPETE
sprzęganie
z
peptydami
leukotrieny
(ugrupowa
nie
trienowe –
3
sprzężone
wiązania
podwójne)
LEUKOTRIENY
LEUKOTRIENY
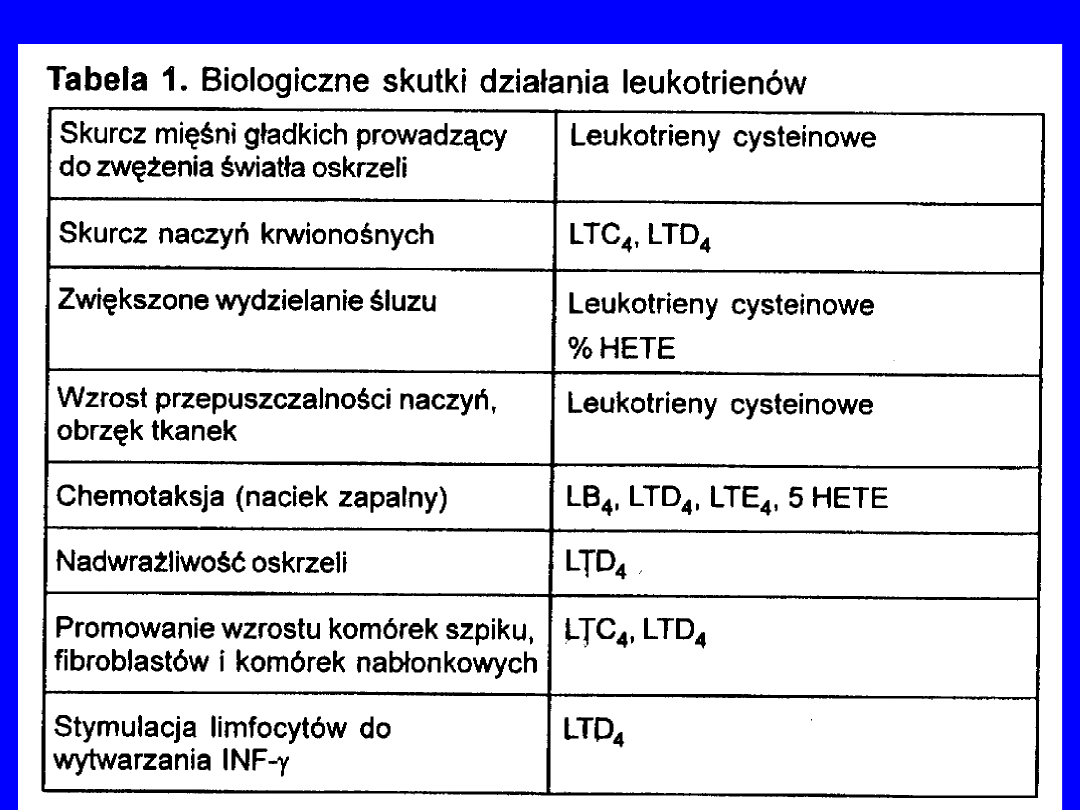

Leukotrieny – właściwości chemotaktyczne (C, D, E)
Powodują nagromadzenie się leukocytów w
ognisku zapalnym
100-1000x silniej kurczą mięśnie oskrzeli niż
histamina
uczestniczą w reakcjach nadwrażliowści
bezpośredniej (np.
dychawica oskrzelowa).
LEUKOTRIENY
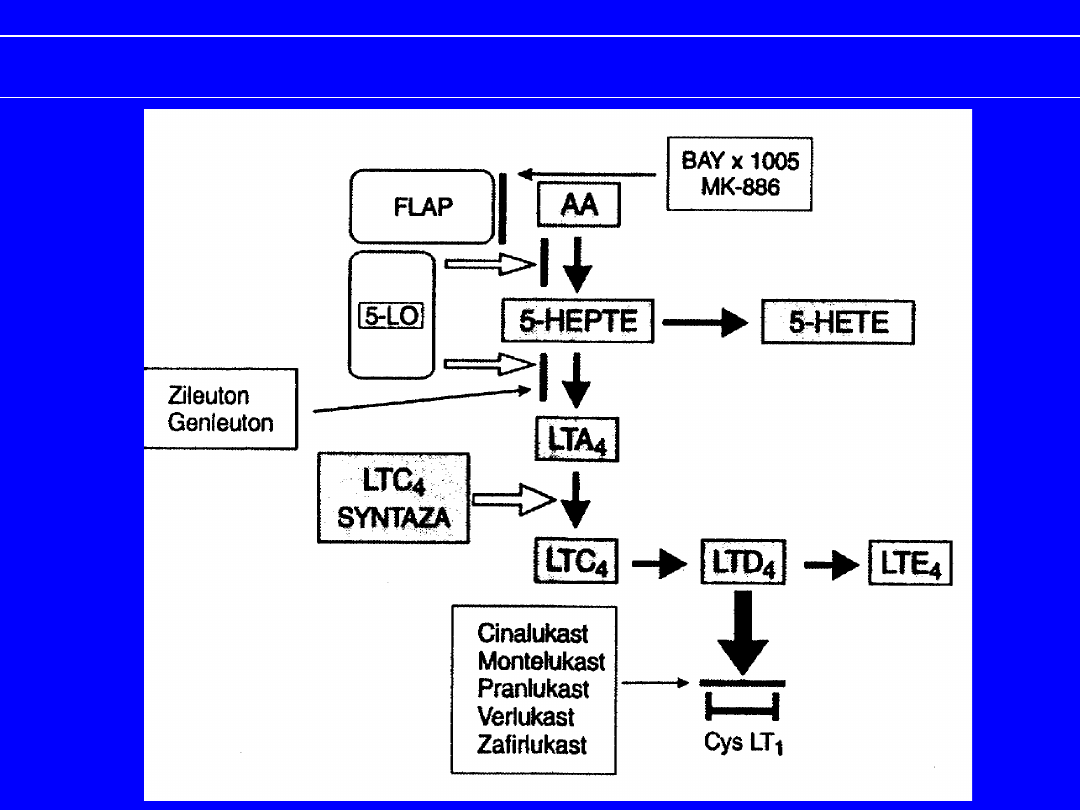
Miejsca wychwytu leków przeciwleukotrienowych.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
Wyszukiwarka
Podobne podstrony:
Metabolizm AA 2003 2
Metabolizm AA 2003
Metabolizm AA 2003 2
Metabolizm AA 2003
Metabolizm kkw tł stud
Metabolizm
(2,3) Działania nieporządane, toksytczne leków Metabolizm, czynniki wpływające na działanie substanc
metabolizm witaminy D3
Zespół metaboliczny tarczyca wykład8
Komponenty metaboliczne
Metabolizm aminokwasów
Zespó Metaboliczny w profilaktyce lekarza medycyny pracy 1
Bilirubin metabolism Applied ph Nieznany (2)
Biochemia TZ wyklad 12 integracja metabolizmu low
więcej podobnych podstron