
OCHRONA ATMOSFERY
Wykład 8
Dr hab. inż. Krzysztof GOSIEWSKI
Profesor AJD
Odsiarczanie gazów
– metody
katalityczne

Kwas siarkowy (H
2
SO
4
)
• Kwas siarkowy jest cennym półproduktem
przemysłu chemicznego i nawozowego.
• Półproduktem gazowym do
wyprodukowania H
2
SO
4
jest SO
2
.
• Skoro w gazach odlotowych mamy SO
2
–
to dlaczego nie produkować z niego
H
2
SO
4
?
Byłaby to najprostsza bezodpadowa
metoda odsiarczania i w dodatku zysk
finansowy!
No właśnie dlaczego?
Po pierwsze: aby produkować kwas siarkowy należy
najpierw
SO
2
utlenić
do
SO
3
.
wg
reakcji:
SO
2
+ ½ O
2
SO
3
Po drugie: Kwas siarkowy ma wartość handlową tylko
wtedy kiedy ma odpowiednio wysokie stężenie !
(najlepiej powyżej 92%
wag
). Można znaleźć nabywców na nie
normowany
kwas
pow.
70%
wag
,
ale
nie
o niższym stężeniu
Po trzecie: Kwas siarkowy, aby mieć wartość handlową musi
być odpowiednio czysty. Czystość kwasu jest dokładnie
określana normą.

Po pierwsze: aby produkować kwas
siarkowy należy najpierw SO
2
utlenić do
SO
3
.
wg reakcji: SO
2
+ ½ O
2
SO
3
• Na skalę techniczną można to prowadzić tylko
w heterogenicznym procesie katalitycznym na
stałym katalizatorze (zwykle wanadowym)
tzw. „kontakcie” w temperaturach powyżej
400
o
C.
• Gazy odlotowe z metalurgii lub spaliny po
oczyszczeniu mają temperaturę znacznie
niższą, więc trzeba by je podgrzać.
• A to niestety to wymaga energii, która
kosztuje!
A skąd bierze się tę energię przy
„normalnej” przemysłowej
produkcji kwasu siarkowego?
• W Polsce głównym surowcem do produkcji H
2
SO
4
była siarka pierwiastkowa (S),
którą spala się wg silnie egzotermicznej reakcji:
S + O
2
SO
2
H = -297 [kJ/mol]
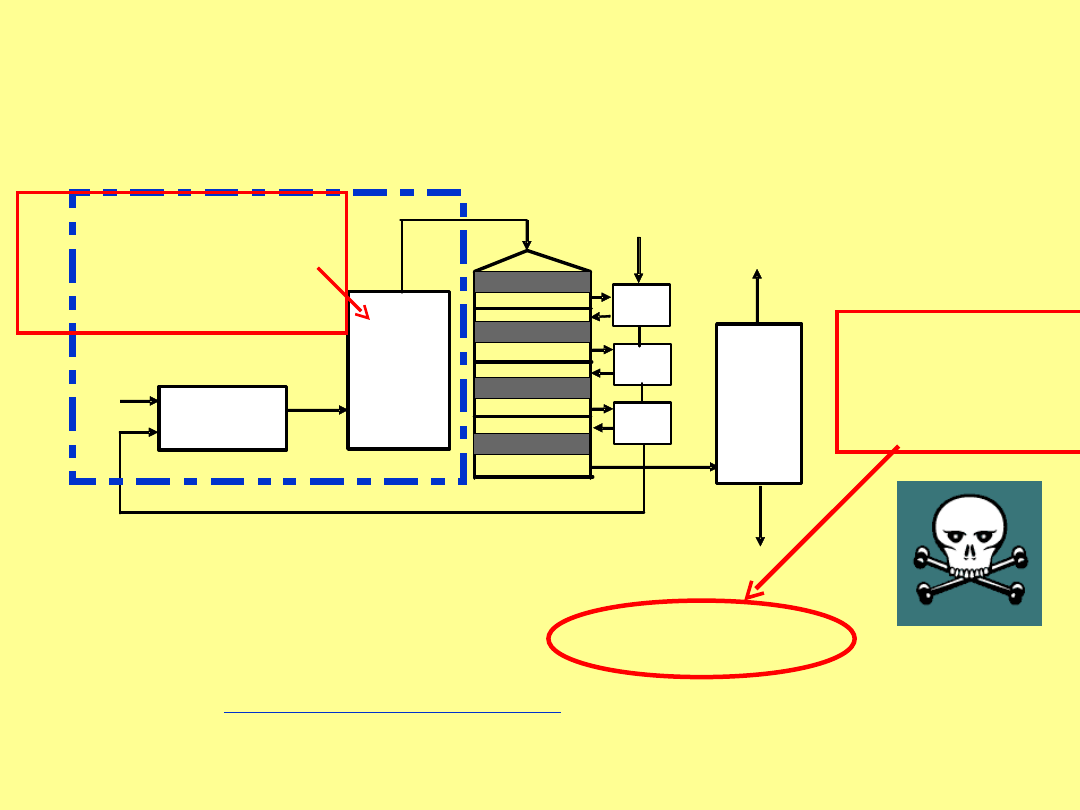
• To nie jest instalacja odsiarczania (czyli usuwania SO
2
z gazów
odlotowych, tylko instalacja produkująca kwas siarkowy. Do tego celu ta
instalacja produkuje, a nie usuwa SO
2.
Piec
siarkowy
Kocioł
(utylizator
ciepła
spalania)
Siarka
Powietrze
1100
o
C
430
o
C
Wym.
ciepła
Wym.
ciepła
Wym.
ciepła
Absorp-
cja
SO
3
gaz
odlotowy
Reaktor katalityczny
Ten fragment nie
występuje w instalacjach
metalurgicznych
To jest
reakcja
silnie
egzotermiczna
Produkowane ciepło
odbiera się w kotle
produkując parę
energetyczną
W instalacji produkującej H
2
SO
4
biegną 3 egzotermiczne
reakcje:
•
spalanie siarki w piecu siarkowym (bardzo silnie
egzotermiczna):
S + O
2
SO
2
H = -297
[kJ/mol]
utlenianie
SO
2
na
katalizatorze
(też
silnie
egzotermiczna):
SO
2
+ ½ O
2
SO
3
H = -99
[kJ/mol]
tworzenie kwasu siarkowego (silnie egzotermiczna,
ale biegnąca w stosunkowo niskich temperaturach):
SO
3
+ H
2
O H
2
SO
4
H = -101
[kJ/mol]
Przy produkcji kwasu w instalacji
odsiarczania znika największe źródło
wysokotemperaturowego ciepła, którym jest
spalanie siarki!
Ciepła reakcji tworzenia kwasu siarkowego nie da
się
wykorzystać
do
podgrzania
gazów
odsiarczanych do ok. 400
o
C, bo absorpcja SO
3
biegnie w zbyt niskich temperaturach.
Wykorzystać można ciepło tylko
tej reakcji !!
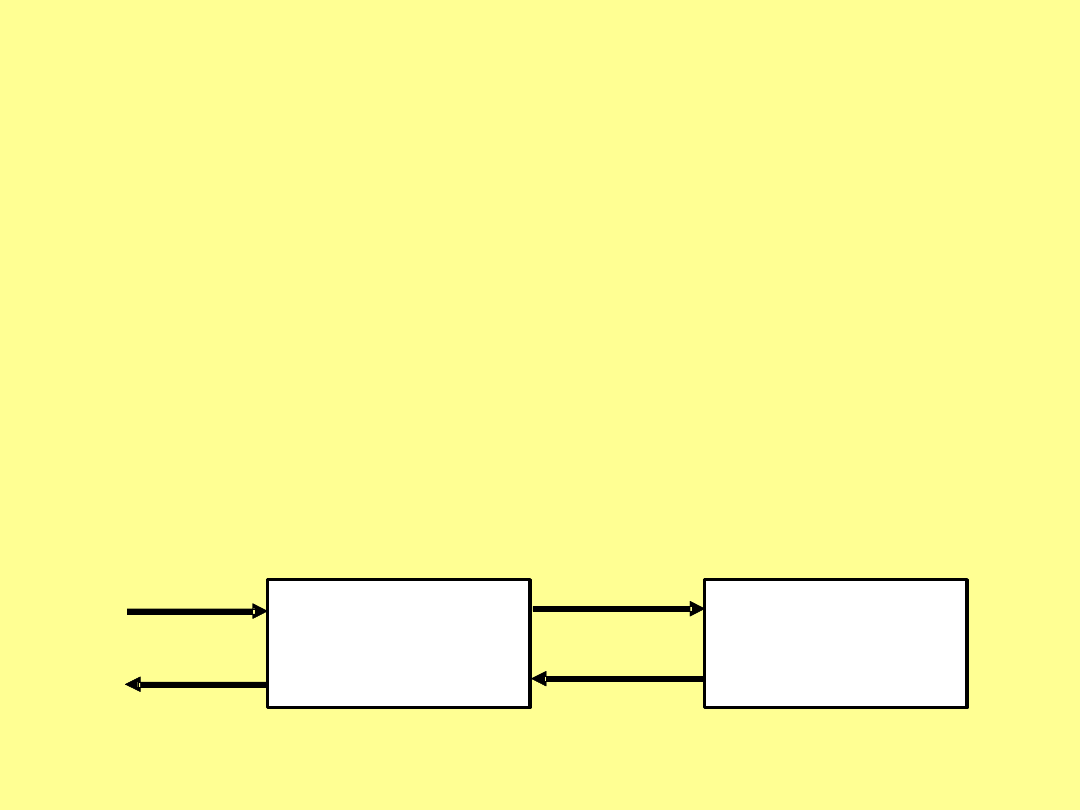
AUTOTERMIA
• Wykorzystanie ciepła zachodzącej
w reaktorze reakcji egzotermicznej do
podgrzania płynu wpływającego do tego
reaktora nazywa się AUTOTERMIĄ!
• Będziemy
często
w
następnych
wykładach wracać do tego pojęcia.
Wymiennik
ciepła
Reaktor
T
1
T
2
T
3
T
4
Uproszczony schemat autotermicznego odzysku ciepła reakcji

Odpowiednio wysokie – to znaczy jakie ?
• Takie, przy którym utlenianie SO
2
do SO
3
produkuje dość
ciepła, by podgrzać odsiarczany gaz do ok. 400
o
C, bo ciepła
tworzenia H
2
SO
4
w procesie absorpcji do tego celu
wykorzystać się nie da.
• Ogólnie możemy powiedzieć, że produkcja H
2
SO
4
z SO
2
zawartego w gazach odlotowych nie nastręcza dziś większych
problemów, jeśli stężenia te są wyższe od 5 %obj. SO
2
.
Z bilansu energii wynika, że łatwe będą
przypadki, kiedy stężenie SO
2
w
odsiarczanym gazie będzie odpowiednio
wysokie.
Z tego względu problematykę odsiarczania
metodami katalitycznymi podzielimy na dwie
grupy zagadnień:
katalityczne odsiarczanie gazów
mocnych
(powyżej 5 % obj. SO
2
)
katalityczne odsiarczanie gazów
słabych
(poniżej 5 % obj. SO
2
)
Katalityczne odsiarczanie gazów
mocnych (powyżej 5 %obj SO
2
)
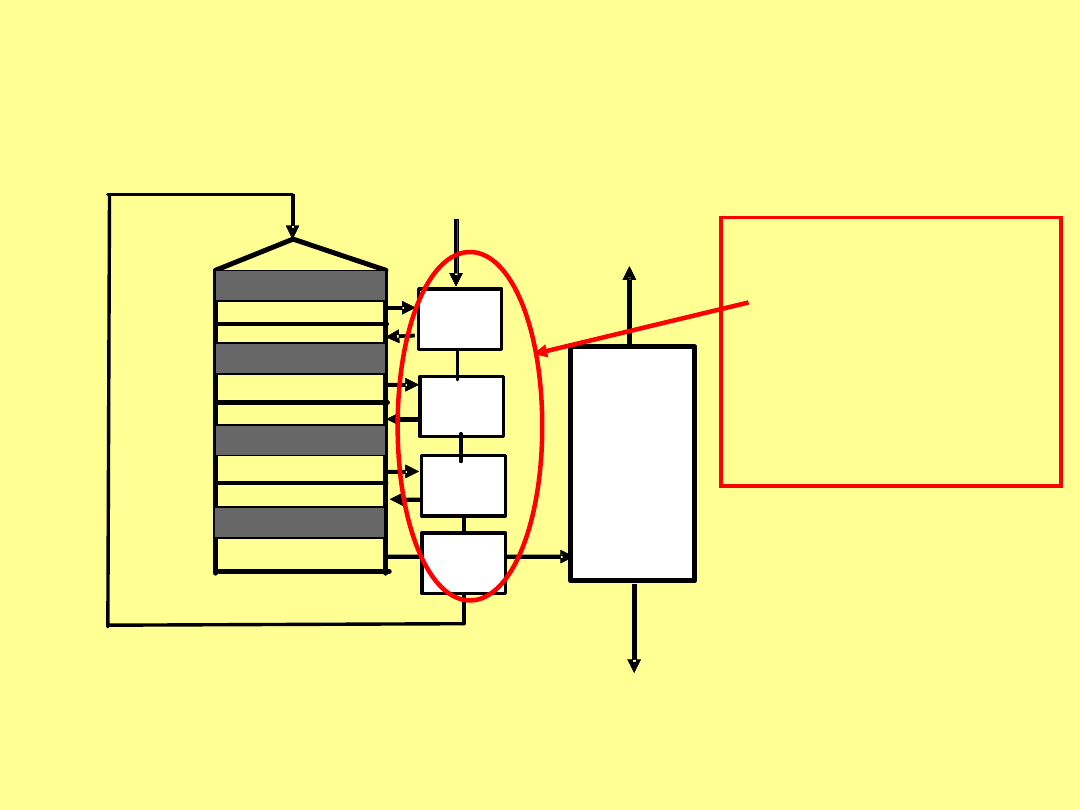
Uproszczony schemat fabryki kwasu
siarkowego z gazów odlotowych
metalurgii kolorowej, z pojedynczą
absorpcją SO
3
Niestety, obecnie
sprawa się
komplikuje, bo w
takiej instalacji
można uzyskać
stopień przemiany
SO
2
do SO
3
max. do
98% - a to dziś za
mało!
Wym.
ciepła
Wym.
ciepła
Wym.
ciepła
Absorp-
cja
SO
3
zasiarczony gaz odlotowy
z procesu metalurgicznego
Temperatura 70
o
C
Reaktor katalityczny
Wym.
ciepła
Te wymienniki
ciepła odbierają
ciepło konwersji
SO
2
do SO
3
,
aby
podgrzać wlotowy,
zasiarczony gaz
(AUTOTERMIA!)
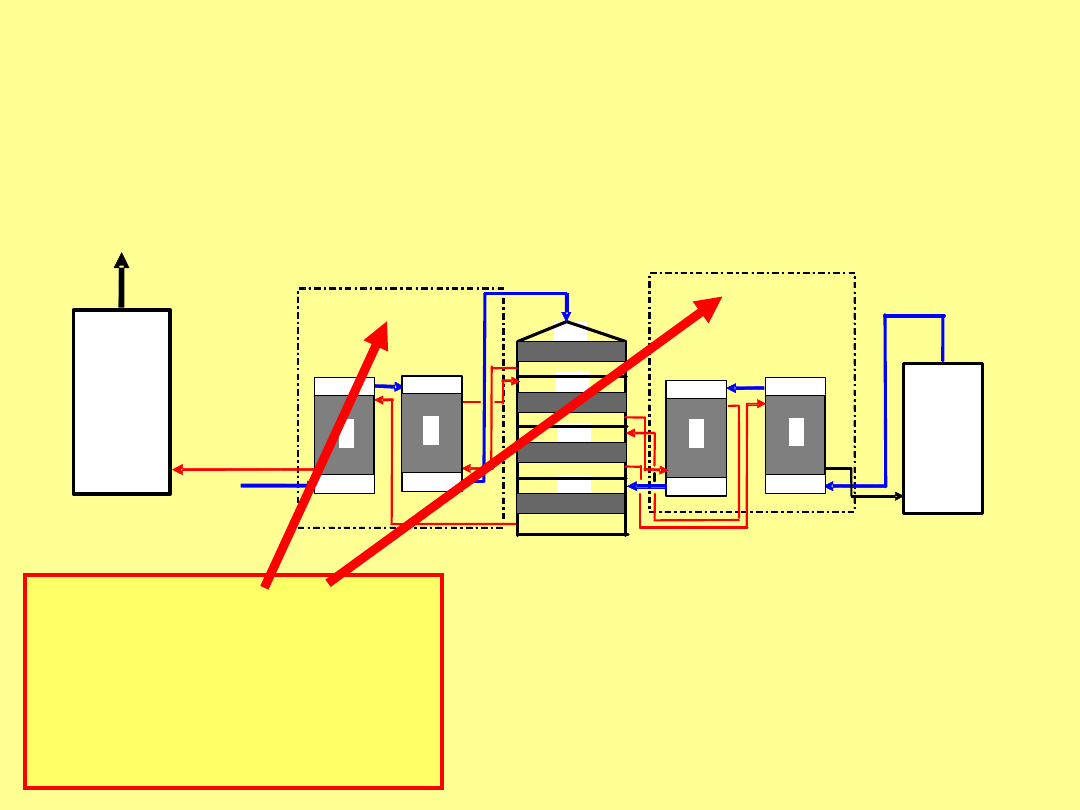
Nowoczesna instalacja metalurgiczna
pracuje w tzw. systemie „podwójnej
konwersji i podwójnej absorpcji”
(DK/DA)
gaz podgrzewany
gaz oddający ciepło
Instalacja DK/DA umożliwia
uzyskiwanie stopnia
przemiany SO
2
do SO
3
dochodzącego do 99,99%
Gaz po
absorpcji
pośredniej
PĘTLA „B”
PĘTLA „A”
Gaz do
odsiarczania
I
I st.
Absorp-
cji
SO
3
Reaktor
katalityczny
4
1
2
3
IV
II
III
Absorpcja
pośrednia
II st.
Absorp-
cji
SO
3
do atmosfery
Absorpcja
końcowa
Instalacja DK/DA
ma 2 pętle
autotermiczneg
o odzysku ciepła
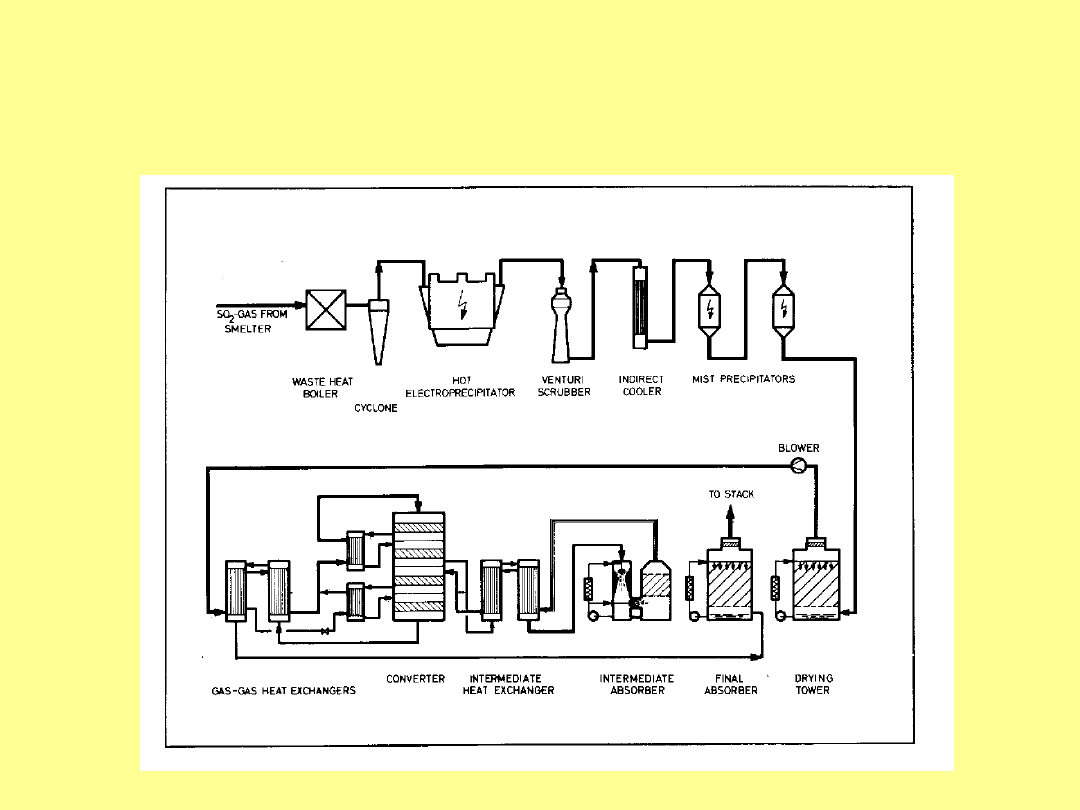
Rzeczywiste instalacje przemysłowe w
rzeczywistości są jeszcze bardziej
skomplikowane.
Poniżej schemat instalacji Firmy Lurgi
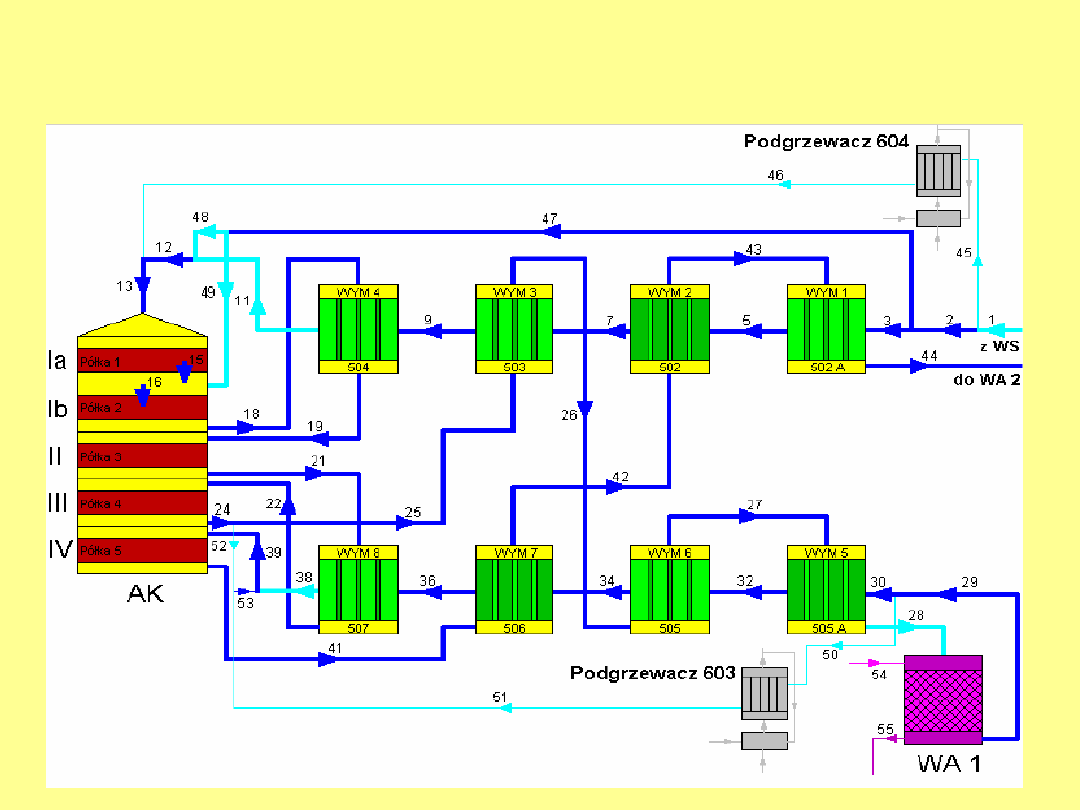
A poniżej instalacja samego węzła utleniania
SO
2
w hucie miedzi Głogów 1

Fotografie tej instalacji
Reaktor kontaktowy
Wymienniki ciepła
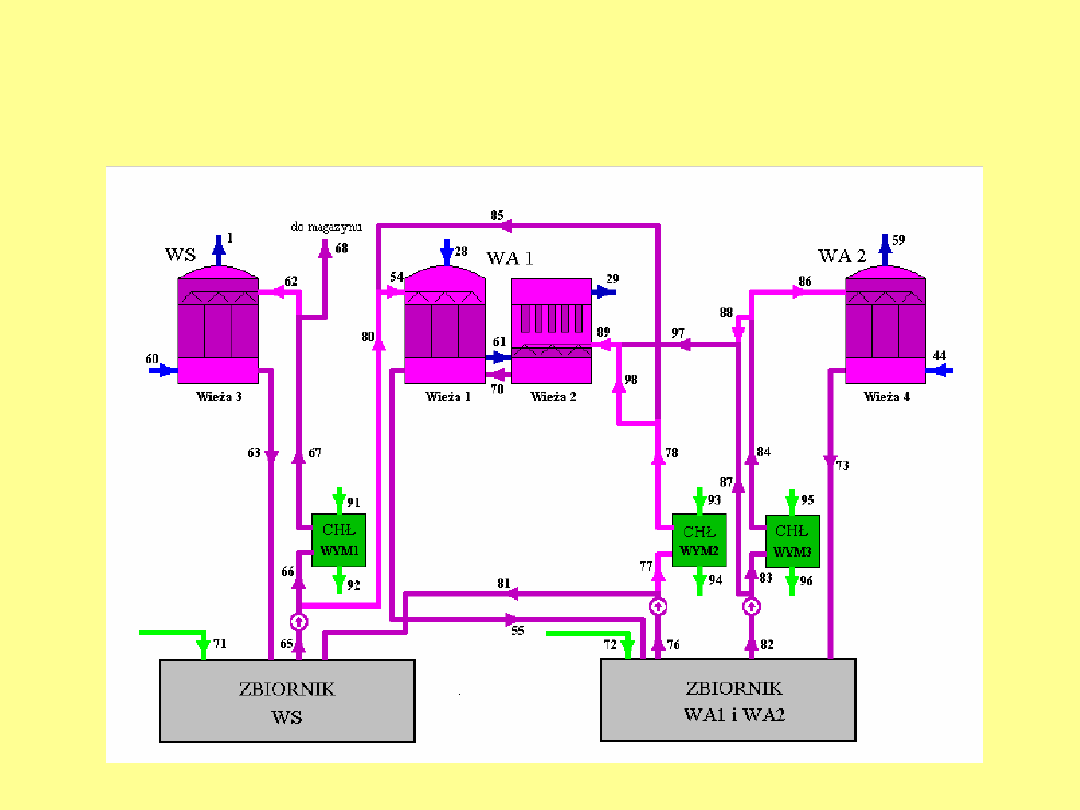
... i jeszcze węzeł suszenia gazów i
absorpcji SO
3
w kwasie siarkowym w tej
instalacji

Cała ta skomplikowana instalacja służy ochronie naszej
atmosfery.
Jest
to
wiele
drogich
urządzeń,
skomplikowana
myśl
naukowa
i techniczna. Nie jest to żaden „filtr z waty” włożony w
komin, jak się niektórym wydaje!
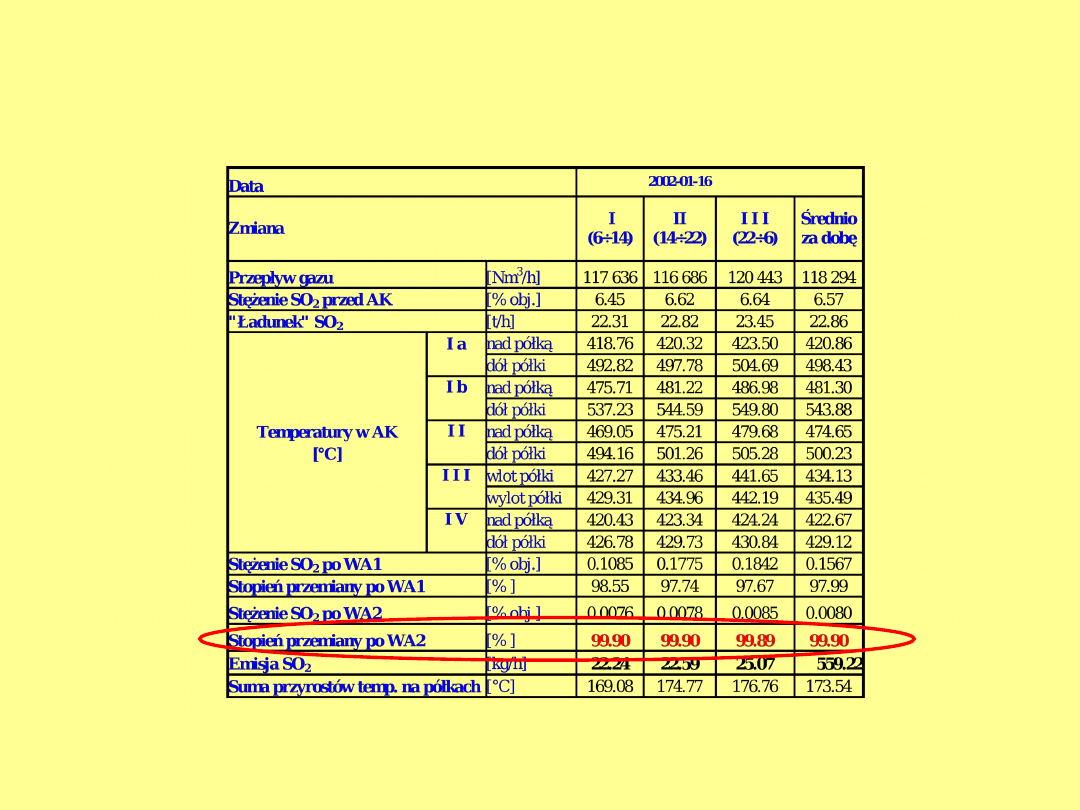
Osiągane w tej instalacji parametry
technologiczne:
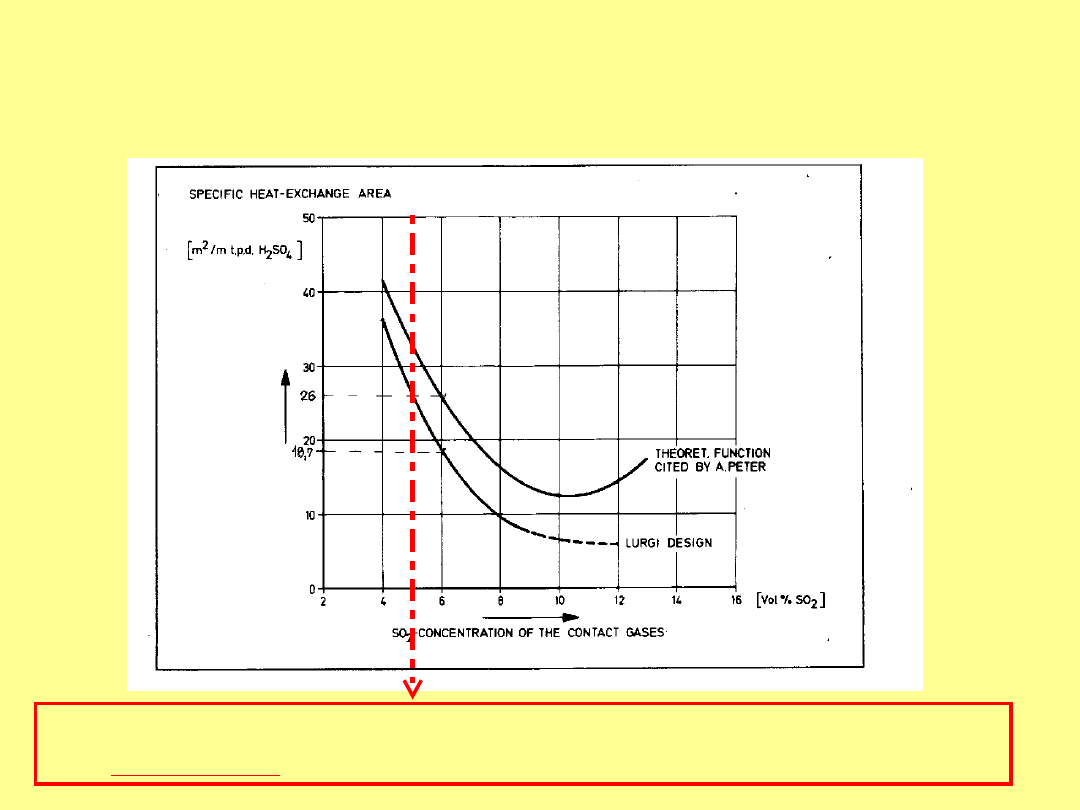
Zależność powierzchni właściwej
wymienników ciepła metalurgicznego węzła
kontaktowego od średniego stężenia gazów.
Gdy stężenia SO
2
są wyższe od 5% obj. to można uzyskać
autotermię przy rozsądnych wielkościach wymienników ciepła.

Reasumując: Metoda klasycznej
produkcji kwasu siarkowego poprzez
katalityczne utlenianie SO
2
i absorpcję
w kwasie siarkowym nadaje się tylko
do gazów o wyższych stężeniach, czyli
praktycznie do gazów odlotowych z
procesów metalurgicznych rud
wysokosiarczkowych, które nazwaliśmy
gazami mocnymi.
A co z zasiarczonymi spalinami
z kotłów energetycznych – czy
pozostają tylko metody
wapniakowe?

Katalityczne odsiarczanie gazów
słabych (poniżej % 5 obj. SO
2
) oraz
wilgotnych
• Zawartość poniżej 5 % obj. SO
2
w obecności
dużych ilości wilgoci może pojawiać się w
2 przypadkach:
w słabo stężonych gazach metalurgicznych gdzie
zawartość ta może mieścić się w granicach
2 do 5 % obj oraz w gazach z innych procesów
(jak np. gazy w koksowniach) zawierających
niskie koncentracje tlenków siarki przy blisko
100% wilgotności względnej
w spalinach kotłów energetycznych, gdzie
zwykle mieści się poniżej 0,3% obj.
Za niskie stężenie kwasu!
Na czym polega kłopot?
• Spaliny energetyczne, a także słabe gazy z
innych procesów zwykle zawierają H
2
O
bliskie stanu nasycenia.
• W procesie absorpcji SO
3
cała wilgoć (H
2
O)
z gazu przechodzi do fazy ciekłej.
• Jeśli w gazie wpływającym do absorpcji jest
mało SO
3
, które łączy się z wodą tworząc
H
2
SO
4
,
to
reszta
H
2
O
niepotrzebne
rozcieńcza powstający kwas. Stąd
jego
stężenie jest bardzo niskie
.
Przykład:
Jeśli gazy zawierają ok. 2 % obj. H
2
O i
około 0.1 % SO
2
to z bilansu molowego
wynika, że przy całkowitej konwersji SO
2
do
SO
3
i całkowitej absorpcji zarówno trójtlenku
siarki
i wody produkowany kwas może mieć
stężenie najwyżej ok. 23 % wag. Jest to
bardzo korozyjny kwas, który w istocie
musi być traktowany tylko jako kłopotliwy
odpad.

Czy jest na to rada?
• Tak!
trzeba tworzyć kwas w procesie,
w którym nie cała woda przechodzi do fazy
ciekłej. W takim procesie „niepotrzebna”
część H
2
O opuści instalację jako para
kominem, a nie przejdzie do produkowanego
kwasu.
• Procesem, który spełnia ten postulat jest
proces kondensacji H
2
SO
4
w temperaturach wyższych, niż normalnie
pracuje absorpcja.
Procesy z kondensacją kwasu
siarkowego
Stosowane są następujące rozwiązania:
procesy z niską temperaturą kondensacji
(zwykle około 140°C)
procesy z wysoką temperaturą kondensacji
(zwykle około 200°C)
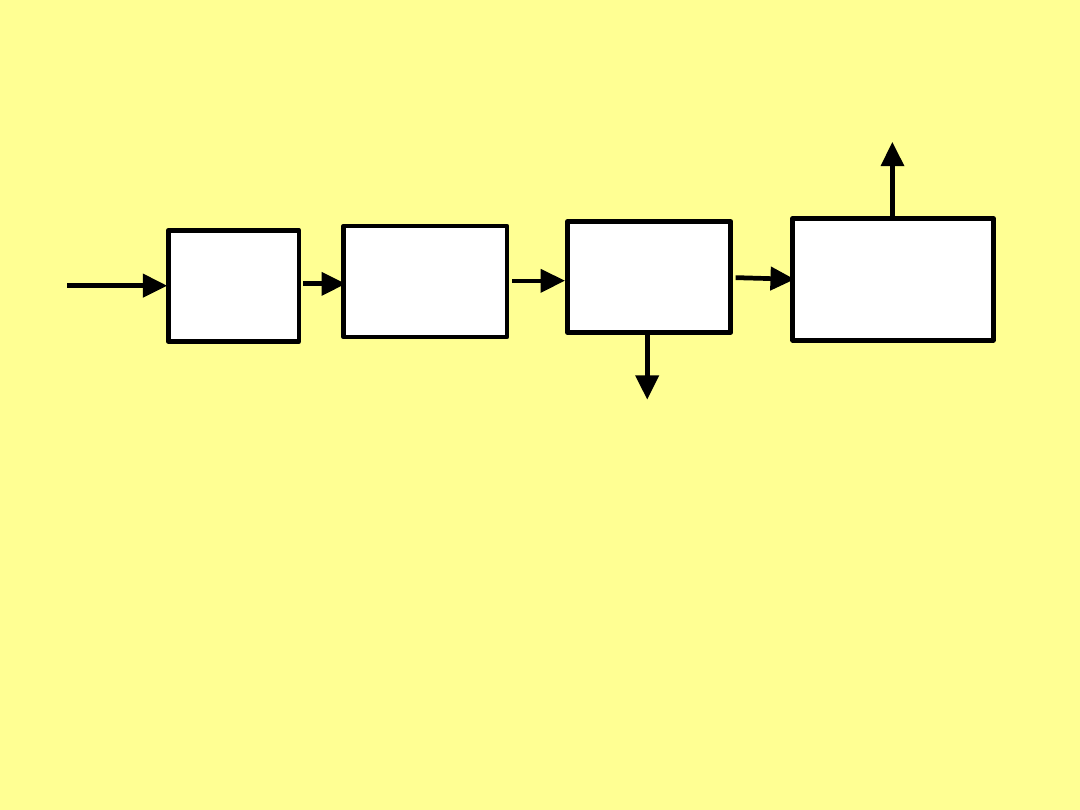
Odpylanie
Katalityczne
utlenianie
SO
2
do SO
3
Kondensacja
H
2
SO
4
Ewentualne
oczyszczanie
(odemglanie)
końcowe
gaz przed
odsiarczaniem
Handlowy kwas siarkowy
gaz
odsiarczony
Schemat blokowy katalitycznego odsiarczania z kondensacją kwasu siarkowego
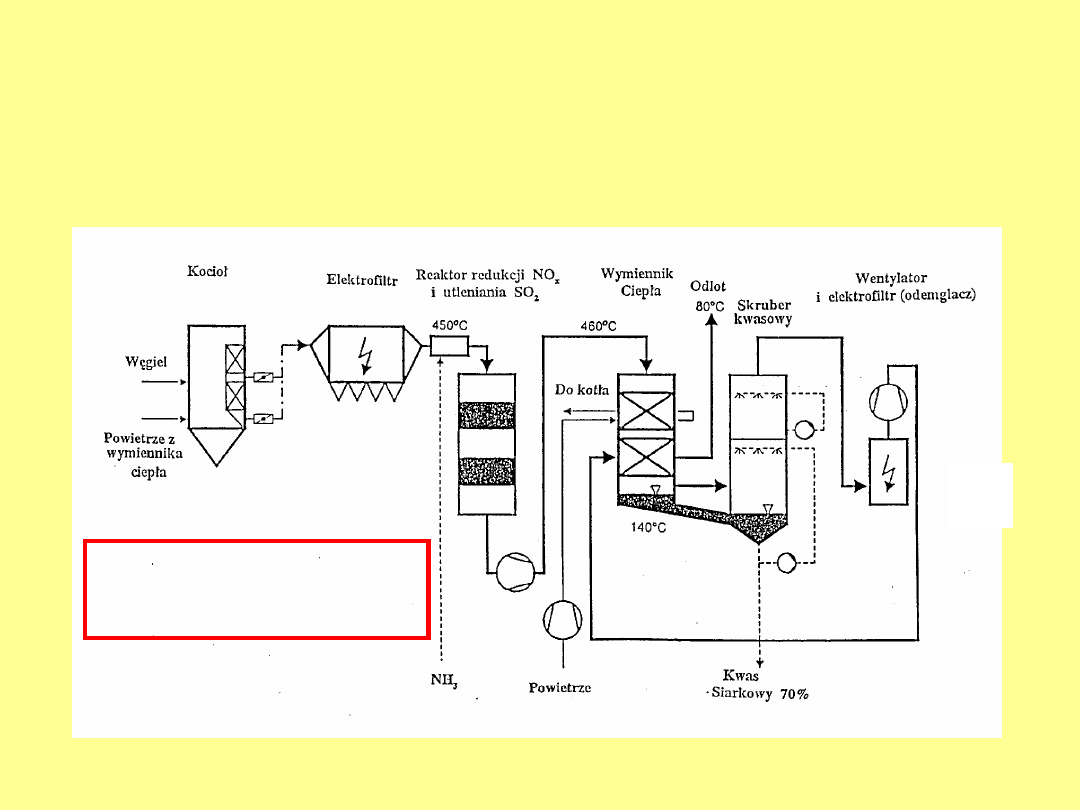
Schemat technologiczny procesu
katalitycznego odsiarczania (i usuwania NO
x
)
z niską temperaturą kondensacji ok.
140
o
C
(firmy Lurgi)
Produkuje kwas
ok. 70% wag.
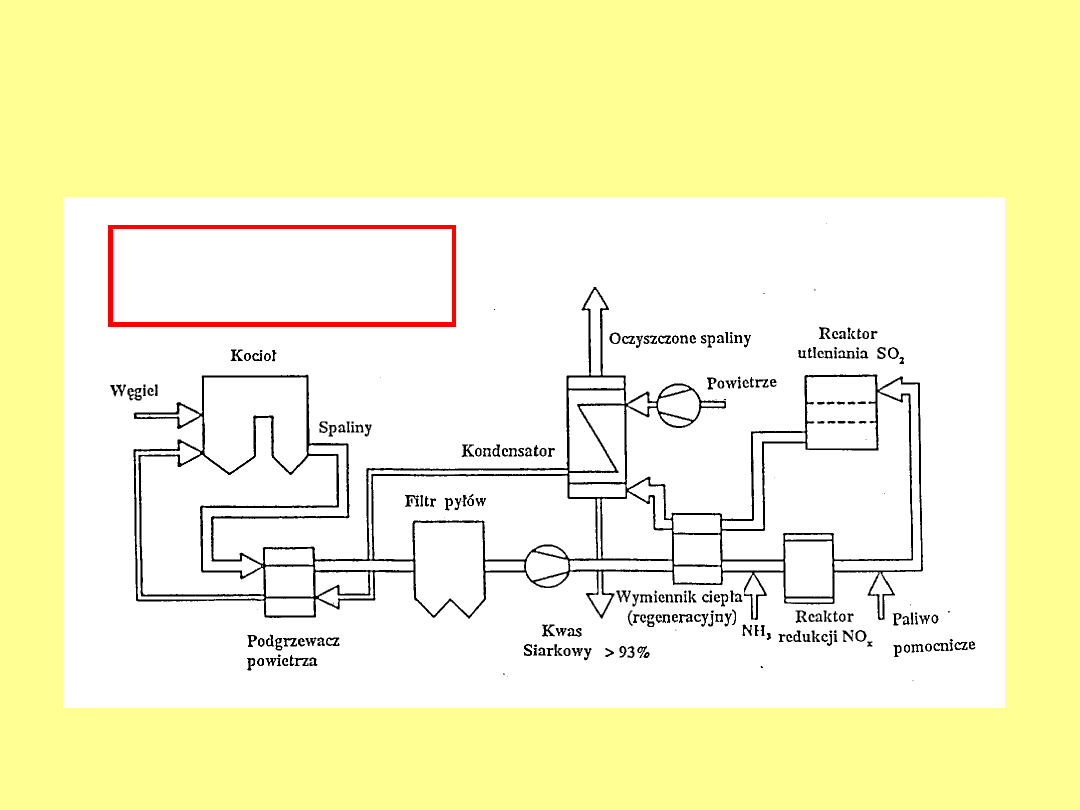
Schemat technologiczny procesu
katalitycznego odsiarczania (i usuwania NO
x
)
z wysoką temperaturą kondensacji
ok.
200
o
C
(firmy Haldor Topsoe)
Produkuje kwas
> 93% wag.
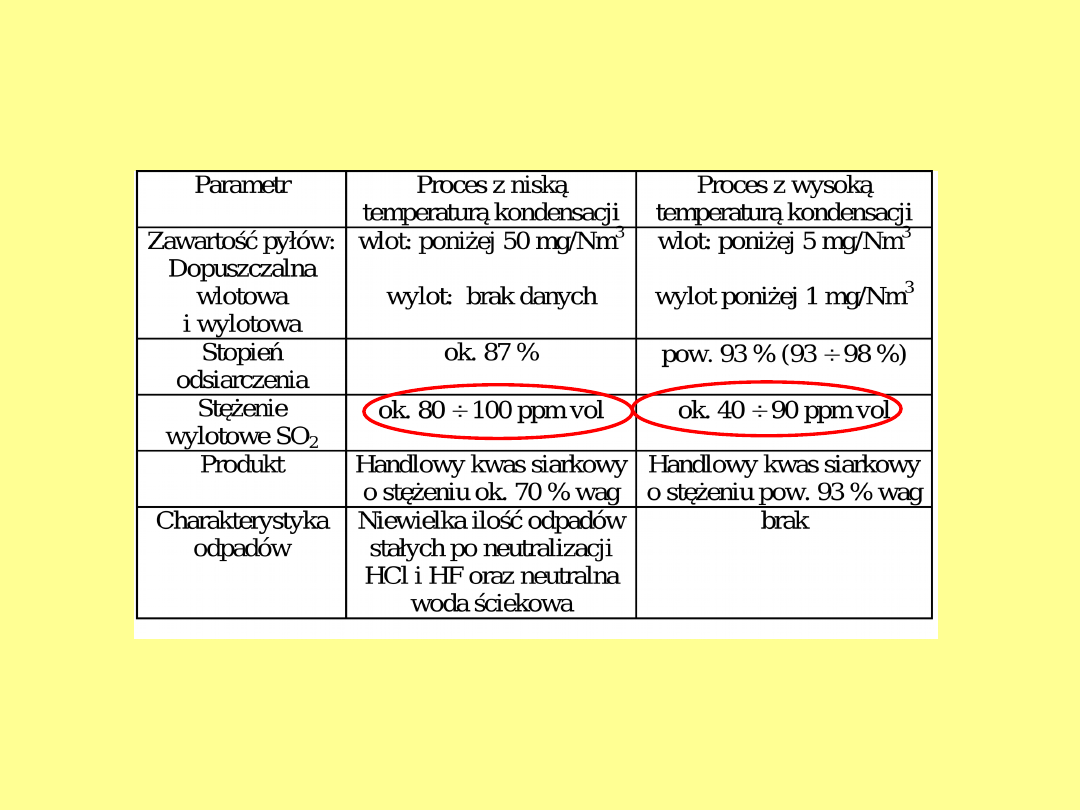
Porównanie parametrów dwu wariantów
odsiarczania katalitycznego dla spalin
energetycznych.
Procesy z kondensacją są stosowane dla
słabych
gazów
metalurgicznych
i
koksowniczych. Dla spalin energetycznych jest
na świecie tylko kilka zastosowań.

Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
Wyszukiwarka
Podobne podstrony:
Wykład 5 OCHRONA ATMOSFERY
Wykład 6 OCHRONA ATMOSFERY
Wykład 1 OCHRONA ATMOSFERY
Wykład 2 OCHRONA ATMOSFERY
Wykład 9 OCHRONA ATMOSFERY
Wykład 4 OCHRONA ATMOSFERY
Wykład 3 OCHRONA ATMOSFERY
Wykład 7 OCHRONA ATMOSFERY
Wykład 14 OCHRONA ATMOSFERY
Wykład 10 OCHRONA ATMOSFERY
Wykład 13 OCHRONA ATMOSFERY
Wykład 12 OCHRONA ATMOSFERY
Wykład 11 OCHRONA ATMOSFERY
ochrona atmosfery zadania
technologie bioenergetyczne wykłady, Ochrona Środowiska, Technologie bioenergetyczne
Wyklad 6, ochrona środowiska
Kopia Rybactwo - wyklady, Ochrona środowiska, semestr 2
Chemizacja srodkow zywienia - wyklady, Ochrona środowiska, semestr 2
więcej podobnych podstron