
PRZEMIANA
NUKLEOTYDÓW
PIRYMIDYNOWYCH

Lokalizacja procesów
Prekursor biosyntezy pirymidyn-
karbamoilofosforan syntezowany
jest w cytozolu.
Ten sam związek służący do
syntezy mocznika powstaje w
mitochondriach.
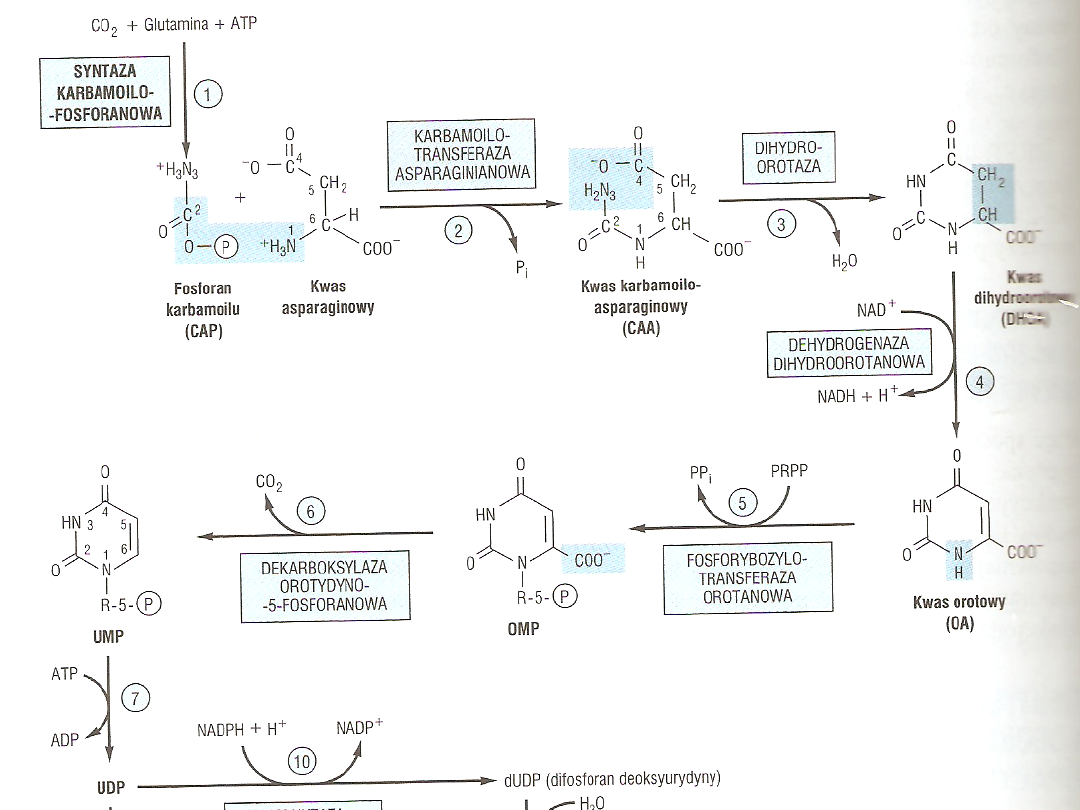

Biosynteza pirymidyn
Enzymy 1,2,3 są połączone w
wielofunkcyjny enzym CAD
Enzymy 5,6 również występują w
formie zasocjowanej
Korzyści:
Koordynacja syntezy enzymów
Minimalizacja reakcji ubocznych
Stabilność zasocjowanych
enzymów

Przekształcenia
mono-, di-,trifosforanów
UMP-> UDP->UTP dzięki obecności
ATP i enzymu- kinazy
UTP-> CTP (syntaza CTP)
Reakcja 10-synteza 2’-
deoksyrybonukleotydów
Metotreksat- inhibitor reduktazy
dihydrofolianowej (reakcja12), jest
używany do leczenia nowotworów.
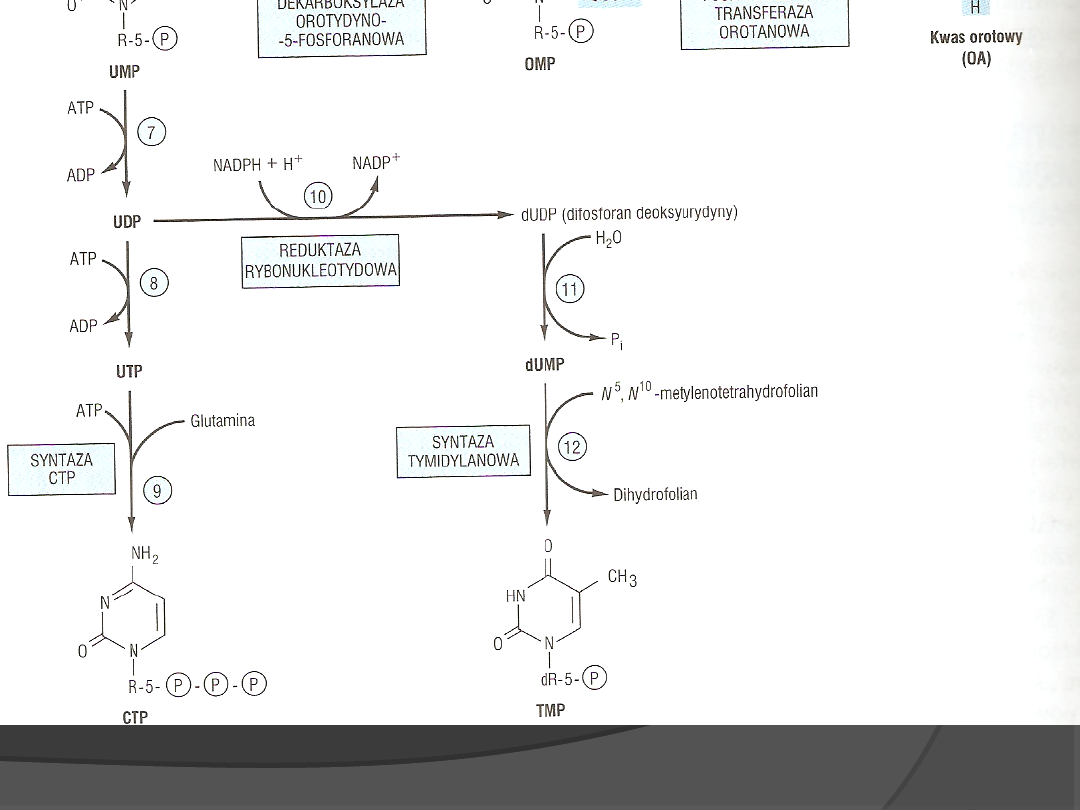

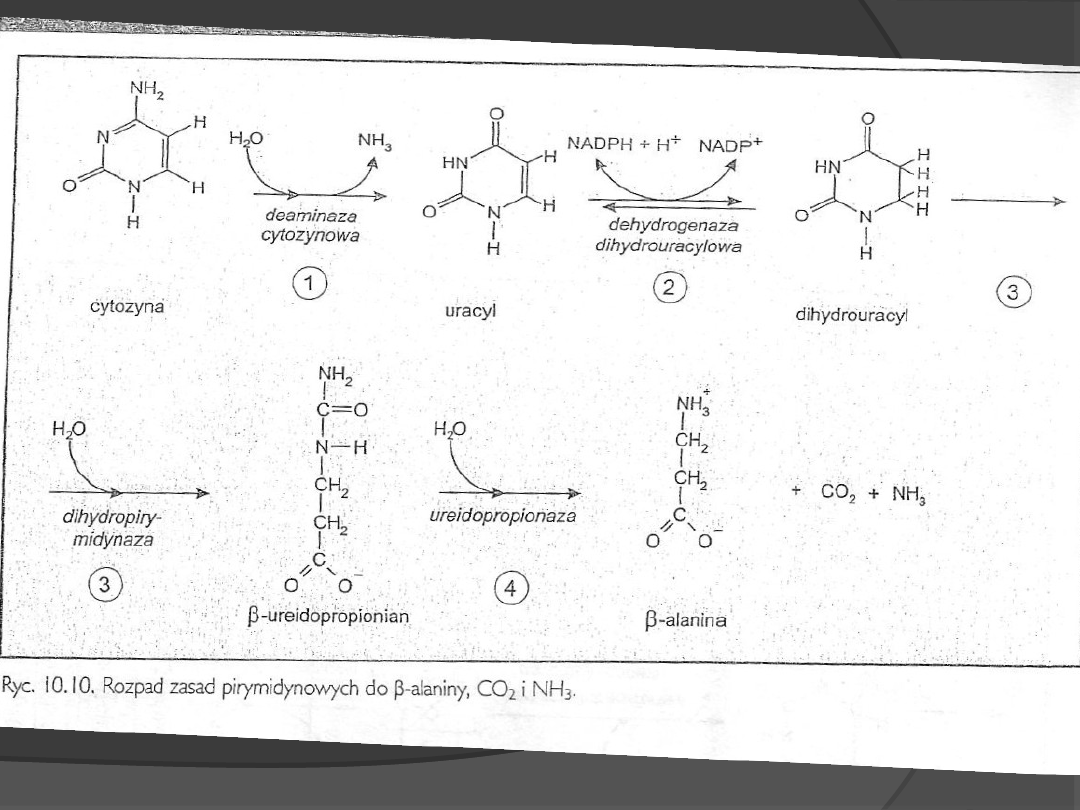
Degradacja pirymidyn
Cytozyna i uracyl- rozkład tym
samym szlakiem.
Rozpad tyminy tym samym
szlakiem, produkt końcowy: β-
aminoizomaślan
Komórki ssaków zużywają niewielką
ilość pirymidyn

Regulacja
Enzym 1- hamowana UTP i
nukleotydami purynowymi, akt.
PRPP.
Enzym 2- hamowana CTP, akt. ATP.
Kompleks enzymów 1,2,3 oraz 5,6
regulowane na poziomie
genetycznym represją lub
derepresją.
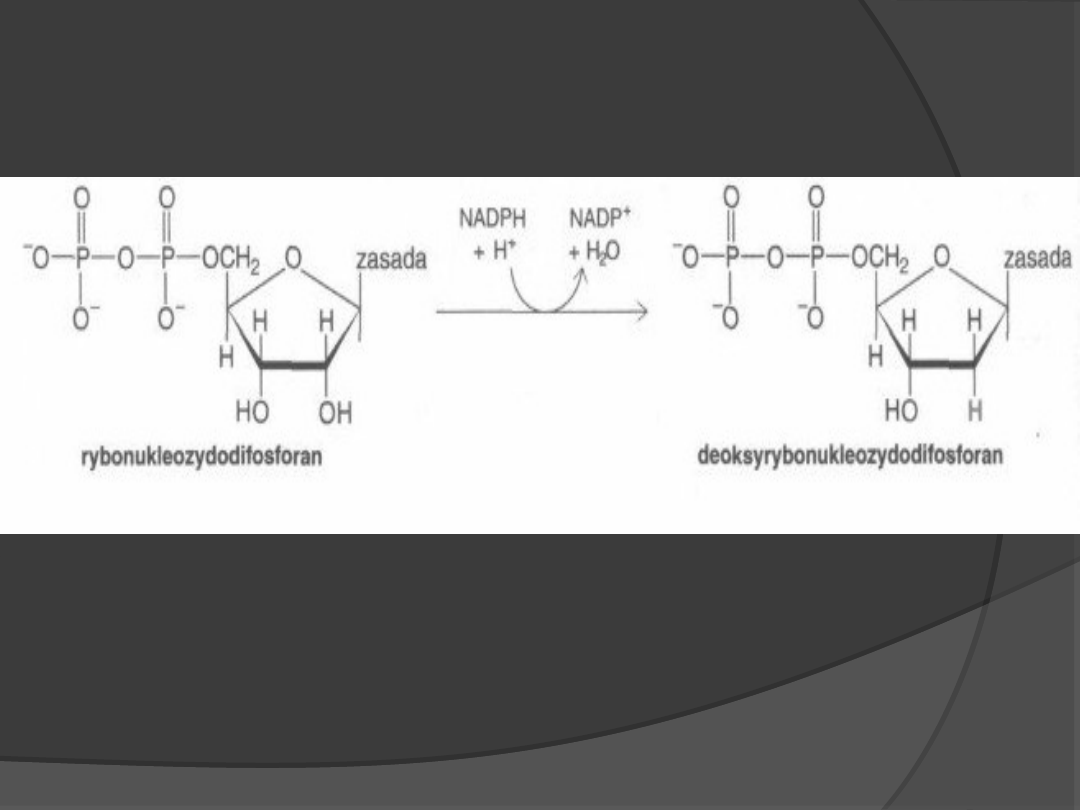
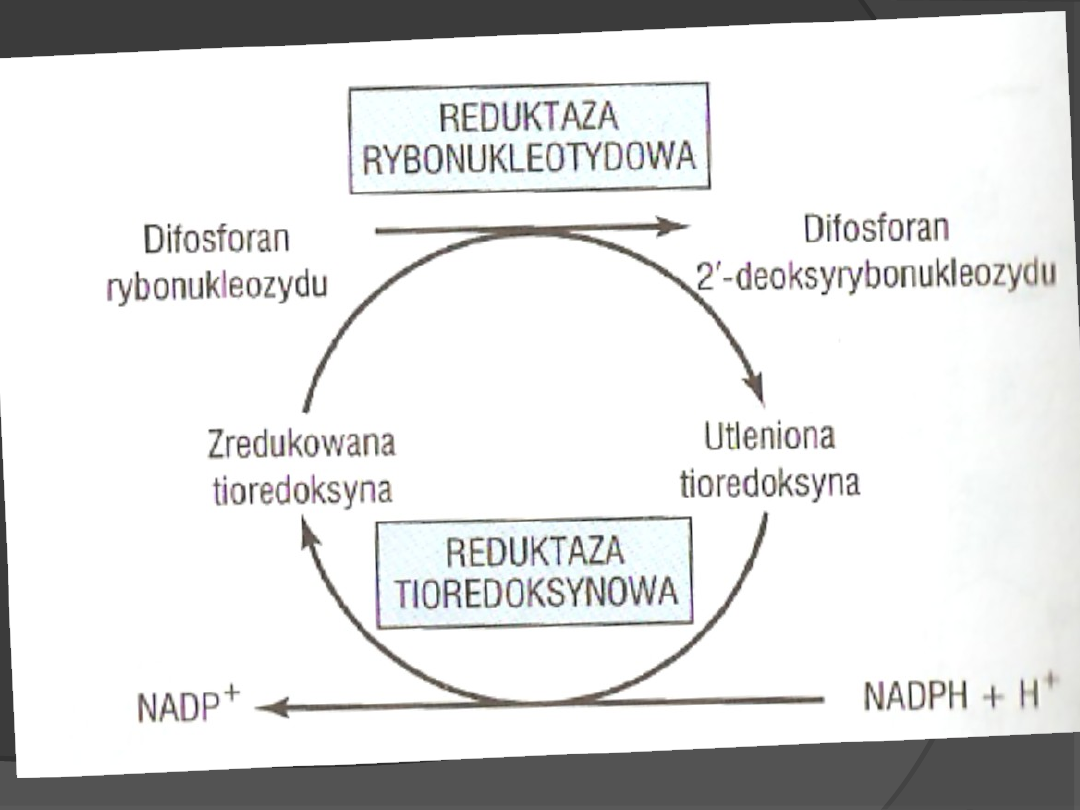
Synteza 2-
deoksyrybonukleotydów
Enzym: reduktaza
rybonukleotydowa
Wymaga: tioredoksyna
(flawoproteina)
reduktazy t. (kolfaktor białkowy)
NADPH
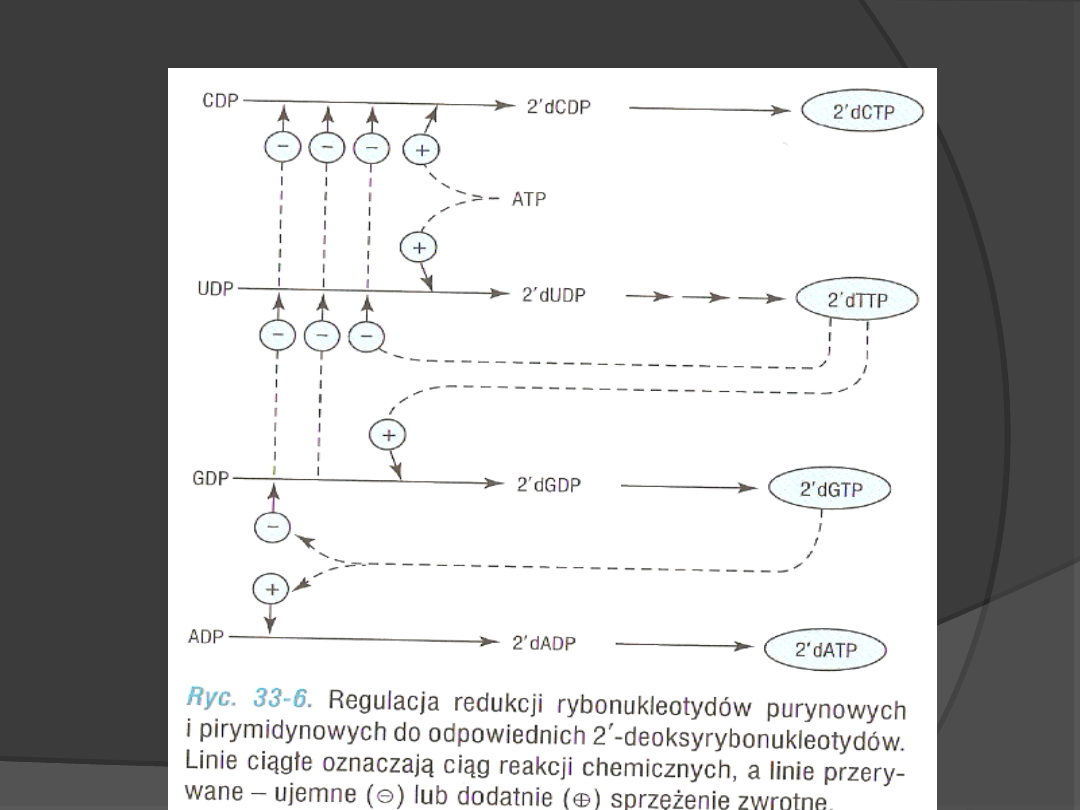
Regulacja
Document Outline
- Slide 1
- Lokalizacja procesów
- Slide 3
- Biosynteza pirymidyn
- Przekształcenia mono-, di-,trifosforanów
- Slide 6
- Degradacja pirymidyn
- Slide 8
- Regulacja
- Synteza 2-deoksyrybonukleotydów
- Slide 11
- Regulacja
Wyszukiwarka
Podobne podstrony:
Przemiany zasad pirymidynowych i zaburzenia przemiany nukleotydów
Biosynteza nukleotydów pirymidynowych
Przemiana nukleotydów purynowych
Zagrozenia zwiazane z przemieszczaniem sie ludzi
Pirymidyny 2003
3 Przemiany fazowe w stopach żelazaPrzemiana martenzytycznaSem2010
przemiennik 1
Przemienienie Jezusa
aldehydy i ketony addycja nukleofilowa
pirymidyny 2003
Przemiany aminokwasów w biologicznie ważne, wyspecjalizowane produkty
lato wedlug pieciu przemian fr
Czujniki przemieszczeń kątowych
cykliczne nukleotydy
PrzemianyPolityczne Sprawdzian TylkoGeografia
ćw 2 Pomiary przemieszczeń liniowych i grubości
Boże Narodzenie według Pięciu Przemian przepisy kulinarne
więcej podobnych podstron