
Przemiana
nukleotydów
purynowych
lokalizacja procesów,
degradacja puryn w wątrobie,
synteza nukleotydów
purynowych,
odzysk puryn

SYNTEZA
NUKLEOTYD
ÓW
PURYNOWY
CH
Synte
za de
novo
Szlaki
rezerwo
we
Fosforybozyla
cja puryn
Fosforylacj
a
nukleozydó
w
purynowyc
h
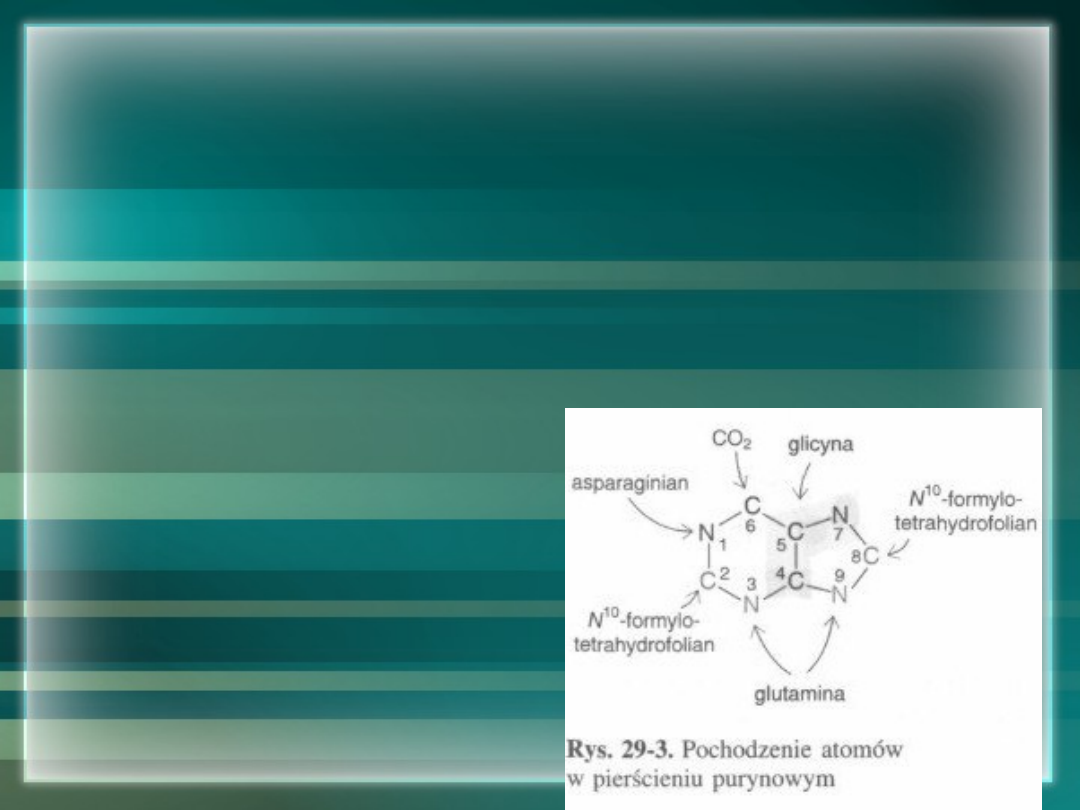
Synteza de novo
• W przeciwieństwie do syntezy
nukleotydów pirydynowych
elementy puryn przyłączane są
stopniowo do pierścienia rybozy
• Głównie w wątrobie
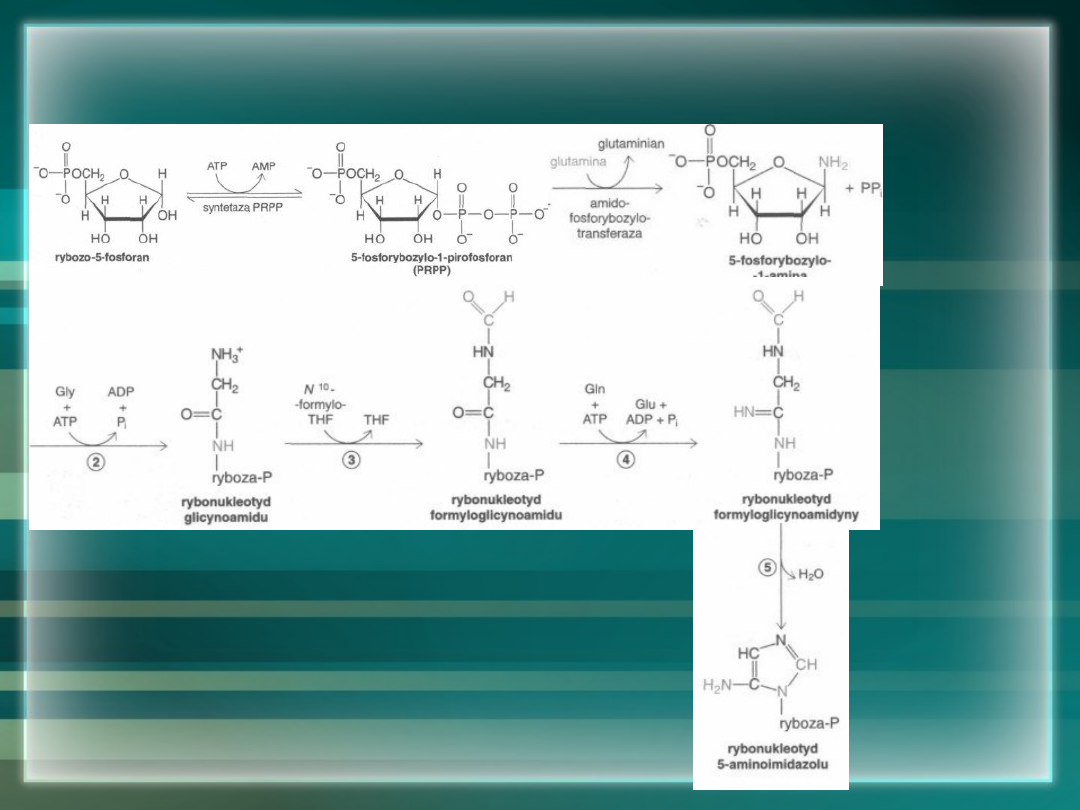
Ogólny schemat
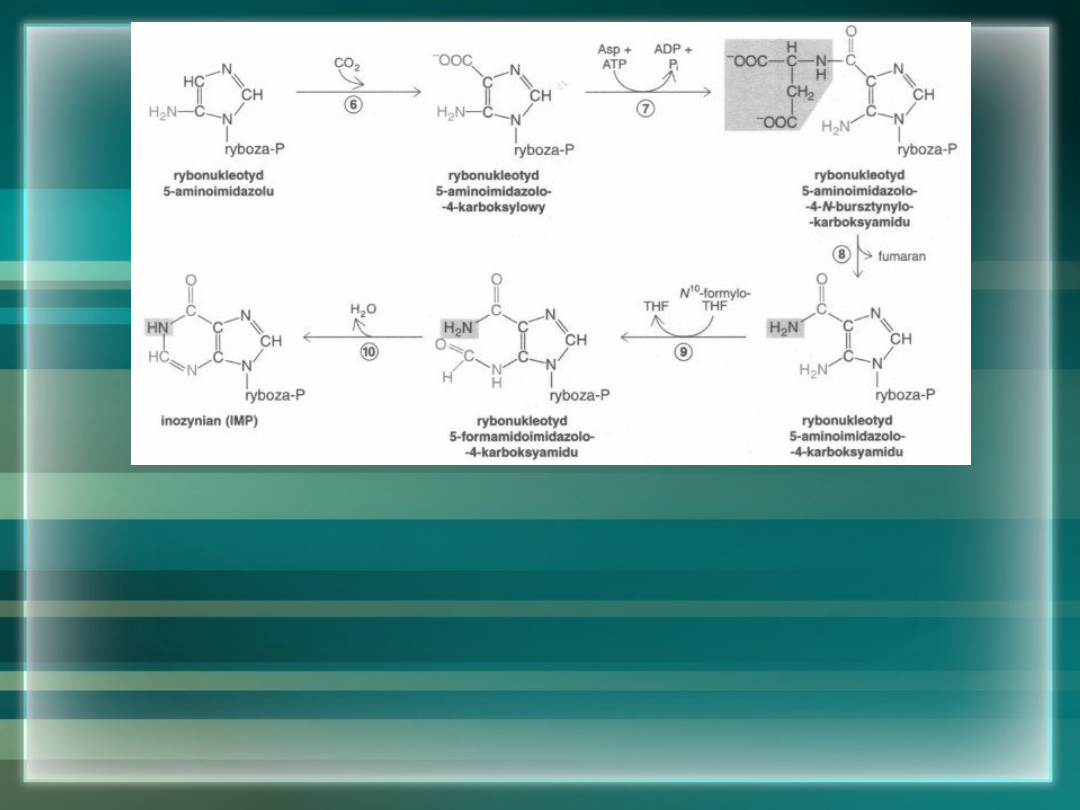
Reakcja po reakcji
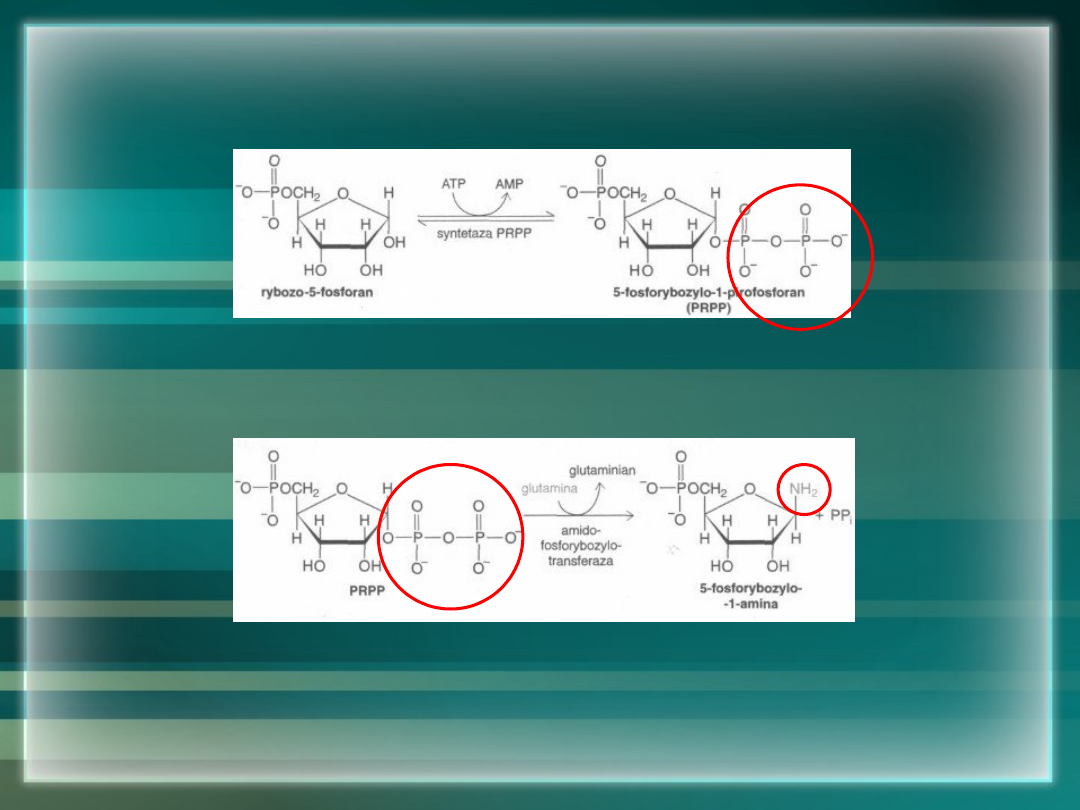
SYNTEZA PRPP Z RYBOZO-5-FOSFORANU
• rybozo-5-fosforan pochodzi z cyklu
pentozofosforanowego
• PRPP bierze udział także w syntezie tryptofanu
WYMIANA PIFOSFORANU NA GRUPĘ AMINOWĄ –
POWSTANIE 5-FOSFORYBOZYLO-1-AMINY
• hamowana przez
diazanorleucynę
•
cysteina na N-końcu enzymu – ułatwia hydrolizę Gln
•
Enzym przyjmuje aktywną konfigurację po
przyłączeniu i PRPP i Gln – ochrona przed
zmarnowaniem subtratów
Mg
2+
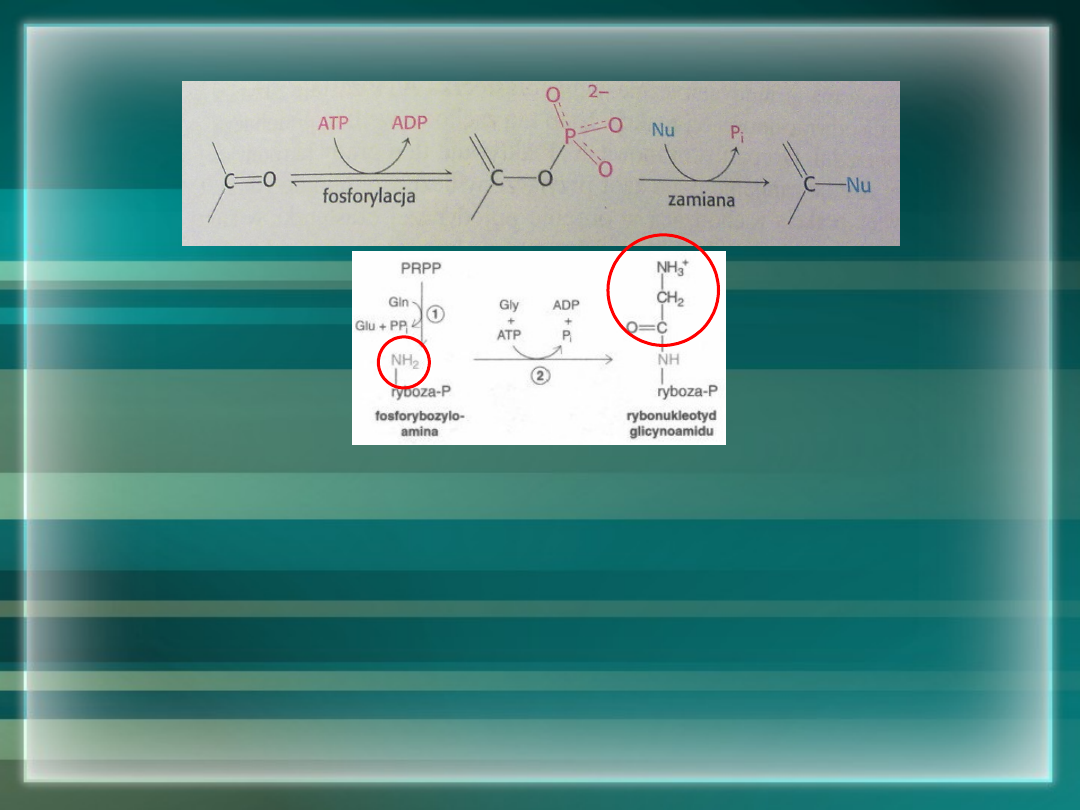
W niektórych reakcjach występuje podobny mechanizm
PRZYŁĄCZENIE GLICYNY DO GRUPY AMINOWEJ
FOSFORYBOZYLOAMINY Z POWSTANIEM RYBONUKLEOTYDU
GLICYNOAMIDU
• grupa karboksylowa glicyny aktywowana przez fosforylację
Mg
2+
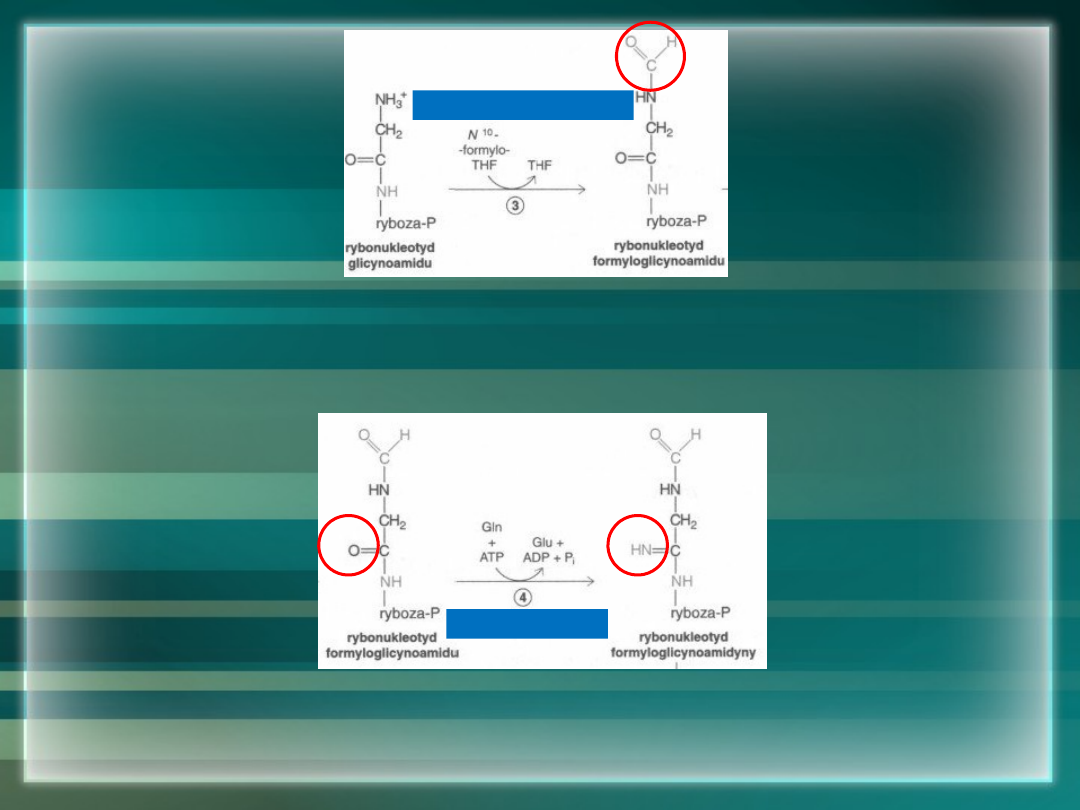
PRZYŁĄCZENIE MRÓWCZANU – POWSTAJE RYBONUKLEOTYD
FORMYLOGLICYNOAMIDU
• donorem jest N
10
– formylotetrahydrofolian
• mrówczan aktywowany do formylofosforanu
FORMYLOTRANFERAZA
PODSTAWIENIE TLENU KARBONYLOWEGO GRUPĄ NH
RYBONUKLEOTYD FORMYLOGLICYNOAMIDYNY
• hamowane przez
azaserynę
VI SYNTETAZA
Mg
2+
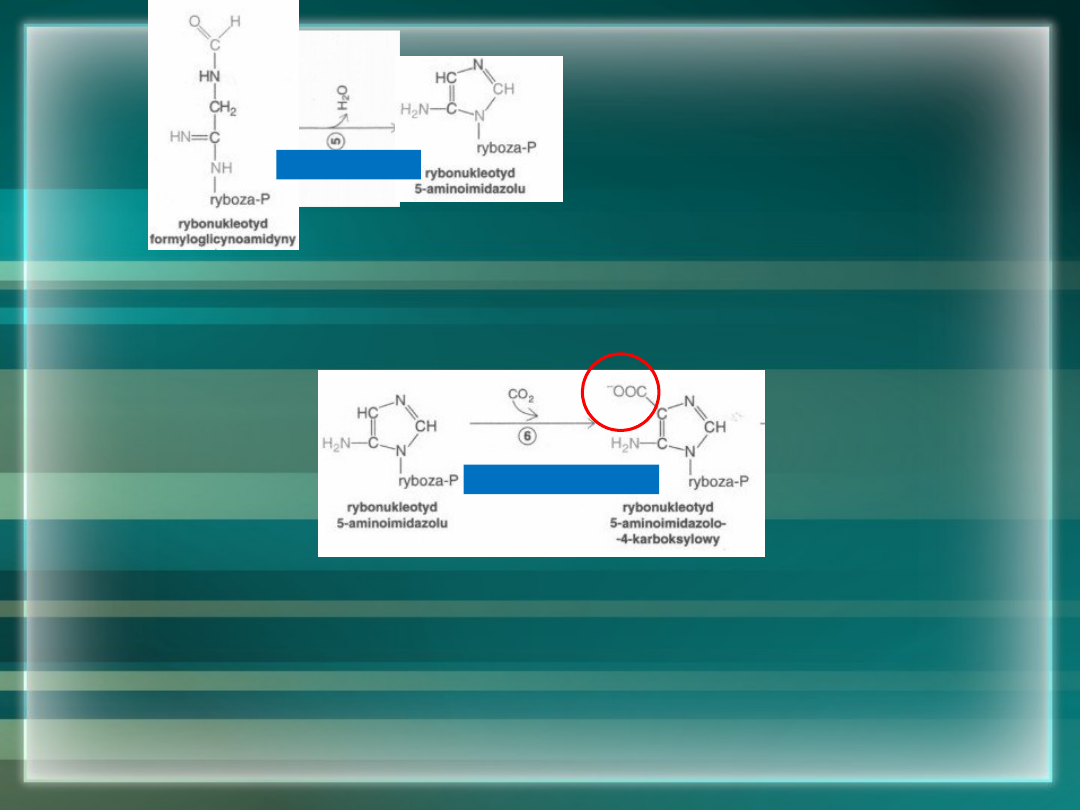
CYKLIZACJA – POWSTAJE RYBONUKLEOTYD 5-
AMINOIMIDAZOLU
• pomimo, że reakcja jest preferowana termodynamicznie to
jedno ATP jest użyte, żeby zablokować odwracalność tej reakcji
VII SYNTETAZA
PRZYŁĄCZENIE JONU WODOROWĘGLANOWEGO – POWSTAJE
RYBONUKLEOTYDU 5-AMINOIMIDAZOLO-4-
KARBOKSYLOWEGO
• jon wodorowęglanowy aktywowany przez fosforylację
Mg
2+
VII KARBOKSYLAZA
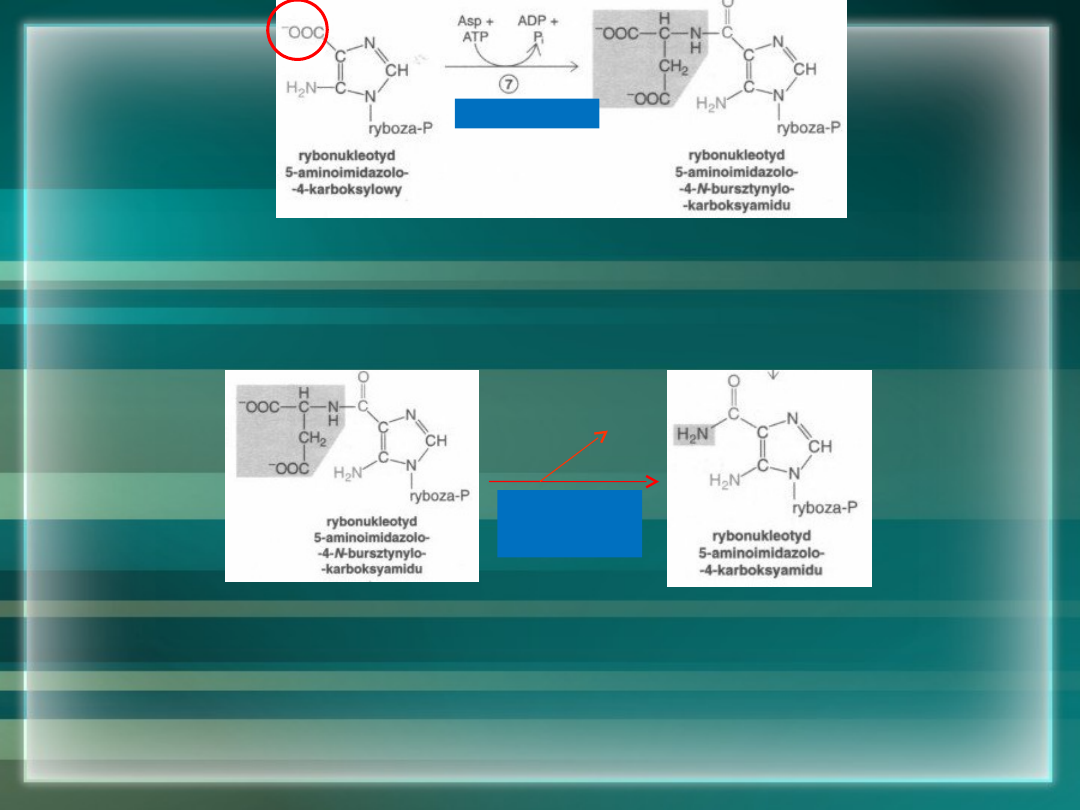
PRZYŁĄCZENIE RESZTY ASN DO GRUPY KARBOKSYLOWEJ IMIDAZOLU
RYBONUKLEOTYD 5-AMINOIMIDAZOLO-4-N-
BURSZTYNYLOKARBOKSYAMIDU
• grupa karboksylowa jest najpierw fosforylowana a powstała grupa
fosforanowa jest zamieniana na grupę aminową asparaginianu
FUMARAN
8
ELIMINACJA FUMARANU Z PRZYŁĄCZONEJ RESZTY ASN RYBONUKLEOTYD
5-AMINOIMIDAZOLO-4-KARBOKSYAMIDU
IXSYNTETAZA
LIAZA
ADENYLOBURS
ZTYNIANOWA
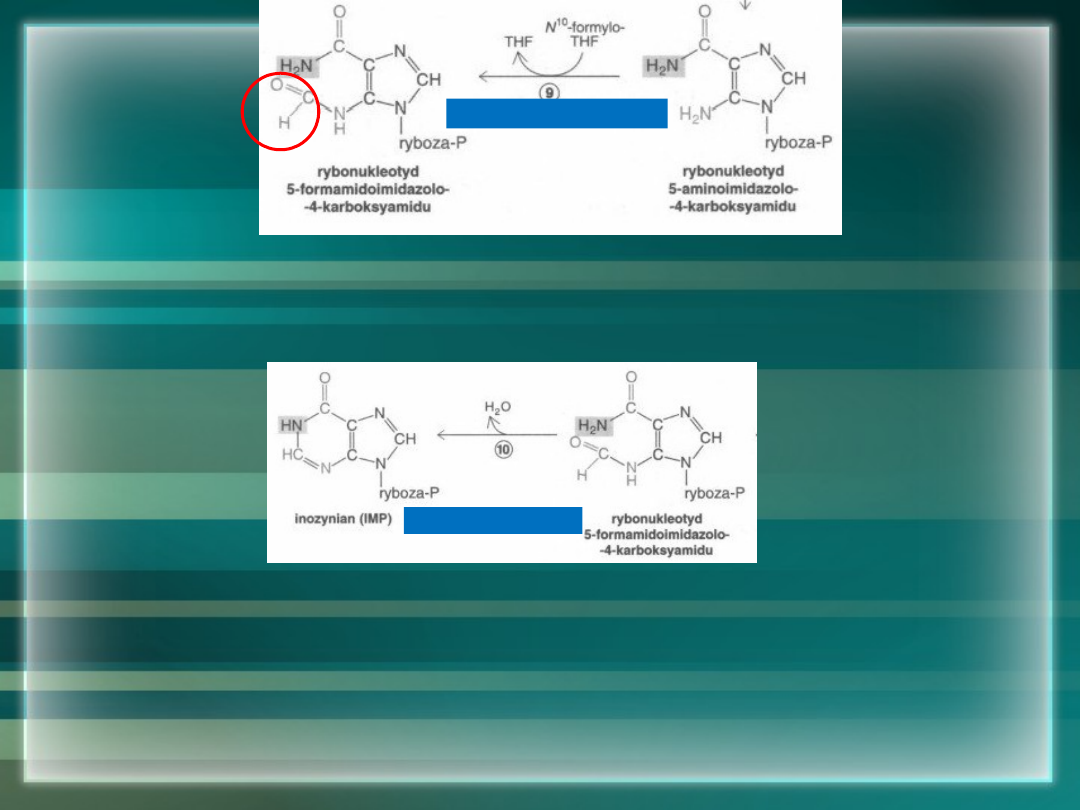
PRZYŁACZENIE GRUPY FORMYLOWEJ RYBONUKLEOTYD
5-FORMAMIDOIMIDAZOLO-4-KARBOKSYAMIDU
• donor – N
10
- formylotetrahydrofolian
CYKLIZACJA POŁACZONA Z UTRATĄ CZĄSTECZKI WODY –
INOZYNIAN (IMP)
FORMYLOTRANFERAZA
CYKLOHYDROLAZA IMP
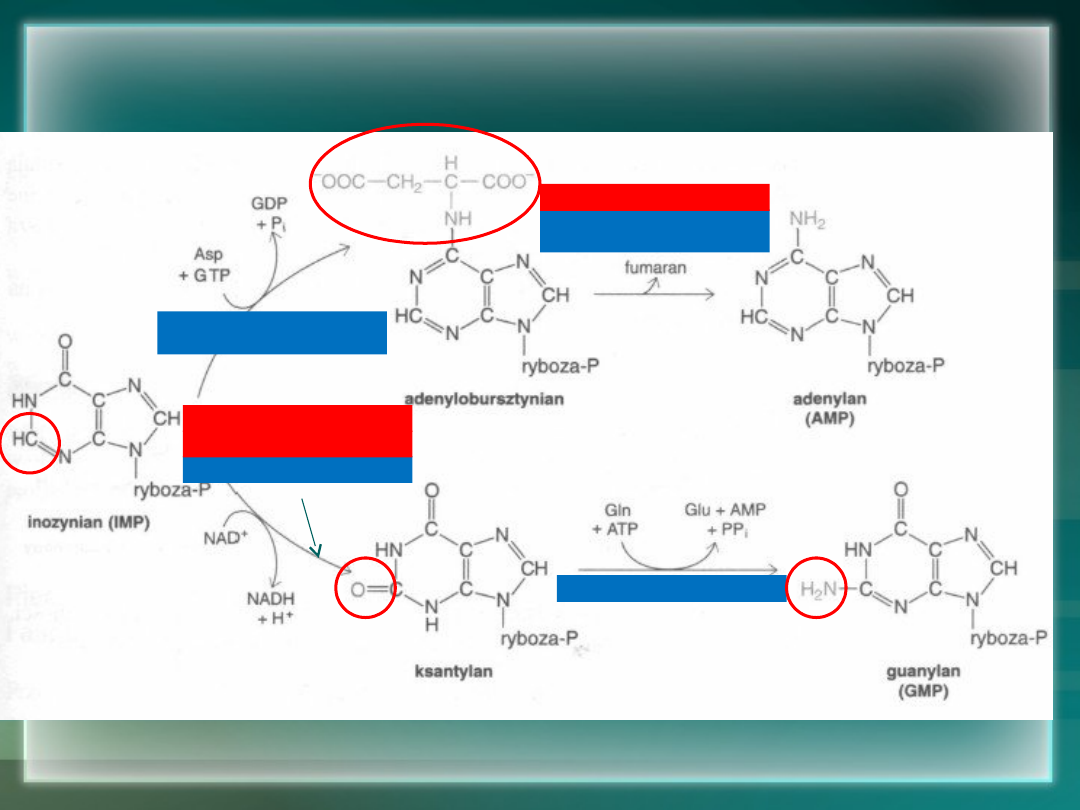
AMP i GMP powstają z IMP
Mg
2+
SYNTAZA
ADENYLOBURSZTYNIANOWA
LIAZA
ADENYLOBURSZTYNIANOWA
H
2
O
TRANSAMIDYNAZA
(-) 6-MERKAPTOPURYNA
DEHYDROGENAZA IMP
(-) 6-MERKAPTOPURYNA
(-)KWAS MYKOFENOLOWY

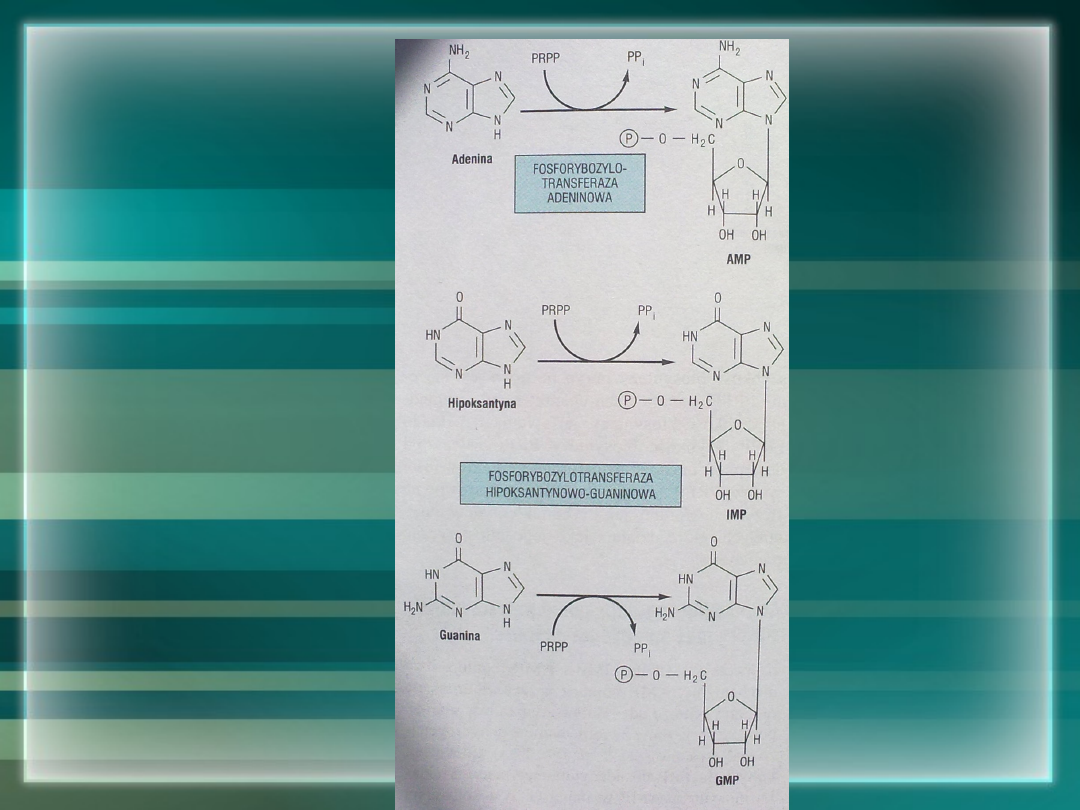
Szlaki rezerwowe (ang.
salvage reactions)
• Wymagają dużo mniej energii niż
synteza de novo
• Ilościowo najważniejsza jest
fosforybozylacja wolnej puryny:
– Puryna + PR-PP Puryna-PR + PP
i
• Drugi mechanizm reutylizacji to
fosforylacja rybonukleozydu
przez ATP:
– PuR + ATP PuR-P + ADP

• Wątroba, jako główne miejsce
syntezy nukleotydów purynowych
dostarcza puryny i ich nukleozydy
do reakcji rezerwowych i
zużywania w tkankach, które nie
mają zdolności do ich biosyntezy:
– W mózgu małe stężenie
amidotransferazy glutamylo-PRPP
– Erytrocyty i leukocyty nie mogą
syntetyzować 5-fosforybozyloaminy
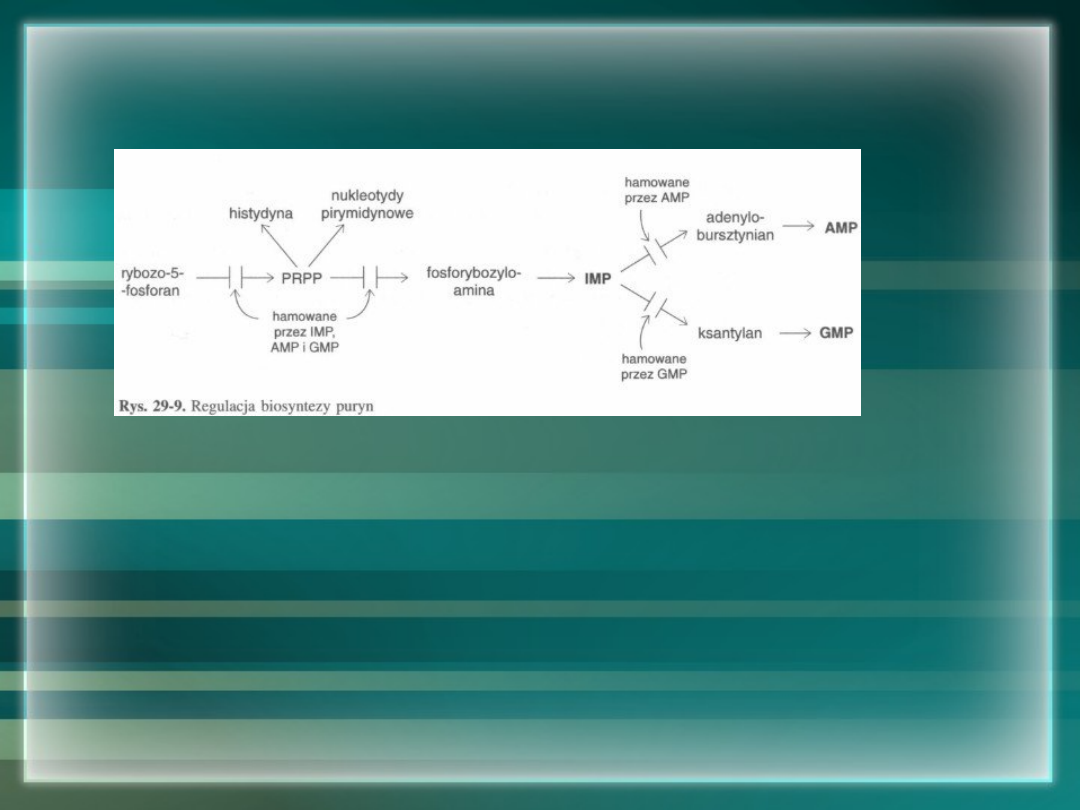
Regulacja syntezy puryn
• przez sprzężenie zwrotne
• główny czynnik regulujący – stężenie PRPP zależne od:
• dostępności rybozo-5-fosforanu
• aktywności syntazy PRPP
• GTP jest substratem wykorzystywanym do syntezy AMP, ATP do
GMP – wzajemna zależność substratowa zapewniająca
zachowanie równowagi pomiędzy syntezą nukleotydów
adeninowych a guaninowych
1
2
3
4

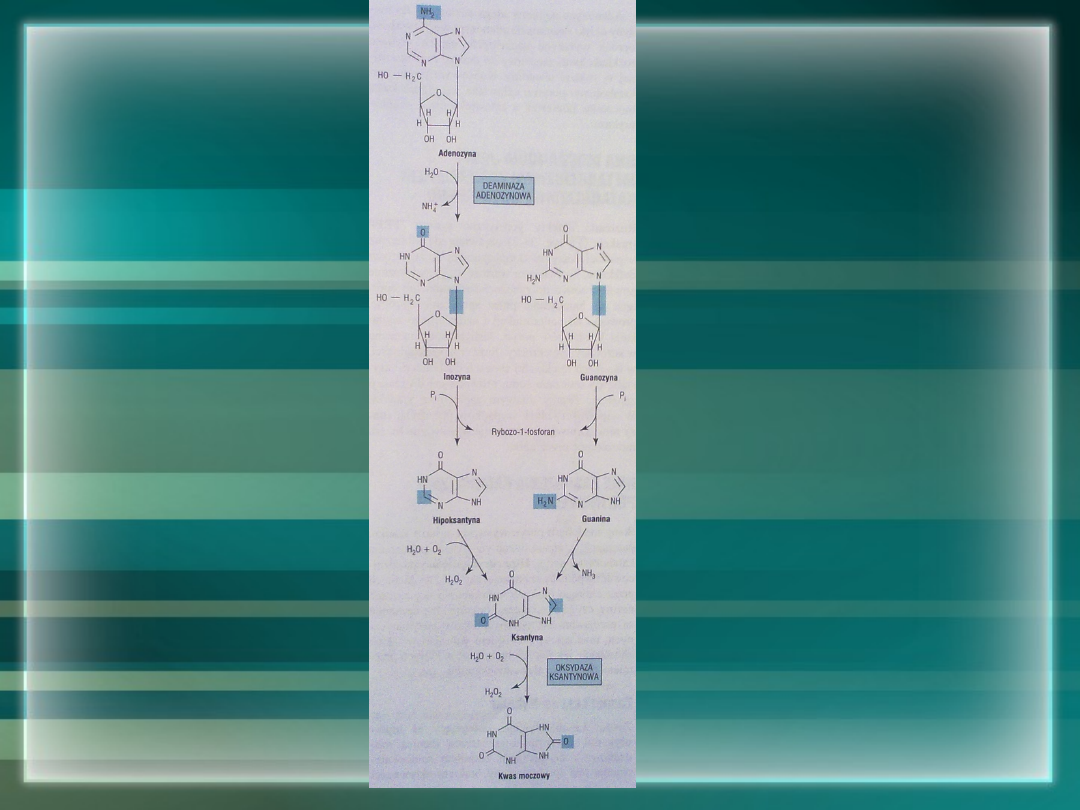
Katabolizm puryn
• Puryny katabolizowane są do kwasu
moczowego (moczanu)
• Kwasy nukleinowe w przewodzie
pokarmowym rozkładane są przez
rybonukleazy, deoksyrybonukleazy i
polinukleotydazy do mononukleotydów
• Mononukleotydy są hydrolizowane do
nukleozydów przez nukleotydazy i
fosfatazy
• Te ulegają wchłonięciu lub są
rozkładane przez fosforylazy jelitowe
do zasad purynowych i
pirymidynowych

Zaburzenia
przemiany
nukleotydów

Dna (skaza) moczanowa
• Defekty genetyczne syntazy PRPP
(zwiększenie aktywności)
• Nadprodukcja i nadmierne
wydalanie katabolitów puryn
• Gdy poziom moczanu w surowicy
przekroczy limit rozpuszczalności,
w tkankach miękkich i stawach
dochodzi do krystalizacji moczanu
sodureakcja zapalnadnawe
zapalenie stawów

Hiperurykemie
• ZESPÓŁ LESCHA-NYHANA
– Brak aktywności
fosforybozylotransferazy
hipoksantynowo-guaninowej
– PRPPnadmierne wytwarzanie puryn
– Hiperurykemia z często towarzyszącą
kamicą moczanową
• CHOROBA VON GIERKEGO
– Nadmierne wytwarzanie puryn i
hiperurykemia – proces wtórny
– Wzmożona generacja rybozo-5-fosforanu
(prekursora PRPP)
– Niedobór
glukozo-6-fosfatazy

Hipourykemia
• Hipourykemia i zwiększone
wydalanie hipoksantyny i
ksantyny
• Niedobór
oksydazy ksantynowej
• Defekt genetyczny lub silne
uszkodzenie wątroby
• W ciężkim zespole niedoboru
ksantynuria i kamica
ksantynowa

• DEFICYT DEAMINAZY
ADENOZYNOWEJ
– Towarzyszy mu ciężki, złożony
deficyt immunologiczny
– Limfocyty T i B nieliczne i
niefunkcjonalne
• DEFICYT FOSFORYLAZY
NUKLEOZYDU PURYNOWEGO
– Towarzyszy mu ciężki deficyt
limfocytów T z pozornie normalną
funkcją limfocytów B

Zaburzenia przemiany
pirymidyn
• Końcowe produkty metabolizmu są
dobrze rozpuszczalne w wodziemało
widocznych zaburzeń
• W hiperurykemi związanej z PRPP
nadmierne wytwarzanie n.
pirymidynowych i wydalanie β-alaniny
• OROTOACYDURIA
– Towarzyszy zespołowi Reye’a
– Zjawisko wtórne – niezdolność
uszkodzonych mitochondriów do
zużywania karbamoilofosforanu nadmiar
kwasu orotowego

• DEFICYT ENZYMÓW W CYKLU
MOCZNIKOWYM
– Niedobór wątrobowej
ornitynotranskarbamoilazy mitochondrialnej
– Niewykorzystany do końca karbamoilofosforan
pojawia się w cytoplaźmiestymulacja syntezy
n. pirymidynowych
– Po zjedzeniu produktu o wysokiej zawartości
azotu pojawia się lekka orotoacyduria
• Analog puryny – allopurinol
współzawodniczy z kwasem orotowym o
fosforybozylację fosforybozylotransferazą
orotanową powodując orotoacydurię i
orotidynurię
• 6-azaurydyna ulegając konwersji do 6-
azaurydylanu, kompetycyjnie hamuje
dekarboksylazę orotydynalanu -
wydalanie kwasu orotowego i orotydyny
Document Outline
- Slide 1
- Slide 2
- Synteza de novo
- Ogólny schemat
- Slide 5
- Reakcja po reakcji
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- AMP i GMP powstają z IMP
- Szlaki rezerwowe (ang. salvage reactions)
- Slide 14
- Slide 15
- Regulacja syntezy puryn
- Katabolizm puryn
- Slide 18
- Slide 19
- Dna (skaza) moczanowa
- Hiperurykemie
- Hipourykemia
- Slide 23
- Zaburzenia przemiany pirymidyn
- Slide 25
Wyszukiwarka
Podobne podstrony:
BIOSYNTEZA NUKLEOTYDÓW PURYNOWYCH
Przemiany zasad pirymidynowych i zaburzenia przemiany nukleotydów
Przemiana nukleotydów pirymidynowych
Zagrozenia zwiazane z przemieszczaniem sie ludzi
3 Przemiany fazowe w stopach żelazaPrzemiana martenzytycznaSem2010
przemiennik 1
Przemienienie Jezusa
aldehydy i ketony addycja nukleofilowa
Przemiany aminokwasów w biologicznie ważne, wyspecjalizowane produkty
lato wedlug pieciu przemian fr
Czujniki przemieszczeń kątowych
cykliczne nukleotydy
PrzemianyPolityczne Sprawdzian TylkoGeografia
ćw 2 Pomiary przemieszczeń liniowych i grubości
Boże Narodzenie według Pięciu Przemian przepisy kulinarne
całość materiału test przemiany demograficzne
więcej podobnych podstron