
KOLUMNY
CHROMATOGRAFICZNE
Magdalena Bialik
Karina Jeleniewska
Paweł Kalinowski
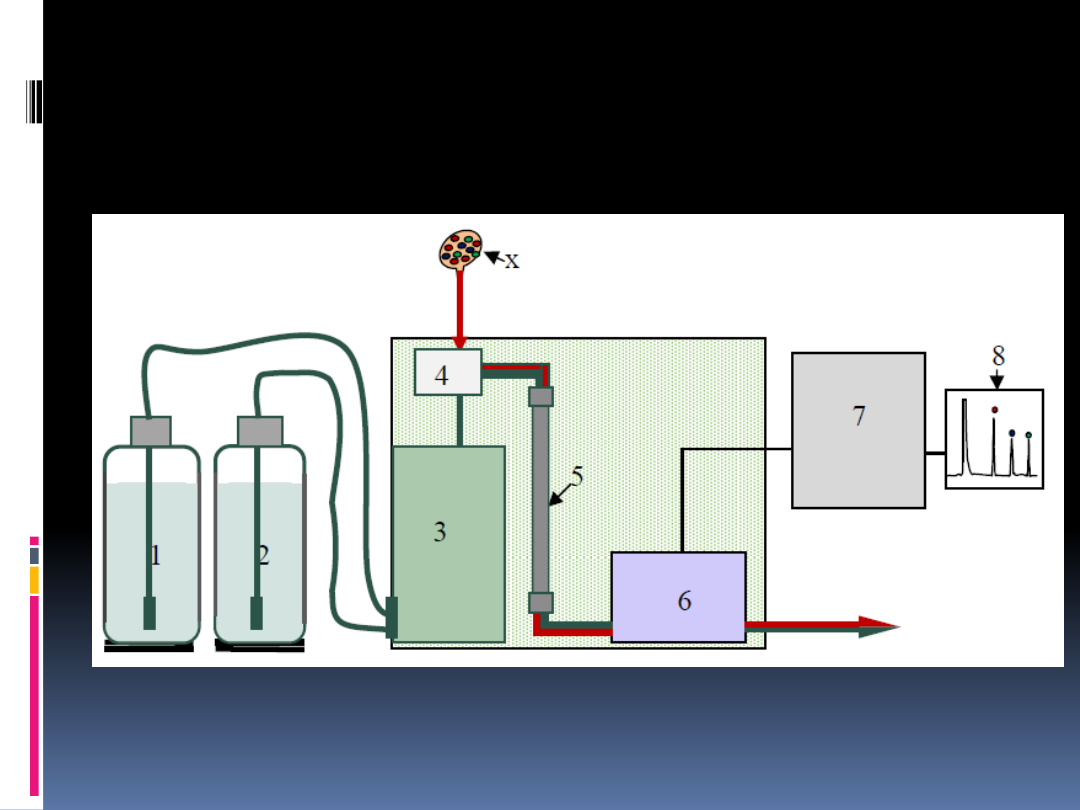

RODZAJE KOLUMN
Mikrokolumny
Kolumny analityczne – stosowane najczęściej
Kolumny preparatywne


Mikrokolumny
Długość 2-2,5cm
Średnica 0,5 –
1mm
Wielkość ziaren 3,
5, 10um

Kolumny analityczne
Długość 5 – 25 cm
Średnica 3 – 5 mm
Wielkość ziaren 3 – 10
um

Kolumny preparatywne
Długość 25 - 100cm
Średnica 1,2- 10cm i
więcej
Wielkość ziaren 10 - 75um

Wypełnienia
Wypełnienia krzemionkowe
Żywice porowate
Wypełnienia krzemionkowe
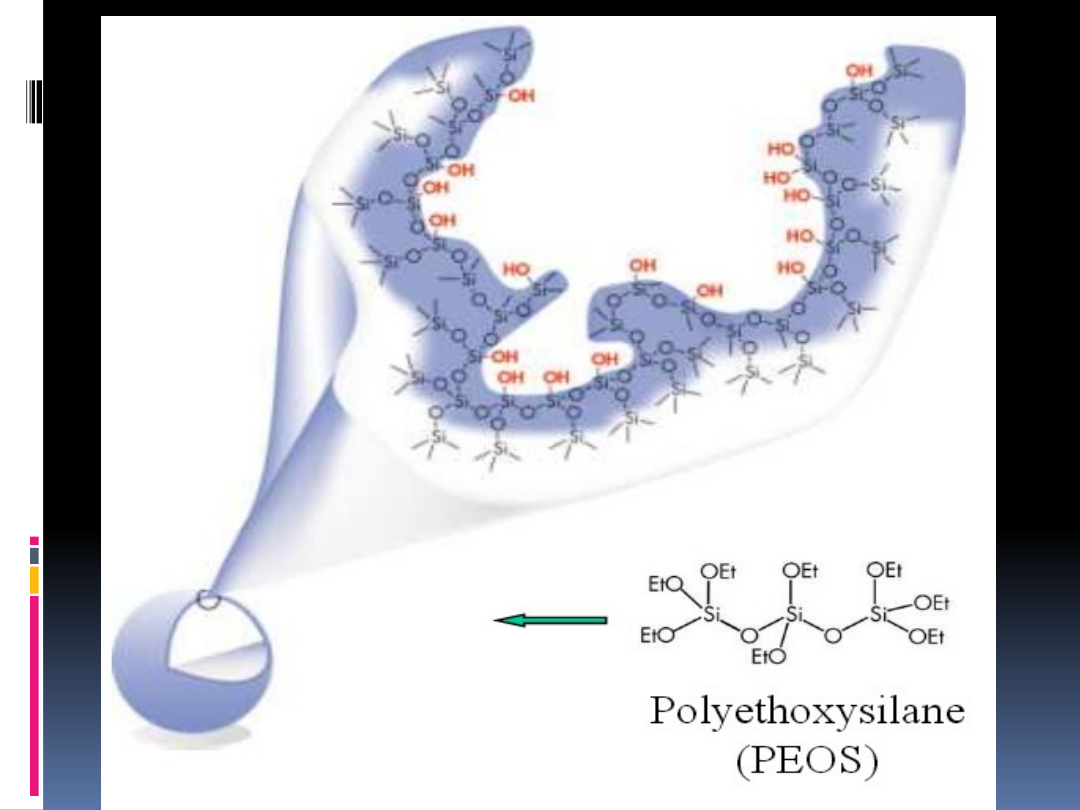
ŻEL KRZEMIONKOWY
Materiał o dużej wytrzymałości mechanicznej,
odpowiednich rozmiarach porów, amorficzny.
Modyfikacja poprzez wiązanie aktywnych grup żelu
krzemionkowego z materiałami organicznymi

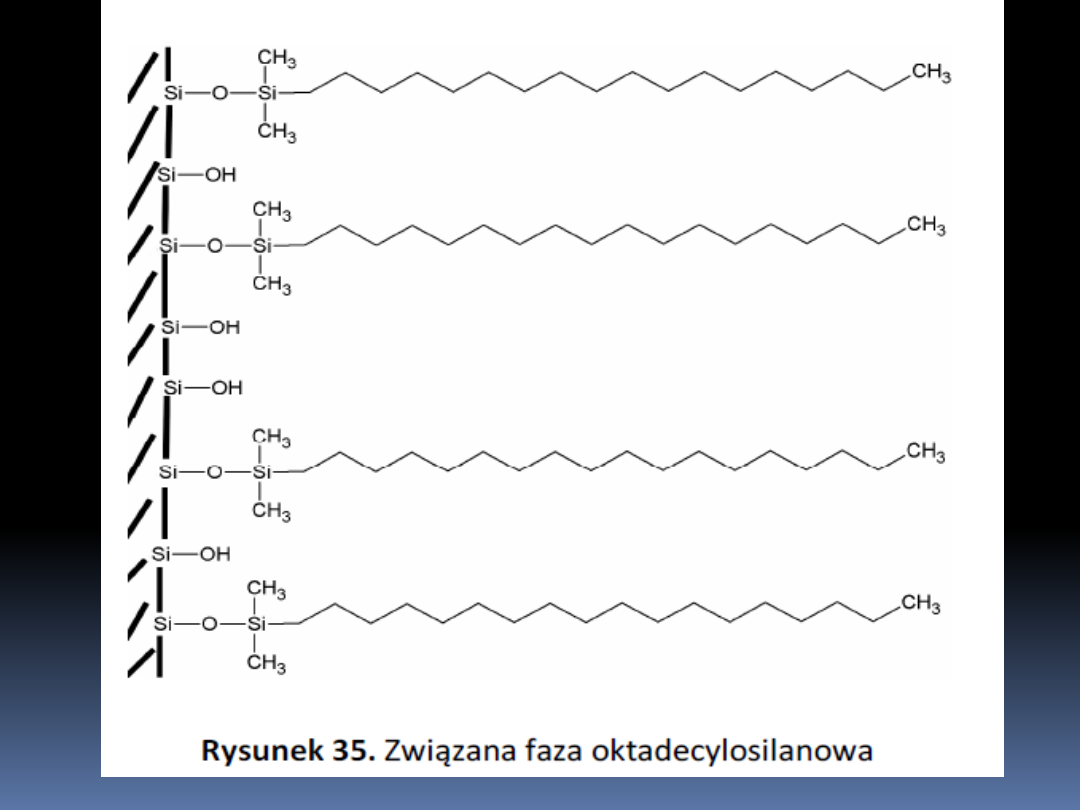
Faza oktadecylosilanowa (ODS)
najpopularniejsza faza niepolarna –
oktadecylosilanolowa o 18 atomach węgla w
łańcuchu
wykorzystywana do rozdzielana różnych
związków – od niepolarnych do
polarnych
stosowana w chromatografii o odwróconym
układzie faz

Normalny układ faz
faza stacjonarna jest bardziej polarna niż faza
ruchoma
z krzemionką związane są grupy polarne:
R-CN;
R-NO
2
R-NH
2
służą do rozdzielania substancji polarnych
Eluenty- heksan, izooktan, chloroform

Odwrócony układ faz
faza stacjonarna jest mniej polarna niż faza
ruchoma
z krzemionką związane są grupy niepolarne:
R-CH
3
;
R-C
8
H
17
R-C
18
H
37
;
Eluenty - metanol, izopropanol, woda ( wodne
roztwory buforowe )
Rozdzielanie substancji niepolarnych

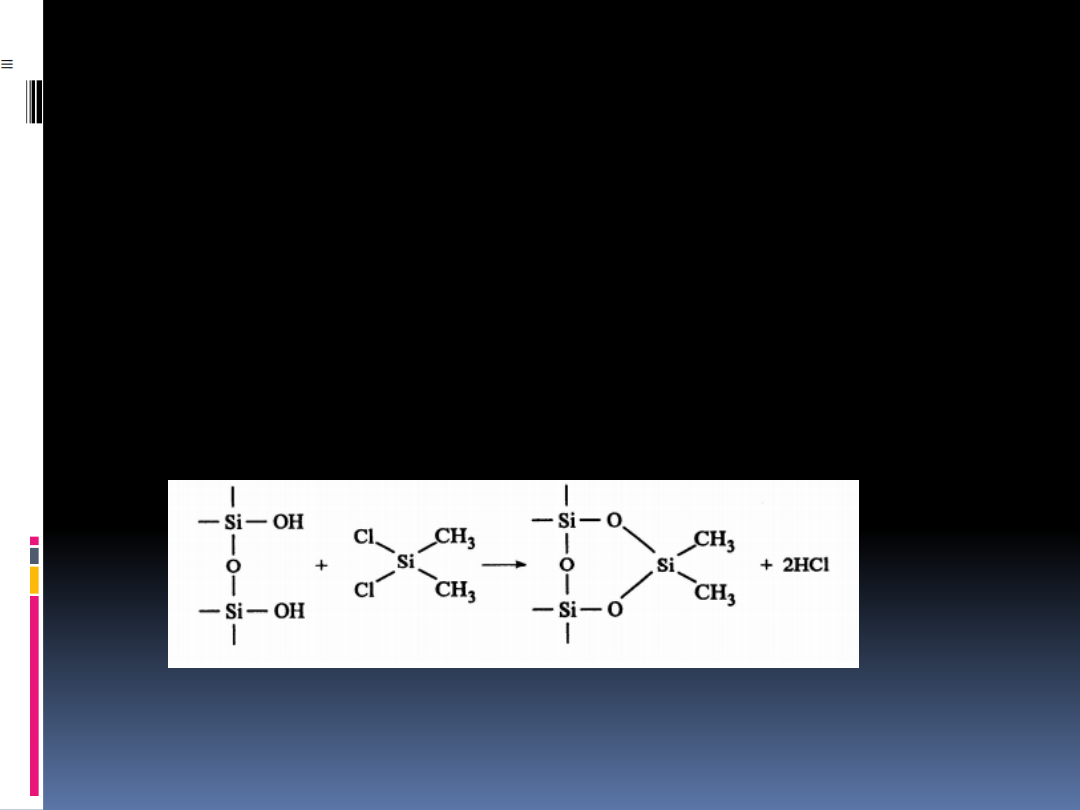
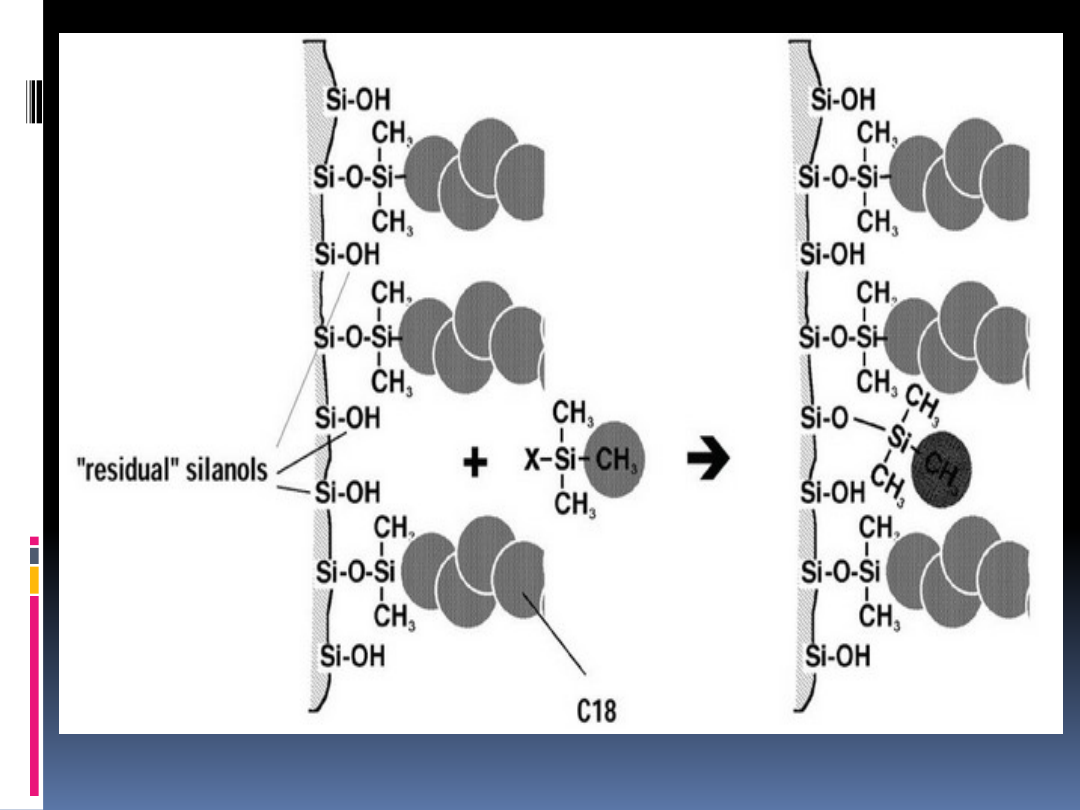
Endcapping
jest to proces stosowany po modyfikacji
żelu krzemionkowego grupami ODS
polega na dezaktywacji za pomocą
trimetylochlorosilanu pozostałych grup
silanolowych, otrzymując mniej aktywną fazę
stacjonarną
efektem tego jest przede wszystkim wzrost
hydrofobowości powierzchni

Liczba półek teoretycznych
mówi o sprawności kolumny
im więcej półek teoretycznych tym sprawność
kolumny większa, a uzyskane piki węższe
liczbę półek teoretycznych oblicza się ze
wzoru
N=16(t
r
/W
B
)
2

Sprawność i selektywność
Sprawność kolumn chromatograficznych
decyduje o tym czy pik chromatograficzny jest
ostry czy rozmyty
gdy każdy składnik mieszaniny wprowadzonej
do układu wykazuje zróżnicowaną retencję,
układ chromatograficzny jest selektywny
wobec składników rozdzielanej mieszaniny

WRPT
najmniejsza długość odcinka kolumny, w
której osiąga się stan równowagi między
stężeniami substancji chromatografowanej w
fazie ruchomej i nieruchomej
im wartość H (WRPT) jest mniejsza, tym
kolumna ma więcej półek i jest sprawniejsza
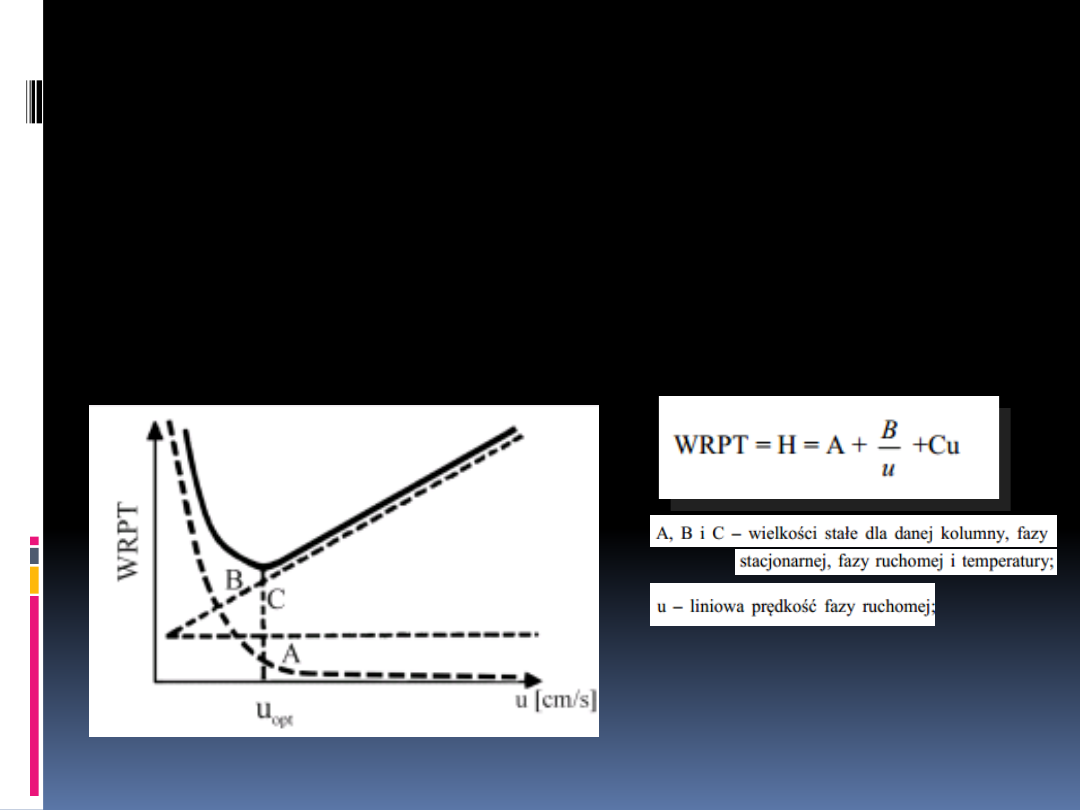
Równanie van Deemtera
Przedstawia zależność wysokości
równoważnej półce teoretycznej od średniej,
liniowej prędkości przepływu fazy ruchomej
przez kolumnę
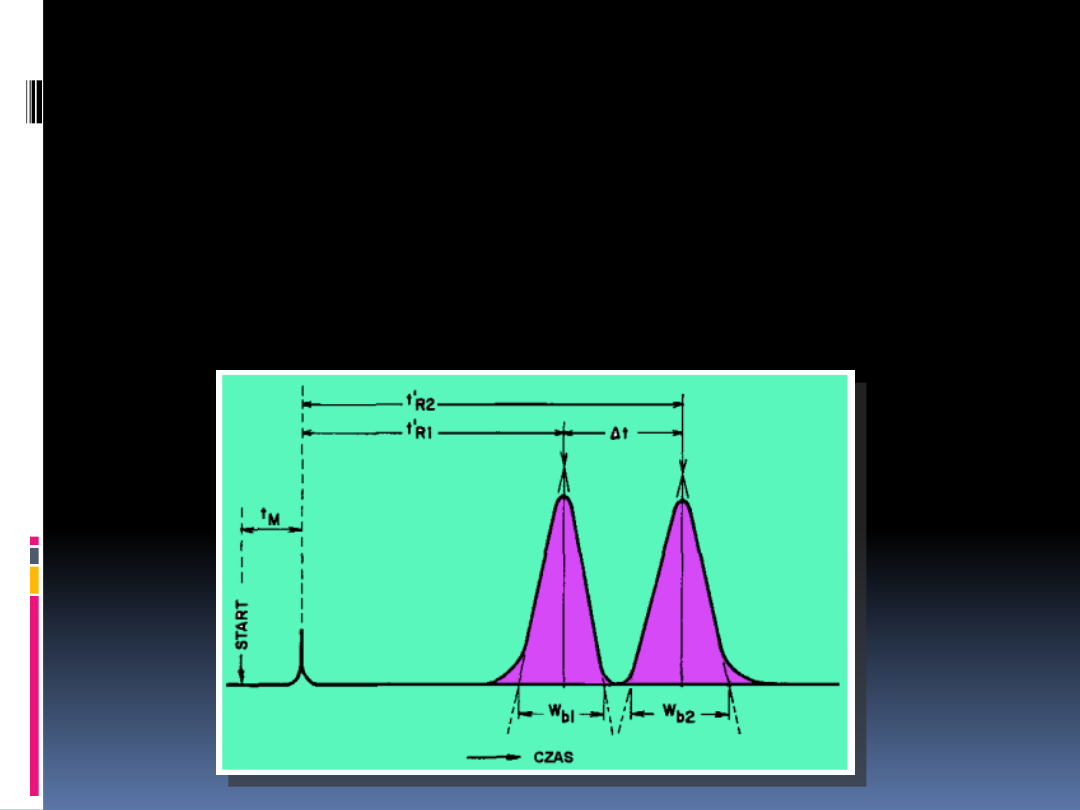
Czas martwy t
M
czas przebywania w kolumnie substancji,
która nie ma powinowactwa do fazy
stacjonarnej np. metanu; czas zerowy jest
równy czasowi przepływu fazy ruchomej przez
kolumnę

Wyznaczanie t
M
wyznaczanie teoretyczne:
Wyznaczanie t
M
Porównanie wartości
eksperymentalnej z
wartością teoretyczną
Najczęściej czas martwy (objętość
martwą kolumny) w układach
faz
normalnych
wyznacza się stosując
skwalan
, albo
fluoroalkany
, jako
substancję wzorcową, a fazą
ruchomą jest rozpuszczalnik o
średniej sile elucyjnej np.
octan
etylu
.
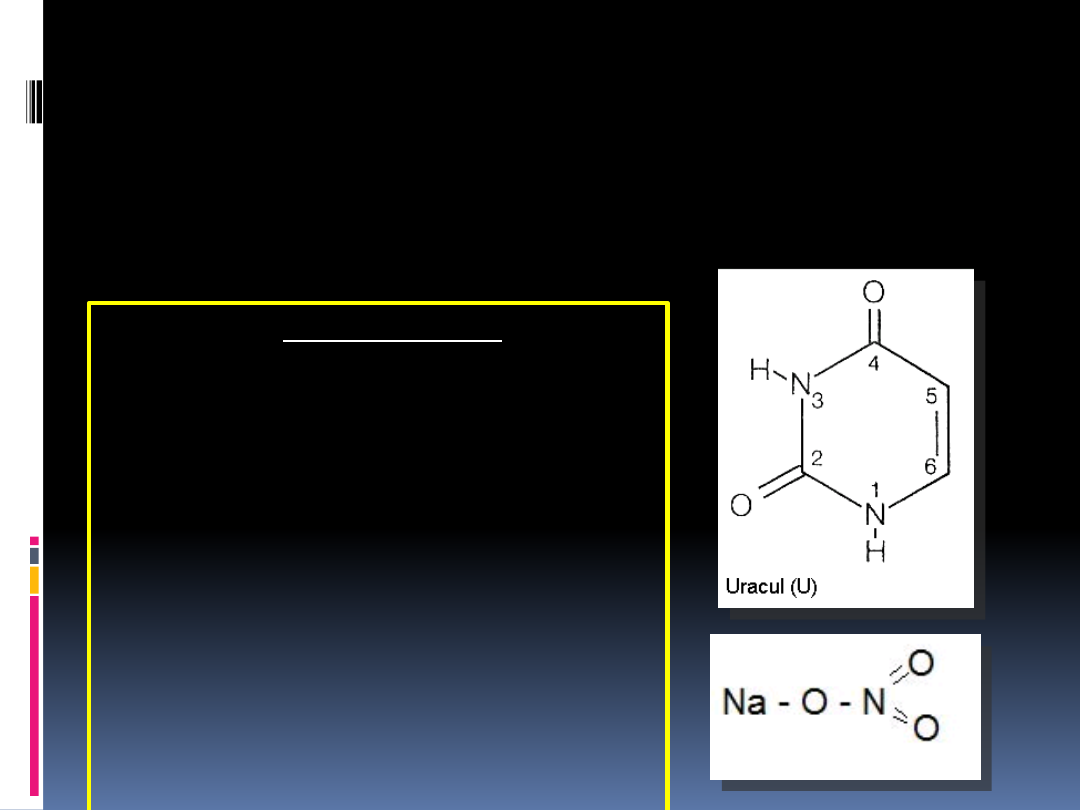
W układach
faz odwróconych
stosuje się często jako substancję
testową
uracil
lub
D2O
lub stężony
roztwór
azotanu potasu
(detekcja
przy długości fali λ=205-280 nm), a
fazą ruchomą może być metanol
albo acetonitryl.

Zależność pomiędzy prędkością liniowa a natężeniem przepływu
ciekłej fazy ruchomej w kolumnie o różnych średnicach

Czynniki wpływające na sprawność kolumn
wielkość cząstek wypełnienia
kolumny
struktura wypełnienia
opory przenoszenia masy
prędkość i profil przepływu cieczy
kinetyka zjawisk sorpcji – desorpcji
itp.
temperatura

Zredukowana wysokość półki teoretycznej
Wyraża się stosunkiem wysokości półki
teoretycznej H do średnicy cząstek d
p
wypełnienia kolumnowego
Kolumna ma dobrą sprawność gdy h=2-3

R
s
= 2 ( t
R2
– t
R1
/ W
1
+ W
2
)
t
R1
= czas retencji pierwszego piku
t
R2
= czas retencji drugiego piku
W
1
= szerokość piku przy podstawie
pierwszego piku
W
2
= szerokość piku przy podstawie
drugiego piku
Rozdzielczość Rs
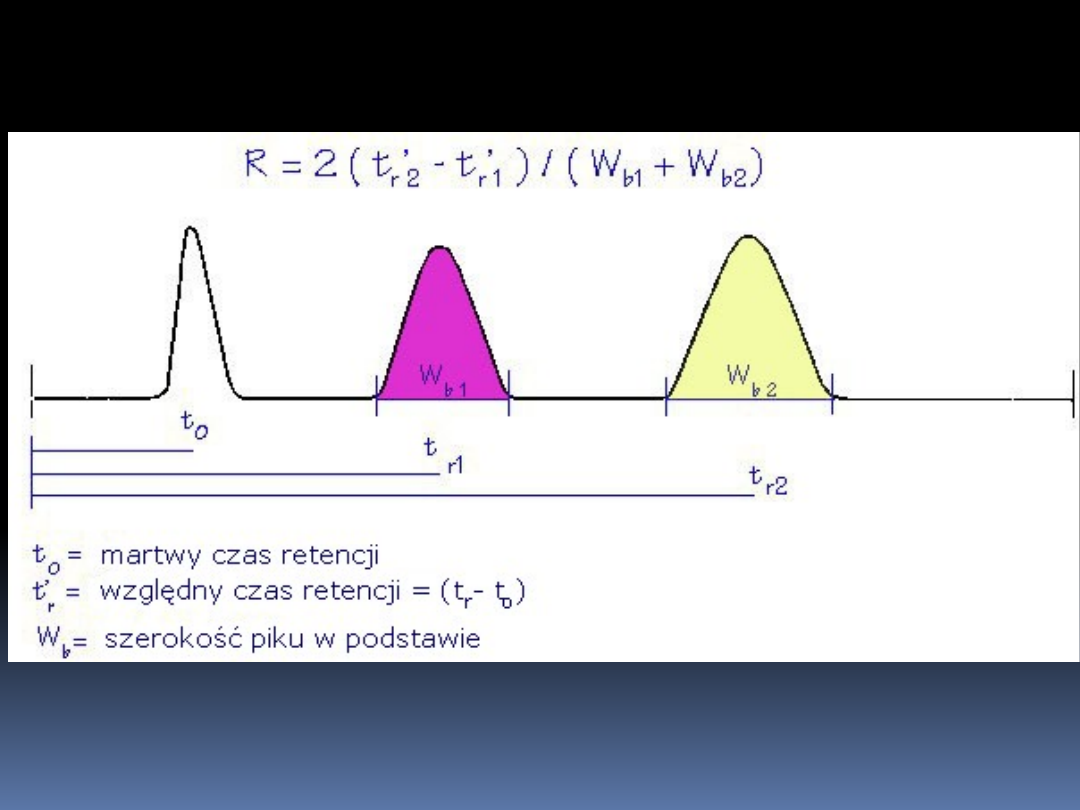
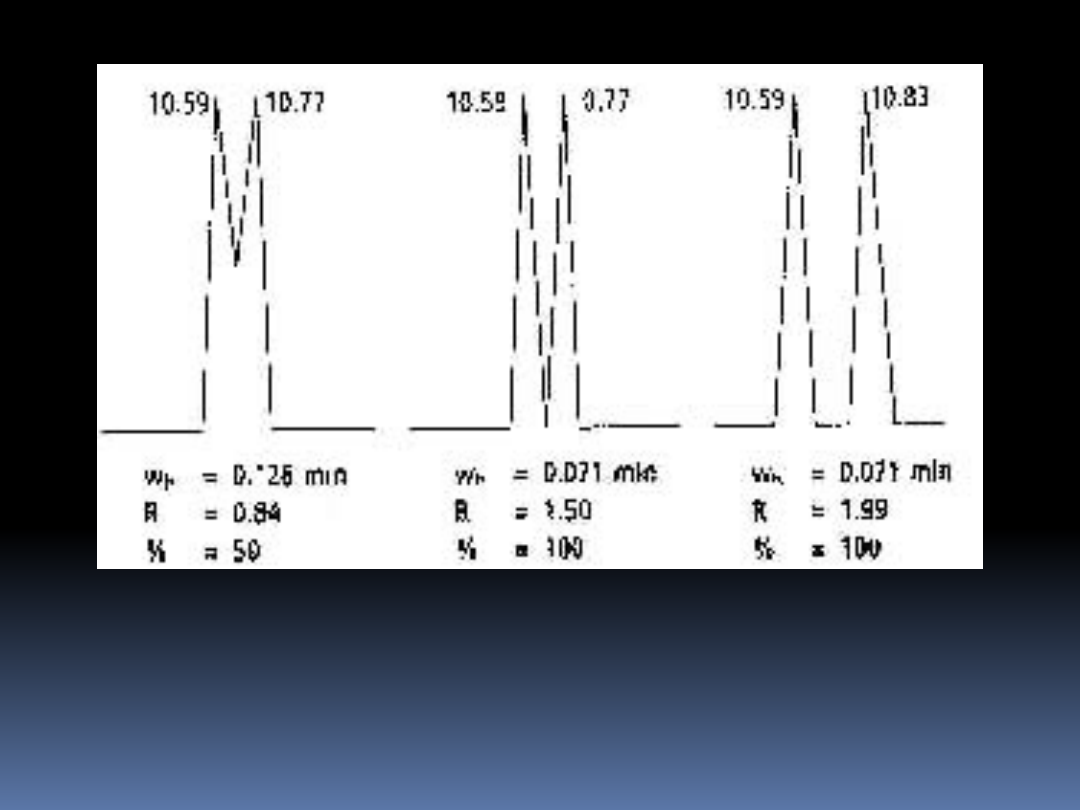
R > 1,5 – wykazuje linię podstawy między pikami
R < 1,5 – wykazuje koelucję piku

Współczynnik retencji k
k = (t
R
– t
M
) / t
M
k = t’
R
/ t
M
t
R
= czas retencji
t’
R
= redukowany czas retencji
t
M
= czas retencji związku nie zatrzymywanego

k = n
s
/ n
m
n
s
– liczba moli w fazie stacjonarnej
n
m
– liczba moli w fazie ruchomej
k = C
s
x V
s
/ C
m
x V
m
Cs – stężenie składnika w fazie stacjonarnej
Cm – stężenie składnika w fazie ruchomej
Vs – objętość fazy stacjonarnej
Vm – objętość fazy ruchomej

Selektywność jako współczynnik
rozdzielczości α
α = ( t
RB
– t
M
) / ( t
RA
– t
M
) = k
B
/ k
A
t
RA
,
t
RB
–czasy retencji substancji A i B
k
A
, k
B
– współczynniki retencji substancji
A i B
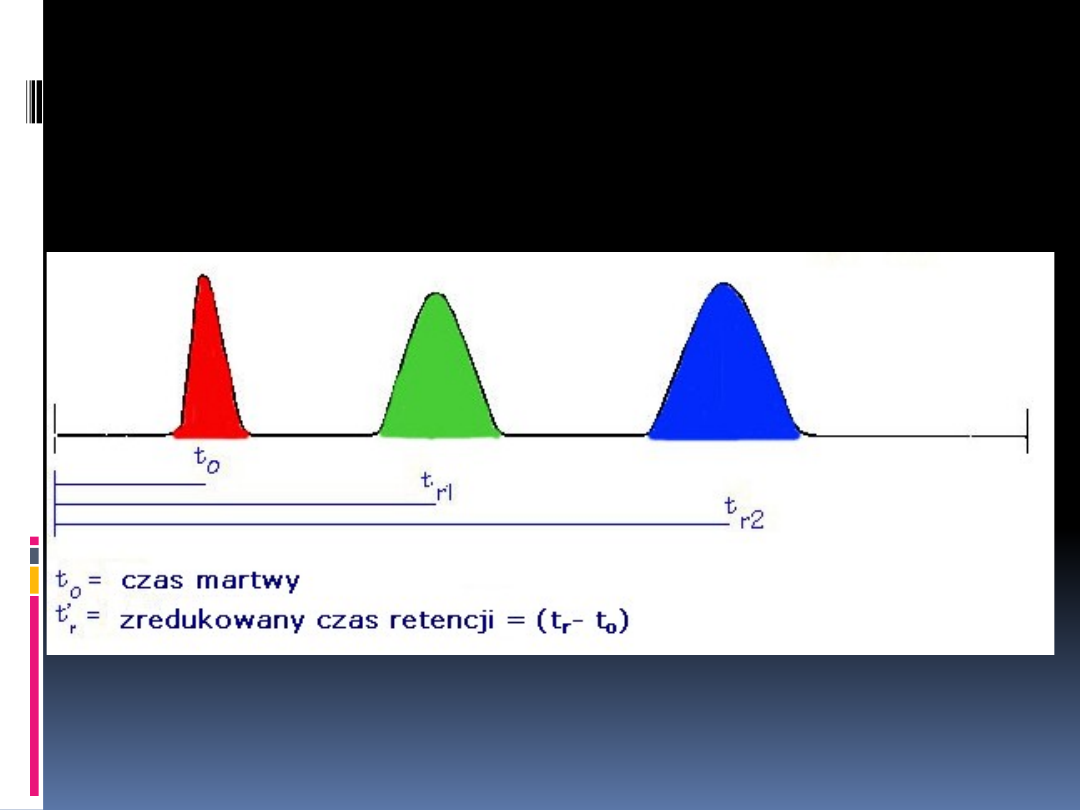
α = k
B
/ k
A
α = t
r2
/ t
r1

Równanie Purnella
√N α - 1 k
2
Rs = ----- ---------- --------
4 α 1 + k
2
k
2
- współczynniki retencji substancji, której
odpowiada pik 2
N – liczba półek teoretycznych kolumny
α- współczynnik rozdzielenia

Wpływ temperatury na
sprawność kolumny
Chromatografia cieczowa wykonywana jest
głównie w temperaturze otoczenia,
dobierając właściwy eluent.
Mało aparatów z fabrycznym termostatem.
Zmiana temperatury chromatografowania
wpływa na sprawność kolumny i czas
retencji substancji.
Znaczne podwyższenie temperatury
zwiększa możliwości zastosowania
chromatografii cieczowej.

Dziękujemy za uwagę
Document Outline
- Slide 1
- Slide 2
- RODZAJE KOLUMN
- Slide 4
- Mikrokolumny
- Kolumny analityczne
- Kolumny preparatywne
- Wypełnienia
- Wypełnienia krzemionkowe
- Slide 10
- ŻEL KRZEMIONKOWY
- Faza oktadecylosilanowa (ODS)
- Slide 13
- Normalny układ faz
- Odwrócony układ faz
- Endcapping
- Slide 17
- Liczba półek teoretycznych
- Sprawność i selektywność
- WRPT
- Równanie van Deemtera
- Czas martwy tM
- Wyznaczanie tM
- Wyznaczanie tM
- Slide 25
- Czynniki wpływające na sprawność kolumn
- Zredukowana wysokość półki teoretycznej
- Rozdzielczość Rs
- Slide 29
- Slide 30
- Współczynnik retencji k
- Slide 32
- Selektywność jako współczynnik rozdzielczości α
- Slide 34
- Równanie Purnella
- Wpływ temperatury na sprawność kolumny
- Dziękujemy za uwagę
Wyszukiwarka
Podobne podstrony:
CHROMATOGRAFIA KOLUMNOWA I CIENKOWARSTWOWA
CHROMATOGRAFIA CIENKOWARSTWOWA I KOLUMNOWA, NAUKA, WIEDZA
Chromatografia kolumnowa id 116 Nieznany
CHROMATOGRAFIA CIENKOWARSTWOWA I KOLUMNOWA
Cz III Kolumny kapilarne do chromatografii gazowej
Chromatografia kolumnowa Instrukcja do cwiczenia
Cz III Kolumny kapilarne do chromatografii gazowej
chromatografia kolumnowa
Chromatografia kolumnowa
chromanie przestankowe 2
Kolumna absorpcyjna z wypelnieniem
Kolumna absorpcyjna
77 Nw 01 Wiertarka kolumnowa dok
192Preparatywna i procesowa chromatografia cieczowa
6Hydrophobic Interaction Chromatography
Chromatografia id 116057 Nieznany
Kolumny DR MENARD
więcej podobnych podstron