Azotowce
Pierwiastki grupy 15
(Grupy VA „głównej”)
Azotowce
Konfiguracja elektronowa powłoki walencyjnej ns
2
np
3
Elektro-
ujemność
E
I
(I/III/V)
[kJ·mol
-1
]
A
e
(X
→
X
3-
)
[kJ·mol
-1
]
r
A
[pm]
r
J
(3+)
[pm]
N
3,0
1402
4578
9445
-20
75
P
2,1
1012
2912
6274
74
110
As
2,2
944
2736
6043
77
122
69
Sb
1,8
832
2440
5400
101
143
92
Bi
1,6
703
2466
5400
100
146
108
Azotowce
Konfiguracja elektronowa cząsteczki azotu N
2
2s
2s
2p
2p
x
y
z
x
y
z
N K2s
2
2p
3
N
2
KK
σ
2s
2
σ
*
2s
2
σ
2p
2
π
2p
2
π
2p
2
N K2s
2
2p
3
σ
2s
σ
*
2s
σ
2p
π
2p
π
*
2p
σ
*
2p
π
2p
π
*
2p
Odmiany alotropowe fosforu
P
biały
P
czerwony
P
fioletowy
450 K
↔
↔
↔
↔
800 K
↔
↔
↔
↔
P
czarny
480 K; 1,2 GPa
hybrydyzacja
sp
3
gęstość
ładunku
Odmiany alotropowe fosforu (2)
W sieci fosforu
czerwonego
,
fioletowego
i czarnego
każdy atom fosforu – podobnie jak w fosforze białym –
ma 3 sąsiadów
~
~
Arsen, antymon i bizmut
Arsen i antymon mają po dwie odmiany
alotropowe:
o
As zwykle jak P
czarny
, oprócz tego
As
4
- arsen żółty
o
Sb zwykle jak P
czarny
, oprócz tego
Sb
4
- antymon żółty
Bizmut ma tylko jedną odmianę, wiązania mają
charakter częściowo metaliczny
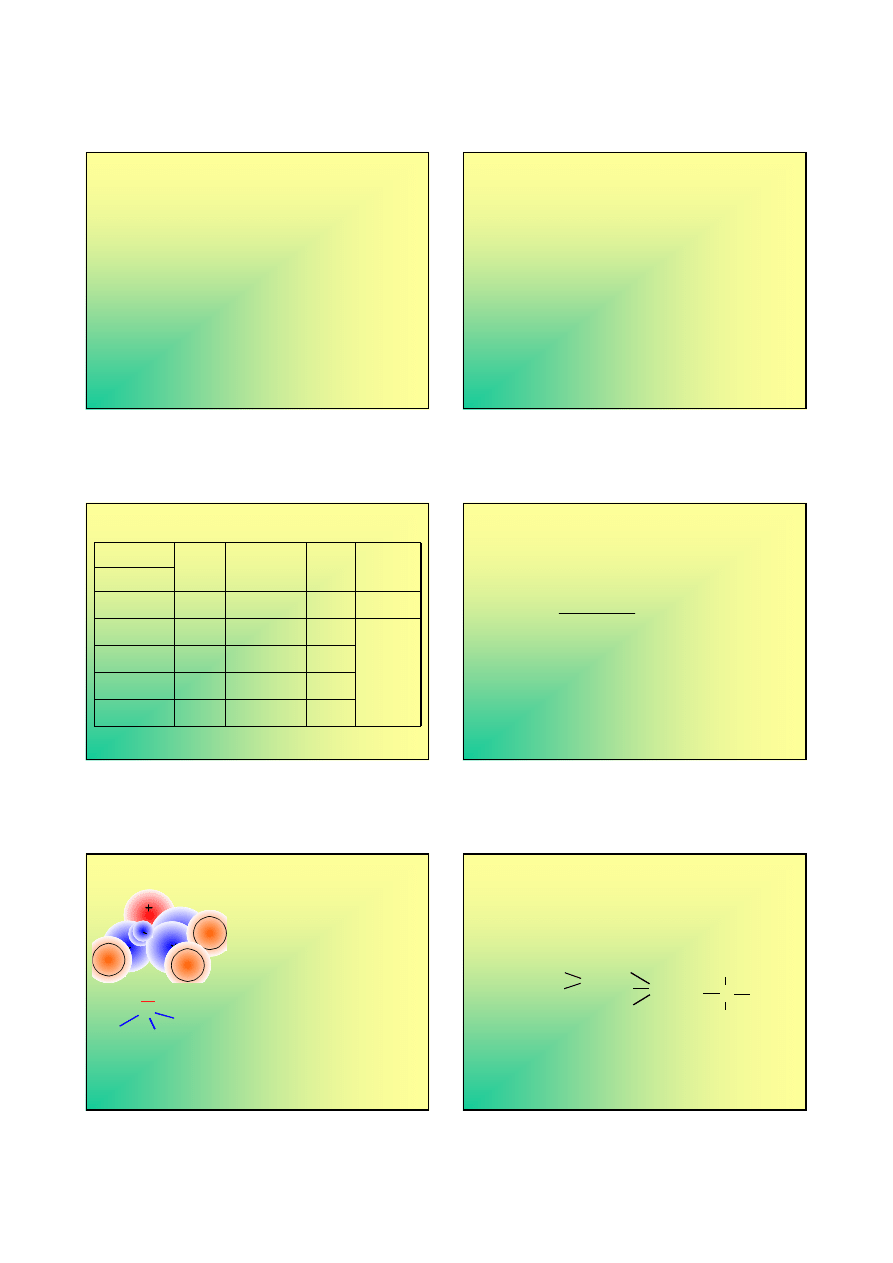
Charakter chemiczny azotowców
Azotowce tworzą wiązania kowalencyjne;
stopnie utlenienia od
-III
do
+V
Kształt izolowanych cząsteczek, a także
kierunki wiązań w kryształach dobrze tłumaczą
reguły hybrydyzacji ...
Charakter połączeń ulega zmianie ze wzrostem
masy molowej, np. tlenki azotu i fosforu mają
charakter
kwasowy
, tlenki arsenu i antymonu -
amfoteryczny
, bizmutu -
zasadowy
W miarę wzrostu masy atomowej oddalają się
od siebie poziomy walencyjne s i p, dlatego Bi
łatwiej tworzy trwałe związki na +III stopniu
utlenienia (bez udziału elektronów poziomu s)
Charakter chemiczny azotowców (2)
O charakterze chemicznym azotowców
ś
wiadczy także ich występowanie w przyrodzie:
azot występuje w stanie wolnym w powietrzu, ale
także w formie azotanów (amoniak jest również
produktem rozkładu związków organicznych
zawierających azot);
fosfor występuje przede wszystkim jako
nierozpuszczalny w wodzie fosforan wapnia
Ca
3
(PO
4
)
3
– fosforyty i apatyty;
arsen, antymon i bizmut występują przede
wszystkim jako kationy w siarczkach odpowiednich
pierwiastków (także siarczkach podwójnych)
Poł
ą
czenia azotowców z wodorem
stopień utlenienia
→
nazwa
- III,
XH
3
BiH
3
bizmutowodór
SbH
3
stiban,
antymonowodór
AsH
3
arsan, arseniak
PH
3
fosfan, fosforiak
NH
3
azan, amoniak
nazwa
-II,
X
2
H
4
N
2
H
4
hydrazyna
P
2
H
4
fosfina
- 1/3,
HX
3
azotowodór,
azydek
wodoru
HN
3
Otrzymywanie amoniaku
W laboratorium:
KCl
O
H
NH
NaOH
Cl
NH
2
3
4
+
+
↑
→
+
W przemyśle (metoda Habera-Boscha):
egzo
H)
(-
2NH
3H
N
3
C,25MPa
500
O
Al
O,
K
,
O
Fe
2
2
3
2
2
4
3
∆
→
←
+
o
Metodę opracował Fritz Haber w latach 1905 -1910
(Nobel 1918), wdrożył Carl Bosch.
Ustala się równowaga przy zawartości ok. 15 %
amoniaku. Wydajność rzędu 100 % osiąga się, usuwając
amoniak (przez wymrażanie) i poddając recyrkulacji
pozostałe gazy (uzupełniając je świeżym wodorem i
azotem)
Właściwości amoniaku
Amoniak ma własności
zasadowe
i
redukujące
. Wolna para
elektronowa, moment dipolowy,
wiązania wodorowe, w wodzie jest
zasadą Brønsteda ...
−
+
+
→
←
+
OH
NH
O
H
NH
4
2
3
K
d
= 1,8·10
-5
Roztwory wodne amoniaku mają
odczyn
słabo zasadowy
, a z kwasami
tworzą sole amonowe, z kationem
NH
4
+
Sole amonowe mają właściwości
zbliżone do soli grupy 1 (litowców).
Własności
zasadowe
wodorków
azotowców słabną ze wzrostem masy
molowej ...
NH
3
N
H
H
H
Pochodne amoniaku
Atom wodoru w cząsteczce amoniaku może być
zastąpiony przez kation metalu:
NaNH
2
- amidek
;
Li
2
NH - imidek
;
Mg
3
N
2
– azotek
lub przez łańcuch węglowodorowy (R) – aminy:
R-NH
2
aminy
I- rz
ę
dowe
aminy
II- rz
ę
dowe
R
1
R
2
NH
aminy
III-rz
ę
dowe
R
1
R
2
N
R
3
aminy
IV-rz
ę
dowe
R
4
R
2
N
R
3
R
1
[ ]
+
Aminy zaliczamy do związków organicznych

Sole amonowe
Bezbarwny jon amonowy NH
4
+
otrzymuje się przez
rozpuszczenie w wodzie amoniaku:
−
+
+
→
←
+
OH
NH
O
H
NH
4
2
3
Otrzymana w ten sposób woda amoniakalna zachowuje
się jak słaba zasada, od której pochodzą sole amonowe;
Prawie wszystkie sole amonowe są rozpuszczalne w
wodzie.
NH
4
Cl
, salmiak, reakcja amoniaku z kwasem solnym,
zastosowanie: ogniwo Leclanchégo, jako nawóz;
NH
4
NO
3
, saletra amonowa, reakcja amoniaku z kwasem
azotowym, nawóz sztuczny, źródło N
2
O;
NH
4
HCO
3
, wodorowęglan amonu, główny składnik
proszku do pieczenia, rozkłada się zgodnie z równaniem:
2
2
3
3
4
CO
O
H
NH
HCO
NH
+
+
→
HN
3
, azydek wodoru
HN
3
,
azydek wodoru
(d. kwas azotowodorowy),
tworzy sole, w których występuje jon N
3
-
:
O
H
NaN
NaNH
O
N
2
3
2
2
+
→
+
azydek
sodowy
4
2
3
4
2
3
SO
Na
2HN
SO
H
2NaN
+
→
+
H
N
N
124
114
N
hybrydyzacja sp, HN
3
N
N
115
N
115
hybrydyzacja sp, jon N
3
-
zhybrydyzowane orbitale azotu tworzą wiązania typu
σ
, a orbitale
2p
z
i
2p
y
nakładają się, tworząc
trójcentrowe, zdelokalizowane orbitale
π
Tlenki azotowców
Stopień
utlenienia
Bi
Sb
As
P
N
N
2
O
+I
NO
+II
Bi
2
O
3
Sb
2
O
3
As
2
O
3
P
4
O
6
N
2
O
3
+III
NO
2
,
N
2
O
4
+IV
Bi
2
O
5
Sb
2
O
5
As
2
O
5
P
4
O
10
N
2
O
5
+V
Wiązania w tlenkach azotu (1)
Hybrydyzacja sp, dwa orbitale zlokalizowane typu σ
zdelokalizowany trójcentrowy orbital π (jak jon
N
3
-
)
N
N
O
112
119
N
N
O
π
N
N
O
π
*
Tlenek azotu (I), tlenek dwuazotu,
podtlenek azotu, odegrał bardzo
ważną rolę w anestezjologii, jako
pierwszy środek znieczulający
(Horace Wells, 1845). Znany także
pod nazwą gazu rozweselającego
2
2
ogrzewanie
2
O
2N
O
2N
+
→
Wiązania w tlenkach azotu (2)
NO
ma taką samą strukturę elektronową jak jon
oksygenylowy
O
2
+
(czyli 1 elektron na orbitalu π*),
ma niezerowy moment dipolowy,
jest
zasadą Lewisa
, może być ligandem
ulega dimeryzacji,
może tracić elektron lub przyjmować elektron –
występując jako kation lub anion (ligand)
N
O
110
N
O
110
240
240
w stanie ciekłym lub
stałym
wy
nitrozonio
jon
e
y
nitrozylow
jon
e
NO
NO
NO
NO
−
+
→
+
→
−
Wiązania w tlenkach azotu (3)
NO
2
N
O
O
120
120
sp
2
wiązania jak w cząsteczce O
3
, o jeden
elektron mniej – orbital
zdelokalizowany niewiążący obsadzony
tylko przez jeden elektron; konfiguracja
elektronowa cząsteczki:
2NO
2
↔
↔
↔
↔
N
2
O
4
1
0
2
2
,
2
2
,
1
2
2
,
2
1
,
2
1
2
1
2
1
)
(
)
(
2
2
2
2
zd
zd
N
O
N
O
O
y
O
y
O
O
N
O
O
p
p
s
s
K
K
K
π
π
σ
σ
Tlenek azotu (IV), dwutlenek (ditlenek) azotu, ulega
dimeryzacji z wytworzeniem N
2
O
4
:
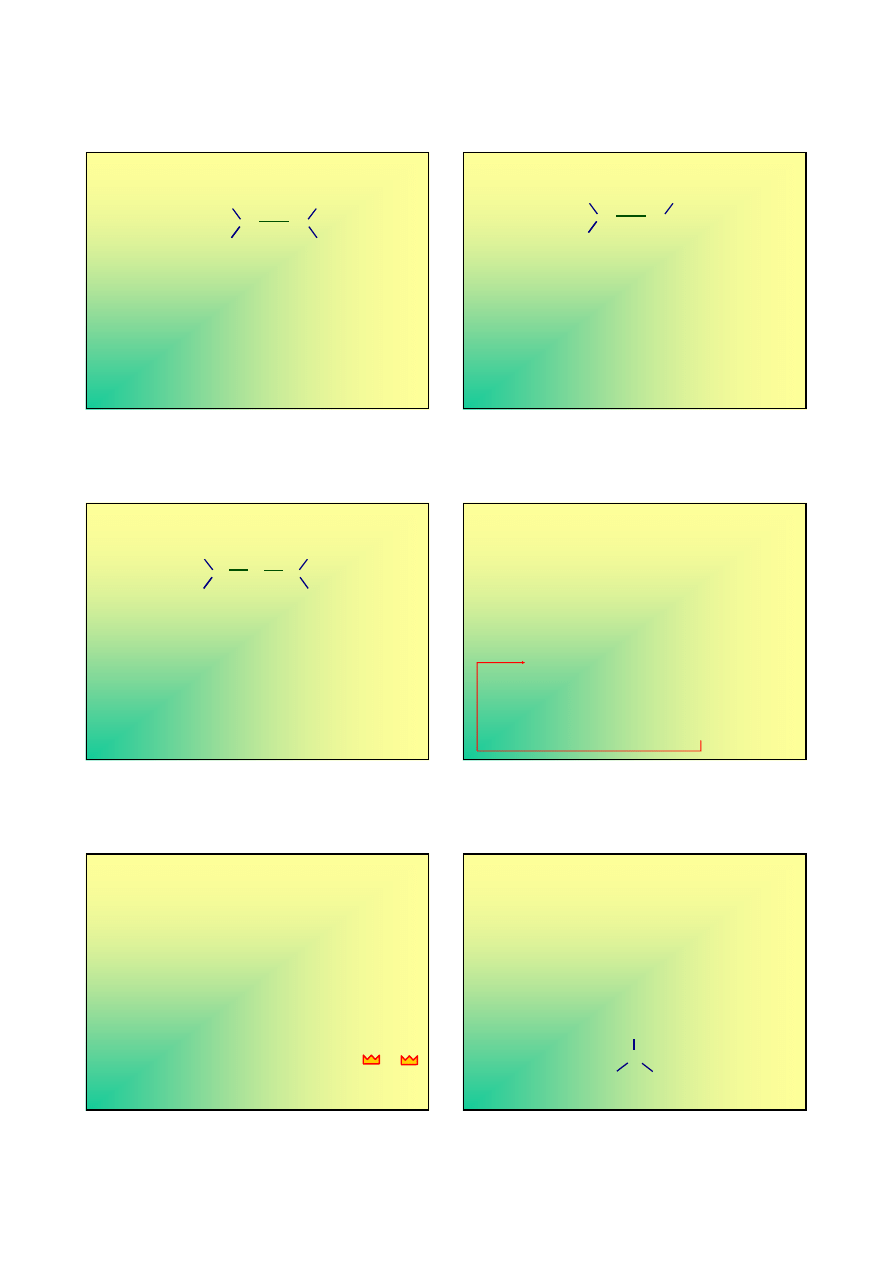
Wiązania w tlenkach azotu (4)
N
2
O
4
N
O
O
sp
2
N
O
O
sp
2
164
117
“Dimeryzacja”
NO
2
prowadzi do utworzenia płaskich
cząsteczek
N
2
O
4
;
wiązanie N-N jest słabe; zdelokalizowany orbital π
rozciąga się na całą cząsteczkę (jest sześciocentrowy)
NO
2
jest bezwodnikiem ‘mieszanym’. W wyniku jego
reakcji z wodą powstaje mieszanina
HNO
2
i
HNO
3
4
2
2
2
O
N
2NO
O
2NO
↔
→
+
Wiązania w tlenkach azotu (5)
N
2
O
3
N
O
O
sp
2
N
O
sp
2
186
Nierównocenne pozycje atomów azotu – w jednym z
nich występuje wolna para elektronowa, cząsteczka
płaska ze zdelokalizowanym (pięciocentrowym)
orbitalem typu π. Tlenek nietrwały.
Jest formalnym bezwodnikiem kwasu azotowego (III),
HNO
2
Wiązania w tlenkach azotu (6)
N
2
O
5
N
O
O
sp
2
N
O
O
sp
2
O
Cząsteczka
N
2
O
5
jest płaska, ze zdelokalizowanym
(siedmiocentrowym) orbitalem typu π. Tlenek nietrwały.
Jest formalnym bezwodnikiem kwasu azotowego (V),
HNO
3
Przemysłowe otrzymywanie HNO
3
1.
Synteza amoniaku metodą Habera-Boscha:
3
C,10MPa
700
500
2
2
2NH
3H
N
→
←
+
−
o
Fe
2
O
3
, katalizator
2.
Katalityczne spalanie amoniaku metodą Ostwalda:
O
6H
4NO
5O
4NH
2
Pt,1100K
2
3
+
→
←
+
3.
Utlenianie NO do NO
2
:
4
2
2
2
O
N
2NO
O
2NO
↔
→
+
4.
Pochłanianie mieszaniny NO
2
i N
2
O
4
w wodzie:
O
H
2NO
HNO
3HNO
HNO
HNO
O
H
O
N
2
3
2
3
2
2
4
2
+
+
→
+
↔
+
Właściwości HNO
3
1.
mocny kwas
, w wodzie ulega prawie całkowitej
dysocjacji:
−
+
+
→
+
3
3
2
3
NO
O
H
O
H
HNO
2
. czysty
HNO
3
ulega
autodysocjacji:
−
+
+
→
←
3
3
2
3
NO
NO
H
2HNO
3.
w podwyższonej temperaturze ulega rozkładowi
2
2
2
3
O
O
2H
4NO
4HNO
+
+
→
4.
stężony
HNO
3
posiada silne
właściwości utleniające
:
O
4H
2NO
)
3Cu(NO
8HNO
3Cu
2
2
3
3
+
+
→
+
5.
mieszanina
HCl
(3 cz. obj.) i
HNO
3
jest
bardzo silnie
utleniająca:
NOCl
Cl
O
2H
HNO
3HCl
2
2
3
+
+
→
+
chlor
chlorek
nitrozylu
woda królewska
aqua regis
Azotany
Solami kwasu azotowego są azotany
Me(NO
3
)
n
.
Azotany (
saletry) stanowią cenne nawozy sztuczne (i
naturalne), dostarczając azotu niezbędnego dla
rozwoju roślin (NPK).
Do najważniejszych należą:
KNO
3
(
saletra indyjska),
NaNO
3
(
saletra chilijska),
NH
4
NO
3
(
saletra
amonowa).
Anion azotanowy jest płaski (hybrydyzacja
sp
2
azotu). Jon azotanowy jest
izoelektronowy z
SO
3
:
N
O
O
O
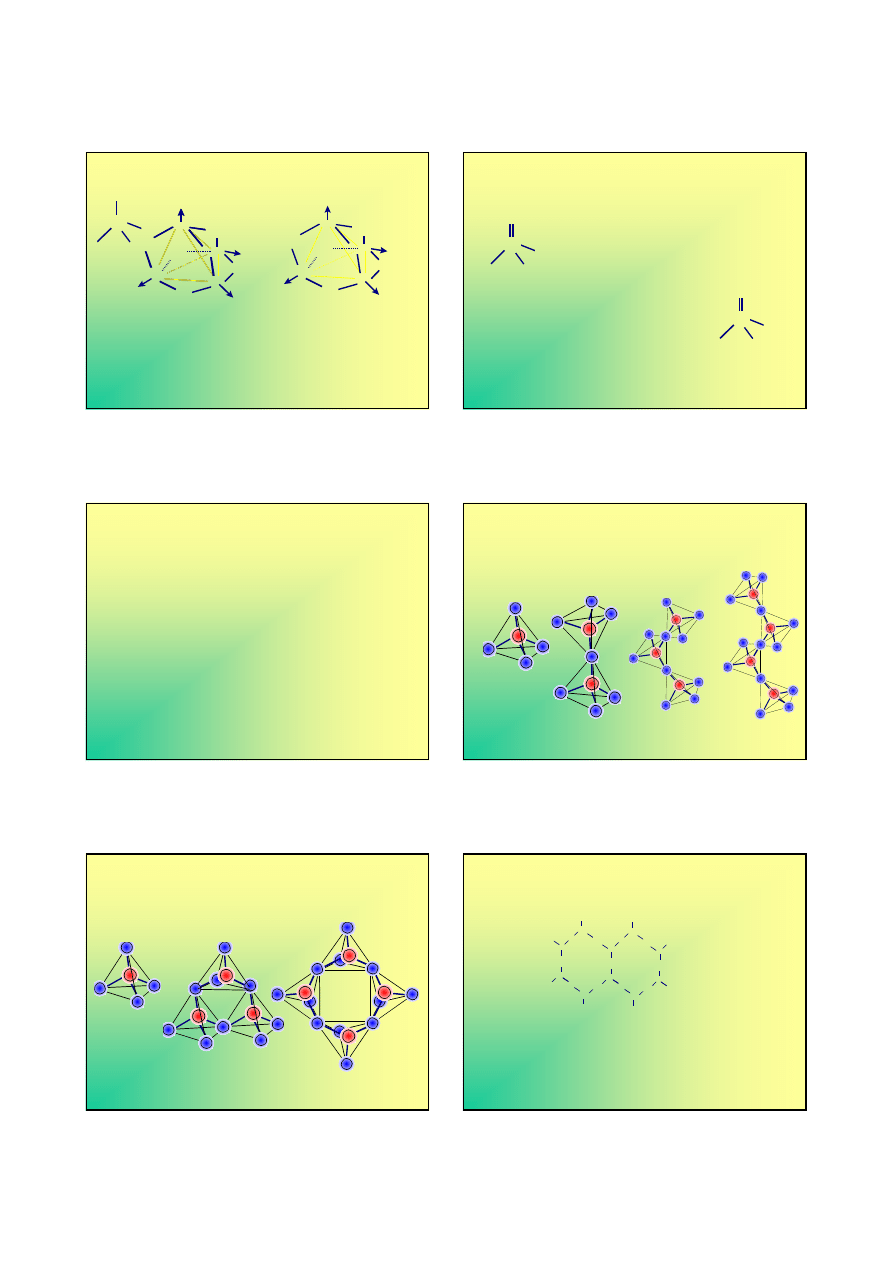
Tlenki fosforu
W większości związków fosfor ulega hybrydyzacji
sp
3
P
P
P
P
P
P
P
P
P
O
O
O
O
O
O
O
O
O
P
P
P
P
O
O
O
O
O
O
O
O
O
O
W cząsteczce
P
4
O
6
każdy
z atomów fosforu tworzy
trzy wiązania z trzema
atomami tlenu, czwarty
orbital zhybrydyzowany
stanowi wolną parę
elektronową
W cząsteczce
P
4
O
10
czwarty atom tlenu jest
wiązany przez ‘wolną
parę’
P
4
O
6
Kwasy tlenowe fosforu i ich sole
1.
kwas fosforowy (III) H
3
PO
3
:
P
OH
OH
H
O
3
3
2
6
4
PO
4H
O
6H
O
P
→
+
P
O
H
O
H
O
H
O
2.
kwas fosforowy (V) H
3
PO
4
:
4
3
2
10
4
PO
4H
O
6H
O
P
→
+
na skalę techniczną:
4
3
4
4
2
2
4
3
PO
2H
3CaSO
SO
3H
)
(PO
Ca
+
→
+
Właściwości kwasu fosforowego (V)
i jego soli (rozpuszczalność!)
H PO
H O
H PO
H O
H PO
H O
HPO
H O
HPO
H O
PO
H O
3
4
2
2
4
3
2
4
2
4
3
4
2
4
3
+
↔
+
+
↔
+
+
↔
+
−
+
−
−
+
−
−
+
2
2
3
K
1
=7,52
@
10
-3
K
3
=2,2
@
10
-13
K
2
=6,23
@
10
-9
Nawozy fosforowe:
4
2
4
2
4
2
3
4
3
2CaSO
)
PO
Ca(H
SO
2H
)
(PO
Ca
+
→
+
superfosfat
2
4
2
4
3
3
4
3
)
PO
Ca(H
3
PO
4H
)
(PO
Ca
→
+
superfosfat
podwójny
Dysocjacja kwasu fosforowego zależy od pH roztworu ...
Polikwasy fosforowe i polifosforany
Polikondensacja kwasu fosforowego i
(wodoro)fosforanów:
O
H
O
P
H
PO
2H
2
7
2
4
4
3
+
→
H
3
PO
4
H
4
P
2
O
7
H
5
P
3
O
10
H
6
P
4
O
13
H
n+2
P
n
O
3n+1
Metakwasy fosforowe
Metakwasy i ich sole stanowią cykliczny produkt
polikondensacji zawierający
3
i więcej
tetraedrów
PO
4
3-
:
H
3
PO
4
H
3
P
3
O
9
H
4
P
4
O
12
Calgon - trójmetafosforan sodowy
Tlenki arsenu – As
2
O
3
As
4
O
6
(arszenik) występuje w formie cząsteczkowej
(jak
P
4
O
6
), a prócz tego w szklistej formie
warstwowej:
As
As
As
As
O
O
O
O
O
As
As
As
As
O
O
O
O
O
As
As
O
3
3
2
6
4
AsO
4H
O
6H
O
As
→
+
kwas trioksoarsenowy
8NO
AsO
12H
O
14H
8HNO
O
3As
4
3
2
3
6
4
+
→
+
+
kwas pentaoksoarsenowy, podobny do H
3
PO
4,
sole ulegają
kondensacji

Wykrywanie arsenu
S
As
3S
2As
3
2
2
3
↓
→
+
−
+
O
H
8
S
As
H
16
S
5
AsO
2
O
H
6
S
As
H
12
S
3
AsO
2
2
5
2
2
3
4
2
3
2
2
3
3
+
↓
→
+
+
+
↓
→
+
+
+
−
−
+
−
−
Próba Marsha – lustro arsenowe z rozkładu AsH
3
za chwilę szczegóły
Obecnie arsen oznacza się przede wszystkim metodami
analizy instrumentalnej (spektroskopia, w sczzególności
absorpcja atomowa, polarografia itp.)
, ale próbki trzeba
przygotować, rozpuścić itd.
Rozwój toksykologii sądowej w
związku z As
2
O
3
Parę słów o arszeniku (
As
2
O
3
, a raczej
As
4
O
6
) i jego
udziałowi w rozwoju chemii analitycznej (a raczej chemii
sądowej i kryminalistyki ....
Próba Marsha ...
lustro arsenowe
Sprawa Marii Lafarge (1840) ...
Toksykologia sądowa – arszenik – od sprawy Marie
Lafarge (1840) do sprawy Marii Besnard (1961)
Sprawa Marii Besnard (1940 -1961) ...
Bezsilność toksykologii w niektórych
przypadkach ... zwłaszcza jeśli sprytni
prawnicy stają naprzeciw niezbyt
starannych ekspertów-chemików ...
Tlenki antymonu – Sb
2
O
3
Sb
Sb
Sb
Sb
O
O
O
O
O
O
O
O
Sb
Sb
Sb
Sb
O
O
O
O
Sb
4
O
6
występuje w formie cząsteczkowej (jak
P
4
O
6
), a
prócz tego w odmianie złożonej z łańcuchów
Tlenek bizmutu – Bi
2
O
3
Bi
2
O
3
występuje w minerale bizmutycie
Należy do kryształów jonowych, przejawiających
polimorfizm, czyli występujących przy tym samym wzorze
w różnych strukturach krystalicznych.
Najważniejszy ze związków bizumtu, stosowany w
ogniwach paliwowych, gdyż jego kryształy w
podwyższonych temperaturach zachowują się jak
elektrolity stałe (ładunek jest przenoszony przez migrujące
jony O
2-
).
Sole antymonu i bizmutu
Antymon i bizmut występują w swoich solach najczęściej
jako kationy – Sb
3+
i Sb
5+
oraz Bi
3+
i Bi
5+
.
Sole Bi
3+
są bardziej trwałe niż sole Bi
5+
.
Do najczęściej otrzymywanych i stosowanych soli
antymonu i bizmutu należą chlorki, siarczany i azotany.
Chlorki ulegają hydrolizie w roztworach wodnych zgodnie
z równaniami:
+
−
+
−
+
+
+
→
+
+
O
2H
3Cl
BiO
O
3H
3Cl
Bi
3
2
3
Chlorek bizmutylu jest nierozpuszczalny w wodzie i
wytrąca się jako biały osad.
+
+
+
+
→
+
O
2H
BiO
O
3H
Bi
3
2
3
Związki bizmutu działają bakteriobójczo; galusan bizmutu
znany jako
dermatol wspomaga gojenie ran
Wyszukiwarka
Podobne podstrony:
chemia lato 04 09 10
chemia lato 04 09 10
chemia lato 04 09 10
chemia lato 06 09 10
chemia lato 05 09 10
chemia lato 07 09 10
chemia lato 12 09 10
chemia lato 03 09 10
chemia lato 13 09 10
chemia lato 01 09 10
chemia lato 02 09 10
HARMONOGR JIKR LATO 08 09 SALE, PWSZ
laboratorium 08 09 10
chemia lato 08 07 08 id 112426 Nieznany
chemia lato 08 13 14 A
2ª Allattamento DUM 08 09 [7 10 08 h15 17] sino all art escluso [modalità compatibilità]
więcej podobnych podstron