
Węglowodory
aromatyczne
Areny
Węglowodory aromatyczne -
to węglowodory
cykliczne, których pierścienie zawierają wiązanie
zdelokalizowane.
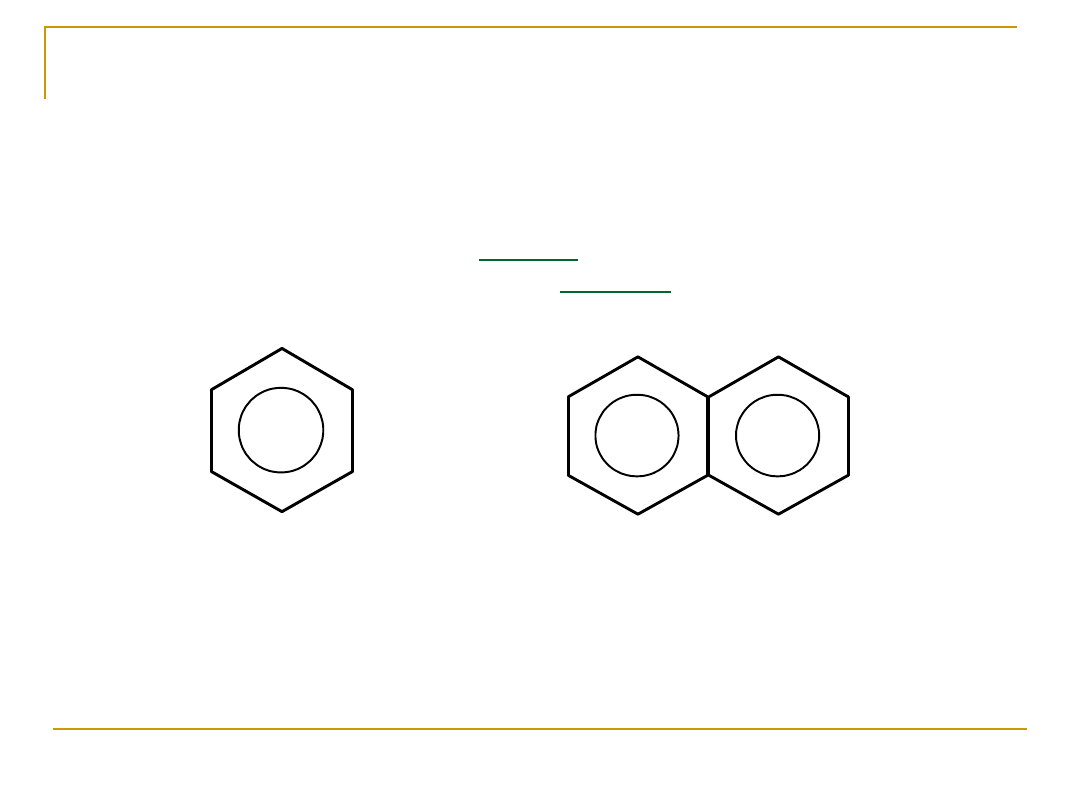
Można wyróżnić węglowodory aromatyczne jednopierścieniowe,
których przedstawicielem jest benzen oraz węglowodory o
pierścieniach skondensowanych np. naftalen, antracen.
Benzen
Naftalen
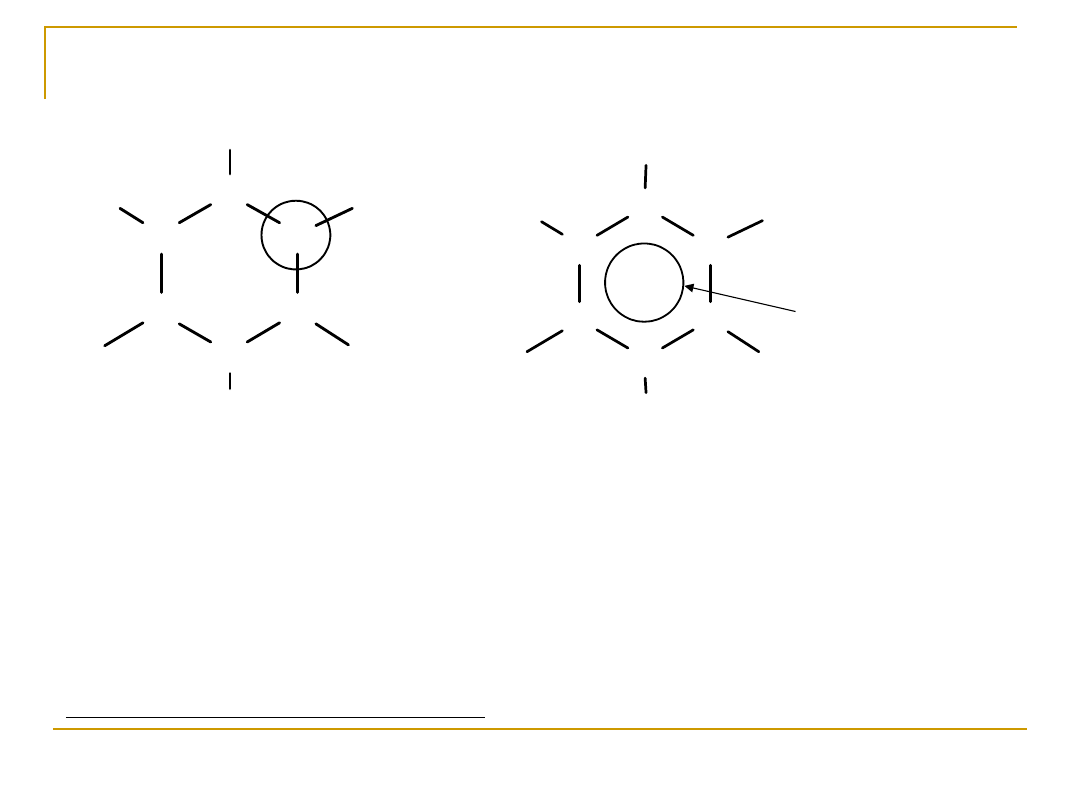
Budowa cząsteczki benzenu:
C
C
C
C
C
C
H
H
H
H
H
H
120
0
120
0
120
0
C
C
C
C
C
C
H
H
H
H
H
H
wiązanie
zdelokalizowane
Benzen jest związkiem cyklicznym. Jego cząsteczka ma kształt
sześciokąta foremnego i jest płaska. Wiązania między atomami węgla
są jednakowej długości. Kąty między wiązaniami wynoszą 120 stopni.
Atomy węgla tworzące pierścień benzenowy połączone są wiązaniami
pojedynczymi oraz jednym wspólnym wiązaniem, które swym
zasięgiem obejmuje wszystkie sześć atomów węgla i nazywane jest
wiązaniem zdelokalozowanym.
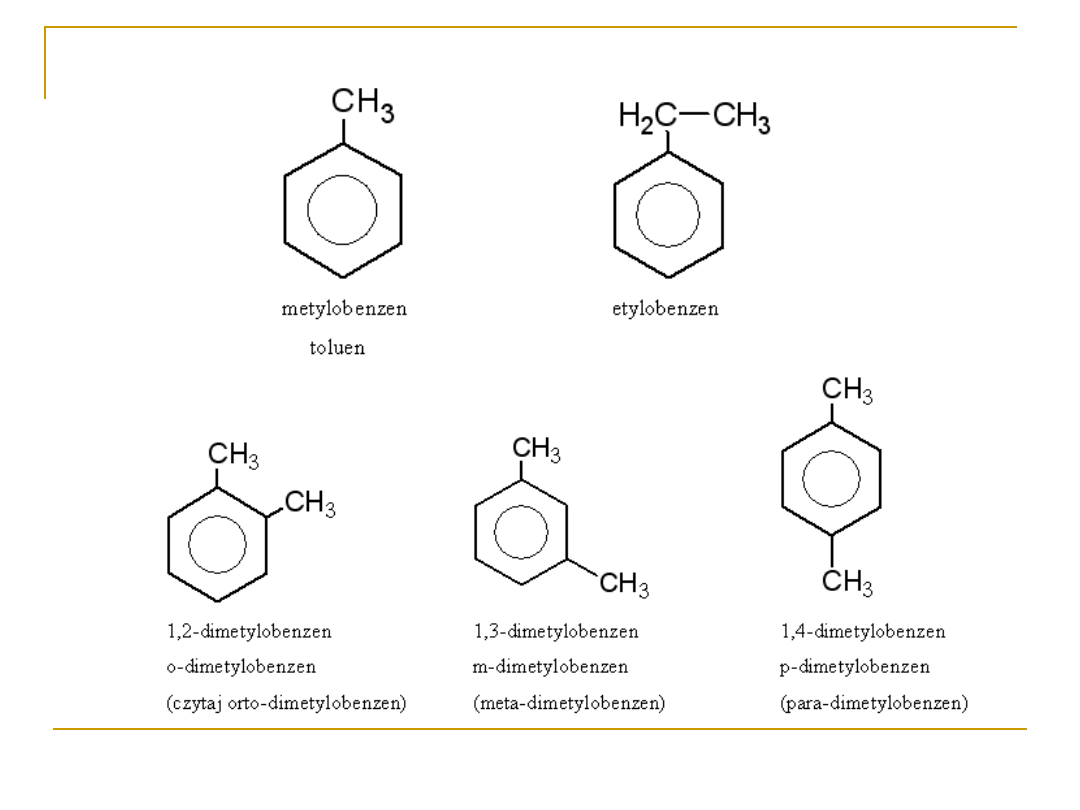
Ustalanie nazw systematycznych arenów i ich
pochodnych:
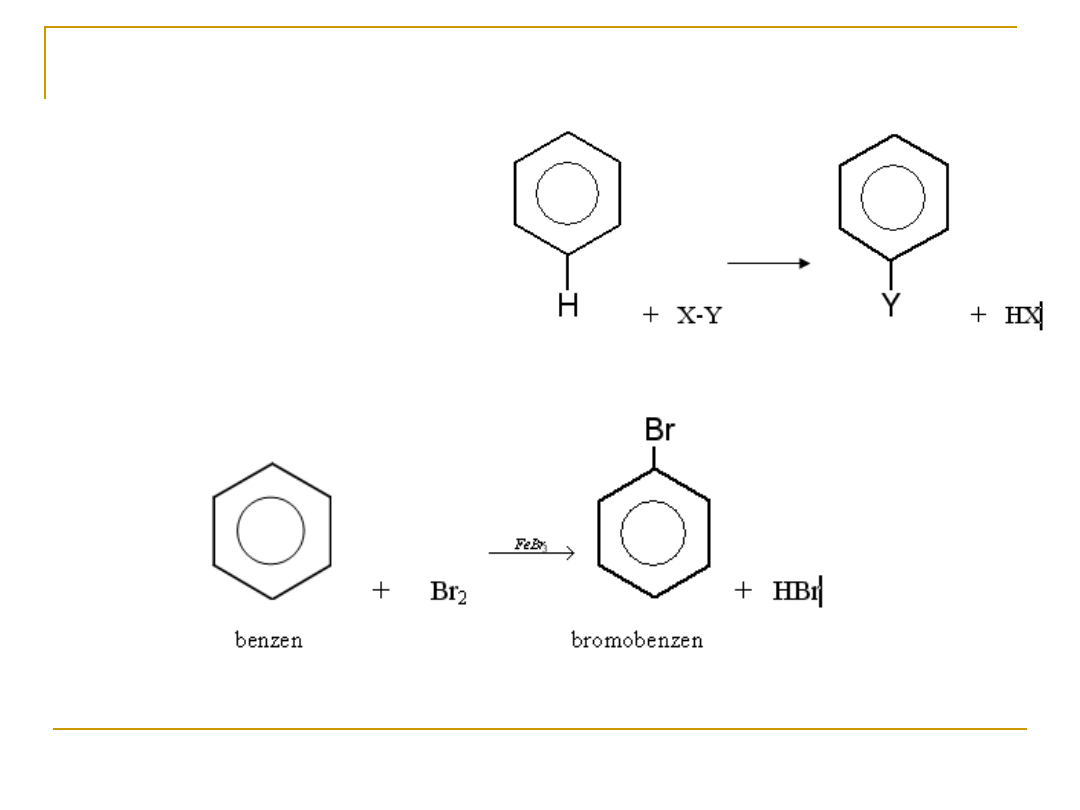
Właściwości chemiczne arenów:
1) reakcja z fluorowcem w obecności katalizatora
Pierścień aromatyczny benzenu
wykazuje wyjątkową trwałość,
dlatego benzen nie ulega łatwo
reakcjom addycji. Ulega
natomiast reakcjom
podstawienia (substytucji), w
których atom wodoru zostaje
zastąpiony innym atomem lub
grupą atomów:
HBr
Br
H
C
Br
H
C
FeBr
5
6
2
6
6
3
Właściwości chemiczne arenów:
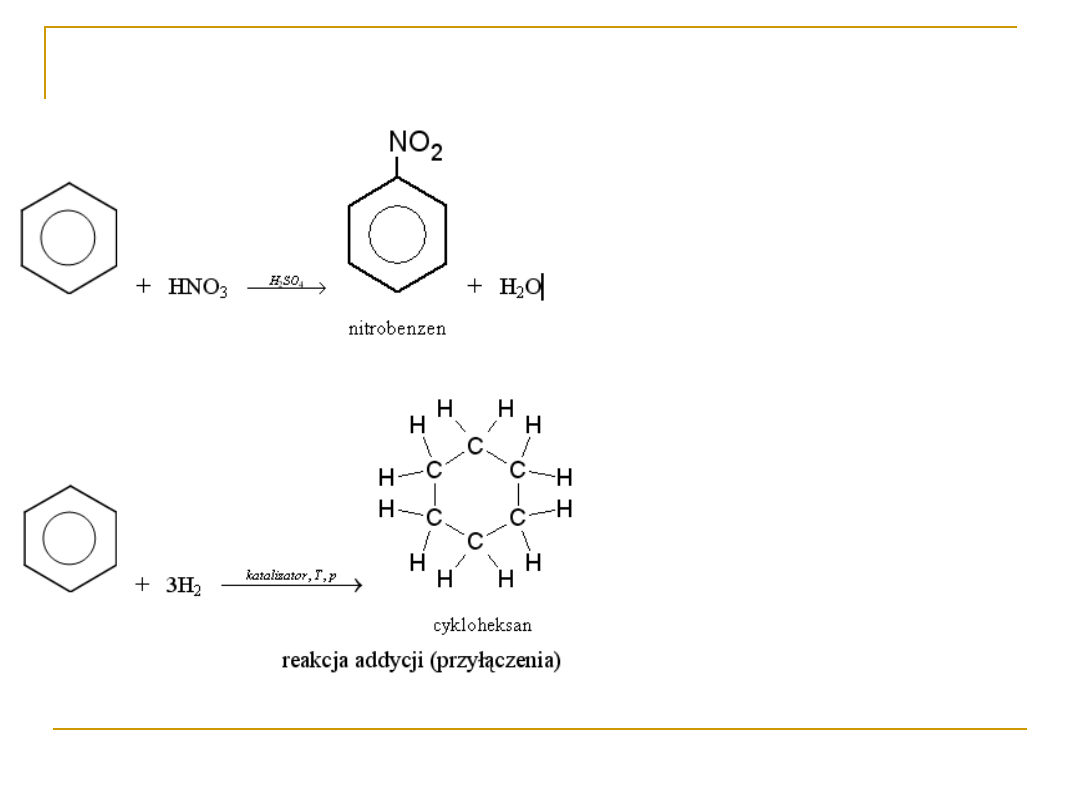
2) reakcja nitrowania:
O
H
NO
H
C
HNO
H
C
SO
H
2
2
5
6
3
6
6
4
2
3) reakcja uwodornienia:
12
6
,
,
2
6
6
3
H
C
H
H
C
p
T
r
katalizato
Areny ulegąją także reakcjom spalania

Wnioski i podsumowanie:
1. Areny są najprostszymi organicznymi
związkami aromatycznymi.
2. Najbardziej charakterystyczną reakcją arenów
jest reakcja substytucji.
3. Areny otrzymywane są głównie w wyniku
przeróbki smoły węglowej i ropy naftowej
4. Areny i ich pochodne są związkami trującymi i
rakotwórczymi
Document Outline
Wyszukiwarka
Podobne podstrony:
Weglowodory aromatyczne Areny
[Beata Świerkocka & Jacek Świerkocki] Węglowodory nasycone alkany
[Beata Świerkocka & Jacek Świerkocki] Alkeny węglowodory nienasycone
wyk 4 węglow aromat
WĘGLOWODORY AROMATYCZNE
BT węglowodory aromatyczne (wykład III)
kl 2, kartkowka-benzen, Benzen - C6H6 Wzór Elektronowy - 6¬¬C KL 1H K Węglowodory Aromatyc
Oznaczanie wybranych węglowodorów aromatycznych przy zastosowaniu chromatografii gazowej(1)
Węglowodory aromatyczne (2) ppt
węglowodory aromatyczne
otrzymywanie-i-reakcje-weglowodorow-aromatycznych
Powtórzenie węglowodory nienasycone i areny
Oznaczanie zawartości węglowodorów aromatycznych w paliwach dieslowych
10.Węglowodory aromatyczne, MATERIAŁY NA STUDIA, Chemia
16-WIELOPIERŚCIENIOWE WĘGLOWODORY AROMATYCZNE, kolo1
WĘGLOWODORY AROMATYCZNE
Węglowodory aromatyczne, chemia(2)
Biodegradacja węglowodorów aromatycznych, Naukowe PL, Biotechnologia, Enzymologia, Genetyka
otrzymywanie i reakcje weglowodorow aromatycznych
więcej podobnych podstron