Biochemia ćwiczenia
Należy pracować w rękawiczkach:
możliwość zakażenia i zatrucia substancjami badanymi lub używanymi odczynnikami (toksyny, bakterie, substancje radioaktywne)
możliwość zakażenia badanych materiałów przez osoby pracujące w laboratorium
Preparaty biochemiczne są nietrwałe możliwość namnażania bakterii
roztwory należy sterylizować
materiał biologiczny i roztwory przechowujemy w chłodni lub mrozimy
naczynia powinny być jednorazowe lub sterylizowane
Analiza chemiczna
Jakościowa - określenie składu badanej substancji
Reakcje charakterystyczne dla danego związku
Ilościowa - określenie ilości badanej substancji
Stężenia
mol/litr - M
mikromol/litr - uM
gram/litr - g/l
miligram/mililitr - mg/ml
C % = (masa substancji rozpuszczonej/masa roztworu) * 100%
Dysocjacja elektrolityczna
NaCl → Na+ + Cl-
H2O + H2O → H3O+ + OH-
Moc jonowa
gdzie: ci, zi - stężenie i ładunek jonu i,
Metody analityczne
Pierwszym etapem jest rozdział
Badaną substancje można wydzielić przez:
Zmiana mocy jonowej
Wysolenie siarczanem amonu (dodatek rzędu 10-100% nasycenia ((NH4)2SO4
Denaturacja - ogrzewanie lub dodanie czynnika denaturującego
Filtracja lub wirowanie
Chromatografia
Elektroforeza
Chromatografia
Polega na przepuszczaniu przez kolumnę roztworu białek. Kolumna jest to rura wypełniona złożem mającym taką właściwość że substancje w trakcie przepływu przez nią cieczy migrują z różną szybkością. Zbierając frakcje o określonej objętości dokonujemy rozdziału. Najpierw zbieramy substancje szybko migrujące przez kolumnę na na końcu te najwolniej migrujące
Kolumna chromatograficzna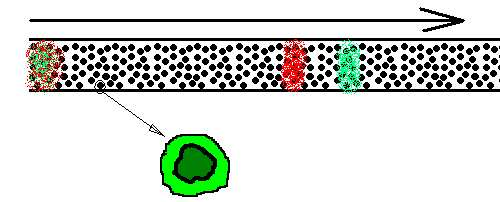
Elektroforeza
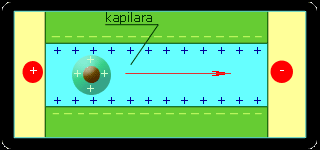
Analiza ilościowa i jakościowa
Metody ilościowe
Analiza wagowa
Miareczkowanie
Spektrofotometria
Metody elektrochemiczne, np. elektrody jonoselektywne
Metody Jakościowe
Reakcje charakterystyczne
Obecnie podstawowe metody analityczne związane są ze spektrofotometria
Spektrofotometria polega na pomiarze pochłaniania światła przez rozpuszczoną substancje.
Światło ma charakter korpuskularno falowy co oznacza ze zachowuje się jak fale ale zarazem jak cząstki energii.
Cząsteczki chemiczne maja ściśle określone poziomy energetyczne i mogą pochłaniać kwanty światła ściśle odpowiadające różnicom między tymi poziomami energetycznymi. Wynika z tego że dana substancja pochłania światło w bardzo specyficzny sposób,
Jeśli naświetlimy barwny roztwór białym światłem zawierającym wszystkie kolory, to zaobserwujemy ze część światła została pochłonięta co powoduje zmianę barwy światła po przejściu przez badany roztwór.
Roztwory miedzi maja kolor niebieski kobaltu różowy a niklu zielony.
Różne substancje pochłaniają światło przy różnych długościach fali,
alkohol etylowy pochłania fale świetlne w zakresie podczerwieni, na tej zasadzie działają profesjonalne mierniki stężenia alkoholu
Białka i nukleotydy (ATP, kwasy nukleinowe) pochłaniają fale świetlne w zakresie UV nadfioletu
Spektrofotometria
Są różne metody spektrofotometryczne, różniące się metodą pomiaru jak i długością fali przy której dokonujemy pomiarów.
Można mierzyć bezpośrednio badaną substancje na przykład roztwory białek przy długości fali 280 nm lub też kompleksy barwne na przykład oznaczenia fosforanów metodą fiske subarowa lub białek przeprowadzając reakcje barwną z biuretem a nastepnie oznaczając stężenie tworzącego się barwnego kompleksu
Można zbudować przyrząd , spektrofotometr wytwarzający światło monochromatyczne o jednej barwie , jednej długości fali a następnie zmieniać długość fali wytwarzanego światła.
Jeśli takie światło przepuścimy przez badaną substancje i będziemy rejestrować zmiany pochłaniania tego światła w zależności od długości fali to otrzymamy widmo absorpcyjne danej substancji.
Ponieważ wiadomo co jak absorbuje światło to z takiego widma można zorientować się co zawiera badana próbka. I tak białka absorbują w nadfiolecie przy długości fali ok. 280 nm (UV) a kwasy nukleinowe przy 260 nm (UV). Takie widma pozwalają określić skład i stężenie zawartych w roztworze substancji.
Spektrofotometr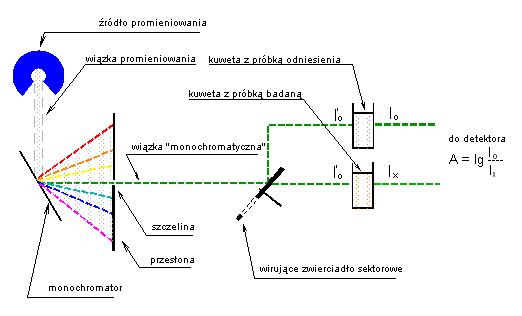
Widmo absorpcyjne
Widmo jest to graficzny zapis zmian wartości absorbancji w zależności od długości fali przechodzącej przez badany roztwór. Głównymi parametrami widma są:
a - położenie pasm (wartość długości fali przy których na widmie można wyróżnić maksima; lmax)
b - molowy (lub właściwy) współczynnik absorpcji związany z danym maksimum.
Transmitancja i absorbancja
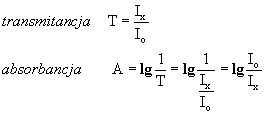
Jeśli badany roztwór pochłonie 90% promieniowania o danej długości fali, to powiemy, że jego transmitancja wynosi 10%, zaś absorbancja będzie wynosić lg(100/10)=1
Prawo Lamberta Beera
A = e·c·l
c =A/(e*l)
Ponieważ l = 1cm można zapisać c =A/e
e - molowy współczynnik absorpcji, równy liczbowo absorbancji, która wystąpiłaby, gdybyśmy mierzyli w danych warunkach roztwór o stężeniu 1 mol/dm3 przy grubości warstwy równej 1 cm;
c - stężenie mierzonego roztworu w mol/dm3;
l - grubość warstwy roztworu w cm.
Prawo Lamberta Beera
A = e·c·l
c =A/(e*l)
Ponieważ l = 1cm można zapisać c =A/e
e - molowy współczynnik absorpcji, równy liczbowo absorbancji, która wystąpiłaby, gdybyśmy mierzyli w danych warunkach roztwór o stężeniu 1 mol/dm3 przy grubości warstwy równej 1 cm;
c - stężenie mierzonego roztworu w mol/dm3;
l - grubość warstwy roztworu w cm.
Najczęściej używa się wspólczynnika absorpcji wyrażonego w jednostkach w jakich wyrażamy stężenia badanych substancji. Dla białek są to mg/ml a nie mole
Prawo addytywności absorpcji
Absorpcja roztworu wieloskładnikowego równa się sumie absorbancji poszczególnych składników:
A = A1 + A2 + … AnGdzie: A1, A2, …, An są to absorbancje poszczególnych składników.
Pomiary spektrofotometryczne
Najczęściej pomiary prowadzi się w kuwetach pomiarowych o długości drogi optycznej 1 cm, często kuwety nie są symetryczne i należy wkładać je do spektrofotometru we właściwy sposób
Kuwety muszą być wykonane z materiału nie pochłaniającego promieniowania w zakresie długości fali przy których dokonujemy pomiaru.
Dla nadfioletu (UV) używamy tylko kuwet kwarcowych oznaczonych literą Q, kuwety plastikowe lub szklane pochłaniają promieniowanie co uniemożliwiłoby pomiary
Najprościej byłoby zmierzyć absorpcje podzielić przez współczynnik absorpcji i odczytać stężenie. W praktyce jest to niemożliwe bo roztwory pochłaniają światło w niespecyficzny sposób na skutek zmętnienia co więcej zawierają zanieczyszczenia np. ATP związek chemiczny bardzo mocno pochłaniający promieniowanie w zakresie nadfioletu (UV)
Posługujemy się zmodyfikowanym wzorem do oznaczania stężenia
Abs(specyficzna) -Abs (niespecyficzna)
C= ---------------------------------------
współczynnik absorbcji
Najprościej byłoby zmierzyć absorpcje podzielić przez współczynnik absorpcji i odczytać stężenie. W praktyce jest to niemożliwe bo roztwory pochłaniają światło w niespecyficzny sposób na skutek zmętnienia co więcej zawierają zanieczyszczenia np. ATP związek chemiczny bardzo mocno pochłaniający promieniowanie w zakresie nadfioletu (UV)
Często oznaczamy nie bezpośrednio daną substancje a powstający w reakcji z nią barwny związek w takich wypadkach należy zastosować krzywą wzorcową gdyż reakcja barwna może zachodzić w różnym stopniu (odczynniki się starzeją)
Przygotowujemy roztwór jak najbardziej zbliżony do roztworu badanego a następnie przygotowujemy kilka próbek zawierających mierzoną substancje o wzrastających stężeniach. dodajemy mierzoną substancje po zmierzeniu absorpcji rysujemy zależność absorpcji od stężenia i otrzymujemy krzywą wzorcową.
Krzywe wzorcowe
Roztwory wzorcowe powinny mieć podobny skład do próbki
Krzywa wzorcowa powinna składać się co najmniej z czterech punktów
Stężenia roztworów wzorcowych powinny być zbliżone do stężenia badanej próbki
1. Struktura pierwszorzędowa - czyli najniższy poziom organizacji strukturalnej cząsteczki jest wyznaczona przez sekwencję aminokwasów w łańcuchu polipeptydowym. Jest ona uwarunkowana jeszcze zanim zostanie zsyntetyzowany łańcuch polipeptydowy, gdyż informacja o kolejności aminokwasów w cząsteczce białka jest zakodowana w DNA, w postaci sekwencji nukleotydowej. Dzięki procesom transkrypcji, a później translacji sekwencja nukleotydowa zostaje odczytana w trakcie syntezy odpowiedniego polipeptydu.
Czy mutacje są potrzebne?
2. Struktura drugorzędowa - są to typy regularnego ułożenia głównego łańcucha polipeptydowego stabilizowane wiązaniami wodorowymi. Odkryto dwa podstawowe, regularne układy drugorzędowe występujące powszechnie w strukturze białek. Są to struktury a -helisy i b -harmonijki.
a -helisa
Struktura a -helisy ma kształt cylindra. Ciasno spleciony łańcuch główny polipeptydu tworzy centralną część cylindra, natomiast boczne łańcuchy reszt aminokwasowych wystają na zewnątrz w ułożeniu helikalnym.
Struktura a -helisy jest stabilizowana wiązaniami wodorowym grup NH i CO głównego łańcucha. Grupa CO każdego aminokwasu wiąże się wiązaniem wodorowym z grupą NH, aminokwasu odległego do przodu o cztery reszty aminokwasowe i leżącego bezpośrednio nad nią. Rezultatem tego jest fakt, że wszystkie grupy CO i NH łańcucha głównego są połączone wiązaniem wodorowym.
Budowa a-helisy 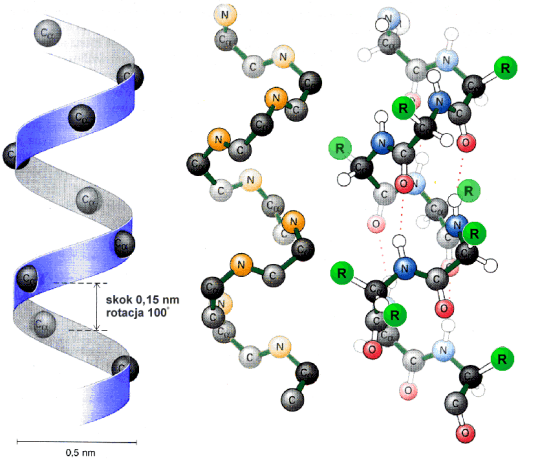
Struktura b -harmonijki (b -kartki)
Struktura b -harmonijki (b -kartki) - W odróżnieniu od cylindrycznej struktury a -helisy, cząsteczka polipeptydu przyjmuje kształt, prawie całkowicie rozciągnięty.
W uformowaniu struktury b -harmonijki, może brać udział więcej niż jeden łańcuch polipeptydowy.
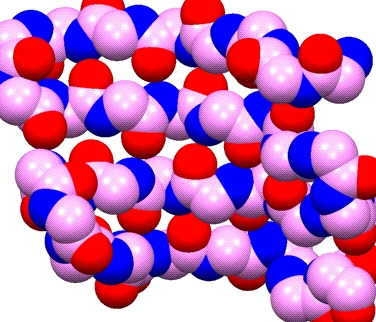
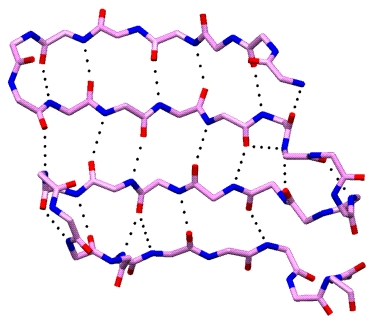
Struktura trzeciorzędowa
Czynniki stabilizujące strukturę trzeciorzędową białek
Wiązania wodorowe
Oddziaływania hydrofobowe
Wiązania jonowe
Kowalencyjne mostki dwusiarczkowe
Oddziaływania międzycząsteczkowe
Struktura czwartorzędowa
Struktura czwartorzędowa powstaje po przez łączenie się kilku podjednostek białkowych.
Stabilizują ją te same siły co strukturę trzeciorzędową
Krwinki czerwone
Najbardziej znane elementy morfotyczne krwi to krwinki czerwone, czyli erytrocyty. W jednym milimetrze sześciennym znajduje się średnio 5,4 miliona erytrocytów u mężczyzn i 4,8 miliona u kobiet.
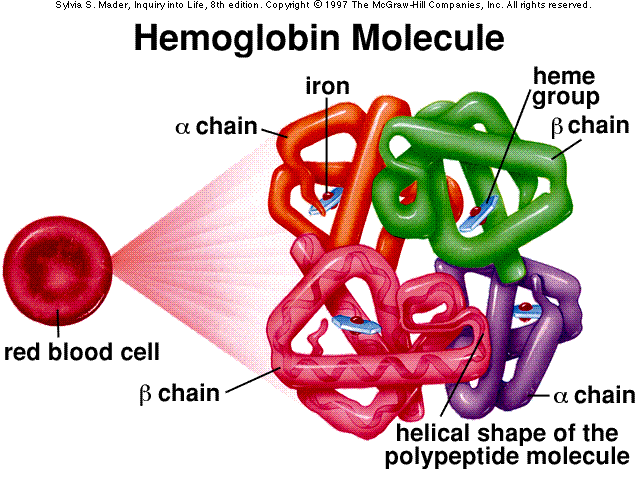
Ich główną rolą jest przenoszenie tlenu z płuc do tkanek. Te funkcje zapewnia obecność hemoglobiny - czerwonego barwnika krwi. Hemoglobina składa się z białka - globiny - oraz z czterech cząsteczek hemu. W hemie ważny jest atom żelaza, który wiąże się z jedną cząsteczką tlenu, tworząc oksyhemoglobinę. Żelazo posiada tę zdolność jedynie na drugim stopniu utlenienia; karboksyhemoglobina, tworząca się z połączenia hemu z tlenkiem węgla. Ten ostatni związek wypiera tlen z oksyhemoglobiny, czyniąc hemoglobinę bezużyteczną.
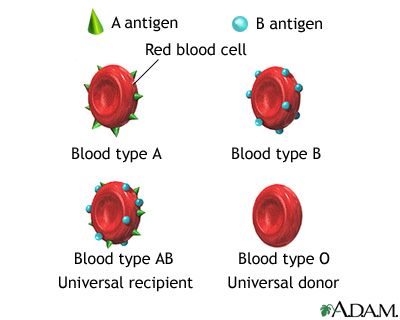
Krwinka
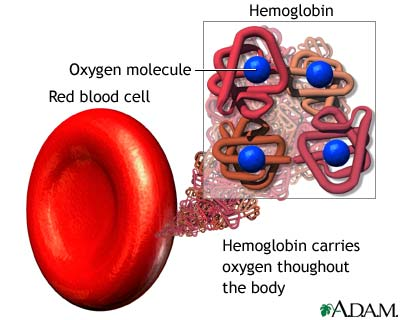
Budowa hemoglobiny
Hem
Cztery wiązania koordynacyjne atomu żelaza wiążą się z 4 azotami grup pierścieni pirolowych piąte z tlenem a szóste z białkiem przez pierścień imidazolowy histydyny
Regulacja allosteryczna polega na wiązaniu aktywatora lub inhibitora enzymu w innym miejscu niż następuje wiązanie substratu
Mioglobina i hemoglobina
Mioglobina jest białkiem wiążącym i magazynującym tlen. Największe jej stężenie znajduje się w mięśniach szkieletowych odpowiedzialnych za ruch oraz w sercu.
Mioglobina jest niewielkim białkiem globularnym o masie około 18 kDa. Nie ma budowy podjednostkowej,
Hemoglobina jest białkiem allosterycznym
Wiązanie tlenu z jedną z podjednostek, wpływa na oddziaływanie pozostałych podjednostek z tlenem. Po związaniu pierwszej cząsteczki tlenu do pierwszej kolejne cząsteczki tlenu przyłączają się coraz łatwiej
Wiązanie tlenu przez mioglobinę i hemoglobinę
Mioglobina najmocniej wiąże tlen przy niskim wysyceniu tlenem
Hemoglobina wiąże tlen słabo przy niskim wysyceniu tlenem a przy większym wysyceniu tlenem wiąże tlen mocno
Efekt Bohra
W zależności od pH zmienia się powinowactwo tlenu do hemoglobiny.
W pracujących mięśniach pH się obniża (środowisko ulega zakwaszeniu) co ułatwia dysocjację tlenu.
Siła wiązania tlenu w środowisku kwaśnym jest mniejsza niż w zasadowym.
Hemoliza krwi
Krwinka czerwona zawiera 280mln cząsteczek hemoglobiny
Umieszczenie krwinek w czystej wodzie prowadzi do pękania błony krwinek czerwonych i uwolnienia cząsteczek hemoglobiny
W roztworze izotonicznym błonę można usunąć rozpuszczając ją w rozpuszczalnikach organicznych (eter aceton)
Wpływ tlenu na absorpcje światła przez hemoglobinę
Hemoglobina pochłania światło w zależności od stopnia utlenowania
Po związaniu tlenu absorbuje światło przy 578 nm i 540 nm (żółta i zielona barwa)
Po uwolnieniu tlenu (warunki redukujące roztworu np.. Dodatek dwutionianu sodu) ma barwę czerwono fioletową 565 nm
Hemoglobina wiąże 300 razy mocniej tlenek węgla i absorbuje światło przy 572 nm i 535 nm
Ilościowe oznaczanie hemoglobiny
Odczynniki
0,04% NH3
Na2S2O4 (dwutionian sodu - reduktor))w stanie stałym
Krew z opuszka palca 0,1 ml wprowadzić do 9,9 ml 0,04% roztworu NH3, Następnie dodać kilka kryształków Na2S2O4. Powstaje fioletowe zabarwienie.
Oznaczać względem wody przy 570 nm spektrofotometrycznie.
Równolegle zmierzyć absorpcje wzorcowego roztworu hemoglobiny. Stężenie hemoglobiny liczyć według wzoru
Apróby
Chemoglobiny= Chwzorca *---------------
A wzorca
Amoniak dodany by przeciwdziałać wytrącaniu się białek
Oznaczanie hemoglobiny na podstawie zawartości żelaza
Odczynniki
Cząsteczka hemoglobiny zawiera 0,34% Żelaza. Z ilości żelaza można obliczyć zawartość hemoglobiny
Odczynniki
72% roztwór HClO4
Perhydrol
25% roztwór amoniaku
20% roztwór kwasu sulfosalicylowego
Roztwór wzorcowy żelaza10 μg/ml. Rozpuścić 86,3 mg
12 hydratu siarczanu żelazowo-amonowego w wodzie z dodatkiem 10 ml stężonego H2SO4 i uzupełnić wodą do1000 ml.
Wykonanie
Do probówki wprowadzić 0,05 ml krwi następnie dodać0,2 ml HClO4 i 0,2 ml perhydrolu. Ogrzewać na wrzącej łażni wodnej do całkowitego odbarwienia roztworu. Po mineralizacji dodać 0,5 ml 20% roztworu kwasu sulfosalicylowego i 1 ml roztworu NH3 uzupełnić wodą do 5 ml i oznaczać absorbancje przy 420 nm wobec próby kontrolnej (skład ten sam ale bez krwi)
Oznaczenia w roztworach wzorcowych żelaza analogicznie jak w badanej próbie
Apróby
μg Fe w próbie=------------------μg Fe w roztworze wzorcowym
Awzorca
Obliczenie stężenia hemoglobiny we krwi
Apróby
Hb [%] =------------------ * (μg Fe w roztworze wzorcowym)* 0,59
Awzorca
Trawienie białek
Żołądek
Sok żołądkowy (kwas solny)
Denaturacja białek
Pepsyna A ( dno żołądka)
Pepsyna B (część odźwiernikowa)
Rozkładają zdenaturowane białko do dużych
polipeptydów, hydrolizują wiązania peptydowe
utworzone przez aminokwasy aromatyczne, dikarboksylowe
Trzustka
Trypsyna
działa swoiście na wiązania peptydowe utworzone przez aminokwasy zasadowe
Chymotrypsyna
działa swoiście na wiązania peptydowe utworzone przez aminokwasy pozbawione ładunku elektrycznego(np. a. aromatyczne)
Elastaza
działa na wiązania peptydowe utworzone przez małe aminokwasy (glicynę, alaninę, serynę)
Karbosypeptydaza
działa na C-końcowe wiązania peptydowe
Jelito cienkie
Aminopeptydaza
działa na N-końcowe wiązania peptydowe
Dipeptydazy
rozkladają dipeptydy do wolnych aminokwsów
Wchłanianie aminokwasów
Wchłanianie odbywa się poprzez transport aktywny
Transportowane są naturalne izomery aminokwasów
W transporcie uczestniczy witamina B6 (fosforan pirydoksalu)
Aminokwasy transportowane są przez rąbek szczoteczkowy (miejsce wchłaniania: jelitoczcze)
Aminokwasy egzogenne
Aminokwasy egzogenne (nazywane też aminokwasami niezbędnymi - jest to grupa aminokwasów, które nie mogą być syntetyzowane w organizmie zwierzęcym i muszą być dostarczane w pożywieniu, w przeciwieństwie do aminokwasów endogennych. Żywienie pokarmami ubogimi w aminokwasy niezbędne może doprowadzić do zaburzeń chorobowych. Do aminokwasów niezbędnych dla człowieka zalicza się 10 aminokwasów egzogennych
Aminokwasy niezbędne
egzogenne
Histydyna (His)
Arginina (Arg)
Izoleucyna (Ile)
Leucyna (Leu)
Lizyna (Lys)
Metionina (Met)
Fenyloalanina (Phe)
Treonina (Thr)
Tryptofan (Trp)
Walina (Val
Aminokwasy endogenne
Aminokwasy endogenne - to aminokwasy, które organizm zwierzęcy może syntetyzować samodzielnie, w przeciwieństwie do aminokwasów egzogennych, które musi przyjmować systematycznie wraz z pożywieniem.
Aminokwasy nie niezbędne
endogenneAlanina (Ala)
Asparagina (Asn)
Kw. asparaginowy (Asp)
Cysteina (Cys)
Glutamina (Gln)
Kw. glutaminowy (Glu)
Glicyna (Gly)
Prolina (Pro)
Seryna (ser)
Tyrozyna (Tyr)
aminokwasy nie mogą być magazynowane,
nadmiar aminokwasów jest na bieżąco przerabiany, wykorzystywany na potrzeby energetyczne
grupa aminowa jest odłączana
szkielet węglowy jest przekształcany w acetylokoenzymA (acetylo-CoA) pirogronian lub jeden z intermediatów cyklu Krebsa
Z aminokwasów mogą powstawać kwasy tłuszczowe, ciała ketonowe lub glukoza
Wydalanie jest procesem fizjologicznym polegającym na usuwaniu z organizmu szkodliwych produktów przemian związków azotowych (amoniak,mocznik,kwas moczowy),dwutlenku węgla oraz wody i nadmiaru soli mineralnych i innych związków zbędnych dla organizmu.
Nadmiar azotu może być wydalany przez zwierzęta jednym z trzech sposobów:
W postaci amoniaku (zwierzęta wodne)
W postaci kwasu moczowego (ptaki)
W postaci mocznika - dotyczy ludzi
Wśród aminokwasów wyróżnić można zasadniczo na trzy grupy.
(1) Te, które w procesie spalania dochodzą do acetylo-CoA,
(2) te, które w procesie spalania dochodzą do pirogronianu
(3) te, które przekształcają się do któregoś ze związków pośrednich cyklu Krebsa
Taki podział aminokwasów wynika z odmiennych losów, jakie mogą te aminokwasy spotkać.
Aminokwasy metabolizujące się bezpośrednio do acetylo-CoA mogą ulec tylko i wyłącznie spaleniu.
Aminokwasy metabolizujące się do pirogronianu lub związków cyklu Krebsa mogą zamieniać się na glukozę i po wejściu w cykl pentozowy dostarczać wodoru do syntezy kwasów tłuszczowych i cholesterolu.
Wydajność energetyczna aminokwasów
Zakładając, że proporcje pomiędzy poszczególnymi aminokwasami są takie, jak to przedstawiono w tabeli, ze 100g białka można uzyskać łącznie 22.5 mola ATP. Jest to wartość porównywalna z węglowodanami, gdzie, ze 100g glukozy uzyskuje się 21 moli ATP.
Zakładając maksymalną sprawność zamiany białka na glukozę. Ze 100g białka uzyskać można 69g glukozy. (Wartość ta zależy oczywiście od proporcji aminokwasów w danym białku.)
Transaminacja
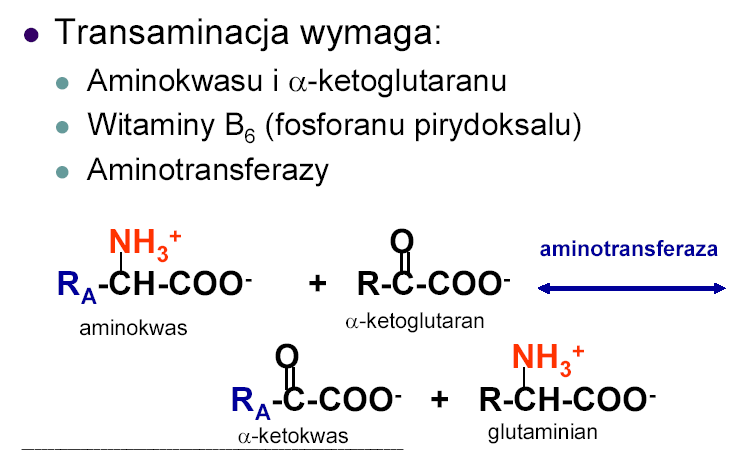
Wyjątki

Oksydacyjna deaminacja glutaminianu
NAD -Dinukleotyd nikotynoamidoadeninowy
Jedna cząsteczka NADH pozwala wyprodukować 2,5 cząsteczki ATP
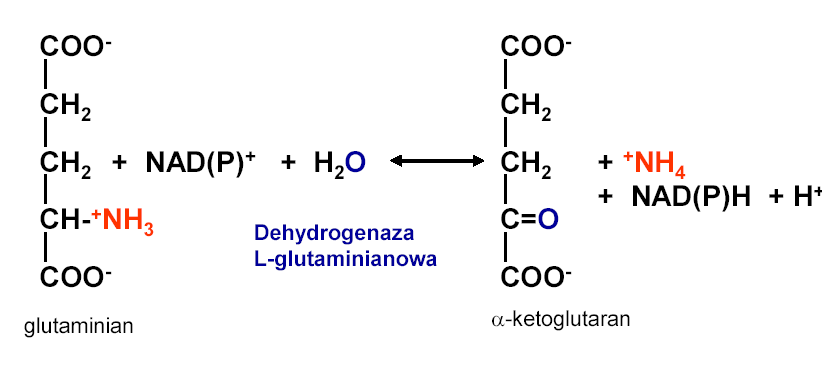
NAD i
NADP
CYKL MOCZNIKOWY
Rozpoczyna się od połączenia wolnych jonów NH4+ i HCO3 - w wyniku czego powstaje karbamoilofosforan.
Reakcja katalizowana jest przez syntetazę karbamoilofosforanową, jest praktycznie nieodwracalna bo zużyciu ulegają dwie cząsteczki ATP
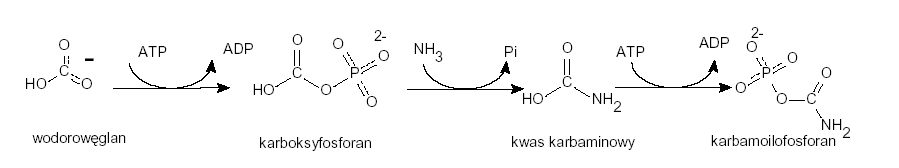
Grupa karbamoilowa karbamoilofosforanu, ze względu na obecność wiązania bezwodnikowego, charakteryzuje się wysokim potencjałem przenoszenia. W reakcji katalizowanej przez
karbamoilotransferazę ornitynową jest ona przenoszona na ornitynę (atom azotu), co prowadzi do powstania cytruliny.
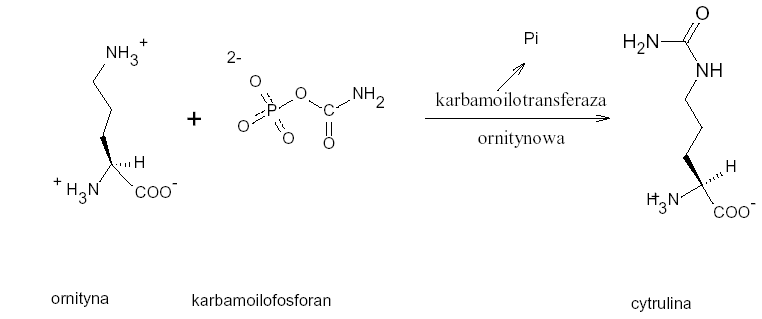
Cytrulina ulega kondensacji z asparaginianem, kosztem energii hydrolizy ATP do AMP i PPi (pirofosforanu), który jest donorem drugiej grupy aminowej włączanej do mocznika.
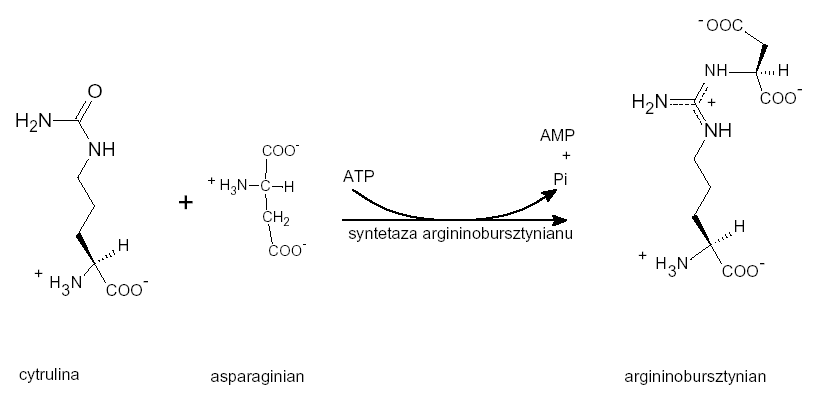
Liaza argininobursztynianowa rozszczepia cząsteczkę argininobursztynianu do argininy i fumaranu.
W ten sposób łańcuch węglowy asparaginianu zostaje zachowany w postaci fumaranu.
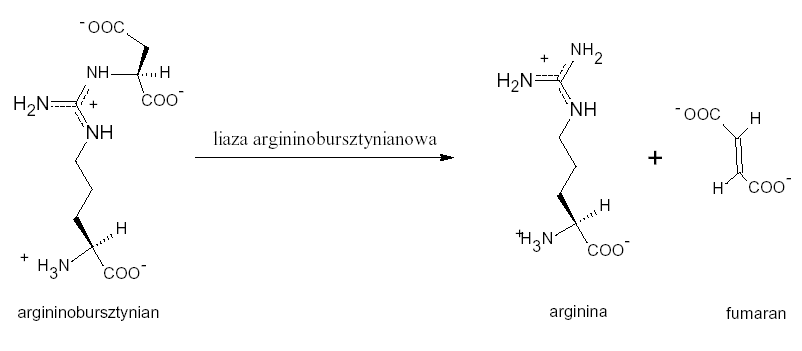
Ostatecznie argininę hydrolizuje arginaza, powstaje mocznik i ornityna. Ornityna jest transportowana z powrotem do mitochondrium gdzie rozpoczyna się kolejny cykl. Mocznik powstały w wyniku cyklu mocznikowego jest wydalany. Człowiek w ciągu roku wydala około 10 kg mocznika.
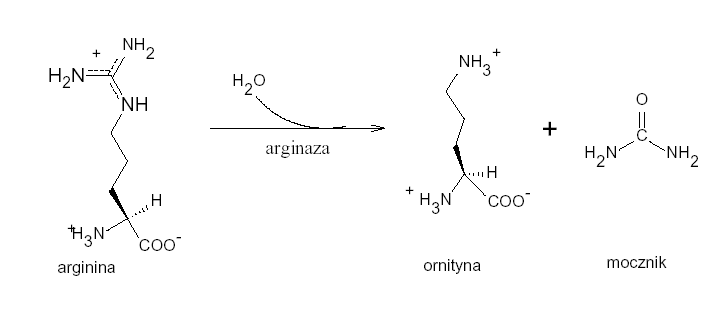
Sumaryczny zapis reakcji cyklu mocznikowego
CO2 + NH4+ + 3 ATP + asparaginian + 2 H2O
mocznik + 2 ADP + 2 Pi + AMP + PPi + fumaran
Schemat cyklu mocznikowego
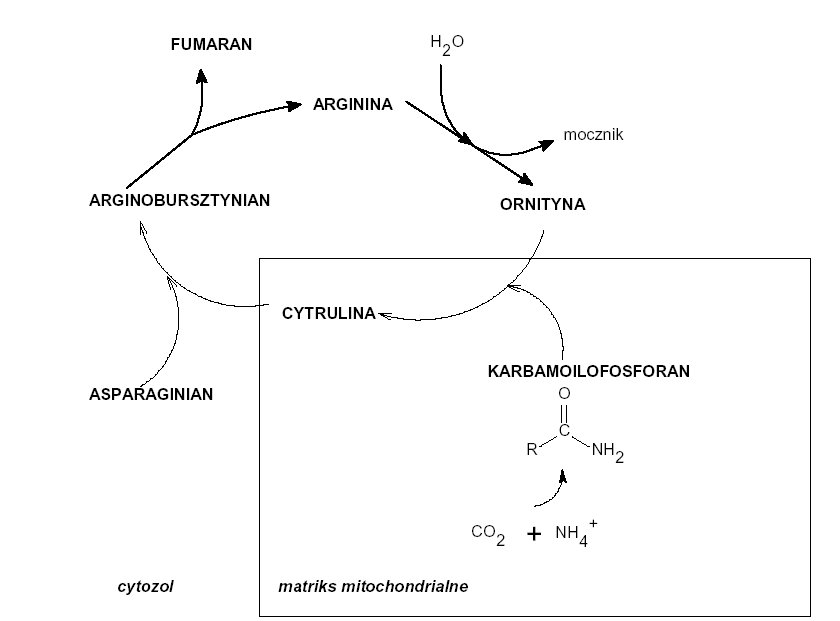
MOCZNIK Jest to główny końcowy metabolit przemiany białkowej. Stężenie mocznika we krwi jest wypadkową produkcji która zachodzi wyłącznie w wątrobie i nerkowego wydalania, zwiększa się ona wraz z wiekiem.
ZAKRES WARTOŚCI PRAWIDŁOWYCH
Norma dla mocznika 2,5-6,4 mmol/l lub 15 - 39 mg/100ml
WARTOŚCI PODWYŻSZONE
Zwiększenie stężenia mocznika jest prawie zawsze dowodem upośledzonej czynności wydalniczej nerek.
- dieta bogata w białka
- nadmierny katabolizm białek w ustroju (gorączka, posocznica)
- krwawienie do przewodu pokarmowego
- niewydolność nerek
- niewydolność pozanerkowa np. zwężenie moczowodów.
Oznaczanie mocznika metodą ureazową
Surowicę lub krew pełną zadaje się ureazą która rozkłada mocznik na amoniak. Po strąceniu białek wprowadza się odczynnik Nesslera dający z amoniakiem żółte zabarwienie w wyniku tworzenia się jodku amidortęciowego(II)
2K2HgI4 + 3NaOH + NH4OH რ O(Hg2)NH2I +4KI +3NaI +3H2O
odczynniki
preparat ureazy
3% roztwór Na2SO4
10% roztwór ZnSO4
0,5 M roztwór NaOH
wzorcowy roztwór NH4Cl zawierający 0,01 mg N w 1 ml ( 25 ml roztworu NH4Cl o stężeniu 1,53 mg/ml + 10 ml 1 M H2SO4 dopełnić do 1 l)
odczynnik Neslera
w kolbie rozpuścić 30 g KI dodać 22g jodu + 30 g metalicznej rtęci.
Mieszaninę wstrząsać . zdekantować roztwór znad metalicznej rtęci. I uzupełnić wodą do 400 ml.
Roboczy odczynnik Neslera: do75 ml roztworu macierzystego dodać 75 ml wody i 350 ml 10% NaOH. Powstały po kilku dniach osad odwirować. Klarowny roztwór używać do oznaczeń. Przechowywać w ciemnej butelce.
Fenyloketonuria
Fenyloketonuria jest chorobą genetyczną spowodowana mutacją genu kodującego enzym hydroksylaze fenyloalaninową
Chorobę rozpoznaje się u ok. 1 na 15000 dzieci, ale częstość jej występowania jest różna w różnych populacjach
.
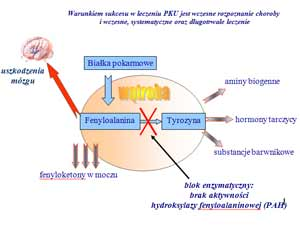
Mutacja powoduje upośledzenie aktywności enzymatycznej PAH, który katalizuje przekształcanie w organizmie aminokwasu fenyloalaniny w inny aminokwas tyrozynę. We krwi dziecka chorego na fenyloketonurię zaczyna gromadzić się fenyloalanina i produkty jej metabolizmu, przy względnym niedoborze tyrozyny. Na skutek tego po pewnym czasie i przy braku odpowiedniego leczenia dochodzi do uszkodzenia mózgu. Szkodliwe produkty są szczególnie niebezpieczne dla układu nerwowego podczas jego rozwoju. Dlatego wśród dzieci robi się testy na fenyloketonurie. Obecnie sądzi się że również dla dorosłych te metabolity są niezdrowe.
Mechanizm fentloketonurii
Dziedziczenie fenyloketonurii
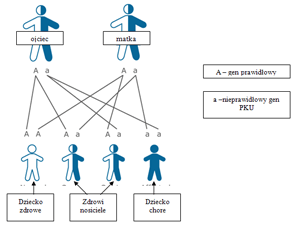
Choroba dziedziczy się w sposób autosomalny recesywny - oznacza to, że dziecko musi odziedziczyć wadliwy allel od obojga rodziców, żeby rozwinęła się choroba. Chorobę rozpoznaje się u ok. 1 na 15000 dzieci, ale częstość jej występowania jest różna w różnych populacjach.
Glukoza
Naszym źródłem energii jest pokarm. Energię kumulują wszystkie podstawowe składniki pożywienia - białka, tłuszcze i węglowodany.
Głównym paliwem organizmu pozostaje tylko jeden z nich - glukoza - cukier pochodzący z przemian niemal wszystkich strawnych węglowodanów.
Po poziomie glukozy organizm rozpoznaje dostatek lub deficyt energetyczny.
Glukoza jest głównym źródłem energii dla naszego mózgu. Mózg zawsze potrzebuje glukozy.
Homeostaza glukozy
Homeostaza glukozy jest wypadkową dopływu glukozy do krwi oraz jej zużycia w komórkach, ważną rolę w jej utrzymaniu odgrywają procesy metaboliczne w mięśniach szkieletowych i wątrobie.
Wpływ na przebieg procesów metabolicznych w tkance mięśniowej wywiera wiele czynników, wśród nich są czynniki genetyczne, regulacja hormonalna a także stężenie substratów. Wśród hormonów biorących udział w tej regulacji najważniejszymi są insulina i glukagon.
Glukoneogeneza
Glukoneogeneza to enzymatyczny proces tworzenia przez organizm glukozy z metabolitów nie będących węglowodanami, np. aminokwasów, glicerolu czy mleczanu. Głównym substratem jest pirogronian.
Glikogenoliza
Glikogenoliza - rozkład glikogenu do glukozo-6-fosforanu (w mięśniach) lub do glukozy (w wątrobie) powodujący uzupełnienie chwilowego niedoboru glukozy w różnych tkankach organizmu m.in. we krwi. Proces pobudzany przez adrenalinę i glukagon.
Insulina
Insulina to hormon peptydowy o działaniu ogólnoustrojowym, odgrywający zasadniczą rolę w metabolizmie węglowodanów, lecz także białek i tłuszczów.
Nazwa insulina z łac. insula - wyspa, pochodzi od wysepek Langerhansa trzustki, gdzie insulina jest produkowana.Insulina produkowana jest przez komórki β (komórki B) wysp trzustki. Najważniejszym bodźcem do produkcji insuliny jest poposiłkowe zwiększenie stężenia glukozy we krwi. Insulina sygnalizuje stan nasycenia substratami energetycznymi i stymuluje ich magazynowanie oraz syntezę białek
Stymuluje syntezę glikogenu w mięśniach i wątrobie
Przyspiesza w wątrobie glikolizę co zwiększa syntezę kwasów tłuszczowych.
Powoduje wnikanie glukozy do mięśni i tkanki tłuszczowej
Glukagon
to hormon produkowany w trzustce przez komórki alfa o działaniu przeciwstawnym do insuliny, podwyższający poziom glukozy we krwi. Działa głównie na wątrobę
Stymuluje rozkład glikogenu i glukoneogenezę
Inhibuje syntezę kwasów tłuszczowych , glikolizę
W czasie wysiłku fizycznego dochodzi do zwiększonego wykorzystywania substratów energetycznych, zwiększone zostaje ich uwalnianie z magazynów tkankowych i udostępnianie do przemian.
Głównym substratem energetycznym, zwłaszcza w pierwszym etapie pracy mięśniowej, jest glukoza pochodząca z glikogenu, krążąca we krwi oraz syntetyzowana w wątrobie. Jednakże zapasy glukozy zmagazynowane w formie glikogenu w mięśniach i wątrobie nie są zbyt duże i przy dłużej trwającym wysiłku fizycznym szybko ulegają całkowitemu wyczerpaniu.
Po zakończeniu pracy następuje resynteza glikogenu, który to proces jest stymulowany przez insulinę
Regulacja poziomu glukozy w organizmie
Regulacja poziomu glukozy we krwi związana jest z pracą trzustki, która wytwarza insulinę (pobudzającą przetwarzanie glukozy w glikogen i ułatwiającą transport glukozy z krwi do komórek) oraz glukagon (wytwarzany przez wysepki Langerhansa i pobudzający rozkład glikogenu do glukozy), a także z wątrobą i mięśniami tak jak wątroba magazynującymi nadmiar glukozy w postaci glikogenu: w przypadku niedoboru glukozy zmagazynowany w wątrobie i mięśniach glikogen zostaje szybko rozłożony do glukozy.
Nadmiar węglowodanów jest przekształcany w organizmie człowieka w tłuszcze i magazynowany w tkance podskórnej.
Poziom glukozy we krwi
Tkanką, która zawsze potrzebuje glukozy jest mózg, dlatego zachowanie homeostazy tego cukru jest ważne dla prawidłowej pracy organizmu.
We krwi stężenie glukozy wynosi ok. 90mg na 100cm3. W czasie intensywnego wysiłku fizycznego jej stan może spaść nawet do 70mg/100cm3, jednak dopiero spadek poziomu tego cukru poniżej 60mg jest określany, jako hipoglikemia i staje się niebezpieczny.
Gdy stan obniżonego poziomu glukozy utrzymuje się dłużej następuje hiperglikemia (odbicie organizmu na skutek niskiego poziomu glukozy, mechanizmy kompensujące, głównie hormon wzrostu powoduje wzrost poziomu cukru we krwi), której objawami są drgawki, utrata przytomności, a często również odwodnienie organizmu i groźne w skutkach zaburzenie ciśnienia krwi.
hipoglikemia
Organizm w czasie hipoglikemii jest zmobilizowany, aby dostarczyć do mózgu jak najwięcej glukozy, gdyż nie gromadzi on zapasów glukozy jak np. wątroba lub mięśnie, by korzystać z nich w trakcie hipoglikemii. Hormonami podnoszącymi stężenie glukozy we krwi są:
adrenalina
glukagon
kortyzol
hormon wzrostu
Adrenalina i glukagon podnoszą stężenie glukozy we krwi przez 2-4 godziny po hipoglikemii. Kortyzol i hormon wzrostu zaczynają działać po ok. 3-4 godzinach i efekt podniesienia stężenia glukozy we krwi utrzymuje się od 5 do 12 godzin po hipoglikemii.
Homeostaza glukozy - schemat
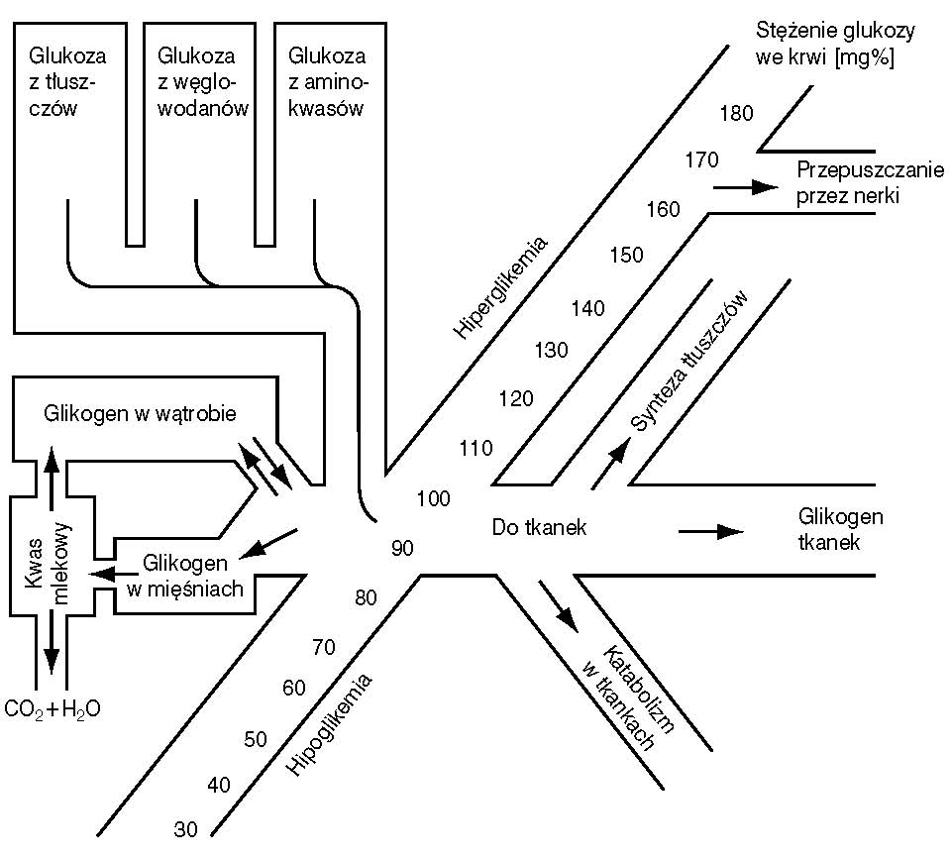
Oznaczanie glukozy
Wszystkie badania dotyczące stężenia glukozy we krwi wykonuje się na czczo.
Po posiłkach stężenie glukozy wzrasta.
Krew ma właściwości glikolityczne, wskutek czego zawartość zawartość cukru we krwi wyrażnie maleje z czasem. Zapobiegamy dodając fluorek sodu 3mg/ml
Krew odbiałcza się koloidalną zawiesiną ZnOH. Przesącz gotuje się z roztworem zawierającym Cu(ii) i Cu(I) wypada z roztworu w postaci Cu2O. Tlenek miedzi rozpuszcza się w odczynniku arsenomolibdenowym, dając niebieskie zabarwienie.
Odczynniki
1) 0,45% ZnSO4
2) 0,1 M NaOH
3) Odczynnik miedziowy I. W 600 ml wrzącej wody rozpuścić 200g bezwodnego Na2SO4. Oddzielnie w 100 ml wody rozpuścić 25 g soli Seignetta (winianu sodowopotasowego). Obydwa roztwory zmieszać dodać 20 g wodorowęglanu sodu i 25 g węglanu sodu i dopełnić do 1 l.
Przesączyć. Przechowywać w 37oC. ( może się wytrącać).
4) Odczynnik miedziowy II 15% roztwór CuSO4 *5H2O + 2 krople H2SO4
5) mieszaninę roztworów miedziowych (I i II) w stosunku 1: 25 sporządzić bezpośrednio przed użyciem.
6) Odczynnik arseno molibdenowy. Rozpuścić 25 g molibdenianu (VI) amonowego w 450 ml wody. Dodać 31 ml stęzonego H2SO4. Rozpuścić 3 g arsenianu(V) sodowego (Na2HAsO4*7H2O) w 25 ml wody. Oba roztwory zmieszać. Inkubować w temp 37oC przez 48 h. Przechwywać w ciemnej butelce.
7) Roztwór wzorcowy glukozy o stężeniu 200 mg/100 ml.
Wykonanie
Przygotować mieszaninę ZnSO4 i 0,1 M NaOH w stosumku 5:1. Do 2,9 ml mieszaniny dodać 0,1 ml krwi z opuszki palca. Próbkę grzać we wrzącej łażni wodnej 5 min.
Po ostudzeniu przesączyć.
Do 1 ml przesączu dodać 1 ml odczynnika 5 (miedziowego) i gotować na łażni 20 min. Po ostudzeniu dodać 1ml odczynnika arseno-molibdenowego i wstrząsać aż rozpuści się tlenek miedzi. Dodać 7 ml wody i oznaczać spektrofotometrycznie przy długości fali 660 nm.
Analogicznie postępować ze wzorcem. Pobrać 0,1 ml roztworu wzorcowego z przyrządzonych roztworów w zakresie 10 do 200 mg/100ml.
Obliczenia
W tym zakresie krzywa ma charakter liniowy
Stężenie wynosi
•mg glukozy /100ml=(Ap/Aw) * Cw*
•Cw= stężenie glukozy we wzorcu
Zadaniem cyklu Krebsa jest utlenić związek o nazwie: acetylokoenzym A (acetylo-CoA) do 2 cząsteczek dwutlenku węgla (CO2), pozyskaną w tym procesie energię ulokować w chemicznych nośnikach energii: GTP, NADH i FADH2.
Sumaryczny wzór cyklu Krebsa to:
acetylo-CoA + GDP + Pi + 3NAD+ + FAD + 2H20 →
CoA + GTP + 3NADH + 3H+ + FADH2 + 2CO2
Powstają wysokoenergetyczne związki wymagające tlenu
Jeśli zabraknie substratów to reakcja nie będzie zachodziła 3NAD+ + FAD
Zadaniem cyklu Krebsa jest utlenić związek o nazwie: acetylokoenzym A (acetylo-CoA) do 2 cząsteczek dwutlenku węgla (CO2), pozyskaną w tym procesie energię ulokować w chemicznych nośnikach energii: GTP, NADH i FADH2.
Sumaryczny wzór cyklu Krebsa to:
acetylo-CoA + GDP + Pi + 3NAD+ + FAD + 2H20 →
CoA + GTP + 3NADH + 3H+ + FADH2 + 2CO2
Powstają wysokoenergetyczne związki wymagające tlenu
Jeśli zabraknie substratów to reakcja nie będzie zachodziła 3NAD+ + FAD
Sumaryczna reakcja glikolizy przekształcenia glukozy w pirogronian jest następująca:
glukoza + 2Pi + 2ADP + 2NAD+ →
→ 2 cząsteczki pirogronianu + 2ATP + 2NADH + 2H+ + 2H2O.
Jeśli zabraknie substratów to reakcja nie będzie zachodziła
przy braku tlenu, podczas intensywnego wysiłku, ilość wytwarzanego NADH przekracza zdolność łańcucha oddechowego do utleniania NADH z powrotem do NAD +.
W warunkach tlenowych pirogronian zostaje przekształcony w acetylo-CoA (dehydrogenaza pirogronianowa)
pirogronian + NAD+ + CoA → acetylo-CoA + CO2 + NADH.
przy braku tlenu, podczas intensywnego wysiłku, ilość wytwarzanego NADH przekracza zdolność łańcucha oddechowego do utleniania NADH z powrotem do NAD +.
Brak NAD + powoduje że pirogronian syntetyzowany w mięśniu szkieletowym podczas glikolizy zostaje przekształcony w mleczan przez dehydrogenazę mleczanową w reakcji generującej NAD+, dzięki czemu glikoliza w dalszym ciągu wytwarza ATP.
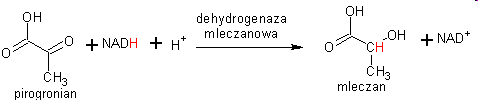
Próg mleczanowy
Próg Mleczanowy zwany, progiem przemian beztlenowych, progiem anaerobowym jest obciążeniem treningowym, po którego przekroczeniu stężenie kwasu mlekowego we krwi wzrasta
Po przekroczeniu tego poziomu energia dostarczana jest w wyniku procesów beztlenowych. Po przekroczeniu progu mleczanowego zmniejszeniu ulega udział wolnych kwasów tłuszczowych w procesie dostarczania energii.
W czasie wysiłku powstaje mleczan, jako produkt uboczny przemian metabolicznych. Krąży we krwi i jest neutralizowany. Stężenie mleczanu we krwi wzrasta wraz z intensywnością wysiłku, gdy powstaje go więcej niż organizm może neutralizować - to ten moment nazywamy progiem mleczanowym.
Przyjmuje się, że mniej niż 2 mmol/l (milimole na litr) jest typowe dla spoczynku,
2 - 4 mmol/l to wartość optymalnego treningu,
4 - 8 mmol/l zakwaszenie mięśni jest już znaczne,
powyżej 8 mmol/l organizm włącza mechanizmy obronne - ATP nie może być dalej resyntezowane, komórki mięśniowe przestają pracować i wysiłek musi zostać przerwany.
Badanie stężenia mleczanu we krwi, zarówno spoczynkowe jak i wysiłkowe,jest bardzo precyzyjnym testem diagnozującym wydolność i zdolność regeneracji człowieka. Przyjmuje się, że próg mleczanowy osiągany jest przy wartości tętna 85% HRmax,
Żeby kolejne testy były ze sobą porównywalne należy je przeprowadzać o podobnych godzinach. Najlepszą porą na przeprowadzenie testu jest poranek. Związane jest to z cyklem okołodobowym, podczas którego wiele wskaźników ulega wahaniom. W dniu badań należy ograniczyć picie kawy a na 3 godziny przed testem spożywania posiłków. Jeżeli podczas badań będzie oznaczana morfologia krwi, należy przyjść na czczo
Hrmax (HEART RATE)
Formuła Sally Edwards - dosyć dokładna metoda obliczania HRmax, bo uwzględnia wagę i płeć.
Mężczyźni HRmax = 210 - 1/2 wieku - 1% masy ciała w funtach + 4
Kobiety HRmax = 210 - 1/2 wieku - 1% masy ciała w funtach + 0
kiedyś liczono: Hrmax= 220 - wiek, bo błąd tutaj zwykle nie przekracza 5%220 bo takie tempo bicia serca noworodka
Trening podprogowy
ćwicząc w tej strefie (tzw. trening podprogowy) stopniowo podnosimy LT (lactate threshold -próg mleczanowy), w efekcie przy większej intensywności dłużej zostajemy w strefie tlenowej, co jest dla organizmu bardzo korzystne.
Częsty trening ponadprogowy (anaerobowy) obniża nasz LT, w konsekwencji wydolność stopniowo spada, czas regeneracji się wydłuża, nękają nas różne dolegliwości, gdyż stały ,wysoki poziom mleczanu we krwi obniża odporność.
Ważne jest przemyślane i kontrolowane przekraczanie progu mleczanowego.
Strefy HR
Strefa 0 (do 50% HRmax) - przebywanie w tej strefie nie przynosi korzyści ze sportowego punktu widzenia
Strefa 1 (50 - 60% HRmax) - obserwuje się korzyści dla kondycji i zdrowia. Dla początkujących lub osób po długiej przerwie w ćwiczeniach. W strefie tej zachodzi już wykorzystanie tłuszczu jako źródła energii, polecana więc jest także dla osób pragnących schudnąć.
Strefa 2 (60 - 70% HRmax) - Jest to pierwsza strefa w której serce zaczyna odnosić korzyści z treningu. Następuje poprawa wydolności serca a komórki mięśniowe zaczynają lepiej wykorzystywać tlen. W tej strefie tłuszcz jest podstawowym źródłem energii jest więc to idealny przedział dla osób pragnących schudnąć.
Strefa 3 (70 - 80% HRmax) - Najlepsza strefa dla poprawiania wydajności sercowo-naczyniowej. Rekomendowana dla poprawy wydolności oddechowej, poprawy transportu utlenionej krwi do komórek mięśniowych i odprowadzania z nich dwutlenku węgla. Organizm spala mniej glukozy niż tłuszczu, poprawia się ogólna siła mięśniowa.
Strefa 4 (80 - 90% HRmax)(85-90%= próg beztlenowy) - w tej strefie przechodzi się od treningu aerobowego (tlenowego) do anaerobowego(beztlenowego). Organizm nie jest już w stanie efektywnie usuwać kwasu mlekowego z pracujących mięśni. Kwas mlekowy jest produktem rozkładu glikogenu, udział tłuszczu jako źródła energii staje się znikomy. Jest to strefa dla osób pragnących poprawic wyniki sportowe. Podczas treningu w tej strefie mięśnie męczą się znacznie. Organizm w tej strefie uczy radzić sobie lepiej z kwasem mlekowym i tolerować go przez dłuższy czas.
Strefa 5 (90 - 100% HRmax)(VO2 Max) - W tej strefie można trenować przez krótki czas. Nie należy trenować bez bardzo dobrej kondycji. Kwas mlekowy powstaje bardzo szybko gdyż dług tlenowy jest bardzo wysoki. Następuje poprawa szybkości
powyższe metody obliczeń oraz opisy stref odnoszą się do ćwiczeń opartych w głównej mierze na pracy dolnej połowy ciała, ze szczególnym naciskiem na marsz i biegi.Aby wyliczać progi i korzystać ze stref w przypadku ćwiczeń angażujących górną połowę ciała trzeba obniżyć progi - średnio o 13 uderzeń serca na minutę.
Dług tlenowy
dług tlenowy, stan fizjologiczny organizmu lub jego narządu związany z czasowym (zwykle krótkotrwałym) przestawieniem procesów oddychania komórkowego z tlenowego na beztlenowy); po przywróceniu warunków tlenowych część energii zużywana jest na zmetabolizowanie nagromadzonych produktów oddychania beztlenowego i odbudowanie rezerw substratów oddechowych wykorzystywanych w warunkach beztlenowych
Wyszukiwarka
Podobne podstrony:
II O- Biochemia cwiczenie 5, Politechnika Wrocławska - ochrona środowiska, biochemia - laboratorium
II O- Biochemia cwiczenie 1, Politechnika Wrocławska - ochrona środowiska, biochemia - laboratorium
II OŚ Biochemia ćwiczenie 3
BIOCHEMIA - ćwiczenia, STUDIA, WSR - Fizjoterpia, Rok I, Semestr 1, Semestr I, Biochemia, Ćwiczenia
Kolo biochemia KOMPLET NOTATEK AMINOKWASY, Szkoła Rolnictwo studia, Szkoła, Materiały studia, bioche
II OŚ Biochemia ćwiczenie 2
II O- Biochemia cwiczenie 4, Politechnika Wrocławska - ochrona środowiska, biochemia - laboratorium
Biochemia Ćwiczenia 8
II OŚ Biochemia ćwiczenie 1
II OŚ Biochemia ćwiczenie 7
II OŚ Biochemia ćwiczenie 4
II OŚ Biochemia ćwiczenie 7
II OŚ Biochemia ćwiczenie 4
II O- Biochemia cwiczenie 3, Politechnika Wrocławska - ochrona środowiska, biochemia - laboratorium
Podział cukrów biochemia ćwiczenia cukry reakcje?rwne
Biochemia ćwiczenie I
II Rok OŚ Biochemia Ćwiczenia harmonogram, II rok, I semestr, biochemia
więcej podobnych podstron