KINETYKA REAKCJI - zadania dodatkowe
Zadanie 1. Obliczyć czas potrzebny do zmniejszenia stężenia substratu:
z 0,15 M do 0,03 M przy stałej szybkości reakcji k = 0,209 1/min.
z 0,5 M do 0,15 M przy stałej szybkości reakcji k = 0,115 min-1.
z 0,1 M do 0,04 M przy stałej szybkości reakcji k = 0,009 s-1.
z 0,25 M do 0,05 M przy stałej szybkości reakcji k = 0,027 min-1.
t - czas reakcji ?
k = stała szybkość reakcji 0,027 min-1
a - stężenie początkowe 0,25 M
(a-x) - stężenie końcowe w danym momencie 0,05 M
zamieniamy k na t miejscami
Zadanie 2.
Ile razy wzrosła szybkość pewnej reakcji, jeśli jej temperaturowy współczynnik wynosi γ=5, a temperatura wzrosła o 8oC?
γ = 5
∆T = 8
Ile razy wzrosła szybkość pewnej reakcji, jeśli jej temperaturowy współczynnik wynosi γ=6, a temperatura wzrosła o 5oC?
Temperaturowy współczynnik pewnej reakcji wynosi γ=3. O ile stopni należy podnieść temperaturę, aby szybkość reakcji wzrosła 10 razy?
γ = 3 Temperaturowy współczynnik pewnej reakcji
∆T = ? Różnica temperatury
Temperaturowy współczynnik pewnej reakcji wynosi γ=5. O ile stopni należy podnieść temperaturę, aby szybkość reakcji wzrosła 10 razy?
Temperaturowy współczynnik pewnej reakcji wynosi γ=2. O ile stopni należy podnieść temperaturę, aby szybkość reakcji wzrosła 3 razy?
Temperaturowy współczynnik pewnej reakcji wynosi γ=4. O ile stopni należy podnieść temperaturę, aby szybkość reakcji wzrosła 3 razy?
Zadanie 3. Po 5 min reakcji przereagowała połowa substratu o początkowym stężeniu 4 . 10.5 mol·dm-3. Szybkość maksymalna reakcji wynosiła 2,04 *10-5 M·min-1. Obliczyć KM oraz stężenie produktu po 10 min.
t = 5 min / połowa substratu / po 10 min
[S] = 4* 10-5 mol * dm -3.
V max = 2,04 *10-5 M·min-1
k = ? Stała szybkości reakcji
v = ? Szybkość początkowa reakcji
KM = ? Stała Michaelisa.
[S]5 = a-x = 50% [S] = 0,5 * 4* 10-5 mol * dm -3 = 2* 10-5 mol * dm -3
Stężenie produktu po 10 min?
t = 10 min
[S] = stężenie substratu 4* 10-5 mol * dm -3.
k = stała szybkość reakcji 0, 139 min-1
( a - x) stężenie substratu po 10 min
x = ? Stężenie produktu po 10 min
Odp. Stężenie substratu po 10 min wynosi 1*10-5 mol/dm-3.
Odp. Po 10 min powstało 3*10-5 mol.*dm-3 produktu.
a) Po 5 min reakcji przereagowała połowa substratu o początkowym stężeniu 3 ⋅ 10-5 mol⋅dm-3. Szybkość maksymalna reakcji wynosiła 4,02 ⋅ 10-5 M⋅min-1. Obliczyć KM oraz stężenie produktu po 10 min.
b) Po 3 min reakcji przereagowała połowa substratu o początkowym stężeniu 4 ⋅ 10-3 mol⋅dm-3. Szybkość maksymalna reakcji wynosiła 12 ⋅ 10-3 M⋅min-1. Obliczyć KM oraz stężenie produktu po 9 min.
Zadanie 4. Stała Michaelisa w reakcji hydrolizy peptydu wynosi 4 . 10-3 M. Przy stężeniu początkowym substratu 8 . 10-5 M, po 2 minutach zhydrolizowało 10% peptydu. Obliczyć stałą szybkości reakcji oraz szybkość maksymalną V max
KM = 4*10-3 M
[S0] = 8*10-5
[S1] = (a-x) zhydrolizowało 10% peptydu to pozostało 90%. 90% z 8 = 0,9 * 8 * 10-5 = 7,02 * 10-5
V max = ?
k = ?
v = ?
Stała Michaelisa w reakcji hydrolizy peptydu wynosi 2 ⋅ 10-3 M. Przy stężeniu początkowym substratu 4 ⋅ 10-5 M, po 2 minutach zhydrolizowało 20% peptydu. Obliczyć stałą szybkości reakcji oraz szybkość maksymalną Vmax.
Stała Michaelisa w reakcji hydrolizy peptydu wynosi 12 ⋅ 10-5 M. Przy stężeniu początkowym substratu 3 ⋅ 10-5 M, po 2 minutach zhydrolizowało 15% peptydu. Obliczyć stałą szybkości reakcji oraz szybkość maksymalną Vmax.
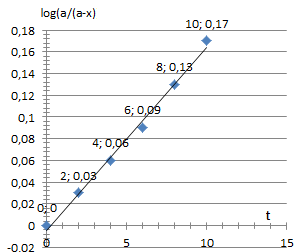
Zadanie 5. Określić rząd reakcji oraz obliczyć stałą szybkości reakcji denaturacji białka o stężeniu 15 mg/cm3, jeśli uzyskano następujące wyniki:
Czas ogrzewania [min] |
Stężenie białka natywnego [mg/cm3](a-x) |
Stężenie białka zdenaturowanego [x] |
log(a/(a-x)) |
1/(a-x) |
|
0 2 4 6 8 10 |
15,0 14,0 13,0 12,0 11,0 10,0 |
0 15-14=1 2 3 4 5
|
0 0,03 0,06 0,09 0,13 0,17 |
0,067 0,071 0,076 0,083 0,091 0,1 |
|
W mianowniku podstawiamy a-x, czyli ilość substratu, tj. 14 mg/cm3 po 2 min. log(15/14)= 0,03, zatem k=0,035 min-1
Ile białka natywnego pozostanie w roztworze po 15 min ogrzewania?
Odp. po 15 min zostało 8,9 mg/cm3 białka natywnego.
Odp. po 15 minutach białka denaturowanego powstanie 6,1 mg/cm3
Zadanie 6.
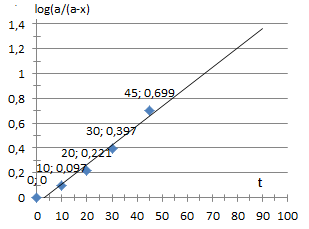
Określić rząd reakcji oraz obliczyć stałą szybkości reakcji hydrolizy skrobi, jeśli uzyskano następujące stężenie produktu:
Czas ogrzewania [min] |
Stężenie produktu [mg/cm3] |
(a-x) 3 |
log(a/(a-x)) i |
1/(a-x) |
|
|||
0 10 20 30 45 60 90 |
0 0,6 1,2 1,8 2,4 3,0 3,0 |
3 3-0,6=2,4 1,8 1,2 0,6 0 0 |
0 0,097 0,221 0,397 0,699 |
0,33 0,42 0,56 0,83 0,42
|
|
|||
120 |
|
0 |
|
|||||
|
||||||||
Ile skrobi pozostanie w roztworze po 120 min ogrzewania?
Jeśli po 60 min i po 90 min powstało 0 to po 120 min ogrzewania zostanie 0 mg/cm3 skrobi.
Zadanie 7.
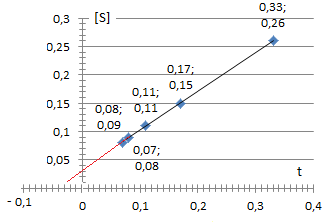
Oznaczono szybkości początkowe v0 dla reakcji enzymatycznej przy różnych stężeniach substratu:
Początkowe stężenie substratu [µM] |
Szybkość początkowa v0 [mg⋅s-1] |
1 [S] |
1 [V0] |
|
3 6 9 12 15 |
3,9 6,7 8,9 10,8 12,1 |
0,33 0,17 0,11 0,08 0,07 |
0,26 0,15 0,11 0,09 0,08 |
|
Wartość szybkości maksymalnej Vmax = 24,0 mg⋅s-1. Obliczyć KM oraz podać dla jakiego stężenia substratu szybkość reakcji osiągnie wartość maksymalną.
Zadanie 8. W wyniku działania dwóch różnych enzymów na substrat o zmiennym stężeniu określono szybkości początkowe:
Początkowe stężenie substratu [μM] |
enzym A |
enzym B |
|
e - A |
e - B |
|
|
v0 [μ M⋅min-1] |
v0 [μ M⋅min-1] |
1 [S] |
1 [V0] |
1 [V0] |
|
5,8 10,2 15,6 25,0 |
8,7 11,1 12,5 13,7 |
5,3 7,4 9,3 11,1 |
0,17 0,09 0,06 0,04 |
0,11 0,09 0,08 0,07 |
0,18 0,14 0,10 0,09 |
|
Określić stałe kinetyczne KM i Vmax metodą podwójnych odwrotności.
Który z enzymów wykazuje większe powinowactwo do substratu? - eB
Określić rodzaj inhibicji - kompetycyjna.
Podać w jaki sposób można cofnąć działanie inhibitora - dodając substratu.
Zadanie 10.
Stała Michaelisa w reakcji hydrolizy peptydu wynosi 3 ⋅ 10-3 M. Przy stężeniu początkowym substratu 6 ⋅ 10-5 M, po 5 minutach zhydrolizowało 30% peptydu. Obliczyć stałą szybkości reakcji oraz szybkość maksymalną Vmax oraz stężenie produktu po 10 min.
KM = 3 ⋅ 10-3 M.
[S]0 = 6 ⋅ 10-5 M
t = 5 min
k = ? 0,071 min-1
v = ?
vmax = ? 15,198*10-5 M
Po 5 minutach zhydrolizowało 30% peptydu to pozostało 70%
[P]5 = 70% = 0,7 * 6* 10-5 M = 4,2* 10-5 M.
v = k *(a-x) = 0,071 * 4,2 *10-3 = 0,298*10-5 M*min-1
Po 5 min reakcji przereagowała połowa substratu o początkowym stężeniu 3 ⋅ 10-5 mol⋅dm-3. Szybkość maksymalna reakcji wynosiła 2,02 ⋅ 10-5 M⋅min-1. Obliczyć KM oraz stężenie produktu po 10 min.
t = 5 min.
[S]0 = 3 ⋅ 10-5 mol⋅dm-3
Vmax = 2,02 ⋅ 10-5 M⋅min-1.
KM = ?
[S]5 = [S]5 = a-x = 50% [S]5 = 0,5 * 3* 10-5 mol*dm-3 = 1,5* 10-5 mol*dm-3.
Po 3 min reakcji przereagowało 15% substratu o początkowym stężeniu 4 ⋅ 10-3 mol⋅dm-3. Szybkość maksymalna reakcji wynosiła 8 ⋅ 10-3 M⋅min-1. Obliczyć KM oraz stężenie produktu po 8 min.
t = 3 min.
[S]0 = 4*10-3 mol⋅dm-3
[S]15 = ? a-x = 15% [S] = 0,15% * 4* 10-3 mol * dm -3 = 6* 10-3 mol * dm -3
V max = 8 ⋅ 10-3 M⋅min-1
KM = ?
v= ? V=k*(a-x)=
[S]8 = ?
6
Wyszukiwarka
Podobne podstrony:
KINETYKA REAKCJI zadania dodatkowe 2
Cw [1][1] 19 Kinetyka reakcji Landalota
cw 19 Kinetyka reakcji Landalota
KINETYKA REAKCJI, Matury i zadania maturalne z chemii
fizyka 4 11 17, SiMR - st. mgr, fizyka mgr, FIZYKA II KOLO, FIZYKA II KOLO, fizyka-kolokwium II,
06 Kinetyka reakcji enzymatycznych
4 Badanie kinetyki reakcji zmy Nieznany (2)
w 1 - wartość pieniądza w czasie - zadania dodatkowe, wszop ZZIP, II semestr, finanse i rachunkowość
04 Kinetyka reakcji chemicznych i kataliza
kinetyka reakcji enzymatycznych I
Świnie ćw kolo nr 3
Noworyta, inżynieria bioreaktorów, równania kinetyczne reakcji
Cwiczenia nr 4 zadanie dodatkowe 4
zadania dodatkowe, Ekonomia- studia, Finanse publiczne i rynki finansowe
Zadania dodatkowe, FINANSE PRZEDSIĘBIORSTW JAWORSKI, finanse przedsiębiorstw
Zadanie dodatkowe nr 1
Zadanie dodatkowe dla chętnych
więcej podobnych podstron