Magdalena Ciekańska
Technologia Chemiczna
IBIR
Sem VIII
PODSTAWY SONOCHEMII I TECHNIK MIKROFALOWYCH
LABORATORIUM
Ćwiczenie 2
Sonochemiczna degradacja polimeru
Data wykonania ćwiczenia: 23.03.2010
Data oddania sprawozdania: 30.03.2010
CEL ĆWICZENIA
Celem ćwiczenia było zbadanie przebiegu sonochemicznej degradacji naturalnego polisacharydu - chitozanu - w roztworze wodnym.
WSTĘP TEORETYCZNY
Pojęcie degradacji polimerów zwykle odnosi się do określenia zmian właściwości fizycznych spowodowanych reakcjami chemicznymi, w wyniku których zachodzi rozerwanie łańcucha polimeru. Konsekwencją tego procesu jest skrócenie łańcucha, a zatem utworzenie nowych cząsteczek o innej masie molowej i właściwościach, różnych od monomerów makrocząsteczek, od których się wywodzą. Ze zjawiskiem degradacji wiążą się zwykle zmiany właściwości oraz pogorszenie funkcjonalności materiału polimerowego.
Ze względu na sposób inicjowania procesy degradacji polimerów degradację dzielimy na:
termiczną - zmiana właściwości polimeru pod wpływem podwyższonej temperatury, bez udziału czynników chemicznych
mechaniczną - dotyczy efektów makroskopowych zachodzących w polimerach pod wpływem działania sił rozciągających
fotochemiczną - zachodzi pod wpływem światła. Oznacza zmiany fizyczne i chemiczne wywoływane w polimerach pod wpływem światła widzialnego lub nadfioletu
radiacyjną - spowodowana promieniowaniem jonizującym
biologiczną - wywoływana działaniem enzymów na polimery. Mikroorganizmy produkują wiele różnorodnych enzymów zdolnych do reagowania zarówno z polimerami naturalnymi jak i syntetycznymi
chemiczną - procesy wywoływane czynnikami chemicznymi takimi jak: kwasy, zasady rozpuszczalniki, reaktywne gazy będące w bezpośrednim kontakcie z polimerem
Pomiędzy poszczególnymi typami degradacji istnieją silne powiązania. Zwykle mamy do czynienia z jednoczesnym zachodzeniem kilku rodzajów degradacji.
Ogólnie reakcje degradacji klasyfikowane są jako:
jednoetapowe - szybkość jest proporcjonalna do szybkości inicjacji ,np.:
- solwoliza wiązań estrowych
- enzymatyczny rozkład wiązań peptydowych
łańcuchowe - charakterystyczny jest samorzutny przebieg zapoczątkowanego wcześniej procesu, oznacza to, że w wyniku zainicjowania powstają produkty zdolne do samorzutnego reagowania z kolejnymi cząsteczkami substratu, tworząc w konsekwencji produkty degradacji, np.:
- autooksydacja
Metody badań służące do wyznaczania zmian zachodzących w materiale polimerowym po procesie degradacji:
określenie zmian właściwości chemicznych:
zmiana ciężaru cząsteczkowego
usieciowanie
tworzenie grup karbonylowych, wodoronadtlenków
zmiany w nienasyconym wiązaniu C=C
tworzenie się przejściowych rodników
zużycie stabilizatora
określenie zmian właściwości fizycznych
zamglenia
tworzenie się pęknięć
utrata połysku
chropowatość powierzchni
właściwości elektryczne
zmiany w morfologii
określenie zmian właściwości mechanicznych
wydłużenie przy zerwaniu
wytrzymałość na rozdzieranie
udarność
kruchość
W celu uodpornienia tworzyw na degradację lub destrukcję zachodzącą pod wpływem ogrzewania, naprężeń mechanicznych podczas obróbki, utleniania i użytkowania tworzywa, podczas produkcji stosuje się stabilizatory. Generalnie substancje te ze względu na sposób działania podzielić można na:
wygaszacze UV
UV absorbery
wygaszacze stanów wzbudzonych
zmiatacze wolnych rodników
zmiatacze tlenu singletowego
antyutleniacze
substancje rozkładające nadtlenki
WYKONANIE ĆWICZENIA
Napełnienie naczynia reakcyjnego 10 ml roztworu chitozanu.
Podłączenie naczynia do linii argonowej i nasycanie roztworu argonem przez 30 minut.
Przygotowanie do pracy reaktora sono chemicznego i doprowadzenie wody w reaktorze do temperatury ok. 20oC.
Poddanie próbki konikowaniu przez 15 minut, przy mocy 100 W.
Przelanie całej próbki do naczynka scyntylacyjnego.
Dodanie do 10 ml każdej próbki (wejściowej i sonikowanej) po 10 ml roztworu A.
Trzykrotne przefiltrowanie każdego roztworu za pomocą strzykawki z nasadką filtracyjną (filtr o średnicy porów 0,45 μm).
Napełnienie naczynka 7 ml roztworu przy czwartej jego filtracji.
Napełnienie naczynka scyntylacyjnego ok. 20 ml roztworu B, czterokrotne przefiltrowanie roztworu i pozostawienie na końcu naczynka całej objętości cieczy.
Kalibracja aparatury laserowej z użyciem benzenu w zamkniętym naczyniu scyntylacyjnym.
Wykonanie dla każdej próbki pomiarów natężenia światła laserowego pod różnymi kątami i dla różnych rozcieńczeń - rozcieńczanie przefiltrowanym roztworem B (usuwanie śladów linii papilarnych oraz zanieczyszczeń z zewnętrznej powierzchni naczynka za pomocą bibuły zwilżonej acetonem przed umieszczeniem naczynka w szczelinie pomiarowej).
OPRACOWANIE WYNIKÓW
Obliczenie dla każdej z próbek wagowo-średniego ciężaru cząsteczkowego za pomocą programu komputerowego wykorzystującego algorytm Zimma i wydrukowanie uzyskanych diagramów.
M = 1,67•105 ![]()
M0 = 1,73•105![]()
M - wagowo-średnia masa cząsteczkowa polimeru po sonikowaniu [g/mol]
M0 - wagowo-średnia masa cząsteczkowa polimeru przed sonikowaniem [g/mol]
Obliczenie dawki ultradźwięków dla sonikowanej próbki (w oparciu o wynik ćwiczenia 1 i założenie, że moc dawki jest jednakowa w naczyniu i w całym reaktorze), na podstawie zależności:
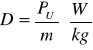
Gdzie:
D - dawka ultradźwięków dla sonikowanej próbki ![]()
m - masa sonikowanego roztworu [kg]
m = 0,5 [kg]
PU - moc ultradźwięków (wyliczona na podstawie wyników poprzedniego ćwiczenia dla mocy elektrycznej 100W) [W]
PU (5 min) = 75,70 [W]
Ponieważ:
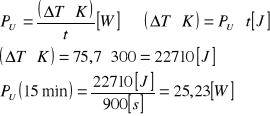
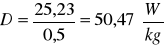
Obliczenie stężenia zerwanych wiązań (pęknięć łańcucha) na podstawie wzoru:
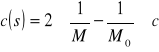
Gdzie:
M - wagowo-średnia masa cząsteczkowa polimeru po sonikowaniu ![]()
M0 - wagowo-średnia masa cząsteczkowa polimeru przed sonikowaniem ![]()
c - stężenie polimeru
c = 1,65 ![]()
c(s) - stężenie zerwanych wiązań ![]()
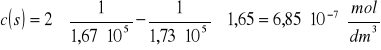
Obliczenie wydajności degradacji na podstawie dawki i wartości c(s), przy wykorzystaniu zależności:
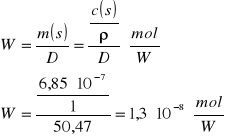
m (s) - ilość zerwanych wiązań ![]()
ρ - gęstość roztworu ![]()
WNIOSKI
Udało nam się zrealizować cel ćwiczenia, jakim było zbadanie przebiegu degradacji chitozanu, powodowanej zastosowaniem ultradźwięków - degradacji sonochemicznej.
Analizy skutków procesu mogliśmy dokonać na podstawie analizy masy polimeru przed i po degradacji, wykonanej komputerowo dzięki zastosowaniu algorytmu Zimma. O tym, że doszło do degradacji świadczy spadek średniej masy cząsteczkowej chitozanu z wartości początkowej M0 = 1,73•105
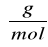
do końcowej M = 1,67•105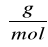
.
Analiza mas pozwoliła nam na wyliczenie stężenia zerwanych w trakcie procesu wiązań. Dla naszego doświadczenia wartość ta wyniosła
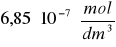
.
Wykorzystując dane z poprzedniego ćwiczenia mogliśmy w sposób dość precyzyjny wyznaczyć dawkę ultradźwięków odpowiednią dla naszej próbki, a to z kolei umożliwiło nam wyliczenie wydajności procesu degradacji polimeru, która wyniosła
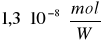
, co dla polimeru jest dobrą wartością.
Podsumowując należy podkreślić największą zaletę degradacji sonochemicznej - nie jest ona tak obciążająca dla środowiska naturalnego jak inne.
Wyszukiwarka
Podobne podstrony:
lab spr 25, Lab 25, Sprawozdanie
spr 9 hydro lab
Wnioski do spr z elektry 3, PW SiMR, Inżynierskie, Semestr V, syf, laborki, Lab. Ukł. Napędowych
ściskanie(lab), Studia, pomoc studialna, Sprawozdania Laborki, Wytrzymałość spr.nr2
spr-122, Labolatoria fizyka-sprawozdania, !!!LABORKI - sprawozdania, Lab, !!!LABORKI - sprawozdania,
SPR-ANKI, Studia, WAT Informatyka, s3 - GK - lab grafika komputerowa, Lab2
Lab 6, Spr. 6, Akademia Górniczo - Hutnicza
Lab 8, Spr 8, Akademia Górniczo - Hutnicza
Metrologia-lab-Pomiary Parametrów Drgań Mechanicznych, Drgania mechaniczne SPR, POLITECHNIKA RADOMSK
Sprawka Lab, Bomba Kalorymetryczna - spr, Ćwiczenie nr:
Metrologia-lab-Pomiary Indukcyjności i Pojemności, Mostki SPR, POLITECHNIKA RADOMSKA
lab pomiary i automatyka spr 7
lab.3, spr 3 Michał Kata Tomasz Kordas L05
Sprawka Lab, pompaciepła - spr, WIMiR
lab.1 4 MwSK Spr 1
spr bioch ćw 2, far, II rok III sem, biochemia, lab
betabartek, Politechnika śląska katowice, Zip, Semestr III, Fizyka, Lab, fizyka lab BURDEL, Fizyka l
lab fiz sem 5, spr, Marta Sołtys
więcej podobnych podstron