Neuron - struktura i funkcja.
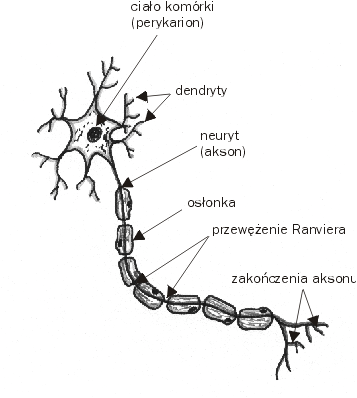
Neuron składa się z perikarionu (ciało komórki) i cylindrycznych wypustek - neurytów (akson i dendryty). Spełnia funkcję przekazywania sygnałów. Przewężenia w osłonkach mielinowych powodują szybsze przekazywanie sygnału.
Kolce dendrytyczne - przystosowane do odbioru specyficznych sygnałów, powodują długoterminowe zmiany w neuronie, odgrywają kluczowa rolę w procesie uczenia się i pamięci.
Klasyfikacja neuronów:
Strukturalne
Wielobiegunowe
Dwubiegunowe
Jednobiegunowe
Długość aksonów
Neurony projekcyjne - przekazują sygnały, długi akson - Golgiego typu II
Interneurony - krótkie aksony - łączą ze sobą neurony, inaczej wstawkowe.
Funkcjonalne
Zmysłowe (aferentne) - czuciowe
Motoryczne (eferentne) - ruchowe
Neurony asocjacyjne
Komórki glejowe - struktura i funkcja.
Komórki glejowe:
Astrocyty
Komórki Schwanna (odpowiedzialne za powstawanie osłonki mielinowej)
Mikroglej (pełni funkcję obronną, odpowiedzialne za układ immunologiczny w mózgu)
Astrocyty:
Pobierają nadmiar jonów K+ i przekazują je do obszarów o małym stężeniu
Regulują neuroprzekaźnictwo
Stanowią zaporę zapobiegająca dyfuzji neuroprzekaźnika poza szczelinę synaptyczną
Błona komórkowa astrocytów zawiera specyficzne białka transportowe, wiążące z dużym powinowactwem neuroprzekaźniki i przenoszą je i wnętrza komórki astrocytarnej
Zaopatruje neurony w glukozę
Pobudza komórki nabłonkowe naczyń włosowatych do tworzenia ścisłych złączy i indukują syntezę enzymów swoistych dla bariery krew - mózg
Odgrywają ważną rolę w odpowiedzi immunologicznej
Biorą udział w metabolizmie kwasu glutaminowego i GABA (neuroprzekaźnik hamujący przez otwarcie kanałów chlorkowych)
Odgrywają rolę w zaopatrywaniu neuronów w glukozę
Synchronizacja w działaniu rożnych neuronów
Mikroglej - są one składnikami układu odpornościowego i wywodzą się z makrofagów. Wykazują zdolność pochłaniania produktów rozpadu tkanki nerwowej.
Komórka Schwanna, także lemocyt, lemmocyt - komórka glejowa obwodowego układu nerwowego występująca w zespołach.
Osłonka Schwanna (zwana neurolemmą) powstaje przez owinięcie się protoplazmy komórki wokół włókien nerwowych. Jedna osłonka pokrywa kilka z nich. Cytoplazma komórki Schwanna wiąże aksony razem ale nie pozwala im się dotykać.
Model i struktura błony.
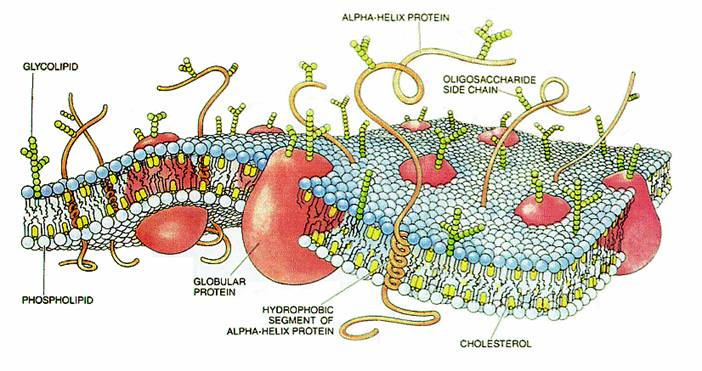
Jest ona złożona z dwóch warstw lipidów, do których należą fosfolipidy, glikolipidy i steroidy, oraz białek.
Charakterystyczną budowę błony zapewnia amfipatyczność cząsteczek - zbudowane są z apolarnego ogona węglowodorowego oraz polarnej głowy, dzięki czemu lipidy układają się w sferyczne pęcherzyki bądź właśnie dwuwarstwę.
Do lipidów błonowych należą:
fosfolipidy cholinowe: fosfatydylocholina (lecytyna)
fosfolipidy aminowe: fosfatydyloetanolamina, fosfatydyloinozytol, fosfatydyloseryna;
glikolipidy obojętne, np. galaktocerebrozyd
steroidy - cholesterol lub estry cholesterolu (zwierzęta), fitosterole (rośliny). U prokariontów występują hopanoidy - inne lipidy cykliczne.
Płynność dwuwarstwy Płynność dwuwarstwy lipidowej zależy od charakteru łańcuchów lipidów, ich długości oraz obecności cholesterolu. Im bardziej nasycone są łańcuchy tłuszczów, tym sztywniejsza jest błona. Nienasycenie zapewnia większą płynność. Obserwujemy to na przykładzie tłuszczów zwierzęcych (nasycone) - np. łój oraz tłuszczów roślinnych (nienasycone), np. olej. Na sztywność błony wpływa także obecność cholesterolu, który jak klin blokuje płynność łańcuchów. Krótkie łańcuchy są znacznie bardziej płynne od długich. Właściwości te wykorzystują m.in. drożdże i bakterie kontrolując skład swojej błony poprzez syntezę odpowiednich lipidów.
Półprzepuszczalność dwuwarstwy Błona komórkowa jest strukturą półprzepuszczalną (zob. membrana półprzepuszczalna). Niektóre z białek znajdujących się w błonie komórkowej uczestniczą w aktywnym transporcie.
Osłonka mielinowa.
Osłonka mielinowa- komórka tworzy wzdłuż aksonów osłonkę mielinową. Osłonka ta spełnia funkcję ochronną dla aksonu, ale przede wszystkim zwiększa tempo przewodzenia impulsów nerwowych (dzięki przewężeniom Ranviera).
Choroby demielinizacyjne - grupa chorób układu nerwowego o różnej etiologii, w których badaniem histopatologicznym wykrywa się w mózgu i rdzeniu, jako zmianę podstawową rozpad osłonek rdzennych (mielinowych) włókien nerwowych.
Potencjał spoczynkowy i czynnościowy.
Komórki nerwowe wykorzystują energię zgromadzoną w postaci gradientów fizycznych i chemicznych. Aksony neuronów transmitują impulsy elektryczne noszące nazwę potencjałów czynnościowych, które przepływają wzdłuż włókien nerwowych, podobnie jak fale przez skakankę. W błonie aksonu znajdują się kanały jonowe, które mogą się otwierać i przepuszczać naładowane elektrycznie jony. Niektóre kanały przepuszczają jony sodowe (Na+) a inne - jony potasowe (K+). Gdy kanały są otwarte, jony Na+ i K+ przepływają do wnętrza komórki i na zewnątrz zgodnie z gradientami chemicznymi i elektrycznymi. Dochodzi do tego w reakcji na depolaryzację błony komórki nerwowej. Gdy potencjał czynnościowy pojawia się w obrębie ciała komórki nerwowej, najpierw otwierają się, zamknięte dotąd, kanały Na+. W efekcie, jony sodowe przedostają się do wnętrza neuronu i w ciągu jednej milisekundy ustala się nowy stan równowagi. W tym krótkim czasie różnica potencjałów elektrycznych po obu stronach błony komórkowej neuronu zmienia się o około 100 mV, ze spoczynkowej wartości ujemnej (około -70 mV) do dodatniej (około +30 mV), w stosunku do środowiska
międzykomórkowego. Zmiana ta wywołuje otwarcie kanałów K+ i wypływanie jonów potasowych na zewnątrz
neuronu. Powoduje to powrót potencjału błony komórki do wartości ujemnych. W trakcie trwania potencjału czynnościowego przez błonę neuronu przepływa zaskakująco niewiele jonów, a stężenia Na+ i K+ w cytoplazmie komórki nie zmieniają się w istotny sposób. Na dłuższą metę, stężenia jonów utrzymywane są na odpowiednim poziomie przez pompy jonowe, których zadanie polega przede wszystkim na usuwaniu z wnętrza neuronu nadmiaru jonów sodowych. Potencjał czynnościowy jest złożonym zjawiskiem elektrycznym. Włókna nerwowe zachowują się jak przewodniki elektryczne (chociaż są one znacznie mniej wydajne niż izolowane druty), w związku z czym potencjał czynnościowy generowany w określonym miejscu powoduje powstanie różnicy napięcia pomiędzy miejscem aktywnym a znajdującymi się w stanie spoczynku, sąsiadującymi fragmentami błony komórkowej. W ten sposób potencjał czynnościowy przemieszcza się aktywnie w postaci fali depolaryzacji od jednego do drugiego końca włókna nerwowego. Szczególnie interesującą cechą włókien erwowych jest to, że po krótkiej przerwie (tzw. okresie refrakcji) „wypalony" fragment błony odzyskuje swoją funkcję i gotowość do wygenerowania kolejnego potencjału czynnościowego. Dzięki stosunkowo dużym rozmiarom aksonów tych komórek badacze byli w stanie umieścić w nich miniaturowe elektrody, pozwalające na pomiary zmian napięcia. Obecnie, nowoczesna technika pomiarowa, tzw. patch-clamp, umożliwia badania przepływu jonów poprzez pojedyncze kanały jonowe w błonach wszystkich komórek nerwowych, co pozwala na dokładne pomiary tych prądów w mózgach podobnych do naszych.
Potencjał czynnościowy
Depolaryzacja i hiperpolaryzacja neuronu.
Zjawisko depolaryzacji i hiperpolaryzacji
Pobudzenie neuronu związane jest ze zjawiskiem depolaryzacji błony komórkowej (EPSP - postsynaptyczny potencjał pobudzeniowy)
Hamowanie neuronu związane jest ze zjawiskiem hiperpolaryzacji (IPSP - postsynaptyczny potencjał hamulcowy)
Kanały jonowe.
Kanały jonowe są to wielocząsteczkowe białka wbudowane w błonę komórkową, których zadaniem jest kontrola przepływu, z lub do komórki, jonów zgodnie z gradientem stężeń i potencjałów w komórce. Kanały jonowe są bardzo wydajne - otwarcie tzw. pory wodnej (czyli hydrofilowego kanału wewnątrz białka) pozwala na przepływ do 10 milionów jonów na sekundę, dlatego do prawidłowego funkcjonowania komórki wystarczy kilka tysięcy kanałów danego typu. Kanały specyficzne i selektywne czyli, że rozróżniają kationy od anionów oraz, że przepuszczają tylko jony danego typu np. kanał dla jonów sodowych, wapniowych czy potasowych. Określenie kanał sodowy oznacza jedynie to, że kanał ten najlepiej przepuszcza jony sodu. Oprócz tych jonów, choć znacznie gorzej, mogą przez ten kanał przechodzić także inne kationy. Ponieważ kanał jonowy może być zamknięty lub otwarty istnieje czynnik, który powoduję otwarcie, inaczej aktywację kanału jonowego. W zależności od rodzaju czynnika aktywującego, kanały jonowe dzielimy na trzy grupy:
kanały napięciowo-zależne, gdzie czynnikiem otwarcia kanału jest zmiana potencjału błonowego (najczęściej jest to depolaryzacja);
kanały aktywowane przez ligandy, gdzie wewnątrz- i zewnątrzkomórkowe czynniki chemiczne (takie jak przekaźniki nerwowe, ATP, GTP, cykliczne nukleotydy jak cAMP, czy jony wapnia) powodują
aktywację kanału;
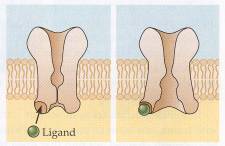
Model kanałów aktywowanych ligandem
(Nicholls i wsp., 2001).
kanały aktywowane naprężeniem mechanicznym, chodzi tu mechaniczne naprężenie błony pojawiające się w wyniku siły zewnętrznej.
Aktywacja kanałów w komórce morze zachodzić pod wpływem jednego z czynników, lub ich dowolnej kombinacji. Działanie kanałów może zostać zablokowane przez substancje chemiczne zwane blokerami, które wiążą się z kanałem jonowym blokując przepływ jonów. Każdy typ kanału posiada specyficzny dla siebie bloker i tak np.: kanał potasowy blokuje tetraetyloamina (TEA), kanał sodowy - tetrodotoksyna (TTX).
Większość kanałów jonowych zbudowana jest z kilku homologicznych podjednostek lub domen, które składają się z sześciu hydrofobowych regionów transbłonowych. Podjednostki ułożone są w taki sposób, aby utworzyć porę wodną, która przebiega zgodnie z osią symetrii kanału. Pora wodna zbudowana jest przeważnie przez helisy, choć zdarzają się fragmenty antyrównoległe kartki beta. Boczne łańcuchy aminokwasów decydują o selektywności kanału czyli które jony chętniej będą przez niego przepływać. Specyficzność kanału jest determinowana wypadkowym ładunkiem zgromadzonym na bocznych łańcuchach aminokwasów. Specyficzne kanały posiadają pierścienie aminokwasów naładowanych ujemnie lub dodatnio. Część z tych pierścieni znajduje się przy wejściu do kanału, co pozwala na odpychanie jonów o tym samym znaku, a co za tym idzie na specyficzność kanału.
Charakterystyka napięciowo-zależnego kanału sodowego i potasowego.
Pompa sodowo - potasowa wymaga nakładu energii, transport tych jonów odbywa się wbrew gradientowi stężeń. uczestniczy w aktywnym transporcie jonów sodu i potasu. Proces enzymatyczny trwa ok. 10 ms. Gradient sodowo - potasowy kontroluje objętość komórki, jest niezbędny dla pobudzenia nerwów i mięśni.
Działanie pompy wymaga:
Stałego dopływu glukozy i tlenu
Stałej syntezy ATP
Zachowania temperatury ok. 37 C
Odprowadzenia CO2
Odpowiedniego stężenia jonów Mg2+
Odpowiedniego stężenia jonów Na+ i K+
Funkcje wapnia w aksonach i dendrytach.
- efekty pobudzające i hamujące.
- poza komórkowy wapń zmniejsza i stabilizuje pobudliwość neuronu,
- przewodzenie potasowe, aktywowane przez zwiększenie stężenia wapnia,
- wzrost stężenie Ca2+ zmniejsza przewodzenie synaptyczne,
- transport aksonalny,
- transport soli i wodny przez komórki jelita cienkiego,
- sekrecja hormonów,
- aktywacja białek kurczliwych lub bezpośrednio, lub przez zmianę poziomu cAMP,
- reguluje poziom cAMP i cGMP przez aktywacje enzymy o nazwie fosfodiestraza,
- aktywacja białek kurczliwych bezpośrednio lub przez zmianę poziomu cAMP,
- organizacja cytoszkieletu - jony Ca2+ wpływają na wiązanie się różnych białek z filamentami aktynowymi. Białka wiążące się z aktyną można podzieli na te, które kontrolują długość filamentów, sieciujące filamenty aktynowe i białka łączące filamenty aktynowy z innymi strukturami,
- regulacja ekspresji genów - wzrost stężenia Ca2+ wpływa na aktywację niektórych genów. Białko wiążące wapń wiąże się z sekwencją i hamuje transkrypcję genu różnych czynników transkrypcyjnych,
- apoptoza - czyli programowana śmierć komórki, jest konsekwencją podwyższonego stężenia jonów Ca2+ w cytoplazmie. To powoduje aktywację proteaz, endonukleaz i transglutaminaz,
- wpływ na cykl komórkowy i transformację nowotworową.
Bierze udział:
- w egzocytozie pęcherzyków synaptycznych i sekrecyjnych,
- tworzy magazynowanie CA w cysterny i przy udziale wtórnych przekaźników zmiana stężenia Ca w cytozolu, i pełni role wtórnego przekaźnika,
- pompa wapniowa.
Kanały wapnia.
W komórkach mięśniowych, w tym w komórkach mięśnia sercowego oraz mięśniówce tętnic - wapń jest niezbędny do silnego skurczu. Mechanizm działania leków z grupy antagoniści wapnia polega na hamowania napływu wapnia przez kanały wapniowe błon komórkowych. Dlatego zastosowanie antagonistów wapnia związane jest z odpowiednio kontolowanym dawką leku osłabieniem siły i częstości skurczu mięśnia sercowego oraz mięśniówki tętnic. Leki te hamują napływ jonów wapnia do wnętrza komórek mięśniowych ściany naczyń i komórek serca. Ponadto skutkiem hamowania napływu wapnia jest też rozszerzenie się obwodowych naczyń krwionośnych i zmniejszenie oporu płynącej krwi. W konsekwencji następuje obniżenie ciśnienia tętniczego.
Typy receptorów.
Rodzaj bodźca: 6 podstawowych typów receptorów: chemoreceptory, termoreceptory, mechanoreceptory, fotoreceptory, magnetoreceptory i elektroreceptory.
Interoreceptory i eksteroreceptory.
Receptory błonowe:
- Receptory hormonów peptydowych
- Receptory prostaglandyny
- Receptory neurotransmiterów
Receptory wewnątrz komórkowe:
- Receptory cytozolu lub jądra
Receptory hormonów steroidowych:
- Żeńskie hormony płciowy estrogen i progesteron, tyroksyna.
Zadaniem receptora jest przemieniać jedną formę energii na druga np. światło, temperaturę na aktywność elektryczna.
Niektóre receptory adaptują się bardzo szybko tzw. adaptacja fazowa, podczas gdy inne bardzo wolno tzw. Adaptacja toniczna. Adaptacja fazowa cechuje receptory reagujące na zmiany ciśnienia czy dotyk. Receptor z adaptacja toniczną to np. odpowiedzialne za odczucie bólu.
Klasyfikacja cytoreceptorów.
Ogólna klasyfikacja cytoreceptorów wg przyrody endogennych ligandów mających duże powinowactwo do receptorów:
Receptory błonowe - receptory hormonów peptydowych, prostaglandyny, neurotransmiterów w tym receptory synaptyczne
Receptory wewnątrzkomórkowe (receptory cytozolu lub jądra)
Receptory hormonów steroidowych - żeńskie hormony płciowy estrogen i progestoreon, tyroksyna.
Kryterium specyficzne dla cytoreceptorów:
Receptor jest to cząsteczka, która zawiera odcinek zdolny do rozpoznawania specyficznych chemicznych cząsteczek endogennych
Inicjacja odpowiedzi przy związaniu agonistyk nie powoduje tworzenia lub rozpad wiązań kowalencyjnych. To odróżnia je od enzymu
Zależności od lokalizacji wyróżniamy receptory pre- i postsynaptyczne
Pierwsze zlokalizowane są na neuronie uwalniającym przekaźnik i są zaangażowane w regulację jego uwalniania.
Receptory enzymatyczne, jonotropowe i metabotropowe. Struktura, funkcja i regulacja.
Prawdopodobnie w najbardziej pierwotnych organizmach wytworzyły się tylko trzy zasadniczo różne typy receptorów błonowych:
receptory będące kanałami jonowymi (jonotropowe)
receptory metabotropowe, produkujące wtórny przekaźnik
receptory o aktywności enzymatycznej (kinaz białkowych)
Receptor metapotropowy - mówi, że zachodzi proces metabolizmu. Jest ich kilka rodzajów. Działa w przeciwnym kierunku: pobudzają albo hamują. Jest związany z białkiem G, bo ma zdolność do wiązania GDP. Związane jest z receptorem i jak nie ma neurotransmitera to jednostki białka alfa, beta i gama złączone między sobą i GTP. Gdy jest neurotransmiter jednostki rozpadają się i odłączają od białka. I wtedy zachodzi proces dysocjacji białka G.
W jaki sposób związanie sie neuroprzekaźnika z receptorem (a raczej jednym z jego podtypów) wpłynąć może
na neuron postsynaptyczny?
=> otóż zachodzi to na jeden z dwóch fundamentalnie różnych sposobów, zależnie od tego, czy receptor jest
jonotropowy czy metabotropowy
- RECEPTORY JONOTROPOWE związane są z aktywowanymi ligandem kanałami jonowymi
- RECEPTORY METABOTROPOWE związane są z białkami sygnałowymi i białkami G
Gdy cząsteczka neuroprzekaźnika wiąże sie z receptorem jonotropowym, związany z nim kanał jonowy zazwyczaj natychmiast otwiera sie lub zamyka - inicjując tym samym natychmiastowy potencjał postsynaptyczny
Receptory metabotropowe są częstsze niż receptory jonotropowe
=> efekty ich pobudzenia wolniej sie rozwijają, trwają dłużej, są bardziej rozlane i bardziej zróżnicowane
=> każdy receptor metabotropowy (a jest ich wiele rodzajów) związany jest z białkiem sygnałowym, które wygląda jak siedmiokrotnie zwinięty sznurek przechodzący przez błonę komórki
- receptor metabotropowy znajduje sie na zewnętrznej części tak „zawiniętego” białka sygnałowego
- białko G znajduje sie na wewnętrznej części białka sygnałowego
Gdy cząsteczka neuroprzekaźnika wiąże się z receptorem metabotropowym, cześć związanego z nim białka G
odrywa sie od wewnętrznej części białka sygnałowego
Budowa i funkcje synapsy.
Elektryczne i chemiczne
Charakterystyczne cechy synaps elektrycznych - bardzo duża prędkość, wysoka wierność (sygnały są przekazywane bez zniekształcenia), brak czasu zatrzymania sygnału i działanie dwukierunkowe. Przeważnie synapsy elektryczne to synapsy pobudzające.
Klasyfikacja synaps chemicznych:
Synapsy akso - dendrytyczne tworzone na dendrytach
Synapsy akso - somatyczne na ciele komórki nerwowej
Synapsy akso - aksonalne na aksonach neuronu
Połączenia synaptyczne:
Nerwowe - nerwowe - połączenie miedzy 2 komórkami nerwowymi
Nerwowo - mięśniowe - następuje przekazanie sygnały z motoneuronu do mięśnia szkieletowego
Nerwowo - gruczłowe
Synapsy pobudzające - aktywność unerwionych struktur. Tu uwalniane są mediatory (acetylocholina, serotonina). Wywołują one wzrost przepuszczalności błony subsynaptycznej dla jonów sodu, depolaryzacja błony oraz powoduje powstanie w niej postsynaptycznego potencjału pobudzającego
Synapsy hamujące - wydzielane przekaźniki GABA, glicyna. Zwiększają one przepuszczalność błony subsynaptycznej tylko dla jonów potasu i chloru. Jony potasu na zewnątrz błony hyperpolaryzuja ją, stabilizując jej potencjał spoczynkowy na takim poziomie, przy którym nie może powstać żaden potencjał czynnościowy. W wyniku tego w błonie powstaje postsynaptyczny potencjał hamujący.
Mediatorem hamowania presynaptycznego w rdzeniu kregowym ma być GABA (antagonista - bikukulina, wywołująca ogólne skurcze mięśni).
Mediatorem hamowanie postsynaptycznego w rdzeniu kręgowym ma być glicyna (antagonista - strychnina oraz toksyna tężcowa skurcze tężcowe wszystkich mięsni).
Molekularne mechanizmy działania synapsy.
Uwalnianie neuroprzekaźnika:
Dokowanie: w którym uczestnicza białka o nazwie SNARE synaprobrewina (v-SNARE) i syntaksyna (t-SNARE)
Aktywacja (priming) kilka białek cytoplazmatycznych tworzy przejściowo kompleks z białkami SNARE, co prowadzi do częściowej fuzji błony pęcherzyka z błoną presynaptyczną.
tworzenie poru fuzyjnego poprzez który zachodzi egzocytoza
Zakończenie procesu fuzji pęcherzyka z błoną presynaptyczną przez związanie Ca2+ przez synaptot
ENDOCYTOZA: okrycie fragmentu płaszczem zbudowanym z białka latryny. Dynamina (białko wiążące GTP) wytwarza kołnierz wokół wpuklenia odszczepienie pęcherzyka opłaszczonego od błony presynaptycznej.
Neuroprzekaźniki.
Neurotransmiter:
- musi być syntezowany w neuronie z którego jest uwalniany,
- musi być składowany w neuronie z którego jest uwalniany,
- stymulacja rejonu presynaptycznego musi powodować uwolnienie `kandydującej' substancji,
- podanie tej substancji w rejon postsynaptyczny jak stymulacja rejonu presynaptycznego,
- czynniki które blokują odpowiedz postsynaptyczna powinny również blokować ja, gdy substancja kandydująca zostaje podana z zewnątrz,
- substancja taka musi mieć szybki metabolizm i rozpadać się niedługo po uwolnieniu z zakończeń aksonów.
Glutaminianergiczne i GABAergiczne przekaźnictwo.
Wiążą się z napięciowo zależnymi kanałami potasowymi w błonie presynaptycznej, powodują ich otwarcie. Wpływ K zmniejsza możliwość aktywacji kanałów wapniowych typu N przez potencjał czynnościowy, wiążąc się bezpośrednio z kanałem wapniowym osłabiając napływ jonów Ca do wnętrza zakończenia. Oba efekty prowadzą do zmniejszenia uwalniania GABA
GABAb receptory w post synapsach aktywują kanał potasowy przez białko G, skutkiem czego jest długotrwała hiperpolaryzacja - postsynaptyczny potencjał hamujący
GABAc receptory- to ten sam stary typ receptorów GABA. Składa się tylko z p podjednostek mają 3 podklasy:p1,p2,p3. Zlokalizowany w siatkówce i hipokampie
Kwas glutaminowy jest podstawowym neuroprzekaźnikiem pobudzającym w ośrodkowym układzie nerwowym ssaków. Ocenia się,że 35-40% synaps używa glutaminianu jako neuroprzekaźnika. Znajdują się one w dużych ilościach w układzie limbicznym, jądrach podstawy i korze mózgu.
Powoduje trwałe zmiany plastyczne i adopcyjne synaps
Istotne dla procesów pamięci i nauczania
Większość głównych dróg czuciowych i ruchowych ma charakter glutaminianergiczny
Wyszukiwarka
Podobne podstrony:
NEUROCHEMIA, dla ludu ;p, Neurochemia
NEUROCHEMIA 1, dla ludu ;p, Neurochemia
NEUROCHEMIA, dla ludu ;p, Neurochemia
opracowanie neuro dla grupy
VOLKSWAGEN-SAMOCHÓD DLA LUDU, NAUKA, WIEDZA
opracowanie neuro part 1
opracowanie neuro part 2
Pieśni i poezye dla ludu roboczego 1897r
Opracowanie redaktorskie dla studentow(1)
opracowanie laborki dla Dawida 25, Labolatoria fizyka-sprawozdania, !!!LABORKI - sprawozdania, 25 -
Riki tiki pakieciki, dla ludu ;p, Biotechnologia ogólna
tekst wykładów paleo, dla ludu ;p, Paleontologia
Opracowali procedury dla sêu╛b medycznych na autostradzie?
PODSTAWY PALEONTOLOGII, dla ludu ;p, Paleontologia
Opracowanie oprogramowania dla symulacji procesu
Objawienia Matki Boskiej w Gietrzwałdzie (dla ludu katolickiego 160 objawień)
więcej podobnych podstron