NIESTABILNOŚĆ GENETYCZNA W NOWOTWORACH.
NIESTABILNOŚĆ MIKROSATELITARNA I UTRATA HETEROZYGOTYCZNOŚCI.
GENETIC INSTABILITY IN CANCER
MICROSATELLITE INSTABILITY AND LOSS OF HETEROZYGOSITY.
Agnieszka Stembalska-Kozłowska1, Robert Śmigiel2, Kamila Schlade-Bartusiak1, Danuta Duś3, Maria Sąsiadek1*
1 Zakład Genetyki Akademii Medycznej we Wrocławiu
2 Katedra Patofizjologii Akademii Medycznej we Wrocławiu
3 Instytut Immunologii i Terapii Doświadczalnej PAN we Wrocławiu
* adres do korespondencji: Maria Sąsiadek, Zakład Genetyki AM we Wrocławiu, ul. Marcinkowskiego 1, 50-368 Wrocław, sasiadek@gen.am.wroc.pl
skrót tytułu: Niestabilność genetyczna w nowotworach
Niestabilność genetyczna, wyrażająca się nagromadzeniem w komórkach aberracji chromosomowych i/lub molekularnych, jest jedną z podstawowych cech nowotworów [Giannini 2000, Greenwood 2002, Simpson 1997, Tomlinson 2002]
Obecnie dyskutowane są dwie główne teorie tłumaczące znaczenie niestabilności genetycznej w etiologii nowotworów. Według jednej, niestabilność genetyczna jest podstawowa cecha warunkujaca transformacje nowotworowa, gdyz możliwia kumulacje kolejnych zmian genetycznych w pojedynczych komórkach. Mutacje spontaniczne w komórkach prawidłowych zachodzą z częstością około 1,4 x 10-10 mutacji na parę zasad, na jeden cykl. Oznacza to, że jedna mutacja zdarza się na 5 komórek w jednym cyklu replikacji (jednej generacji komórek). Bez wystąpienia dodatkowych mechanizmów sprzyjających zwiększeniu liczby mutacji w komórkach, czyli niestabilności genetycznej, nie byłaby możliwa transformacja nowotworowa [Loeb 2001]. Druga teoria opiera się na założeniu, że proces karcinogenezy może zostać zapoczątkowany w komórkach o prawidłowej stabilności genetycznej drogą nabycia przez komórki zwiększonego potencjału proliferacyjnego. W trakcie podziałów komórki tracą stabilność genetyczną, co sprzyja dalszym etapom transformacji [Cheah 2000].
Do wystąpienia niestabilności genetycznej i kumulacji zmian genetycznych w komórkach może prowadzić utrata funkcji genów: i) z grupy „caretakers”, kodujących białka biorące udział w naprawie DNA [Cheng 2000, Berwick 2000], ii) z grupy „gatekeepers”, kontrolujących przejście komórki w kolejne fazy cyklu podziałowego (G1/S; G2/M) [Bartek 2001, Robels 2001], iii) kontrolujących proces mitozy (mitotic checkpoint) [Gemma 2000].
Niezależnie od tego czy niestabilność genetyczna jest zjawiskiem pierwotnym, czy wtórnym w transformacji nowotworowej, prowadzi do kumulacji w komorce aberracji chromosomowych, mutacji lub/i wystapienia niestabilności mikrosatelitarnej.
Niestabilność chromosomowa została opisana przez Autorów w części I niniejszego artykułu pt. "Niestabilność chromosomowa w nowotworach”.
Niestabilność mikrosatelitarna:
Mikrosatelity są to krótkie sekwencje DNA, które składają się z powtarzających się 1-6 nukleotydowych motywów (mono, di, tri, tetra, penta, sexta - nukleotydowych). Sekwencje mikrosatelitarne są równomiernie rozmieszczone w genomie, zarówno w obszarach kodujacych, jak i niekodujących [Bal 2001].
Badania nad mechanizmem powstawania MSI w nowotworach doprowadziły do zidentyfikowania genów kodujących białka, które rozpoznają błędnie dobrane zasady, wycinają je i wymieniają na właściwe nukleotydy. Ten system naprawy DNA został nazwany systemem usuwania błędnie sparowanych zasad (ang. Mismatch Repair System; MMR). Do tej pory zostało rozpoznanych kilka genów, zwanych mutatorowymi, które kodują białka usuwające błędnie sparowane zasady (MLH1 3p31; MSH2 2p21-22; MSH6 2p16; PMS2 7p22; PMS1 2q31-33; MLH3 14q24.3) [Eshelman 1995, Simpson 1997].
Mutacje, które w genach MMR mają charakter inaktywujący, powodują utratę lub obniżenie sprawności naprawy błędów powstałych w procesie replikacji DNA. W efekcie mutacje zachodzą od 100 do 1000 razy częściej niż w komórkach prawidłowych i dotyczą różnych genów, również krytycznych dla transfomacji nowotworowej [Simpson 1997]. Zjawisko to jest określane jako niestabilność mikrosatelitarna (ang. Microsatellite Instability; MSI) i polega na zmianie długości (wielkości) alleli na skutek zwiększenia lub zmniejszenia liczby powtórzeń nukleotydowych.
MSI warunkuje powstanie tzw. fenotypu mutatorowego (Replication Error Phenotype; RER). Nowotwory, w których stwierdzono niestabilność mikrosatelitarną, są klasyfikowane jako RER+.
Niestabilność mikrosatelitarna i fenotyp mutatorowy zostały po raz pierwszy opisane w dziedzicznym niepolipowatym raku jelita grubego (ang. hereditary nonpolyposis colorectal cancer; HNPCC). Fenotyp RER+ jest obserwowany u prawie 92% pacjentów z HNPCC i u około 15% chorych ze sporadycznym rakiem jelita grubego [de la Chapelle 1995, Samowitz 1999]. Niestabilność mikrosatelitarna jest wykazywana również w 2-64% innych nowotworów zarówno dziedzicznych, jak i sporadycznych. Rozbieżności, w ocenie częstości występowania w nowotworach MSI § przez różnych autorów, mogą wynikać z różnic w metodyce badań, jak np. doborze i liczbie analizowanych markerów mikrosatelitarnych, interpretacji wyników oraz w kryteriach rozpoznawania MSI. Do oceny MSI w HNPCC obecnie rekomendowane jest stosowanie pięciu markerów mikrosatelitarnych: dwóch mononukleotydowych i trzech dinukleotydowych [....]. Przyjęto następujące kryteria klasyfikacji MSI w tych nowotworach:
MSI-H (microsatellite instability, high) - przynajmniej 2 spośród 5 badanych markerów lub ponad 30-40% (gdy badanych jest więcej markerów), wykazuje niestabilność,
MSI-L (microsatellite instability, low), jeden z pięciu badanych markerów wykazuje niestabilność bądź mniej niż 30-40%,
MSS (microsatellite stability), gdy żaden z badanych markerów nie wykazuje niestabilności [Boland 1998].
Według Bolanda i wsp. do określenia MSI wystarczająca może być ocena tylko dwóch mononukleotydowych i jednego dinukleotydowego markera [Boland 1998]. Mononukleotydowymi markerami mogą być: BAT26 (26 powtórzeń deoksyadenozyny - sekwencja zlokalizowana w obrębie intronu 5 genu MSH2), BAT25 (sekwencja (T)7A(T)25 zlokalizowana w obrębie intronu onkogenu c-kit) albo BAT40 (sekwencja zlokalizowana w obrębie intronu genu dehydrogenazy 3-β-hydroksysteroidu) (tabela 1). Są one wysoce specyficzne i szczególnie przydatne do oceny MSI-H [Boland 1998]. Kolejno De la Chapelle i wsp.[de la Chapelle 1995], Hong i wsp.[Hoang 1997] oraz Boland i wsp. [Boland 1998] wykazali, że do wykrywania MSI można zastosować tylko jeden mononukleotydowy marker, BAT26-poli(A)26. W opinii cytowanych autorów marker ten jest tak swoisty, że do oceny MSI wystarczy stwierdzenie zmiany liczby powtórzeń poli(A), bez konieczności porównania wyników z guza z wynikami z tkanki prawidłowej [de la Chapelle 1995, Boland 1998, Hoang 1997].
Rozróżnia się dwie grupy nowotworów, które wykazują podwyższoną częstość występowania MSI:
Nowotwory należące do tzw. „spektrum HNPCC”: rak jelita grubego, endometrium????????czy nie ma polskiej nazwy, jajnika, jelita cienkiego, żołądka, dróg żółciowych, guzy gruczołów łojowych, raki komórek podstawnych skóry, rogowiaki i inne raki skóry. Charakteryzują się fenotypem MSI podobnym do występującego w HNPCC i wykazują niestabilność w jedno- i dwunukleotydowych markerach [Ikichawa 1999].
Nowotwory piersi, płuc, skóry, pęcherza moczowego, mięsaków oraz raków głowy i szyi. Wykazują MSI tylko w niektórych powtórzeniach nukleotydowych [Peltomaki 2001].
W większości guzów sporadycznych wykazujących MSI, nie stwierdzono mutacji w genach MMR, co może znaczyć, że fenotyp RER+ w tych nowotworach może być skutkiem uszkodzenia innych genów. Gianni i wsp. w 2002 r. stwierdzili, że w „mismatch-repair-defficient cancers“ mutacji ulega gen MRE11, którego mutacje były obserwowane dotychczas w zespołach podobnych do ataksji-teleangiektazji (ang. ataxia-teleangiectasia- like syndrome). MER11 formuje kompleks z NBS1 i RAD50 (ang. M-N-R complex), którego integralność jest konieczna do sprawnego funkcjonowania punktu kontrolnego fazy S oraz relokalizacji tego kompleksu w miejsca uszkodzeń DNA [Giannini 2002].
Mechanizm molekularny niestabilności mikrosatelitarnej nie jest do końca wyjaśniony.
W odniesieniu do guzów ze spektrum HNPCC przyjmuje się obecnie dwie główne teorie:
1) nieprawidłowości podczas rekombinacji DNA (procesu crossing-over) oraz 2) tzw. efekt poślizgu polimerazy DNA. Podczas replikacji odcinka DNA, dwa łańcuchy DNA (matrycowy i nowo syntetyzowany) rozdzielają się, a następnie łączą się ponownie w błędnej konfiguracji. Jeżeli błędnie sparowane pary zasad są zlokalizowane w nowo syntetyzowanym łańcuchu, to kontynuowanie wydłużania łańcucha będzie powodować zwiększenie długości odcinka DNA. Niewłaściwie sparowane zasady zlokalizowane na matrycowym łańcuchu DNA będą powodować utratę jego krótkich odcinków [Kunkel 1993].
Utrata heterozygotyczności:
Zjawisko utraty heterozygotyczności (ang. loss of heterozygosity; LOH) wiąże się z utratą jednego z dwóch różnych alleli tego samego genu (heterozygota), co prowadzi do hemizygotyczności (obecność pojedynczego allelu) danego genu. LOH odgrywa ważną rolę w genetycznej etiologii nowotworów, gdyż delecja jest jednym z głównych mechanizmów odpowiedzialnych za utratę funkcji genów supresorowych i mutatorowych. Geny obu tych grup mają recesywny efekt działania na poziomie komórkowym, tzn. mutacje muszą dotyczyć obu alleli danego genu, aby doszło do jego inaktywacji [Knudson 1971].
Zjawisko utraty heterozygotyczności odgrywa kluczową rolę zarówno w inicjacji procesu nowotworowego, jest też obserwowane we wczesnych i zaawansowanych stadiach karcinogenezy [Knudson 1971, Lee 1992].
Występowanie LOH opisano w różnych typach nowotworów w tym białaczkach, chłoniakach, mięsakach, najczęściej jednak w nabłonkowych nowotworach złośliwych, jak § rak jelita grubego, nerki, sutka, płuc i pęcherza moczowego i innych [...].
Utrata heterozygotyczności stwierdzana w mniej niż 20% badanych przypadków dla danego locus, jest określana jako przypadkowa i interpretowana jako wyraz uogólnionej niestabilności genetycznej. LOH obserwowany w ponad 20% przypadków dla badanego markera jest interpretowany jako specyficzny [Li 1994, van der Riet 1994, Ah-See 1994, Nawroz 1994]. Badania nad specyficzną utratą heterozygotyczności są wykorzystywane do identyfikacji genów supresorowych i mutatorowych poprzez określanie tzw. najmniejszych obszarów delecji (minimal critical region of allelic loss), w obrębie których poszukiwane są następnie geny, krytyczne dla rozwoju badanego typu nowotworu (Tomlinson I. i wsp. 2002].
Utrata heterozygotyczności w markerach zlokalizowanych w pobliżu specyficznych loci (tzn. sprzężonych z danymi genami) w różnych częściach genomu może mieć znaczenie prognostyczne w niektórych nowotworach, zwłaszcza stwierdzenie LOH w więcej niż 2 loci (czy to nie jest utrata przypadkowa?). Nagromadzenie zmian typu LOH w komórce, np. w raku jelita grubego (HNPCC), wiąże się z patogenezą i progresją procesu nowotworowego. W gruczolakach jelita grubego stwierdzane są pojedyncze przypadki LOH, a w około 90% gruczolakoraków obserwowane są więcej niż 2 utraty (LOH). Równocześnie w zaawansowanych postaciach HNPCC stwierdza się niską częstość występowania LOH, co wiązać się może z dominacją określonego klonu komórek mającego najwyższy potencjał proliferacyjny [Vogelstein 1993, Kinzler 1996]. W rakach głowy i szyi natomiast, utrata heterozygotyczności stwierdzana w więcej niż 1 locus wiąże się z gorszą prognozą [Li 1994, Gleich 1996, Gleich 1999, El-Naggar 1995].
Metody badań niestabilności mikrosatelitarnej i utraty heterozygotyczności:
Do badania niestabilności mikrosatelitarnej i utraty heterozygotyczności wykorzystuje się polimorfizm długości markerów mikrosatelitarnych (tabela 2). DNA jest amplifikowane ze starterami swoistymi dla wybranych markerów mikrosatelitarnych. Otrzymane produkty są następnie rozdzielane na żelu (najczęściej poliakrylamidowym) i uwidaczniane za pomocą barwienia bromkiem etydyny, srebrzeniem, audioradiografią lub analizowane w sekwenatorach DNA z użyciem markerów fluorescencyjnych. Badania polegają na porównaniu markerów mikrosatelitarnych pomiędzy DNA wyizolowanym z tkanki nowotworu a DNA tkanek prawidłowych (głównie z krwi obwodowej), pochodzących od tego samego pacjenta. MSI jest rozpoznawana na podstawie każdej zmiany długości allelu, bedacej wyrazem zmiany liczby jednostek powtarzalnych w mikrosatelitach w komórkach guza w porównaniu z tkanką prawidłową. Rowniez nieswoista utrata heterozygotycznosci, wyrazajaca sie utrata jednego z dwoch alleli danego markera w mniej niz 20% badanych guzow, jest traktowana jako wyraz MSI. Analizę niestabilności mikrosatelitarnej w automatycznym sekwenatorze można przeprowadzać zarówno u konstytucjonalnych homozygot, jak i heterozygot w odniesieniu do badanego markera.
Referencyjny panel mikrosatelitów, rekomendowany przez Bolanda i wsp. do badań niestabilności mikrostelitarnej w HNPCC oraz kryteria interpretacji wyników zostały przedstawione w tabeli 2 [Boland 1998]. Kryteria oceny MSI w żelach denaturujących zostały przedstawione w tabeli 3. Przykłady wyników badań MSI przedstawiono na rysunkach 1a, b.
Utrate heterozygotycznosci rozpoznaje sie na podstawie oceny markerow informatywnych, tzn. takich, które występują w komorkach prawidlowych w postaci heterozygotycznej (posiadają różne allele w badanym locus). W żelu poliakrylamidowym heterozygota rozpoznawana jest na podstawie obecnosci dwoch prazkow, a w automatycznym sekwenatorze na podstawie wystepowania dwoch krzywych dla badanego locus (rysunek 3a, b, c). Homozygoty są klasyfilowane nieinformatywne i wylaczane z analizy. LOH rozpoznawana jest jako utrata jednego z prazkow w DNA guza w porównaniu z DNA komórek prawidłowych. Analiza LOH w sekwenatorze polega na porównaniu pola pod krzywymi § odpowiadającymi allelom badanego markera mikrosatelitarnego. Swoista utrata heterozygotycznosci jest rozpoznawana tylko w guzach nie wykazujacych MSI, gdyz w guzach o fenotypie mutatorowym nie mozna odroznic LOH swoistego od przypadkowego (wynikajacego z niestabilności mikrosatelitarnej) [Canzian 1996]. Utrata heterozygotyczności oceniana jest według wzoru (T1xN2)/(T2xN1), gdzie N1 i N2 stanowią pola pod krzywymi otrzymanymi z DNA z tkanki prawidłowej, a T1 i T2 krzywe z DNA z tkanki nowotworowej. Wynik obliczeń powinien znajdować się w granicach od 0,0 do 1,0. Wynik >1,0 wymaga odwrócenia wzoru: (T2xN1)/(T1xN2) [Cawkwell 1993]. Opracowanie i analiza danych prowadzona jest za pomocą programów komputerowych.
Całkowita utrata allelu oznacza teoretycznie wynik 0,0, ale ponieważ tkanki nowotworowe są zawsze heterogenne i zawierają część komórek prawidłowych (nawet do 50%), to całkowitą utratę allelu rozpoznaje się już, gdy wynik wynosi 0,5 [Cawkwell 1993]. LOH jest rozpoznawany jeśli wyniki obliczeń zawarte są pomiędzy 0,0 a 0,5. Można także przyjąć wynik LOH jako zawarty między 0,0 a 0,7, przy założeniu, że tkanka guza może zawierać tylko około 30% prawidłowych komórek zrębowych [Karnik 1998].
Inną metodę oceny LOH zaproponowali Vida i wsp. [Vida 2000]. Według cytowanych autorów LOH może być była oceniana poprzez porównanie stosunku wysokości (peak height) krótkiego (Sn) i długiego (Ln) allelu badanego markera, uzyskanych DNA tkanki prawidłowej do stosunku wysokości odpowiednich alleli (St i Lt), uzyskanych z DNA guza (Sn:Ln / St:Lt). LOH jest rozpoznawany, gdy tak liczona zmiana wielkości allelu w DNA guza wynosi, co najmniej 50% (wynik< 0,5 lub >2,0).
Podsumowanie:
W nowotworach rozwijających się na podłożu dziedzicznych mutacji genów kodujących białka naprawy DNA, jak np. uwarunkowany autosomalnie, dominujaco dziedziczny niepolipowaty rak jelita grubego, czy tez niektóre nowotwory układu krwiotwórczego, rozwijające się na podłożu autosomalnie recesywnie uwarunkowanych defektów naprawy DNA, niestabilność genetyczna jest zjawiskiem pierwotnym. W innych natomiast nowotworach, jak np. dziedziczny polipowaty rak jelita grubego, pierwotną zmianą jest mutacja genu nie zaangażowanego w kontrolę stabilności genetycznej. Wydaje sie wiec, ze zarowno etiologia genetyczna jak i sekwencja zdarzeń genetycznych w różnych nowotworach jest różna, zgodna z teorią o heterogennej etiologii nowotworów.
Tabela 1. Charakterystyka mononukleotydowych markerów mikrosatelitarnych.
Marker |
Lokalizacja |
Gen |
Wielkość (bp-pary zasad) |
Temperatura przyłączania (C°) |
BAT25 |
4q12 |
c-kit |
90 |
58 |
BAT26 |
2p16 |
MSH2 |
80-100 |
58 |
BAT40 |
1p13.1 |
Dehydogenase 3-β-hydroksysteroid gene |
80-100 |
58 |
Tabela 2. Panel referencyjny, rekomendowany przez Boland i wsp. do oceny niestabilności mikrosatelitarnej w nowotworach jelita grubego [Boland 1998]
Marker |
Jednostka powtórzeniowa |
BAT25 BAT26 D5S346 D2S123 D17S250 |
mononukleotydowe mononukleotydowe dinukleotydowe dinukleotydowe dinukleotydowe |
Kryteria interpretacyjne |
||||||
|
loci analizowanych =5 |
loci analizowanych >5 |
Interpretacja |
|||
No markerów Wykazujący MSI |
≥2 1 0 |
≥30%-40% <30%-40% 0 |
MSI-H MSI-L MSS lub MSI-L |
|||
Alternatywne loci |
||||||
BAT40 |
APC |
D18S64 |
D13S153 |
D7S519 |
||
BAT34C4 |
D20S100 |
D18S69 |
D13S175 |
D5S107 |
||
TGF-β-RII |
D18S55 |
D17S787 |
D10S197 |
D3S1029 |
||
ACTC |
D18S58 |
D17S588 |
D8S87 |
D2S123 |
||
CCD1 |
D18S61 |
D17S250 |
||||
Tabela 3. Kryteria oceny MSI w denaturujących żelach PAA.
|
Rozdział w żelu PAA denaturującym + metoda srebrzenia |
Analiza fragmentów w sekwenatorze z użyciem markerów fluoroscencyjnych |
Kryteria oceny MSI |
|
|
Rysunek 1. Badanie MSI w automatycznym sekwenatorze.
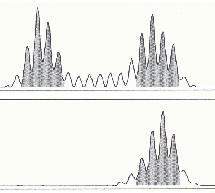
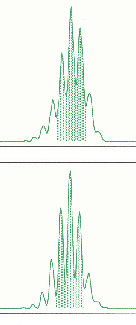
a) MSI b) brak MSI
Rysunek 3. Badanie utraty heterozygotyczności w automatycznym sekwenatorze.
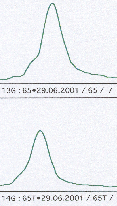
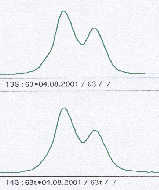
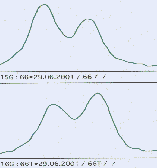
a) przykład homozygoty b) przykład heterozygoty c) przykład LOH
Piśmiennictwo:
[1] AH-SEE K, COOKE TG, PICKFORD IR, SOUTAR D, BALMAIN A. An allelotype of squamous carcinoma of the head and neck using microsatellite markers. Cancer Res 1994; 54: 1617-1621.
[2] BAL J [red.], Badania molekularne w medycynie. Wyd Nauk PWN 2001, wyd. I.
[3] BARTEK J, LUKAS J. Mammalian G1- and S-phase checkpoints in response to DNA damage. Curr Opin Cell Biol 2000; 6: 734-747.
[4] BEN YEHUDA A, Globerson A, Krichevsky S, Bar On H, Kidron M, Friedlander Y, Friedman G, Ben Yehuda D. Ageing and the mismatch repair system. Mech Ageing Dev 2000; 121:173-179.
[5] Berwick M, Vineis P. RESPONSE re: markers of DNA repair and susceptibility to cancer in humans: an epidemiologic review. J Natl Cancer Inst 2000; 92:1537.
[6] Boland CR, Thibodeau SN, Hamilton SR, Sidransky D, Eschelman JR, Burt RW, Meltzer SJM, Rodriguez-Bigas MA, Fodde R, Ranzani GN, Srivastava S. A National Cancer Institute Workshop on Microsatellite Instability for Cancer Detection and Familial Predisposition: Development of International Criteria for the Determination of Microsatellite Instability in Colorectal Cancer. Cancer Res 1998; 58: 5248-5257.
[7] CANZIAN F, SALOVAARA R, HEMMINKI A, KRISTOP, CHADWICK RB, AALTONEN LA, DE LA CHAPELLE A. Semiautomated assessment of loss of heterozygosity and replication error in tumors. Cancer Res 1996; 14: 3331-7.
[8] CAWKWELL L et al. Rapid detection allele loss in colorectal tumours using microsatelites and fluorescent DNA technology. Br J Cancer 1993; 67: 1262-67.
[8] CHeah PY, Eu KW, Seow FC. Update of genetics in colorectal carcinomas: genomic instability and somatic evolution. Ann Acad Med Singapore 2000; 29: 331-336.
[9] Cheng L, Spitz MR, Hong WK, Wie Q. Reduced expression levels of nucleotide excision repair genes in lung cancers: a case-control analysis. Carcinogenesis 2000; 21: 1527-1530.
[10] de la Chapelle A, Peltomaki P. Genetic of hereditary conol cancer. Annu Rev Gen 1995; 29: 329-348.
[11] EL-NAGGAR AK, HURR K, BATSAKIS JG, LUNA MA, GOEPFERT H, HUFF V. Sequential loss of heterozygosity at microsatellite motifs in preinvasive and invasive head and neck squamous cell carcinoma. Cancer Res 1995; 55: 2656-2659.
[12] Eshelman JR, Marcowitz SD. Microsatellite instability in inherited and sporadic neoplasms. Curr Opin Oncol 1995; 7: 83-89.
[13] Gemma A, Seike M, Seike Y, Uematsu K, Hibino S, Kurimoto F, Yoshimura A, Shibuya M, Harris CC, Kudoch S. Somatic mutation of the hBUB1 mitotic checpoint gene in primary lung cancer, Genes Chromosomes Cancers 2000; 3: 213-218.
[14] Giannini G, RISTORI E, CERIGNOLI F, RINALDI C, ZANI M., VIEL A, OTTIN L. Human MRE11 is inactivated in mismach repair-deficient cancers. EMBO Rep 2000; 3: 248-254.
[15] GLEICH LL, LI YQ, BIDDINGER PW, GARTSIDE PS, STAMBROOK PJ, PAVELIC ZP, GLUCKMAN JL. The loss of heterozygosity in retinoblastoma and p53 suppressor genes as a prognostic indicator for head and neck cancer. Laryngoscope 1996; 106: 1378-1381.
[16] GLEICH LL, LI YQ, WANG X, STAMBROOK PJ, GLUCKMAN JL. Variable genetic alterations and survival in head and neck cancer. Arch Otolaryngol Head Neck Surg 1999; 125: 949-952.
[17] Goukassian D, Gad F, Yaar M, Eller MS, Nehal US, Gilchrest BA.
Mechanisms and implications of the age-associated decrease in DNA repair capacity.
FASEB J 2000; 14: 1325-34.
[18] Greenwood E. Genomic instability. Let's stick together. Nature Reviews Cancer 2002; 2: 78.
[19] Hoang JM, Cottu PH, Thuille B, Salmon RJ, Thomas G, Hamelin R. BAT-26, an indicatior of the replication error phenotype in colorectal cancers and cell lines. Cancer Res 1997; 58: 300-303.
[20] KARNIK P, PARIS M, WILLIAMS BRG, CASEY G, CROWE J, CHEN P. Two distinct tumor suppressor loci within chromosome 11p15 implicated in breast cancer progression and metastasis. Hum Mol Genet 1998; 7: 895-903.
[21] KINZLER KW, VOGELSTEIN B. Lessons form hereditary colorectal cancer. Cell 1996; 87: 159-170.
[22] Knudson AGJ: Mutation and cancer: statistical study of retinoblastoma. Proc Natl Acad Sci 1971; 61: 820-823.
[23] Kunkel TA. Slippery DNA and diseases. Nature 1993; 365: 207-208.
[24] LEE NK. Tumor suppressor gene. Head Neck 1992; 14: 407-414.
[25] LI X, LEE NK, YE YW, WABER PG, SCHWEITZER C, CHENG QC, NISEN PD. Allelic loss at chromosomes 3p., 8p., 13q, 17p. associated with poor prognosis in head and neck cancer. J Natl Cancer Inst 1994; 86: 1524-1529.
[27] Loeb LA. A mutator phenotype in cancer. Cancer Res 2001; 61: 3230-3239.
[28] NAVROZ H, VAN DER RIET P, HRUBAN RH, KOCH W, RUPPERT JM, SIDRANSKY D. Allelotype of head and neck squamous cell carcinoma. Cancer Res 1994; 54: 1152-1155.
[29] Ponder B. Cancer. Gene losses in human tumours. Nature 1988; 335: 400-402.
[30] Robels AI, Harris CC. P53-mediated apoptosis and genomic instability diseases Acta Oncol 2001; 40: 696-701.
[31] Samowitz WS, Slattery ML. Regional Reproducibility of Microsatellite Instability in Sporadic Colorectal Cancer. Genes Chromosomes Cancer 1999; 26: 106-114.
[32] Simpson AJ. The natural somatic mutation frequency and human carcinogenesis. Adv Cancer Res 1997; 71: 209-240.
[33] TOMLINSON I, LAMBROS M, ROYLANCE R. Loss of heterozygosity analysis: Practically and conceptually flawed? Genes Chromosomes Cancer 2002; 34: 349-353.
[34] TOMLINSON I, SASIENI P, BODMER W. How many mutations in a cancer? Am J Pathol 2002;160: 755-8.
[35] van Houten VM, Tabor MP, van den Brekel MW, Denkers F, Wishaupt RG, Kummer JA, Snow GB, Brakenhoff RH. Molecular assays for the diagnosis of minimal residual head-and-neck cancer: methods, reliability, pitfalls, and solutions. Clin Cancer Res 2000; 6: 3803-3816.
[36] VAN DER RIET P, NAVROZ H, HRUBAN RH, CORIO R, TOKINO K, KOCH W, SIDRANSKY D. Frequent loss of chromosome 9p21-22 early in head and neck cancer progression. Cancer Res 1994; 54: 1156-1158.
[37] VOGELSTEIN B, KINZLER KW. The multistep nature of cancer. Trends Genet 1993; 9: 138-141.
nowotwór
krew
krew
nowotwór
krew
nowotwór
Wyszukiwarka
Podobne podstrony:
niestabilnosc chrmosomowa wysl. (1), AM, rozne, genetyka, genetyka, praca prof
algorytm 2[2], AM, rozne, genetyka, genetyka, praca prof
Alzheimer 5 wysl, AM, rozne, genetyka, genetyka, praca prof
prenat. bad-nowe, AM, rozne, genetyka, genetyka, praca prof
Badanie niestabilnosci genetycznej, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
genetyka 2 kolo, AM, rozne, genetyka, genetyka, geny
PCR, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
sciaga genetyka, AM, rozne, genetyka, genetyka
achondroplazja, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
sca ca mn, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
wykład 3 i 4, AM, rozne, genetyka, genetyka
Cwiczenie7, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
Poronienia i niemożnosć zajscia w ciażę, AM, rozne, genetyka, genetyka, GENETYKA, Genetyka ze strony
więcej podobnych podstron