221

0 < 90°), czy też niezwilżającą (0 > 90°). W pierwszym przypadku siły adhezji (przylegania) są większe od sił kohezji (spójności), w następstwie czego wypadkowa sił oddziałujących spowoduje podniesienie się cieczy na krótkim odcinku wzdłuż ścian naczynia.
Jeżeli, z drugiej strony, oddziaływanie między cieczą a powierzchnią ciała stałego polega na odpychaniu (siły kohezji są większe od adhezji), to powierzchnia cieczy (menisk) przybierze kształt krzywizny skierowanej w dół. Jeżeli odległość pomiędzy dwiema równoległymi ścianami naczynia jest równa lub mniejsza od promienia krzywizny menisku cieczy, to obserwuje się zjawisko podciągania kapilarnego (rys. 3.53). Wielkość h można wyrazić również liczbami ujemnymi dla cieczy niezwiiżających ścian naczynia (obniżenie poziomu cieczy).
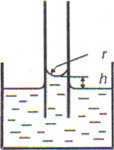
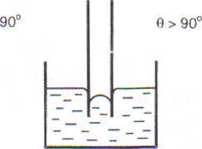
Rys. 3.53. Zachowanie się cieczy niezwilżającej i zwilżającej w kapilarze Wysokość, do której podnosi się poziom cieczy w kapilarze h, określona jest równaniem
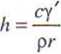
(3.102)
gdzie:
h
c
/
y
p
r
wysokość podciągania kapilarnego, m; stała;
napięcie powierzchniowe cieczy, N/m; gęstość cieczy, kg/m3; promień krzywizny, m.
W 1921 r. Washburn pierwszy zasugerował użycie rtęci pod ciśnieniem do określenia rozkładu porów dla porowatych soli. Rtęć posiada bowiem przeciętny kąt zwilżania ciał stałych w temperaturze pokojowej około 140°, co gwarantuje uniknięcie zjawiska podciągania kapilarnego. Opór ten może być przezwyciężony przez ciśnienie zewnętrzne. Zależność między rozmiarem porów r, do których może wniknąć ciecz, a zewnętrznym ciśnieniem p na nią wywieranym, wyrażona jest następującym równaniem
|
27try'cos0 = rcr2p |
(3.103) | |
|
r |
- promień porów, m; | |
|
P |
- ciśnienie, N/m2; | |
|
0 |
- kąt zwilżania, deg. |
a po uproszczeniu
pr = 2y'cos0 (3.104)
221
Wyszukiwarka
Podobne podstrony:
12 zmęczeniowych nisko- i wysokocyklowych [64], W pierwszym przypadku obciążeń, w którym obciążenia
strona0005 (11) ;iu Maria /.uhrowsku czy też w złym środowisku, z jakiego dziecko pochodzi. Wychowan
strona0005 (11) ;iu Maria /.uhrowsku czy też w złym środowisku, z jakiego dziecko pochodzi. Wychowan
Berlin, Korzenie romantyzmu, pierwszy szturm na oświecenie (3) Czy też dobrem jest jedynie coś, co p
bolsche0090�01 djvu 90 wiano kwestję otwartą, czy naprawdę tylko wówczas na początku samorodztwo ist
img045 (8) 90 Jak w przypadku rzeczowników niepoliczalnych, mówiący ma jednak możliwość narzucenia k
PICT5940 przedmiot wymieniony jest przez większość uczniów na pierwszym miejscu, czy też zajmuje jed
DSC00102 (34) iiJarnm ze sfifte zaleca słą utrżymywanle możliwie wysoki) temperatury ** do 90-95° C.
72464 Scan0166 Pierwszy jeździec. Żadnych skoków,; ostróg ani uniesionej ręki czy też głosu. ■165
według nazwisk autorów, w braku zaś tychże, według pierwszych wyrazów, czy też rzeczowników tytułu,
13 kwesty a żołądka jest i być musi pierwszo-rzędnem zagadnieniem. Dla chleba codziennego, czy też
DSC?46 ~tmrAlcter Pierwsza teza rozbijała (czy też lepiej: ich> ur“m£j£t mtypie” Istoty Najwyższ
img058 (45) 58 nia, czy to przy robocie grubszych rzeczy, jak np. siekier i dłót. powstałe, czy też
więcej podobnych podstron