LastScan5(2)

|
WPŁYW TEMPERATURY | |
|
NA AKTYWNOŚĆ ENZYMÓW • Temperatura może działać na enzymy jako (górny rysunek): aktywator - reguła van’t Hoffa - | |
|
podwyższenie temperatury o 10°C szyi*ou |
Szybkość |
|
powoduje około dwukrotny wzrost |
maksymalna |
|
szybkości reakcji enzymatycznych. |
reakcji / , \ |
|
Temperatura optymalna - szybkość |
/ ' \ |
|
reakcji jest największa. |
/ ! \ |
|
inhibitor - niska temperatura hamuje działanie enzymów ze względu na niską energię kinetyczną reagujących |
/ \ \ |
|
cząsteczek; |
j' Temperatura |
|
inaktywator - przy wzroście | |
|
temperatury powyżej optymalnej następuje gwałtowne obniżenie szybkości reakcji, co jest związane z denaturacją cieplną białka enzymu. | |
• Wpływ pH na aktywność enzymu związany jest z wartością stałych dysocjacji:
1. grup czynnych w centrum aktywnym enzymu uczestniczących w wiązaniu substratu.
2. grup funkcyjnych w cząsteczce substratu, którymi wiąże się on z enzymem.
3. grup funkcyjnych w cząsteczce enzymu, oa których zależy kataliza.
4. innych grup w cząsteczce enzymu, których stan zionizowaniamoże gwarantować katalitycznie aktywną konformację.
Każdy enzym ma optymalną wartość pH, przy ktorei szybkość reakcji jest maksymalna. Niewielkie odchylenia od optimum powodują zmniejszenie szybkości reakcji, a duże odchylenia prowadzą do denaturacji białka enzymu.

WPŁYW JONÓW METALI NA AKTYWNOŚĆ ENZYMÓW
Jony metali mogą pełnić funkcje:
katalityczne - biorąc udział w katalizie, np. przenosząc elektrony (jony Cu2*, Fe2*);
strukturalne - łącząc podjednostki enzymów lub stabilizując strukturę przestrzenną enzymów;
aktywatorów - szereg enzymów wymaga obecności kationów lub anionów jako wewnątrzkomórkowych aktywatorów ich działania.
Metaloenzymy- enzymy, które do swojego działania wymagają obecności jonów metali, np: dehydrogenaza alkoholowa
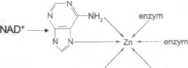
enzym afcohol
(substral)

Wyszukiwarka
Podobne podstrony:
LastScan5 (4) WPŁYW TEMPERATURY NA AKTYWNOŚĆ ENZYMÓW • Temperatura może działać na enzymy jako (gó
PB030078 WPŁYW TEMPERATURY NA AKTYWNOŚĆ ENZYMÓW • Temperatura może działać na enzymy jako (górny
Ich mechanizm katalizy wymaga triady aminokwasowej w centrum aktywnym enzymów. Restza serynowa dział
Zdjęcie0182 Wpływ temperatury i pH na aktywność enzymów immmi C
Wpływ temperatury na aktywność enzymów Prędkość reakcji enzymatycznej w pewnym przedziale temperatur
SDC10488 (2) © •Wpływ temperatury na aktywność enzymów Wzrost temperatury zwiększa szybkość reakcji
Laboratorium biochemiiWpływ temperatury na aktywność enzymów (ćw E)1. Cel
56 Agnieszka Głowacka, Tadeusz Trzmiel I I Rys. 2. Wpływ temperatury na aktywność proteolityczną
Zdjęcie0181 Temperatura wpływa na aktywność enzymów Dla większości enzymów można określić tzw optimu
WPŁYW TEMPERATURY OGRZEWANIA 1 STĘŻENIA SOU NA AKTYWNOŚĆ AMINOTR/INSFERAZ... 19 GOT [15]. Jak sugero
WPŁYW TEMPERATURY OGRZEWANIA I STĘŻENIA SOLI NA AKTYWNOŚĆ AM1NOTRANSFERAZ... 23 Tabela 4 Analiza
Zadanie 2. Wpływ temperatury na aktywność inwertazy drożdży. Wykonanie: Przygotować 6 probówek, a
Rys. 2. Wpływ temperatury na aktywność polifenolooksydazy obecnej w wyciągach z truskawek. Fig. 2. E
skanuj0006 (243) 11-5. Wpływ temperatury na szybkość wzrostu Escherichia coli. Linią ciągłą oznaczon
więcej podobnych podstron