DSCN6244 (Kopiowanie)
,0,97. NaCl
przez substancję rozpuszczoną, albowiem wytwarzają jej otoczkę hydratacyjną. Tc cząsteczki zostają wyeliminowane jjc zderzeń - dość trwale połączyły się z substancją rozpuszczoną, a ta przecież nie może przenikać przez błonę.
-h2o
■b.p.
A zatem znacznie więcej cząsteczek rozpuszczalnika przepływa pracz błonę w stronę substancji rozpuszczonej, aniżeli w stronę przeciwną. Ilość roztworu po jednej stronie rośnie - poziom cieczy w probówce się podnosi i podniesie się tak wysoko, aż ciśnienie wywierane przez słup wody stanie się równe sile, która zmusza wodę do przenikania do wnętrza probówki.
Ciśnienie wywierane przez słup wody w probówce nazywamy KaSmeniero osmotycznym roztworu.
k-to.
B
Ryc. 5 - 70. Doświadczenie ilustrujące proces osmozy (opis w tekście).
A - początek;
B - koniec doświadczenia, h - wysokość słupa cieczy;
H.O - czysta woda;
b.p. - błona półprzcpuszczalna (JD).
W komórce ciśnieniem osmotycznym jest ciśnienie wywierane przez zawartość komórki na jej błonę. Jest ono równe ciśnieniu osmotycznemu 0,9% roztworu wodnego chlorku sodu lub 5% roztworu glukozy. A zatem komórkę — znajdującą się w warunkach prawidłowych pod względem ciśnienia osmotycznego możemy porównać z użytą w naszym doświadczeniu probówką, wypełnioną opisanymi roztworami. Jeżeli komórkę umieścimy w 0,9% roztworze NaCl bądź 5% roztworze glukozy, ciśnienie osmotyczne w komórce będzie takie samo, jak ciśnienie osmotyczne środowiska. Płyn pozostający w równowadze osmotycznej z cytoplazmą nazywamy płynem izotonicznym albo Kzoośmotyęznym. W normalnych warunkach osocze krwi, limfa i wszystkie ciecze tkankowe są izotoniczne — tzn. posiadają takie samo ciśnienie osmotyczne, czyli taką samą ilość (molową) substancji rozpuszczonych, jak komórka.
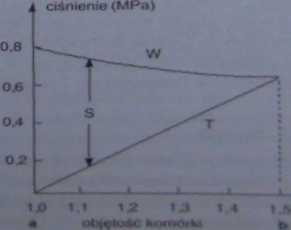
Jeżeli natomiast komórkę przeniesiemy do płynu łiipotonicznego. a więc o mniejszym stężeniu substancji rozpuszczonych niż w cytoplazmie (np. do czystej wody), wówczas woda będzie wnikać do wnętrza komórki. Możemy powiedzieć, że każda komórka zasysa wodę. Siłę. z jaką rozpuszczalnik wnika do wnętrza, nazywamy siłą ssącą i zależy ona głównie od tzw. wartości osmotycznej (ryc. 5-71). Ponieważ w komórce ilość wody narasta, a zatem coraz to większa liczba cząsteczek wywiera coraz większe ciśnienie osmotyczne i rozpycha błonę komórki (jej objętość rośnie). W przypadku komórek pozbawionych ścian, nazbyt wysokie ciśnienie osmotyczne może spowodować ich rozerwanie. Dla przykładu - prawidłowe erytrocyty człowieka, umieszczone w 0,6% roztworze NaCl. pęcznieją i pękają. Natomiast komórki roślinne osiągają pewne maksymalne uwodnienie (ryc. 5-71) - przed pękaniem chroni je ściana komórkowa. Dlatego szereg grzybów, glonów i roślin może bytować w „słodkich" wodach.
Ryc. 5 - 71. Wykres, będący ilustracją doświadczenia nad zależnością pomiędzy siłą ssącą (S), wartością osmotyczną (W), Magurom komórki (T) oraz ciśnieniem osmotycznym (ciśnienie) ■ objętością komórki roślinnej. Komórkę roślinną w stanic jjngżowlizy (a) umieszczono w roztworze lupolonicznyin i badano ' du momentu uzyskania pełnego tutgoru <b). /.wróć uwagę, te ■ wzrostu turgoru maleją: wartość osmotyczną i siła ssąca pa< i-ąlliii k - W, w punkcie b: S - 0) OD).
Wyszukiwarka
Podobne podstrony:
DSCN6244 (Kopiowanie) 227 227 jtjjzcz substancję rozpuszczoną, albowiem wytwarzają jej otoczkę hydra
DSC00438 (12) Zmiana fizycznych właściwości rozpuszczalnika spowodowana przez substancję rozpuszczon
skanuj0040 (Kopiowanie) Oznaczając całkowite stężenie substancji leczniczej w osoczu przez C, a prze
P1100077 i redukcja substancji elektroaktywmych, jest określony przez własności rozpust czalnika om
DSC01277 W Separacja substancji rozpuszczonych o różnych rozmiarach r cząsteczkowych i jonowych prze
DSCN6226 (Kopiowanie) w formylomctioninę przez enzym transformylazę. Ten kompleks z kolei wykazuje n
DSCN6226 (Kopiowanie) w formylometioninę przez enzym transformylazę. Ten kompleks z kolei wykazuje n
DSCN6241 (Kopiowanie) 124 Biologia - repetytorium dla kandydatów na akademie medyczne Substancję łąc
DSCN6241 (Kopiowanie) 224 Biologia * repetytorium dla kandydatów na akademie medy*r$* Substancję łąc
DSCN6243 (Kopiowanie) 5 dyfuzja T* DIALIZA 5.4.4. lYansport przez błony Przez błony komórkowe przeni
DSCN6243 (Kopiowanie) 5.4.4. Transport przez błony Przez błony komórkowe przenika nic tylko informac
DSCN6272 (Kopiowanie) Przez ich skrzyżowanie otrzymuje się 16 połączeń (genotypów), wśród których wy
DSCN6272 (Kopiowanie) Przez ich skrzyżowanie otrzymuje się 16 połączeń (genotypów), wśród których wy
DSCN6285 (Kopiowanie) j, Diinl:ic:iwść 267 Heterozyjne są często również mieszańce jcdnogatunkowc. a
DSCN6285 (Kopiowanie) K Dńed:ic:ność 267 Heterozyjne są często również mieszańce jcdnogatunkowc. ale
SL275487 ZAPACH Kształtowany jest przez substancje lotne
IMG@98 Mianowanego (o dokładnie znanym stężeniu) roztworu KMn04 nie można otrzymać przez zwykłe rozp
więcej podobnych podstron