3582325159
Grzegorz Zdziebło Krzysztof Warzecha
Sprawozdanie Ćwiczenie 3 Estryfikacja
1. Wstęp
Celem ćwiczenia było zapoznanie się z metodą Estryfikacji. Polega ona na wydzieleniu składnika z mieszaniny związków chemicznych przez jego rozpuszczeniu w odpowiednio dobranym rozpuszczalniku. Po dodaniu rozpuszczalnika wydzielają się dwie fazy. Jedna to roztwór wydzielanego składnika a druga to mieszanina pozostała po ekstrakcji.
2. Opis ćwiczenia
Celem ćwiczenia była ekstrakcja kwasu benzoesowego z toluenu.
Do uszczelnionego rozdzielacza dodano 25cm3 kwasu benzoesowego w toluenie oraz 25cm3 5 % roztworu NaOH. Po dodaniu NaOH roztwór zaczęto mieszać odkręcając co chwile korek w celu ulotnienia się powietrza, po czym zaczęto mieszać energicznie. W czasie tego procesu powstał benzoesan sodu Po wymieszaniu rozdzielacz umieściliśmy na statywie i po krótkiej chwili dolną fazę zlaliśmy do zlewki(faza wodna z benzoesanem sodu) a w rozdzielaczu pozostała faza toluenowa. Do Zlewki dodaliśmy kwasu solnego aż do uzyskania odczynu kwaśnego po czym ogrzaliśmy w celu rozpuszczenia powstałego osadu Po ogrzaniu od razu przesączyliśmy przez sączek. Za 1 razem wykrystalizowało nam w sączku wiec powtórzyliśmy operacje podgrzewania ponownie dodając 10cm3wody i wrzucając sączek z kryształkami po czym ponownie przesączyliśmy z małymi strat. Wykrystalizowany związek przesączyliśmy w podciśnieniu i włożyliśmy do pudełek w celu zważenia na następnych zajęciach. Masa pudełka bez kwasu wynosiła 0.34 g. Po przesuszeniu waga samego proszku wyniosła 0,30g. Temperatura topnienia kwasu benzoesowego wyniosła 123-124 “C Warstwę toluenową która pozostała w rozdzielaczy przemyliśmy dwu krotnie wodą destylowaną o objętości 25cm3, za każdym razem mieszając i odpowietrzając rozdzielacz. Po wymieszaniu i oddzieleniu się faz, fazę wodną z zanieczyszczeniami zlewaliśmy do zlewki. Tak przemyty toluen przelaliśmy do kolbłri stożkowej po czym dodaliśmy środka suszącego (bezwodny siarczan magnezu) i odstawiliśmy na parę minut. Następnie odsączyliśmy środek suszący przez sączek karbowany. Tak przesączony toluen przedestylowaliśmy metodą destylacji prostej. Temperatura wrzenia Toluenu wyniosła 107 °C a objętość powstałego toluenu wyniosła 19 cm3
3. Opracowanie wyników
a) Na podstawie wyodrębnionego kwasu benzoesowego obliczyć jego stężenie molowe w
roztworze użytym do ekstrakcji
Dane:
V=2 5 cm3=0,02 5dm3
mskwm= masa kwasu benzoesowego po oczyszczeniu; 0,3 g Mkwas= Masa molowa kw. benzoesowego: 122 g/mol
M 122
— = 2,459-10“3[mo/]
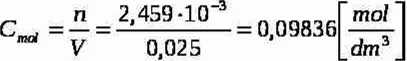
Wyszukiwarka
Podobne podstrony:
Sprawozdanie Ćwiczenie 5 Estryfikacja Grzegorz Zdziebło Krzysztof Warzecha1. Wstęp Celem ćwiczenia
SprawozdanieĆwiczenie 4 Sulfonowanie p-ksylenu Grzegorz Zdziebło Krzysztof Warzecha.1. Wstęp Celem
01.04.2009 Grzegorz Zdziebło Krzysztof Warzecha Gr P6 zespół F lab 8Sprawozdanie z Ogniwa
Grzegorz Zdziebło Krzysztof Warzecha Gr P6 zespół F lab 11 12.05.2009Liczby przenoszenia 1. Cel
28.05.2009 Grzegorz Zdziebło Krzysztof Warzecha Gr P6 zespół F lab 11Sprawozdanie zSzybkość roz
26.05.2009 Grzegorz Z dziebło Krzysztof Warzecha Gr. P6 zespół F lab 3Sprawozdanie z Lepkości 1
SprawozdanieĆwiczenie 2 Krystalizacja Grzegorz Z dziebło Krzysztof Warzecha1.
1 WSTĘP Celem projektu było zastosowanie programowania ograniczeniowego do rozwiązywania problemów z
Krzysztof Warzecha Grzegorz Zdziebło Gr 6 4.03.2009Sprawozdanie z Diagramu Fazowego
1. Wstęp. Celem ćwiczenia jest zapoznanie się z działaniem i zastosowaniami diody
Wstęp Celem naszego ćwiczenia było wyznaczenie gęstości bezwzględnej cieczy i ciała stałego za pomoc
Badanie tranzystora bipolarnego Wstęp: Celem ćwiczenia jest poznanie właściwości statecznych
Obiekt dynamiczny liniowy 1. Wstęp Celem ćwiczenia było zapoznanie sią z podstawowymi obiektami
1. Wstęp Celem ćwiczenia jest zbadanie właściwości sterowania prędkością silnika
skanuj0001 (4) INSTRUKCJA do ĆWICZENIA "IDENTYFIKACJA POLIMER t 1. Wstęp Celem badań identyfika
1) Wstęp Celem ćwiczenia jest pomiar względnego wydłużenia drutu pod wpływem temperatury, a co za ty
więcej podobnych podstron