8719220264
Jeżeli chodzi o aa z rodnikiem polarnym i jonizującym, sytuacja przedstawia się odmiennie dla kwasów oraz zasad. W przypadku kwasu najpierw tracony jest proton z własnej reszty karboksylowej, następnie z grupy bocznej, a na samym końcu z własnej grupy aminowej; wobec tego pi oblicza się podobnie jak dla aa z R niepolamym, czyli: pi = Vi x (pK, + pK2). Natomiast w przypadku zasady najpierw tracony jest proton z reszty karboksylowej, następnie z grupy bocznej, a ostatecznie z własnej grupy aminowej; wyrażenie opisujące pi przyjmuje zatem postać: pi = Vi x (pK2 + pK3).
f) właściwości chemiczne - reakcje aa
Aa posiadają kilka grup funkcyjnych - a-aminową, a-karboksylową oraz reaktywne grupy w obrębie R (niektóre aa) - dzięki czemu mogą ulegać wielu rozmaitym przemianom.
• Reakcje grupy karboksylowej:
> dysocjacja i tworzenie soli (aa + zasada):
H2N-CH(R)-COOH —OH — H2N-CH(R)-COO H2N-CH(R)-COOH + NaOH — H2N-CH(R)-COONa (sól sodowa aa)
> tworzenie estrów (aa + alkohol):
H2N-CH(R)-COOH + R|-OH — H2N-CH(R)-CO-0-R,
> tworzenie amidów
> tworzenie bezwodników kwasowych
> dekarboksylacja (pod wpływem ogrzewania lub enzymatycznie):
H2N-CH(R)-COOH —AT, -CCb— R-CH2-NH2
• Reakcje grupy aminowej:
> dysocjacja i tworzenie soli:
H2N-CH(R)-COOH —H*— H,N+-CH(R)-COOH
H2N-CH(R)-COOH + HC1 — Cl H3N+-CH(R)-COOH = HC1 H2N-CH(R)-COOH (chlorowodorek aa)
> estryfikacja, acylacja, N-formylacja
> dezaminacja (gł. enzymatyczna):
H2N-CH(R)-COOH —— R-CO-COOH (ketokwas)
• Grupa hydroksylowa (Ser, Thr, Tyr) - estryfikacja
• Grupa sulfhydrylowa (Cys):
> utlenianie
S do cystyny: 2 Cys-SH —-2H— Cys-S-S-Cys
S do kwasu cysteinowego (przez silne utleniacze, np. kwas nadmrówkowy):
Cys —HCOOOH— H02S-CH2-CH(NH2)-C00H
> alkalizacja
• Jeżeli grupa aminowa znajduje się w dalekim położeniu w stosunku do grupy karboksylowej (tj. przy C4-C6), wówczas w wyniku ogrzewania następuje wewnętrzna cyklizacja i powstają cykliczne amidy -laktamy. Np. kwas 6-aminoheksanowy tworzy kaprolaktam, będący surowcem do produkcji poliamidów.
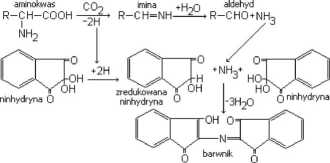
• Jak wcześniej wspomniano, aa mają postać bezbarwnych ciał stałych. Można jej jednak wybarwić poprzez reakcję z ninhydryną. Jest to reakcja charakterystyczna aa, pozwalająca na ich identyfikację. Jej produktami są aldehydy poch. od aa oraz złożony barwnik, którego anion posiada intensywnie purpurową barwę.
Reakcja powstawania i charakterystyka wiązania peptydowego - patrz punkt I-2-a.
Wyszukiwarka
Podobne podstrony:
204 KINEZYTERAPIA wyniki na miarę światowych. Lepiej sytuacja przedstawia się w narciarstwie biegowy
Standing przedsiębiorstwa ■ Ocena sytuacji przedsiębiorstwa dokonywana jest w różnej skali oraz
VII Na koniec 1997 roku sytuacja przedstawiała się następując I OFICJALNY SEKTOR P
Ekonomika turystyki R Łazarek (128) Wielka Brytania) można przyjąć, że na początku łat dziewięćdz
172 Mapa nr 5.3.1.1 Skala przedsiębiorczości absolwentów - zróżnicowanie przestrzenne Jeżeli chodzi
Obraz (7) 172 VII. Przedsiębiorstwo Jeżeli chodzi o zasady rozdziału premii pomiędzy poszczególnych
img119 Jeżeli chodzi o wspólukarane czyny następcze, to dotyczą one postępowania z przedmiotami poch
img293 (8) 120 Druidzi Musimy zatem uważnie odróżniać propagandę od prawdy. Jeżeli chodzi 0
skanuj0560 W strukturach niecentrosymetrycznych znajomość fazy K nie eliminuje niejednoznaczności, j
skanuj0145 288 Dla sytuacji przedsta- przesłona wionej na rys.2, gdzie n i r2 są odpowiednio odległo
IMG?21 Jeżeli chodzi o niewspółmierność środków użytych do zatrzymania podejrzanego (liczba funkcjon
page0245 WROŃSKIEGO ŻYCIE I PRACE. 235 społecznycłi przedstawiają się mu prosto i wyraźnie. Jeżeli s
Nartowska Różnice indywidualne0019 omawiając zachowania dzieci w różnych sytuacjach. Przedstawione p
funkia LiliaceaeHosta • funkia Jeżeli chodzi o zastosowanie w ogrodzie i uprawę, wszystkie średnio w
S5006269 28 YLODZ13UEKZ IIOŁUBOTICZ FOLKLOR Nie udało mi się zdobyć żadnego niateriałir jeżeli chodz
domach użytkowych to szeroki wachlarz rozwiązań technicznych w pigułce. Jeżeli chodzi o budowni
więcej podobnych podstron