Temat zajęć: Czynniki warunkujące aktywność enzymów na przykładzie fosfatazy kwaśnej
Prowadzący: Dr inż. Sławomir Orzechowski
Skład zespołu: xxxx
Cel ćwiczenia: Celem ćwiczenia jest badanie wpływu takich czynników jak: stężenie enzymu, stężenie jonów wodorowych (pH), temperatura, obecność inhibitora na przebieg reakcji.
Wstęp teoretyczny: Aktywność fosfatazy oznacza się używając sztucznych substratów: fenylofosforanu, fosforanu fenoloftaleiny, 2-glicerofosforanu i p-nitrofenylofosforanu (pNPP). Ostatni jest najczęściej stosowanym substratem - ze względu na tworzenie kolorowych kompleksów. Podczas ćwiczenia wykorzystywałyśmy fosfatazę kwaśną uzyskaną z siewek pszenżyta. W trakcie ćwiczeń zachodziła reakcja:
Powstający p-nitrofenol, w środowisku zasadowym, przyjmuje barwę żółtozieloną.
Zadanie 1. Obliczanie szybkości reakcji
Dane do kolejnych doświadczeń każda z nas zbierała oddzielnie.
Obliczamy szybkość reakcji na podstawie wzoru:
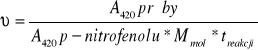
Korzystamy z programu Microsoft Excel 2002 i zestawiam dane w tabelce:
(przyjmując za Absorbancję dla p-nitrofenolu przy 420 nm wartość 0,002 , a za masę molową 139 g/mol)
Absorbancje(420) |
Warunki |
reakcji |
Czas |
|
Szybkość reakcji |
|
|
|
|
|
|
|
|
Doświadczenie 1 |
|
|
|
|
|
|
0,148 |
0,25 |
ml |
15 |
min |
0,035 |
μmol/min |
0,238 |
0,5 |
ml |
15 |
min |
0,057 |
μmol/min |
0,339 |
0,75 |
ml |
15 |
min |
0,081 |
μmol/min |
0,429 |
1 |
ml |
15 |
min |
0,103 |
μmol/min |
0,629 |
1,25 |
ml |
15 |
min |
0,151 |
μmol/min |
Doświadczenie 2 |
|
|
|
|
|
|
0,14 |
3 |
pH |
15 |
min |
0,034 |
μmol/min |
0,174 |
4,4 |
pH |
15 |
min |
0,042 |
μmol/min |
0,217 |
5,2 |
pH |
15 |
min |
0,052 |
μmol/min |
0,206 |
6 |
pH |
15 |
min |
0,049 |
μmol/min |
Doświadczenie 4. |
|
|
|
|
|
|
0,211 |
30 |
ºC |
15 |
min |
0,051 |
μmol/min |
0,202 |
40 |
ºC |
15 |
min |
0,048 |
μmol/min |
0,194 |
50 |
ºC |
15 |
min |
0,047 |
μmol/min |
0,163 |
60 |
ºC |
15 |
min |
0,039 |
μmol/min |
Doświadczenie 5. |
|
|
|
|
|
|
0,181 |
z |
inhibitorem |
15 |
min |
0,043 |
μmol/min |
0,248 |
bez |
inhibitora |
15 |
min |
0,059 |
μmol/min |
Zadanie 2. Sporządzanie wykresów.
Sporządzamy wykresy za pomocą programu Graph(v.4.3):
Zadanie 3. Aktywność fosfatazy kwaśniej w różnych temperaturach
Obliczenia: Zestawiamy w tabelce (obliczonej w Excelu) wyniki aktywności fosfatazy w różnych temperaturach w stosunku do temperatury 30 ºC.
30 |
ºC |
0,051 |
μmol |
100,00% |
40 |
ºC |
0,048 |
μmol |
95,73% |
50 |
ºC |
0,047 |
μmol |
91,94% |
60 |
ºC |
0,039 |
μmol |
77,25% |
Wnioski: Aktywność enzymu fosfatazy kwaśniej spada w temperaturach powyżej 30 ºC. Jest to spowodowane powolną denaturacją enzymu.
Zadanie 4. Porównanie aktywności fosfatazy kwaśniej z inhibitorem z aktywnością fosfatazy kwaśnej bez inhibitora.
z |
inhibitorem |
0,043405 |
μmol |
72,98% |
bez |
inhibitora |
0,059472 |
μmol |
100,00% |
Wnioski: Zastosowanie inhibitora zahamowało reakcję w 72,98 %. Dowodzi to faktowi, iż obecność inhibitora wpływa ujemnie na szybkość reakcji.
Wyszukiwarka
Podobne podstrony:
ćwiczenia 2, bio2, Temat zajęć: Właściwości aminokwasów i białek
Chemia żywnosci Cwiczenie laboratoryjne nr 1 wyodrebnianie i badanie własciwosci fizykochemicznych b
Właściwości fizykochemiczne białek
Scenariusz. Seplenienie.Temat zajęć - zimowy wiatr, LOGOPEDIA- MATERIAŁY
Temat zajęć- szaman!!!, wychowanie zdrowotne
BIOCHEMIA Metabolizm aminokwasów i białek
Ćwiczenia oddechowe w czasie zajęć ruchowych
Ćwiczenia z retoryki - Temat 2
Ćwiczenie z asertywności, Konspekty zajęc, Zajęcia z aserywności. Komunikat ja
ćwiczenia, Konspekt do zajęć gimnastyki korekcyjno, Konspekt do zajęć gimnastyki korekcyjno - kompen
Celem ćwiczenia jest doświadczalne przedstawienie właściwośc, 1)
Filozofia religii cwiczenia dokladne notatki z zajec (2012 2013) [od Agi]
DZIENNIK PRAKTYK - u pedagoga szkolnego, temat dla klasy 4a, Temat zajęć: Czym jest przyjaźń
konspekty, Ćwiczenie 2 - konspekt, Temat: Oznaczanie parametrów fizycznych i mechanicznych przy pomo
Gleboznawstwo AK, Ćwiczenie 10, Oznaczanie powierzchni właściwej gleb
Ćwiczenia excell, SCENARIUSZ ZAJĘC dnia 6 Września 2010
więcej podobnych podstron