

Zakażenia układu oddechowego
• Jest najbardziej narażony na kontakt ze światem zewnętrznym,
stąd zakażenia układu oddechowego są jedną z najczęstszych
przyczyn wizyt u lekarza, zarówno dzieci, jak i dorosłych.
• Stanowią około 50-60% wszystkich wizyt ambulatoryjnych.
• Zakażenia dróg oddechowych dzielimy na:
zakażenia górnych dróg oddechowych (GDO), zapalenia gardła
i migdałków, zapalenie ucha środkowego, zapalenia zatok
przynosowych, zapalenia nagłośni i zapalenia krtani.
Zakażenia dolnych dróg oddechowych (DDO)
ostre zapalenia oskrzeli, ostre zapalenie oskrzelików
i zapalenia płuc.

Przyczyny zakażeń
• Przyczyną zakażeń GDO są w zdecydowanej większości
(60 do 90% przypadków) wirusy.
• Infekcje te należą do samoograniczających się i najczęściej
nie wymagają stosowania antybiotykoterapii.
• Dolne drogi oddechowe, w odróżnieniu od górnych, które są
kolonizowane przez bakterie do wysokości strun głosowych,
są w warunkach zdrowia jałowe i dlatego stwierdzenie
drobnoustrojów poniżej rozwidlenia tchawicy zawsze jest
potwierdzeniem etiologii zapalenia.

Przyczyny zakażeń
• Ekspozycja DDO na działanie drobnoustrojów, w połączeniu
z takimi czynnikami, jak: wiek (wczesnodziecięcy
i podeszły), stan zdrowia (choroby współistniejące)
oraz miejsce pobytu (żłobek, przedszkole, szkoła, domy
akademickie, koszary lub domy dla przewlekle chorych),
może prowadzić do zaburzeń równowagi obronnej ustroju,
a w efekcie do wystąpienia zapaleń oskrzeli, oskrzelików
i płuc, jak również wielu klinicznych następstw tych zakażeń.
• Wśród czynników etiologicznych zapaleń DDO znacznie
większy udział mają bakterie i te zakażenia wymagają
stosowania antybiotykoterapii.

Przyczyny zakażeń
• 80% ostrych zakażeń układu oddechowego (bez względu na
wiek chorego) jest spowodowana zakażeniami wirusowymi.
• Najczęściej są to rhinowirusy, adenowirusy, coronawirusy,
wirusy RS, enterowirusy, wirusy paragrypy i wirusy grypy.
• Poszczególne typy wirusów mają swoje predylekcje
lokalizacyjne.
Rhinowirusy
najczęściej
powodują
zapalenie
nosa,
zatok i gardła,
Adenowirusy - zapalenia gardła,
Wirusy paragrypy - zapalenie krtani i tchawicy,
Wirusy RS i grypy - zapalenia dolnych dróg oddechowych.

Przyczyny zakażeń
Wirusy RS, paragrypy i grypy uszkadzają nabłonek dróg
oddechowych i ułatwiają wniknięcie bakteriom, zwłaszcza
tym, które kolonizują drogi oddechowe, co sprzyja
powstawaniu zapaleń dolnych dróg oddechowych (w tym
zapalenia płuc).

Diagnostyka zakażeń układu oddechowego
•
RTG klatki piersiowej
Zacienienia miąższowe o różnej lokalizacji i rozległości; torbiele,
ropnie, odma opłucnowa, płyn w jamach opłucnowych
•
Badanie morfologii krwi z rozmazem-
Leukocytoza z przewagą granulocytów obojętnochłonnych
przemawia za infekcją bakteryjna
•
Oznaczenie CRP we krwi (różnicowanie zakażenia dróg oddechowych
z innymi przyczynami ostrych chorób układu oddechowego);
•
Pulsoksymetria / RKZ
W ciężkich zapaleniach płuc często występuje hipoksemia
PaO2<60mmHg. Ocena utlenowania krwi na podstawie pomiaru
wysycenia Hb tlenem jest jednym z ważniejszych badań u chorego,
niezbędnym do rozpoznania niewydolności oddechowej
.
Sat O2 <90%

Diagnostyka zakażeń układu oddechowego
• Badania mikrobiologiczne
Identyfikacja czynnika etiologicznego i ocena wrażliwości na antybiotyki w
wybranych sytuacjach klinicznych jest istotna dla właściwego leczenia.
Materiał do badania: plwocina, wydzielina z drzewa oskrzelowego,
popłuczyny oskrzelowo- pęcherzykowe, płyn opłucnowy, krew obwodowa,
mocz (dotyczy Streptococcus pneumoniae, Legionella pneumoniae)
• Badania serologiczne
Szczególnie przydatne do diagnostyki zakażeń wirusami i drobnoustrojami
atypowymi (Chlamydia, Mycoplasma, Legionella).
Obserwacja wzrostu miana przeciwciał klasy IgG 4- krotne w odstępie
ok. 3 tyg (wymagane 2 próbek krwi) – rozpoznanie najczęściej po
zakończeniu lub w trakcie leczenia
• Inne badania: np. oznaczenie mocznika, kreatyniny, AST, ALT, bilirubiny całk.,
w surowicy; bronchoskopia

Nikotynizm
• Nikotyna i inne substancje dymu tytoniowego powodują
zaburzenia zarówno w odporności ogólnej, jak i miejscowej
w drzewie oddechowym.
• Zmiany te zależą od intensywności palenia, a u byłych
palaczy od czasu
zaprzestania palenia.
• Ekstrakt z papierosów moduluje mechanizm obronny
drzewa oskrzelowego poprzez wpływ na komórki T
i nabłonek drzewa oskrzelowego.
• U palaczy dochodzi do zaburzeń stosunku limfocytów CD4
do CD8, do obniżenia aktywacji limfocytów T, zmniejszenia
ich proliferacji i ekspresji białek cytotoksycznych.

Nikotynizm
• Wzrost częstości występowania infekcji dróg oddechowych
u nałogowych palaczy zależy również od zaburzonej
proliferacji i zróżnicowania limfocytów B i syntezy
immunoglobulin.
• Przewlekłe
palenie
papierosów
zaburza
odpowiedź
immunologiczną przeciw adenowirusom, zmniejsza liczbę
komórek dendrytycznych w płucach, a także powoduje
redukcję liczby aktywowanych limfocytów CD4 i CD8.
• Zmniejsza się też ilość specyficznych immunoglobulin
przeciwko tej infekcji.
• Tłumaczy to częściowo częste występowanie infekcji
wirusowych u chorych na POChP

Zakażenie oportunistyczne
Zakażenie oportunistyczne – endogenne zakażenie charakterystyczne dla
osobników o obniżonej odporności(u człowieka głównie spowodowane przez
AIDS), ale także wskutek immunosupresji oraz przy stosowaniu antybiotyków
(niszczenie flory fizjologicznej). Czynnikiem tych zakażeń są głównie
patogeny uznawane do niedawna za niechorobotwórcze.
pierwotniakowe
– Toksoplazmoza (zajęcie ośrodkowego układu nerwowego lub jako
zapalenie płuc)
– Kryptosporydioza (wodnista biegunka)
grzybicze
– Kandydoza jamy ustnej, przełyku i dalszych odcinków przewodu
pokarmowego, a także płuc
– Kryptokokoza (zapalenie płuc, ciężkie zapalenie opon mózgowo-
rdzeniowych i mózgu)
– zakażenie Pneumocystis jiroveci- najczęściej spotykane zakażenie
oportunistyczne u chorych na AIDS - zapalenie płuc o ciężkim i
nawracającym przebiegu, wymagające leczenia szpitalnego; w 50 proc.
przypadków jest pierwszym objawem AIDS

Zakażenie oportunistyczne
wirusowe
– cytomegalia (CMV) - zajęcie układu pokarmowego,
siatkówki, zapalenie płuc)
– HSV
– Półpasiec (VZV) o ciężkim przebiegu
bakteryjne
– poantybiotykowe zapalenie jelit (Clostridium difficile)
– wywołane przez prątki gruźlicy (gruźlica płuc, częste są
postacie nietypowe – Mycobacterium avium complex)

Testy diagnostyczne w rozpoznawaniu
zakażeń oportunistycznych
• W rozpoznawaniu większości infekcji oportunistycznych,
w tym wywołanych przez grzyby, mykobakterie niegruźlicze
i Pneumocystis, pierwszym badaniem powinno być badanie
mikroskopowe plwociny jako łatwo dostępne, szybkie i tanie.
• Tą metodą można badać inne materiały, w tym wydzielinę
oskrzelową
lub
płyn
z
płukania
oskrzelowo-
pęcherzykowego(BAL).
• Te same materiały należy posiewać na odpowiednie podłoża.
• Wadą hodowli jest długi okres wzrostu takich drobnoustrojów,
jak grzyby czy mykobakterie, lub niemożność wyhodowania na
pożywce, jak w przypadku Pneumocystis.
• W diagnostyce grzybic inwazyjnych znajdują zastosowanie
metody immunologiczne.

Testy diagnostyczne w rozpoznawaniu
zakażeń oportunistycznych
• Prostsze z nich, jak poszukiwanie przeciwciał w surowicy
chorego nie mają wartości z powodu upośledzonej
odpowiedzi immunologicznej chorych w immunosupresji.
• Praktyczne znaczenie mają testy na wykrywanie antygenów
grzybów we krwi lub innych składników, jak galaktomannan
w rozpoznawaniu inwazyjnej aspergillozy oraz 1-3 β-Dglikanu
(BG) w rozpoznawaniu aspergillozy i kandydiazy.
• Test na obecność antygenu Legionella pneumophila w moczu
jest stosowany w rozpoznawaniu legionelowego zapalenia
płuc.

Pneumocystoza
• Zapalenie płuc wywołane przez Pneumocystis jiroveci
(kosmopolityczny grzyb, w dawnej klasyfikacji uznawany za
pierwotniaka) występuje najczęściej u chorych zakażonych
wirusem HIV, chorych po przeszczepach narządów i komórek
macierzystych, chorych leczonych z powodu nowotworów
oraz chorych na choroby z autoagresji otrzymujących leczenie
immunosupresyjne. Objawy są niespecyficzne:
• Występuje gorączka, kaszel, duszność, hipoksemia.
• Zwykle nie stwierdza się osłuchiwaniem trzeszczeń typowych
dla zapaleń płuc o innej etiologii.
• W badaniu radiologicznym najczęściej widoczne są zmiany
rozsiane, symetrycznie rozmieszczone w obu płucach o typie
guzków lub matowej szyby.

Testy diagnostyczne w rozpoznawaniu
zakażenia Pneumocystis jiroveci
• U chorych HIV-negatywnych narastanie objawów, które
zmuszają chorego do kontaktu z lekarzem trwa krócej,
choroba ma ostrzejszy przebieg, częściej są oni leczeni w
oddziałach intensywnej terapii niż chorzy zakażeni HIV.
• Rozpoznanie należy oprzeć na stwierdzeniu cyst lub
trofozoitów. Pneumocystis w popłuczynach oskrzelowo-
pęcherzykowych, indukowanej plwocinie lub w materiale z
przezoskrzelowej lub otwartej biopsji płuca.
• Te same materiały należy badać na obecność drobnoustroju
metodą PCR, która jest bardziej czuła, ale równocześnie mniej
swoista.
• Lekiem z wyboru jest kotrimoksazol, który stosowany jest
również profilaktycznie
.

Alergiczne zapalenie pęcherzyków płucnych
• Alergiczne
zapalenie
pęcherzyków
płucnych
(AZPP)
to
ziarniniakowata
śródmiąższowa
choroba
płuc
indukowana
immunologicznie (trzecia pod względem częstości po idiopatycznym
włóknieniu płuc i sarkoidozie)
• W literaturze obecnie najczęściej stosuje się określenie
hypersensitivity pneumonitis określającą heterogenną grupę chorób
płuc o podłożu immunologicznym, spowodowanych wdychaniem
przez osoby wrażliwe organicznych i
nieorganicznych pyłów środowiskowych.
• Postacie AZPP:
Płuco hodowców ptaków,
płuco farmera,
płuco drwali,
młynarzy, hodowców grzybów,
płuco klimatyzacyjne i inne.

Alergiczne zapalenie pęcherzyków płucnych
• W powietrzu atmosferycznym znajdują się różnorodne
cząsteczki, które wdychane do dróg oddechowych , mogą
powodować zróżnicowaną reakcję immunologiczną.
• Przyczyną AZPP mogą być:
antygeny grzybicze (aspergillus fumigatus) ,
bakteryjne (bacillus subtilis),
pasożytnicze (naegleria gruberi),
białka zwierząt (białka surowicy i odchodów ptasich,)
a także wysoce reaktywne substancje chemiczne (izocyjanki,
siarczanek miedzi),
wśród leków wymienia się leki stosowane w onkologii głównie
imatinib.

Alergiczne zapalenie pęcherzyków płucnych
• W AZPP dochodzi do zmian zapalnych w dystalnym odcinku
dróg oddechowych, obejmujących obszary płuc, w którym
dochodzi do wymiany gazowej.
• W patogenezie choroby biorą udział dwa typy odpowiedzi
immunologicznej: tworzenie kompleksów immunologicznych
oraz naciek komórkowy z udziałem limfocytów T
i makrofagów.
• W odpowiedzi immunologicznej biorą udział zarówno
komórki Th1 i Th2 jak i cytokiny produkowane przez CD4+
i CD8+.
• Rozpoznanie kliniczne AZPP nie jest proste i brak jest
kryteriów określających „ złoty standard”
• Rozpoznanie ustala się na podstawie kompleksowej oceny
klinicznej, radiologicznej, czynnościowej, laboratoryjnej,

Alergiczne zapalenie pęcherzyków płucnych
• W typowych ostrych przypadkach przy narażeniu na znane
antygeny charakterystyczny obraz kliniczny, śródmiąższowe
zmiany radiologiczne w płucach i wykrycie swoistych
przeciwciał IgG pozwalają na ustalenie rozpoznania.
• W innych przypadkach rozpoznanie można ustalić bądź
odrzucić na podstawie obrazu kliniczno – radiologiczno –
czynnościowego i płukania oskrzelowo – pęcherzykowego
(BAL)

Alergiczne zapalenie pęcherzyków płucnych
Do rozpoznania AZPP konieczna jest obecność
>= 4 dużych i >= 2 małych kryteriów:
Kryteria duże
Kryteria małe
1. Objawy występujące po
ekspozycji (2-9 godz)
2. Potwierdzenie ekspozycji
(wywiad, badania środowiskowe,
precypityny w surowicy)
3. Typowe zmiany w RTG i TK
klatki piersiowej
4. Limfocytoza w BAL
5. Typowe zmiany w obrazie
morfologicznym wycinka płuca
6. Dodatni naturalny test
prowokacyjny
1. Trzeszczenia nad podstawami
płuc
2. Zmniejszenie DLco(badanie
zdolności dyfuzyjnej)
3. Hipoksemia w gazometrii krwi
tętniczej w spoczynku i podczas
wysiłku

Alergiczne zapalenie pęcherzyków płucnych
Badania laboratoryjne
• W rozpoznaniu choroby stwierdzenie w surowicy swoistych
przeciwciał IgG odgrywa ważną rolę
• Po zaprzestaniu ekspozycji na alergen (antygen) przeciwciała
są wykrywane w surowicy pacjenta przez 2- 3 lata.
• W ostrej fazie choroby w krótkim czasie po ekspozycji
obserwuje się wysoką leukocytozę z neutrofilią lub eozynofilią
• Stwierdza się również przyspieszone OB. Oraz zwiększoną
aktywność LDH
• W monitorowaniu aktywności choroby pomocne jest
oznaczenie stężenia w surowicy KL-6 (antygen
glikoproteinowy związany z mucyną)oraz ICAM-1( cząsteczka
adhezyjna śródbłonka) ale badania te nie są powszechnie
stosowane.

Alergiczne zapalenie pęcherzyków płucnych
• W płynie z płukania oskrzelowo – pęcherzykowego (BAL)
charakterystyczna jest limfocytoza 60-80%
• Po kontakcie z antygenem w BAL dominują neutrofile
i dopiero po 48h napływają limfocyty CD8+
• Dla AZPP charakterystyczne jest zmniejszenie stosunku
limfocytów CD4+/CD8+ < 1
• W przewlekłej postaci choroby zwiększa się liczba limfocytów
CD4+ co powoduje wzrost CD4+/CD8+
• W fazie włóknienia zwiększa się odsetek neutrofilów w BAL
• U dzieci nie obserwuje się zmiany stosunku CD4+/CD8+ w BAL
lecz stwierdza się zwiększenie odsetka naturalnych zabójców -
limfocytów NK

To niebieskawe zabarwienie skóry i błon śluzowych, będące
wynikiem zwiększonej ilości hemoglobiny odtlenowanej we krwi
włośniczkowej › 5g/dl lub obecności hemoglobiny patologicznej
(najczęściej methemoglobiny› 0,5g/dl)
Sinica centralna – spowodowana jest zmniejszeniem
wysycenia hemoglobiny krwi tętniczej tlenem lub obecnością,
Hb patologicznej; występuje na skórze i błonach śluzowych
głównie warg, jamy ustnej i języka (niewydolność oddechowa,
spowodowana głownie zaburzeniem stosunku wentylacji do
perfuzji np. zapalenie płuc, POChP, niektóre wrodzone wady
serca z przeciekiem tętniczo-żylnym, obniżenie ciśnienia tlenu
we wdychanym powietrzu).
Pojawia się, gdy PaO
2
‹ 60mmHg- SaO
2
‹ 85%

Sinica obwodowa – widoczna jedynie na skórze dystalnych
części ciała, które jest zwykle zimna. Jest objawem
nadmiernego odtlenowania Hb w tkankach obwodowych
(wychłodzenie ciała, zmniejszenie obj. wyrzutowej serca np.
wstrząs kardiogenny, miejscowe zaburzenia ukł tętniczego np.
miażdżyca, zaburzenia naczynioruchowe, upośledzenie
odpływu krwi żylnej, np. zakrzepica, zwiększenie lepkości krwi,
np.czerwienica)

Płyn w jamie opłucnowej
Zaburzenia wytwarzania i wchłaniania płynu opłucnowego prowadzi do
gromadzenia się jego zwiększonej ilości w jamie opłucnowej, w której w
warunkach prawidłowych znajduje się 10-20ml.
Mechanizmy gromadzenia płynu:
• ciśnienia hydrostatycznego w naczyniach krążenia opłucnej
• ciśnienia onkotycznego osocza
• Utrudnienie odpływu chłonki przez pory i naczynia chłonne opłucnej
ściennej np. w następstwie nacieków lub przerzutów nowotworowych
Badanie przedmiotowe:
• Stłumienie wypuku i zniesienie drżenia głosowego przy >= 300-400ml
płynu w jamie opłucnej
• Zazwyczaj jednorazowo nie usuwa się >1500ml płynu

Płyn w jamie opłucnowej
Przesięk
Wysięk
•Niewydolność krążenia
•Choroby osierdzia
•Marskość wątroby
•Zespół nerczycowy
•Dializa otrzewnowa
•Zatorowość płucna
•Zakażenia bakteryjne w tym
gruźlica
•Pierwotne nowotwory płuc lub
oplucnej, przerzuty do opłucnej
•Zatorowość płucna
•Choroby przewodu
pokarmowego
•Choroby
autoimmunologiczne(RZS, SLE)
•Po zabiegach
kardiochirurgicznych i
radioterapii
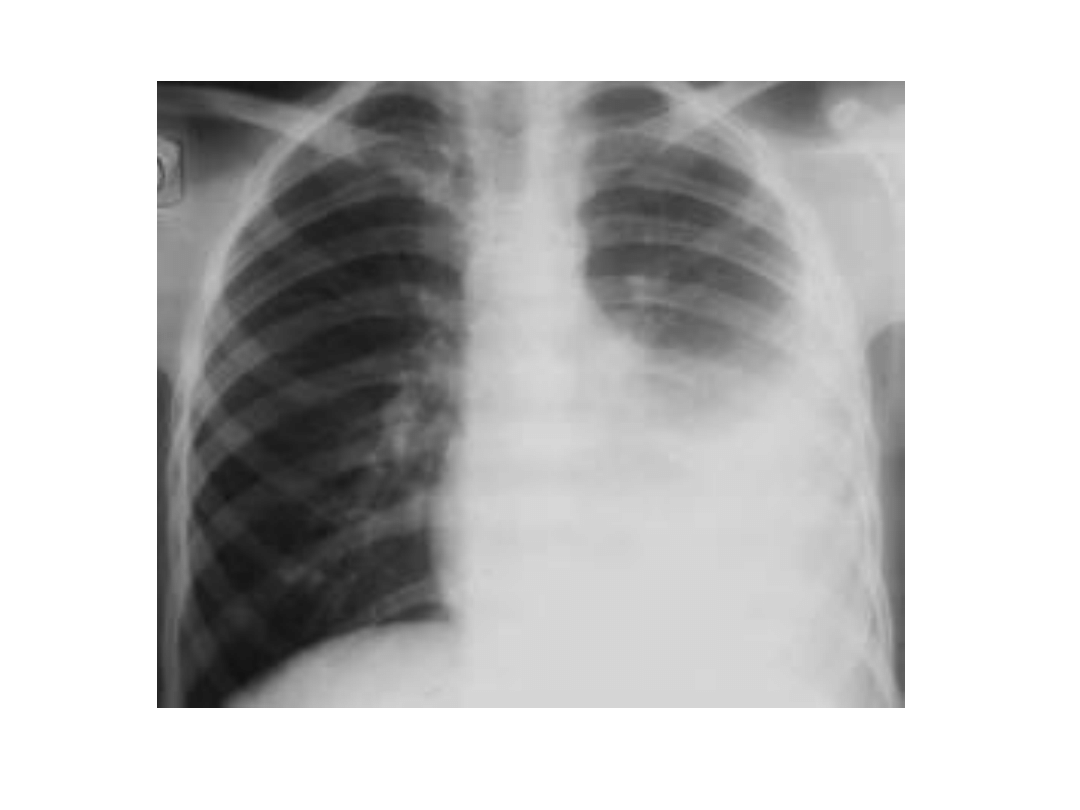
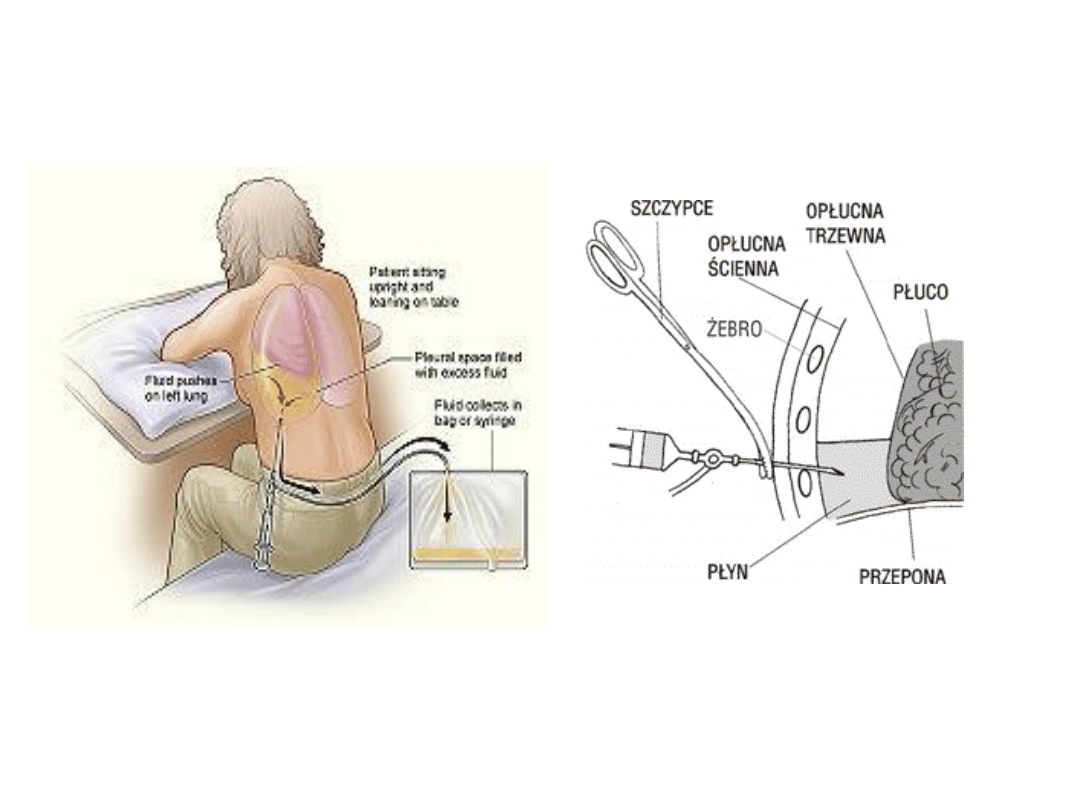
Torakocenteza

Badanie płynu opłucnowego
1. Ocenia makroskopowa
-
Płyn krwisty (nowotwór złośliwy, uraz klatki piersiowej, zator
tętnicy płucnej)
-
Płyn mleczny (wysięk chłonny)
-
Płyn mętny (ropniak opłucnej)
2. Badania biochemiczne
-
Białko i LDH; konieczne do różnicowania przesięku od
wysięku (kryteria Lighta). Jednoczesne oznaczenie w
surowicy krwi
-
Glukoza; stężenie < 60mg% obserwuje się w wysiękach
nowotworowych, ropniaku, gruźlicy
-
pH<7,2 jest złym czynnikiem prognostycznym, może
świadczyć np. o zaawansowanym procesie zapalnym

Badanie płynu opłucnowego
- CHC i TG; stężenie TG <110mg/dl może sugerować wysięk
chłonny
- Amylaza- zwiększona aktywność stwierdzana jest w ostrym
zapaleniu trzustki i pęknięciu przełyku
- Deaminaza adenozynowa(ADA)- oznacza w przyp podejrzenia
gruźliczego zapalenia opłucnej
3. Skład komórkowy
- Neutrofilia – zakażenie bakteryjne; zatorowośc płucna
- Limfocytoza – często w gruźlicy i nowotworach
- Eozynofilia (>10%)- azbestoza, inf pasożytnicza, zespół Churga
i Strauss, odczyn polekowy itd

Badanie płynu opłucnowego
3. Hematokryt płynu
>= 50% wartości Ht krwi obwodowej wskazuje na krwiaka
opłucnej
4. Cytologiczne: rozpoznanie komórek nowotworowych na podst
pojedynczego badania płynu w ok. 60% przypadków
5. Mikrobiologiczne: niska skuteczność; w przyp. podejrzenia
gruźliczego zapalenia opłucnej rozmaz na obecność prątków
jest dodatni jedynie w 20-40%.
6. Niekiedy oznaczane: składowe układu dopełniacza, p-ciała
przeciw jądrowe, RF, markery nowotworowe

Palce pałeczkowate-
to niebolesna proliferacja tkanki łącznej na
grzbietowej powierzchni dystalnych paliczków rąk i stóp (kształt
pałeczek dobosza), prowadząca do uniesienia paznokci przyjmujących
kształt szkiełka zegarkowego.
Zmianom tym towarzyszy często rumień okołopaznokciowy.
Przyczyny:
płucne: rak płuca i inne nowotwory płuc,
włóknienie płuc,
przewlekłe choroby zapalne (ropień płuca, ropniak opłucnej rozstrzenie
oskrzeli, gruźlica płuc),
mukowiscydoza

Osteodystrofia przerostowa to bolesne tworzenie nowej kości
podokostnowo w dystalnych częściach kończyn (zmiany w obrębie
stawów nadgarstkowych, skokowych z równoczesnym zajęciem
okostnej dystalnych części kości długich, przedramienia lub
podudzia).
Towarzyszy palcom pałeczkowatym, choć występuje znacznie
rzadziej i częściej współistnieje z chorobami nowotworowymi
płuc.
Klinicznie osteodystrofia przerostowa przypomina stan zapalny
(ból, obrzęk, zaczerwienienie).
Przyczyny:
• nowotwory złośliwe, zwłaszcza rak płuca ( w – 90% przypadków),
• przewlekłe choroby zapalne płuc

Opis przypadku
Siedemnastoletni chłopiec (P.M.), chorujący dotychczas sporadycznie na
infekcje górnych dróg oddechowych o łagodnym przebiegu, zgłosił się do lekarza
z powodu utrzymującego się od kilku dni uporczywego, męczącego kaszlu o
charakterze napadowym z towarzysząca gorączką do 38,5°C. Kaszel był suchy,
występował zarówno w dzień jak i w nocy. Rozpoznano zapalenie gardła i
zalecono doustnie cefalosporynę II generacji (aksetyl cefuroksymu). Po 3
dniach leczenia z powodu braku poprawy (kaszel nasilał się, chłopiec nadal
gorączkował) ponownie konsultowany w poradni rejonowej. Ze względu na
stwierdzenie asymetrii szmeru pęcherzykowego i podejrzenie zapalenia płuc,
skierowano chłopca do szpitala.
Przy przyjęciu chłopiec był w stanie ogólnym dość dobrym, bez gorączki, zwracał
uwagę suchy, męczący kaszel. W badaniu przedmiotowym stwierdzono
zaczerwienienie gardła, stłumienie odgłosu opukowego, ściszenia szmeru
pęcherzykowego i rzężenia drobnobańkowe po stronie prawej. W pozostałych
narządach nie stwierdzono odchyleń od normy.

• W badaniach dodatkowych stwierdzono podwyższone
wskaźniki stanu zapalnego:
• białko ostrej fazy (CRP) 94,3mg/l (norma do 5,0mg/l),
• przyspieszony odczyn opadania krwinek czerwonych (OB) do
65mm/godz.,
• podwyższone stężenie prokalcytoniny ≥ 10ng/ml (norma
<0,5ng/ml).
• W rozmazie krwi obwodowej przewaga granulocytów
obojętnochłonnych (79,6%).
• W gazometrii krwi włośniczkowej stwierdzono hipoksemię
PO
2
– 51,9 mmHg oraz obniżoną saturacją krwi SaO
2
– 87,0%.
• Ponadto stwierdzano podwyższoną aktywność
aminotransferazy alaninowej (ALAT 128U/L).
• W pozostałych badaniach odchyleń od normy nie
stwierdzano.

• W badaniu radiologicznym klatki piersiowej występowały
masywne zagęszczenia zapalne miąższu płucnego, głównie w
zakresie dolnego płata płuca prawego. Zastosowano dożylnie
cefalosporynę II generacji (cefuroksym) oraz nebulizację z
mukolitykiem (ambroxol).
• Podejrzewając zakażenie drobnoustrojami atypowymi
dołączono do leczenia antybiotyk z grupy makrolidów (dożylny
preparat klarytromycyny). W poszukiwaniu czynnika
etiologicznego wykonano szereg badań w kierunku zakażeń
atypowych. Po 4 dniach hospitalizacji, metodą
immunoenzymatyczną stwierdzono podwyższone stężenie
przeciwciał antychlamydiowych w klasie IgG (indeks) – 2,2
(norma <1,1) i IgM (indeks) – 1,26 (norma <1,1).
• Wykonane badanie ultrasonograficzne jamy brzusznej nie
wykazało odchyleń od normy, a badania w kierunku zakażeń
EBV i HCV nie wskazywały na zakażenia.
• Rozpoznano: chlamydofilowe zapalenie płuc

Immunopatologiczne zapalenie nerek
• Dowody na to że kłębuszkowe zapalenia nerek występuję
u człowieka są zaburzeniami immunologicznymi pochodzą
z badań eksperymentalnych.
• Znane są dwa mechanizmy indukujące kłębuszkowe zapalenie
nerek:
Odkładanie się krążących kompleksów antygen – przeciwciało
w obrębie kłębuszka – „kompleksowe zapalenie nerek”
(choroba kompleksów immunologicznych)
Reakcję krążących przeciwciał z antygenami osiadłymi
w
kłębuszkach
nerkowych
lub
z
komponentami
antygenowymi śródbłonka naczyń nerkowych.

Nefropatia IgA łac. nephropathia IgA
• Choroba Bergera, glomerulopatia, w której dochodzi do
odkładania się złogów immunoglobuliny A (IgA) w mezangium
• Klinicznie objawia się nawracającym krwinkomoczem lub
krwiomoczem
• Ocenia się, że Nefropatia IgA stanowi 15-40% wszystkich
pierwotnych glomerulopatii, jest to najczęstsza idiopatyczna
postać kłębuszkowych zapaleń nerki
• W mikroskopie świetlnym stwierdza się kłębuszki
o prawidłowym wyglądzie obok kłębuszków o różnie nasilonej
proliferacji
• Mikroskop fluorescencyjny jako jedyny może rozpoznać tą
glomerulopatię
na
podstawie
badania
immunofluorescencyjnego, w którym stwierdza się depozyty
IgA.

Nefropatia IgA łac. nephropathia IgA
• U chorych z nefropatią IgA, IgA1 ma zwiększoną zdolność do łączenia się
w większe konglomeraty z powodu nieprawidłowej galaktozylacji
w regionie zawiasowym tzw. O-glikozylacji, której przypisuje się obecnie
kluczową rolę w patogenezie IgAN.
• U chorych z IgAN stwierdza się w limfocytach B defekt
β1,3-galaktozylotranferazy odpowiedzialnej za przyłączenie galaktozy do
IgA.
• W stanie zdrowia IgA1 jest katabolizowana w wątrobie poprzez łączenie
z receptorem asialoglikoproteinowym (ASGPR), w wyniku O-glikozylacji
wątrobowy klirens IgA1 jest znacznie zmniejszony
• Cząsteczki IgA1 z obniżoną zawartością galaktozy, tworzą kompleksy
immunologiczne, które łatwiej łączą się na terenie mezangium
z fibronektyną, lamininą i kolagenem IV, co wyzwala powstanie
nieswoistego odczynu zapalnego, w tym aktywację C3 dopełniacza
i prowadzi do rozwoju nefropatii

Nefropatia IgA – opis przypadku
• 4 letni chłopiec zgłosił się z trwającymi 18 miesięcy
nawracającym bezbólowym krwiomoczem, który zwykle
pojawiał się po nasilonym wysiłku oraz w okresach częstych
przeziębień i bólów gardła.
• W badaniu ogólnym moczu stwierdzono mikroskopowy
krwiomocz (+++) i ślad białka.
• Poziom Hb, WBC, stężenie mocznika w surowicy i klirens
kreatyniny były w normie a dobowe wydalanie białka z
moczem wynosiło 0,95g.
• Wykonano biopsję nerki ze względu na czas trwania
krwinkomoczu(wszystkie klębuszki wykazywały rozlaną
proliferację komórek mezangium)
• Badanie immunofluorescencyjne pokazało złogi mezangialne
IgAi C3dopełniacza.

Ostre kłębuszkowe zapalenie nerek
• Ostre kłębuszkowe zapalenie nerek (OKZN) to choroba o ostrym
początku i w większości przypadków samoograniczającym się
przebiegu.
• Występuje najczęściej w następstwie zakażenia paciorkowcem
beta-hemolizującym grupy A ( Streptococcus pyogenes, GAS –
group A Streptococcus).
• Chorobę mogą powodować także niektóre paciorkowce grupy C i
G, Streptococcus pneumoniae, inne bakterie (gronkowce,
Salmonella w tym Salmonella typhi, Klebsiella, Treponema
pallidum), wirusy (ECHO, Coxsackie, wirusy różyczki, ospy
wietrznej, odry, świnki, EBV, CMV, WZWB, HIV), grzyby (
Histoplasma capsulatum), a także pierwotniaki (zarodźce malarii i
Toxoplasma gondii).
• Ostatnio opisano ostre KZN u dziecka z zakażeniem skóry
wywołanym
odzwierzęcym
paciorkowcem
Streptococcus
zooepidemicus

Ostre kłębuszkowe zapalenie nerek
• Przyczyną uszkodzenia kłębuszków nerkowych jest odkładanie się w nich
kompleksów immunologicznych.
• Istnieją dwie teorie dotyczące miejsca powstawania patogennych dla
nerek kompleksów immunologicznych.
• Pierwsza zakłada tworzenie się kompleksów w krążeniu, według drugiej
formowanie się kompleksów ma miejsce bezpośrednio w kłębuszkach
nerkowych.
• Według pierwszej koncepcji krążący we krwi antygen paciorkowca
reaguje z przeciwciałami gospodarza, co doprowadza do powstania
rozpuszczalnych kompleksów, które są filtrowane, lecz nie usuwane przez
kłębuszki nerkowe.
• W ich skład w ostrym popaciorkowcowym kłębuszkowym zapaleniu
nerek (OPKZN) wchodzą różne antygeny paciorkowcowe, skierowane
przeciwko nim przeciwciała oraz składowe układu dopełniacza.
• Do dziś nie zostały jednoznacznie wyizolowane nefrotoksyny
odpowiedzialne za uszkodzenie kłębuszków.

Ostre kłębuszkowe zapalenie nerek
• Zmiany morfologiczne w OKZN mają charakter uogólniony i
rozlany.
• W biopsji nerki charakterystyczne jest powiększenie wszystkich
kłębuszków z wyraźnym rozplemem komórek śródbłonka naczyń
włosowatych kłębuszka i mezangium oraz liczne napływowe
komórki zapalne (głównie neutrofile, a także makrofagi, rzadko
limfocyty i komórki plazmatyczne) naciekające naczynia kłębuszka
i mezangium.
• W nielicznych (5-15%) kłębuszkach widoczny może być rozplem
komórek nabłonka torebki Bowmana.
• Gromadzenie się komórek zapalnych w pęczku naczyniowym wraz
z tworzącymi się złogami fibryny powoduje powiększenie się
wymiarów kłębuszka nerkowego i wypełnienie przestrzeni
Bowmana.
• Światła włośniczek ulegają zwężeniu, czasami stają się
niewidoczne.

Ostre kłębuszkowe zapalenie nerek
• W zapaleniach o ciężkim przebiegu można zaobserwować
skrzepliny w świetle włośniczek, może także dojść do
powstawania półksiężyców komórkowych (szczególnie
w przypadkach przebiegających z niewydolnością nerek) oraz
zmian w obrębie cewek i śródmiąższu.
• W miarę zdrowienia zmniejsza się ilość granulocytów,
a światło włośniczek staje się lepiej widoczne.
• Najdłużej utrzymuje się rozplem komórek mezangium.

Ostre kłębuszkowe zapalenie nerek
• W badaniu immunofluorescencyjnym stwierdza się ziarniste
złogi frakcji C3 dopełniacza i IgG (rzadko IgM) zlokalizowane
wzdłuż ścian włośniczek kłębuszka, rzadziej w mezangium.
• Zależnie od umiejscowienia złogów IgG i C3 wyróżnia się trzy
typy zmian:
• – typ mezangialny – złogi zlokalizowane głównie w obrębie
mezangium; najczęściej u pacjentów młodszych, wiąże się z
dobrym rokowaniem;
• – „girlandowaty” typ zmian – złogi w obwodowych
odcinkach ścian włośniczek kłębuszka; częściej u
chłopców/mężczyzn z nerczycowym białkomoczem, ten typ
zmian histopatologicznych wiąże się ze złym rokowaniem;

Ostre kłębuszkowe zapalenie nerek – opis przypadku
• 9 letni chłopiec został przyjęty do szpitala jako ostry
przypadek z powodu obrzęku twarzy, oczu i tułowia
• Tydzień wcześniej skarżył się na ból gardła
• W badaniu stwierdzono gorączkę 37 °C
oraz nadciśnienie RR170/110
• W badaniu ogólnym moczu stwierdzono białkomocz oraz
wałeczki erytrocytarne
• Poziom Hb - 10,7mg/ml, WBC oraz wzór Schilinga w normie
• Wymaz z gardła wykazywał wzrost prawidłowej flory
bakteryjnej, natomiast obecne były w wysokim mianie
przeciwciała
przeciwko
antygenom
paciorkowcowym:
antystreptolizyna 0 (ASO) miano 1600IU/ml (n <300IU/ml)

Zespół nerczycowy
łac. syndroma nephroticum
• Zespół objawów chorobowych wywołany nadmierną
nieskompensowaną utratą białka z moczem.
• Stan ten nazywa się białkomoczem: w przypadku zespołu
nerczycowego przekracza ilość 3,5 g/dobę lub 50 mg/kg
masy ciała/dobę.
• Do
objawów
choroby
należą
obok
białkomoczu
hipoalbuminemia,
lipiduria,
hiperlipidemia,
obrzęki
i przesięki do jam ciała.
• Do zespołu nerczycowego może doprowadzić każdy stan
chorobowy przebiegający z białkomoczem.

Zespół nerczycowy
• Do białkomoczu dochodzi wskutek uszkodzenia kłębuszków
nerkowych
wywołanego
najczęściej
przez
procesy
immunologiczne w przebiegu kłębuszkowych zapaleń nerek,
które stają się nadmiernie przepuszczalne do cząsteczek
białka.
• Przyczyną wrodzonego zespołu nerczycowego może być
genetycznie uwarunkowany brak nefryny (wrodzony zespół
nerczycowy typu fińskiego).
• Rozróżnia się białkomocz selektywny, gdy nadmiernemu
przesączaniu
ulegają
tylko
albuminy
i
białkomocz
nieselektywny, gdy oprócz albumin ucieczce ulegają większe
cząsteczki białka i lipidy.
• Długotrwała utrata białka doprowadza do spadku ciśnienia
onkotycznego i powoduje powstanie przesięków i obrzęków
do jam ciała.

Zespół nerczycowy
• Rozpoznanie można postawić, gdy spełnione są kryteria:
• białkomocz >50 mg/kg masy ciała/dobę lub >40 mg/m²
powierzchni ciała/ godzinę, lub >1 g/m²/dobę.
• stosunek stężenia białka do kreatyniny w moczu (w mg/dL)
>1,8
• Hipoalbuminemia <25 g/L w surowicy
• Hipercholesterolemia >250 mg/dL
• obecność obrzęków.

Zespół Goodpasture'a
• Choroba autoimmunologiczna o gwałtownym i ciężkim
przebiegu. Zapadalność roczna 1-2/mln.
• Przyczyną choroby są immunoglobuliny klasy IgG (rzadziej
IgA,gM) skierowane przeciwko błonie podstawnej (GBM),
zwykle przeciw niekolagenowej części łańcucha α3 włókien
kolagenu typu IV budującego błonę podstawną kapilar w
pęcherzykach płucnych i kłębuszkach nerkowych.
• Przeciwciała aktywując układ dopełniacza, prowadzą do
powstawania tzw. kompleksu ataku błonowego złożonego ze
składowych C5-C9 uszkadzającego tkanki.
• W badaniu biopunktatów nerek oraz wzdłuż pęcherzyków
płucnych stwierdza się badaniem immunofluorescencyjnym
linijne złogi IgG wzdłuż GBM.

Zespół Goodpasture'a
• Objawy ogólne: grypopodobne, ubytek m.c.
• Zmiany w płucach związane z krwawieniem
pęcherzykowym: duszność, kaszel,
krwioplucie!; osłuchowo trzeszczenia
przypodstawne
• Zmiany w nerkach: szybko postępujące KZN
powodujące obrzęki obwodowe, nadciśnienie
tętnicze
• W rezultacie rozwija się niewydolność nerek i
niewydolność oddechowa

Zespół Goodpasture'a
Badania laboratoryjne:
- OB, CRP
- Niedokrwistość mikrocytarna u 100% pacjentów, Hb <10g/dl
jeszcze przed wyst. niewydolności nerek
- Leukocytoza
- Narastające wartości kreatyniny, mocznika, K+
- Krwinkomocz w >90% przyp, wałeczki ziarniste i erytrocytowe.
Białkomocz (>3g/d)
- Przeciwciała w surowicy:
anty- GBM (80-90%)- oznaczone metodą ELISA; znikają po 2-3
tyg skutezcnej terapii
p-ANCA (10-40%)- sprzyjają ogólnej reakcji zapalnej i zajęciu
płuc

Zespół Goodpasture'a
• Leczenie:
• GKS
• Plazamfereza
• Hemodializy
• Wspomaganie oddychania

Opis przypadku
• 35- letni, dotychczas zdrowy, palący od 5 lat papierosy mężczyzna
• Przed hospitalizacją: duszność początkowo wysiłkowa, następnie
spoczynkowa o charakterze napadowym, suchy kaszel z
krwiopluciem- leczony ambulatoryjnie antybiotykiem; w rtg kp-
początkowo bez zmian
• Po około 7 dniach od początku objawów trafił do szpitala w stanie
ciężkim, z silną dusznością, temp 39stC, dreszczami; przy przyjęciu
nad polami płucnymi liczne trzeszczenia
• Na powtórnie wykonanym zdjęciu RTG KP (kilka dni po poprzednim
badaniu) stwierdzono rozlane zmiany śródmiąższowe w obu
płucach.
• Kreatynina 3,5 mg%, Mocznik 41 mg%,
• GFR wg MDRD 21,4 ml/min/1,73 m2 (IV stopień NN)
• W moczu masywny krwinkomocz oraz białkomocz

Opis przypadku
• Hgb 8,4 g% i Hct 24,9%,
• Gazometria krwi włośniczkowej — pO2 50 mm
Hg, pCO2 38 mm Hg, SatO2 85%.
• Oznaczony w tym czasie poziom przeciwciał
antyGBM wynosił 281,7 j./ml (N: <15j./ml)
• p-ANCA ujemne
• Rozpoznanie: zespół Goodpasture’a
(po zastosowanym leczeniu poziom p-ciał po 3
m-cach spadł do 7j./ml)
Wyszukiwarka
Podobne podstrony:
205 Krew i choroby ukladu krwio Nieznany
PP 06 choroby ukladu krazenia i Nieznany
1DIAGNOSTYKA CHORÓB UKŁADU ODDECHOWEGO I CHORÓB NEREK
CHOROBY UKLADU NERWOWEGO U DZIE Nieznany
Choroby ukladu oddechowego osob Nieznany
CHOROBY UKLADU KOSTNO MIESNIOWE Nieznany
Choroby ukladu nerwowego w ciaz Nieznany
CHOROBY UKLADU NERWOWEGO U DZIE Nieznany
Choroby ukladu oddechowego osob Nieznany
Choroby układu nerwowego ppt
Krew i choroby układu krwionośnego
Leki w chorobach układu pokarmowego
Sem 3 Wywiad w chorobach układu oddechowego
SPECYFIKA CHORÓB UKŁADU NERWOWEGO OKRESU ROZWOJOWEGO
Wywiad w chorobach układu pokarmowego
Choroby układu krążenia III
Choroby ukladu krazenia J L
więcej podobnych podstron