11. Zjawiska korpuskularno-falowe
11.1. Promieniowanie termiczne
Podstawowe źródła światła: - ogrzane ciała stałe lub gazy, w których zachodzi
wyładowanie elektryczne.
Emisja
↔ absorpcja
R
- widmowa zdolność emisyjna promieniowania
R
d
λ
- szybkość z jaką jednostkowy obszar
powierzchni wypromieniowuje energię z zakresu
długości fal
λ
,
λ
+d
λ
.
Całkowita zdolność emisyjna promieniowania –
szybkość z jaką jednostka powierzchni
wypromieniowuje energię do przedniej półkuli:
∫
∞
=
0
R
edynie
tefana-
λ
λ
d
R
(analogia
do
rozkładu Maxwella dla prędkości!)
Własności widma termicznego:
- nie zależy ani od rodzaju substancji ani od kształtu, a j
od temperatury ciała;
- widmo jest ciągłe;
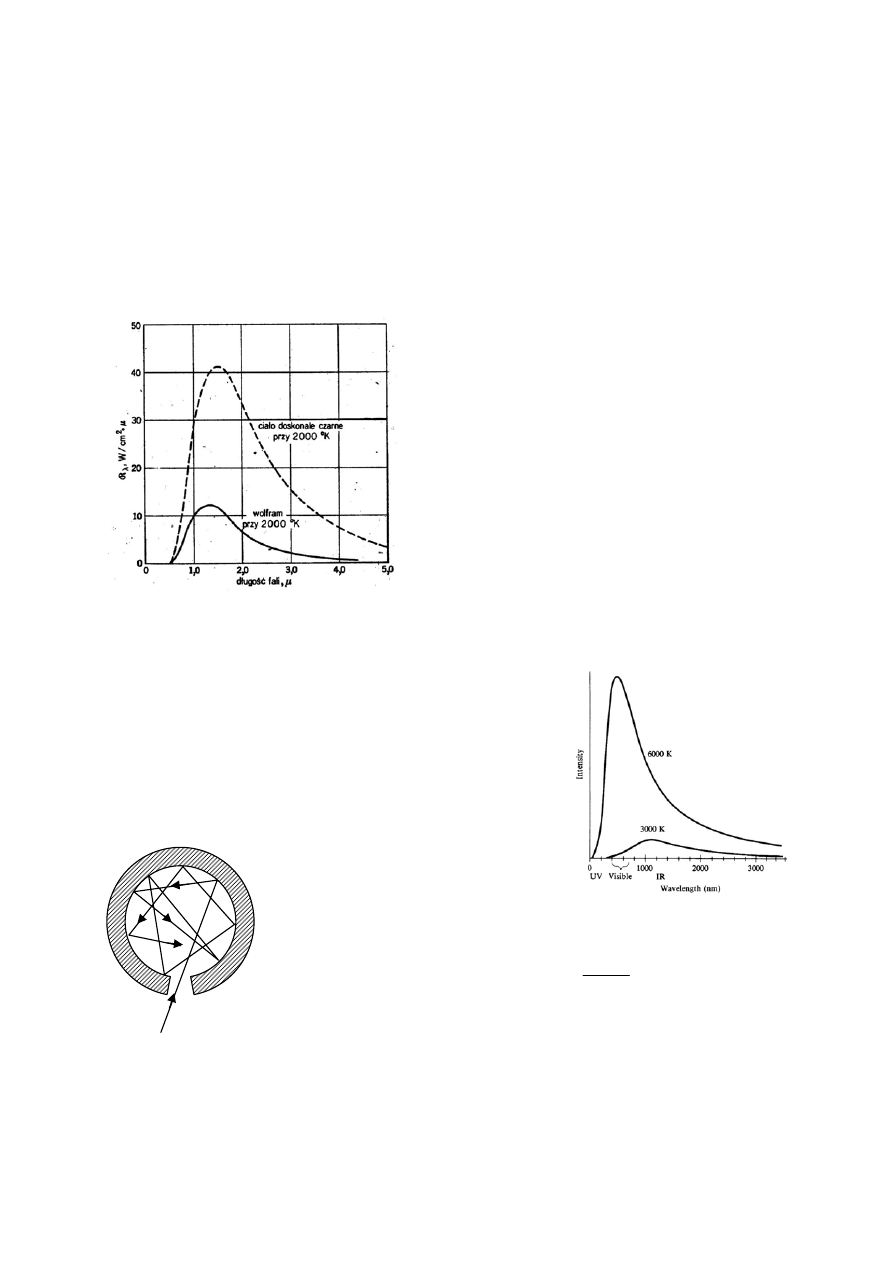
- opisane jest dla ciała doskonale czarnego (ciała, którego
powierzchnia absorbuje całe promieniowanie termiczne).
Emisja energetyczna promieniowania
ciała doskonale czarnego zmienia się z
temperaturą zgodnie z prawem S
Boltzmana:
R
=
σ⋅
T
4
gdzie
σ
=
⎥⎦
⎤
4
K
W
⎢⎣
⎡
⋅
−
2
8
10
67
,
5
m
Zauważmy, że maksima natężenia promieniowania dla różnych temperatur przypadają na
różne długości fal. Tzn. można to zapisać:
λ
1
T
1
=
λ
2
T
2
=
λ
3
T
3
=…. Ogólnie
λ⋅
T = const - prawo Wiena
Zastosowanie: pomiar temperatury gwiazd na podstawie analizy widmowej. Mierzymy
λ
⇒
λ⋅
T = 2,898
⋅10
-3
[m
⋅K] i stąd obliczmy temperaturę gwiazdy.
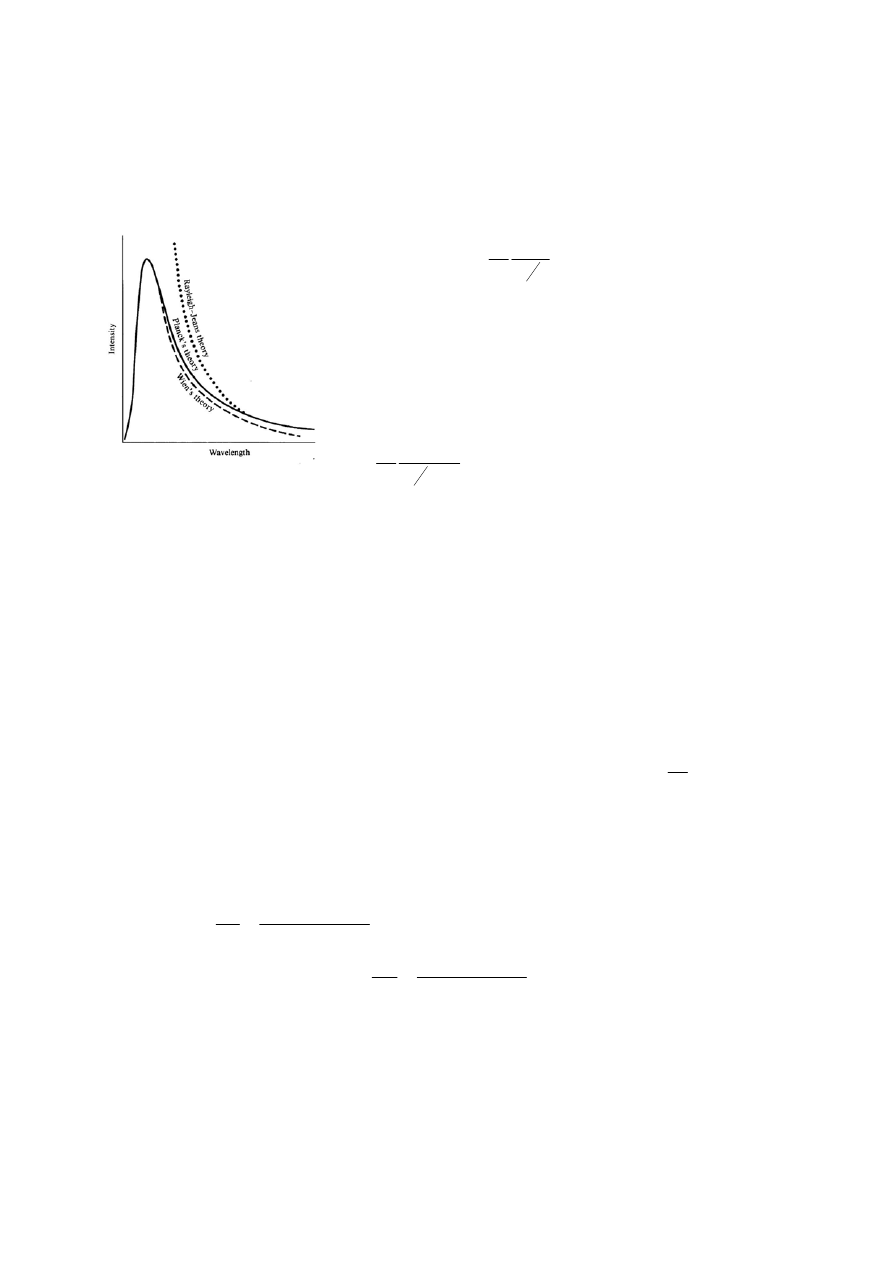
Podejmowano różne próby oparte na fizyce klasycznej, wyjaśnienia rozkładu promieniowania
ciała doskonale czarnego.
Teoria Wiena:
T
c
e
c
R
λ
λ
λ
2
1
5
1
=
gdzie c
1
, c
2
to stałe
wyznaczane doświadczalnie. Pokrywała się ona z wynikami
doświadczalnymi jedynie dla małych długości fal. Z kolei
teoria Rayleigh’a była zgodna z doświadczeniem tylko dla
dużych
λ
.
Dopiero Max Planck (1900) zmodyfikował wzór Wiena:
1
1
2
5
1
+
=
T
c
e
c
R
λ
λ
λ
otrzymując pełną zgodność z wynikami
doświadczalnymi.
Chcąc zbudować teorię wyjaśniającą otrzymaną zależność założył, że atomy ciała doskonale
czarnego zachowują się jak oscylatory harmoniczne o charakterystycznych częstościach
drgań:
1. Energia oscylatora jest kwantowana i dana wzorem: E = nh
ν
gdzie n = 1, 2, 3… -
liczba kwantowa, h = 6,63
⋅10
-34
- stała Plancka.
2. Oscylatory nie wypromieniowują energii w sposób ciągły, ale kwantowany, tzn.
wypromieniowana ilość energii
Δ
E = h
ν
. Oscylator znajdujący się w stanie
stacjonarnym (jeden ze stanów kwantowych) nie emituje ani ni absorbuje energii.
Planck wyznaczył wówczas na drodze teoretycznej stałe:
,
h
c
c
2
1
2
⋅
=
π
k
hc
c
=
2
gdzie c –
prędkość światła, k – stała Boltzmana. (1918 – nagroda Nobla)
Przykład:
Klasyczny oscylator o częstotliwości
ν
= 0,5 Hz i energii E = 0,1 J. Liczba kwantowa takiego
oscylatora
32
34
10
01
,
3
5
,
0
10
63
,
6
1
,
0
⋅
=
⋅
⋅
=
=
−
ν
h
E
n
(!) Jeżeli n zmienia się o jedność, to
względna zmiana energii oscylatora
33
34
10
3
,
3
1
,
0
5
,
0
10
63
,
6
−
−
⋅
=
⋅
⋅
=
Δ
E
E
co jest praktycznie
niemierzalne, czyli kwantowa natura drgań obiektów makroskopowych jest niewidoczna.
11.2. Zjawisko fotoelektryczne
U
h
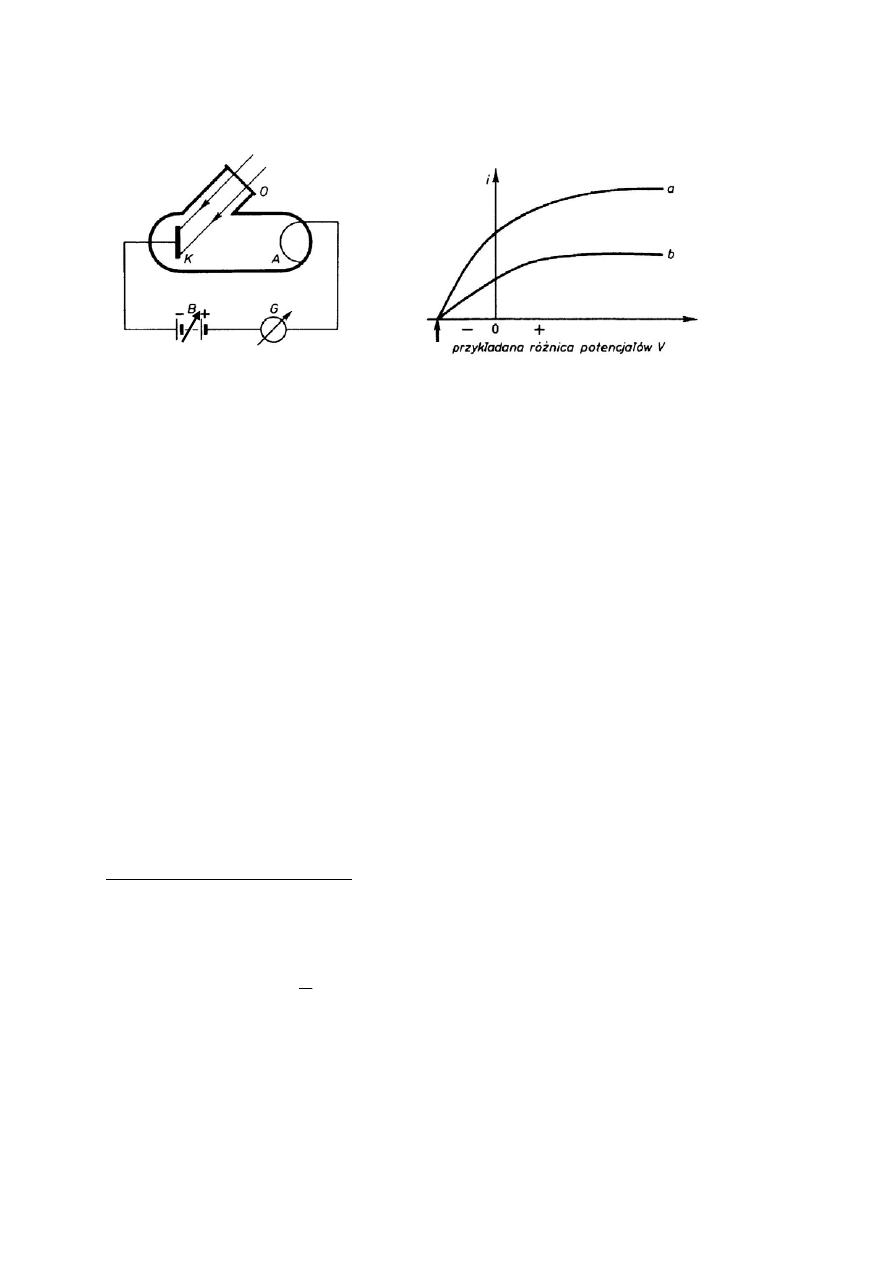
Fotoelektrony wybijane z katody, przyspieszane przez pole elektryczne, tworzą prąd
elektryczny, który płynie miedzy katodą a anodą nawet po przyłożeniu przeciwnego
potencjału do anody. Natężenie prądu fotoelektrycznego spada do zera przy potencjale anody
równym U
h
– potencjał (napięcie) hamujące. E
kmax
= e
⋅
U
h
Na wykresie natężenia fotoprądu od przyłożonego napięcia, krzywą b otrzymano przy
dwukrotnym zmniejszeniu natężenia światła.
Stosowane katody: Li, Cs, Rb
Wyjaśnienie zjawiska:
Planck: światło to fala elektromagnetyczna, rozchodząca się w postaci kwantów energii.
Jednakże wówczas, zgodnie z teorią falową:
1. energia kinetyczna fotoelektronów powinna wzrastać wraz z natężeniem światła,
2. efekt ten powinien występować dla dowolnej częstotliwości światła (o odpowiednio
dużym natężeniu),
3. przy małym natężeniu światła, fotoelektrony powinny wykazywać opóźnienie wybicia
w stosunku do czasu rozpoczęcia naświetlania, aby zmagazynować energię.
Tych efektów się nie obserwuje !!
Einstein: światło rozchodzi się w postaci cząsteczek – fotonów, z których każdy unosi kwant
energii:
λ
ν
c
h
h
E
=
=
A zatem w zjawisku fotoelektrycznym spełniona jest zasada zachowania energii:
h
ν
= W + E
k
gdzie
W – praca wyjścia elektronu, charakterystyczna dla danego
metalu katody.
Jeżeli E
k
= 0 to
W
hc
W
hc
h
gr
gr
gr
=
⇒
=
=
λ
λ
ν
jest to graniczna długość światła, przy
której zachodzi zjawisko fotoelektryczne.
Z zasady zachowania energii:
e
W
e
h
U
h
−
=
ν
ν
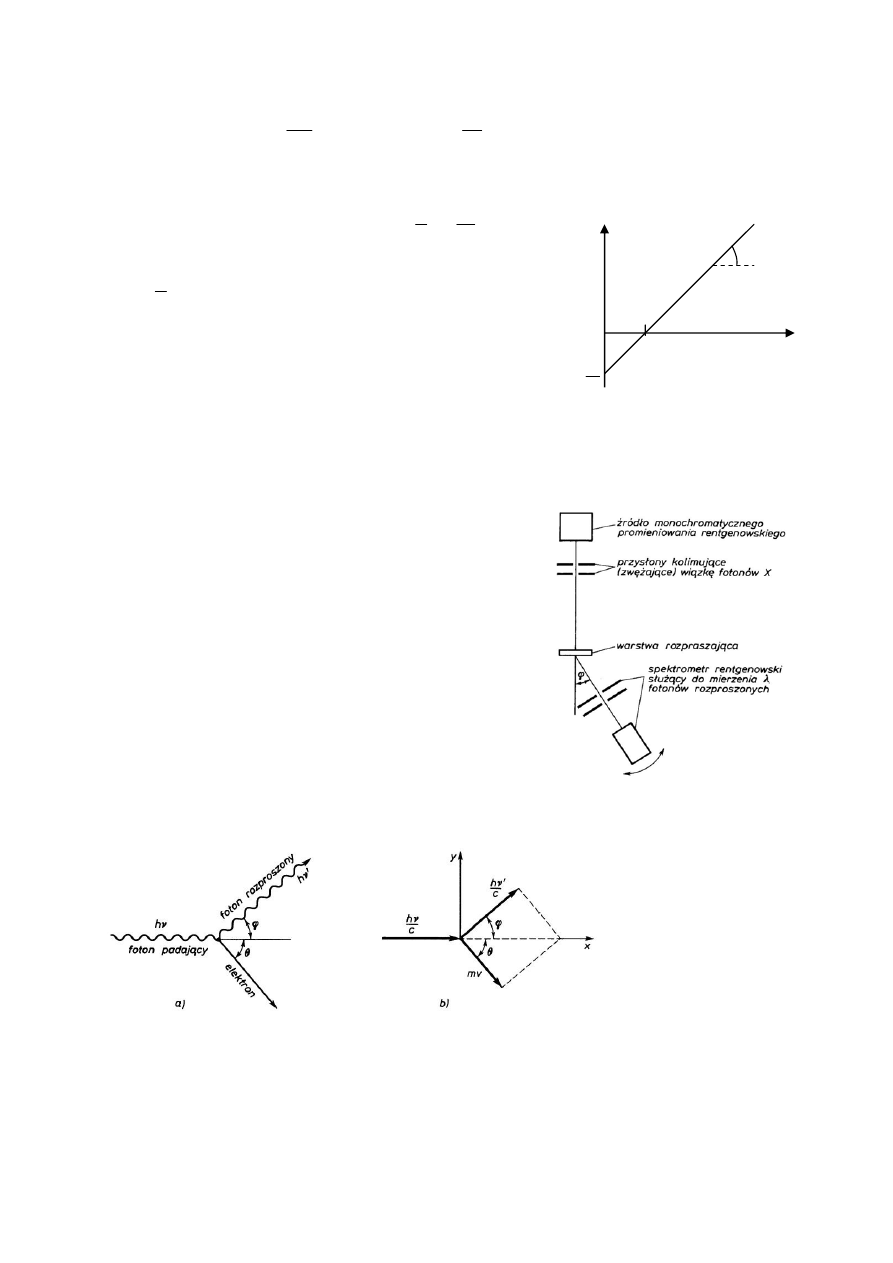
U
h
ν
o
e
W
−
α
α
α
tg
e
h
e
h
tg
⋅
=
⇒
=
Jest to więc sposób wyznaczenia pracy wyjścia
oraz wartości stałej Plancka.
11.3. Zjawisko Comptona
Jest to drugi efekt wskazujący na korpuskularna naturę
światła. Compton (1923) zaobserwował rozproszone
promienie X o zmienionej długości fali. Klasyczna teoria
fal elektromagnetycznych zjawisko rozproszenia
tłumaczyła jako pobudzenie do drgań elektronów ośrodka
rozpraszającego, które staja się wtórnym źródłem fal – ale
bez zmiany długości !
Według teorii kwantowej zjawisko polega na zderzeniu
padającego fotonu z elektronem swobodnym. Podczas
zderzenia foton oddaje elektronowi jedynie część energii.
Zasada zachowania energii:
Zasada zachowania pędu:

Zasada zachowania energii:
Zasada zachowania pędu dla osi OX:
( )
2
2
0
2
0
1
'
c
v
c
m
hc
c
m
hc
−
+
=
+
λ
λ
( )
4
4 3
4
4 2
1
4
3
42
1
elektron
foton
c
v
v
m
h
h
ϕ
ϕ
λ
λ
cos
1
cos
'
2
0
−
+
=
Zasada
zachowania
pędu dla osi OY:
( )
4
4 3
4
4 2
1
3
2
1
elektron
foton
c
v
v
m
h
ϕ
ϕ
λ
sin
1
sin
'
0
2
0
−
−
=
Po wyeliminowaniu z równań v oraz
ϕ
otrzymujemy:
)
cos
1
(
'
0
ϕ
λ
λ
λ
−
=
−
=
Δ
c
m
h
W zjawisku Cmptona zmiana długości fali nie zależy od energii fotonu
padającego, a zależy jedynie od kata jego rozproszenia.
Dla
ϕ
= 0
0
Δλ = 0; dla
ϕ
= 180
0
Δλ = 2
Λ
(rozproszenie wsteczne), a dla
ϕ
= 90
0
Δλ =
Λ
Oba opisy światła: falowy i korpuskularny są poprawne: w pewnych przypadkach
promieniowanie elektromagnetyczne zachowuje się jak fala o określonej długości i
częstotliwości, a w innych jak zbiór fotonów o określonym pędzie i zerowej masie
spoczynkowej. Przejście od obrazu falowego do korpuskularnego opisują wzory:
mv
h
h
p
h
E
=
=
=
λ
λ
ν
Dokładniej omówiony ten problem będzie w rozdz.12.
11.4. Model atomu Bohra
Postulaty Bohra:
I.
Atom wodoru może znajdować się jedynie w ściśle określonych stanach
stacjonarnych, w których nie promieniuje energii.
II.
Elektron atomu w stanie stacjonarnym porusza się tylko po takich orbitach kołowych,
dla których moment pędu jest skwantowany, tzn. spełnia zależność:
π
2
h
n
L
n
=
gdzie
n = 1, 2, ..
III.
Warunkiem wypromieniowania energii jest przejście atomu ze stanu o energii wyższej
E
k
do stanu o energii niższej E
j
: h
ν
= E
k
- E
j
Skoro elektron porusza się po orbicie kołowej pod wpływem siły kulombowskiej będącej siłą
dośrodkową, to z tego warunku można obliczyć prędkość elektronu. A zatem pęd p elektronu
i jego moment pędu L można zapisać:
0
2
0
2
4
4
πε
πε
r
me
pr
L
r
me
mv
p
=
=
=
=
Uwzględniając warunek kwantyzacji momentu pędu otrzymujemy wyrażenia na promień
orbity i energię kinetyczną elektronu.
2
2
0
4
2
0
2
2
8
n
h
me
E
me
h
n
r
n
n
ε
π
ε
−
=
=
A zatem promień orbity rośnie jak n
2
, a energia całkowita rośnie (do zera) jak 1/n
2
. Jonizacji
atomu odpowiada n =
∝. Wówczas całkowita energia atomu E = 0, a r = ∝.
Energia atomu w stanie podstawowym n = 1 :
E
1
= -13,6 eV
Na podstawie powyższych wzorów otrzymujemy wzór na częstość linii widmowych atomu
wodoru:
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
⋅
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
=
2
2
2
2
3
2
0
4
1
1
1
1
8
k
j
c
R
k
j
h
me
ε
ν
gdzie
R jest stałą Rydberga.
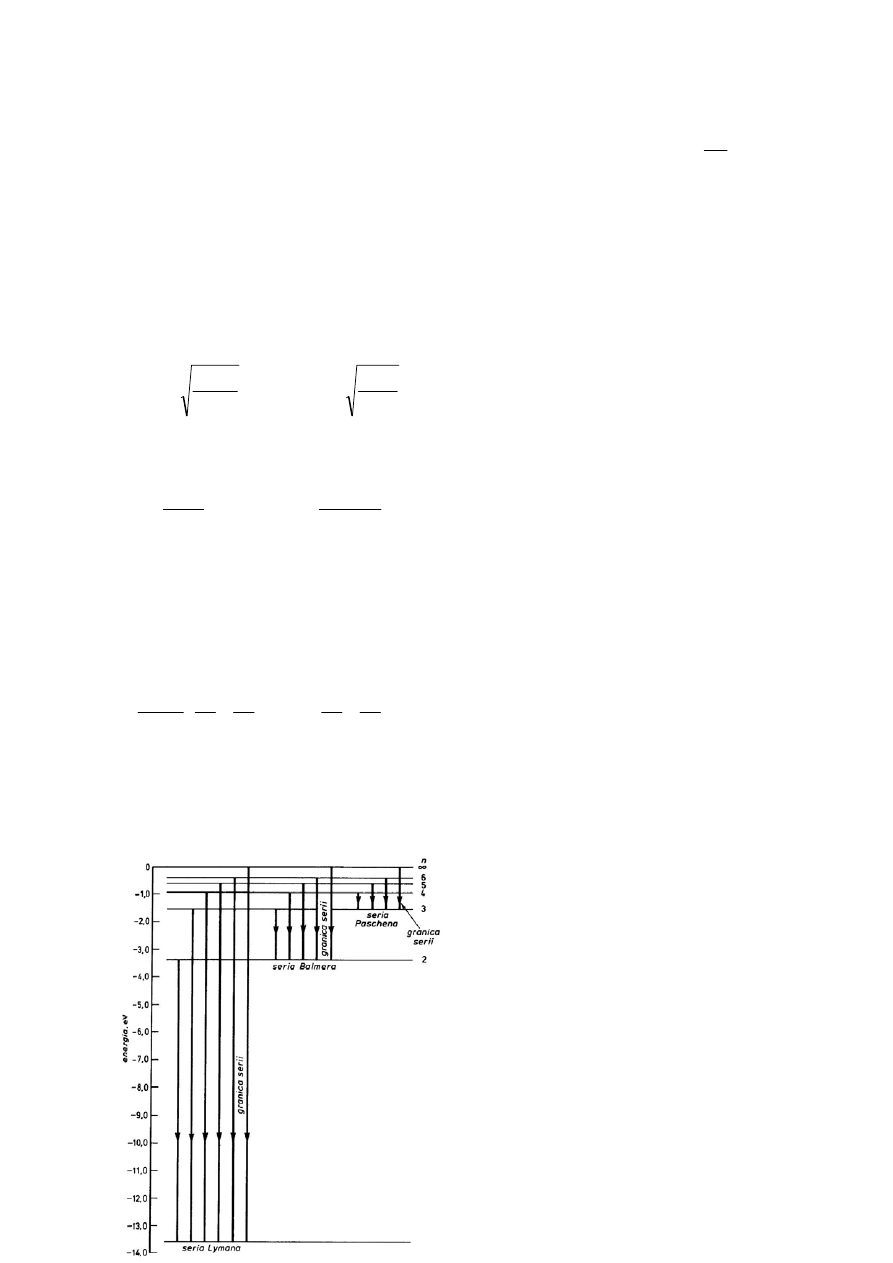
Przejścia elektronu miedzy kwantowanymi poziomami energetycznymi można przedstawić w
postaci tzw. serii widmowych.
Linie serii zagęszczają się w kierunku fal krótkich, a każdą serię ogranicza linia
odpowiadająca najmniejszej długości fali
danej serii.

Przykład:
Obliczyć długość fali emitowanej przy przejściu elektronu z orbity 3 na pierwszą.
31
31
1
3
λ
ν
hc
h
E
E
=
=
−
9
1
3
1
1
2
1
2
1
31
E
E
E
E
hc
−
=
⎟
⎠
⎞
⎜
⎝
⎛−
−
⎟
⎠
⎞
⎜
⎝
⎛−
=
λ
1
31
1
31
8
9
9
8
E
hc
E
hc
=
⇒
=
λ
λ
Wyszukiwarka
Podobne podstrony:
11 Porównanie stanowisk monizm, dualizm i pluralizm
Zarz[1] finan przeds 11 analiza wskaz
11 Siłowniki
11 BIOCHEMIA horyzontalny transfer genów
PKM NOWY W T II 11
wyklad 11
R1 11
CALC1 L 11 12 Differenial Equations
Prezentacje, Spostrzeganie ludzi 27 11
zaaw wyk ad5a 11 12
budzet ue 11 12
EP(11)
W 11 Leki działające pobudzająco na ośrodkowy układ
Zawal serca 20 11 2011
11 Resusc 2id 12604 ppt
11 pomiay dlugosci tasma
więcej podobnych podstron