
FARMAKOLOGIA – WYKŁAD 1
Farmakologia ogólna
farmakologia
pharmacon (=lek)
logos (=nauka)
! Podział farmakologii:
farmakodynamika – nauka o zmianach czynności organizmu pod wpływem leku i mechanizmach działania
leku
farmakokinetyka – nauka o losach leku w organizmie oraz o tym jak lek wpływa na organizm
farmakoterapia – nauka o zastosowaniu terapeutycznym leków
farmakologia kliniczna – nauka o metodach badań i działaniu leków na organizm człowieka zdrowego
oraz chorego
farmakogenetyka – nauka o wpływie czynników dziedzicznych na działanie leków
farmakologia rozwojowa – pediatryczna i geriatryczna; dotyczy dzieci i osób starszych
farmakosologia – nauka o niepożądanych efektach działania leku
chronofarmakologia – nauka o działaniu leków w zależności od rytmu dobowego
toksykologia – nauka o truciznach, skutkach ich działania, o leczeniu i zapobieganiu zatruciu
receptura – nauka o postaciach leku, ich zapisywaniu i sposobach przyrządzania
! Definicja leku:
Lek – substancja pochodzenia roślinnego, zwierzęcego lub powstała w syntezie chemicznej bądź
biotechnologicznej, która po przedostaniu się do organizmu łączy się odpowiednimi receptorami, w wyniku czego
dochodzi do pobudzenia lub hamowania czynności komórek, narządów, organów odwracalnie (w przypadku
efektu nieodwracalnego mamy do czynienia z trucizną)
! Źródła leków:
zwierzęta (hormony np. insulina, ACTH)
rośliny (np. rumianek, chmiel)
minerały
synteza chemiczna
mikroorganizmy, synteza biotechnologiczna
leki rekombinowane np. insulina z bakteriami, ludzka rekombinowana erytropoetyna, tkankowy
aktywator plazminogenu
! Drogi podania leków:
miejscowe
wewnętrzne:
doustnie
podjęzykowo
doodbytniczo, dopochwowo
parenteralnie
domięśniowo, dordzeniowo, dootrzewnowo
! Rodzaje działania leków:
działanie przyczynowe (etioterapeutyczne) – usunięcie przyczyny choroby
działanie objawowe (symptomatyczne) – usunięcie lub złagodzenie objawów chorobowych
działanie ośrodkowe – działanie leków bezpośrednio na komórki OUN po wchłonięciu się ich do krwioobiegu
działanie obwodowe – działanie na inne tkanki poza OUN, zwłaszcza na zakończenia receptorów obwodowego
układu nerwowego
działanie miejscowe – działanie leków w miejscu ich podania
działanie ogólne(systemowe) – działanie leków po ich wchłonięciu do krwioobiegu
działanie wybiórcze – niektóre leki podawane w małych dawkach oddziałują wyłącznie na czynność
określonych narządów
akrytocyna – działanie wyłącznie na macicę kobiety ciężarnej, po porodzie na wrażliwość się
kończy

! Mechanizm działania leków:
jest to sposób oddziaływania leku ze składnikami żywego organizm, w wyniku czego dochodzi do wyzwolenia
efektu farmakologicznego
wyróżniamy 2 główne mechanizmy działania:
mechanizm biochemiczny, którego istota sprowadza się do teorii receptorowej
mechanizm fizykochemiczny (chlorek etylu – niska temperatura chłodzi zbolałe mięśnie)
receptor (farmkoreceptor) – określona struktura biogazy posiadająca właściwości swoistego wiązania się z
cząsteczkami leku
wyróżniamy 2 główne typy receptorów:
jonotropowe
regulujące przepływ jonów przez kanały jonowe, czyli ich działanie
metabotropowe
działające za pomocą tzw. wtórnego przekaźnika, a będące rodzajem mechanizmu
spustowego
przyłączenie leku (agonisty) do tego receptora uruchamia kolejne etapy procesu
biochemicznego i reakcje farmakologiczną (działanie poprzez podwyższenie lub
obniżenie stężenia cAMP, cykl fosfatydyloinozytolowy, wpływ na gospodarkę wapniową)
aktywność wewnętrzna leku – zdolność leku do pobudzania receptora i wyzwalania efektu farmakologicznego
agonista – lek mający powinowactwo do receptora i aktywność wewnętrzną, w następstwie czego dochodzi do
wyzwolenia efektu farmakologicznego w komórce
antagonista – związek mający powinowactwo do receptora, lecz nie mający aktywności wewnętrznej, przez co
powoduje on blokowanie receptora i uniemożliwia wyzwalanie efektu właściwym agonistom (antagonizm
kompetycyjny)
efekt allosteryczny – zmiana konfiguracji przestrzennej receptora pod wpływem leku
aktywacja allosteryczna – zwiększenie powinowactwa do agonisty
hamowanie allosteryczne – zmniejszenie powinowactwa do agonisty
mechanizm wyzwalania efektu farmakologicznego:
teoria okupacyjna – lek długo wiąże się z receptorem
teoria dynamiczna – efekt krótki (np. nitrogliceryna)
punkty „uchwytu” leków:
target (cel) – miejsce, w którym działa lek; takimi punktami są:
enzymy i koenzymy – większość leków bezpośrednio lub pośrednio wpływa na aktywność
enzymów hamując lub pobudzając ten parametr
substraty – niektóre leki eliminują z procesów biologicznych określone składniki ustrojowe (np.
mocznik)
kwasy nukleinowe – niektóre leki zmieniają funkcje komórkowe poprzez wpływ na kwasy
nukleinowe
! Zależność działania leku od dawki:
efekt farmakologiczny leku – zmiana czynności komórki, narządów czy całego organizmu pod wpływem leku
aktywność leku – właściwość wyzwolenia określonego efektu przez określoną dawkę leku
intensywność działania leku – właściwość wyzwolenia maksymalnego efektu określonej wielkości
dawka minimalna – najmniejsza dawka leku wywołująca efekt farmakologiczny
dawka maksymalna – największa dawka leku, która może być stosowana w lecznictwie
dawka efektywna – dawka wywołująca określony efekt farmakologiczny
wskaźnik leczniczy (indeks terapeutyczny) – stosunek dawki wywołującej objawy toksyczne lub śmierć
organizmu do dawki leczniczej
siła działania leku jest wprost proporcjonalna do ilości leku wprowadzonego do organizmu (dawki leku) – np.
fenobarbital:
10 mg – działanie uspokajające
100 mg – działanie nasenne
200 mg – działanie p/drgawkowe
> 300 mg – działanie toksyczne
1g – śmiertelne

! Inne pojęcia farmakologiczne:
tachyfilaksacja – zjawisko szybkiego wygaszania działania leku np. przy dożylnym podaniu efedryny następuje
coraz słabszy wzrost ciśnienia tętniczego krwi, aż do całkowitego zaniku reakcji mięśniówki naczyń
krwionośnych
tolerancja – proces podobny do tachyfilaksacji, lecz rozwijający się wolniej; do uzyskania tej samej reakcji staje
się konieczne stosowanie coraz większych dawek leku
kumulacja – gromadzenie się leku w organizmie, zjawisko swoiste dla niektórych związków; proces ten
zachodzi w przypadku podania leku w zbyt krótkich odstępach czasu tak, że organizm nie potrafi wydalić
poprzedniej dawki leku przed podaniem następnej
nadwrażliwość na lek – zjawisko uwarunkowane genetycznie lub nabyte; występuje na tle uczuleniowym u
osób z wrodzoną skłonnością do reagowania w sposób gwałtowny, nietypowy na minimalne nawet dawki
leków; nadwrażliwość na leku występuje często u pacjentów z chorobami alergicznymi
idosynkrazacja – stan zwiększonej odczynnowości organizmu na określony związek chemiczny; jest to zależna
od ilości leku reakcja organizmu i wynika z nieprawidłowości przemian biochemicznych leku w organizmie;
stan ten, uwarunkowany genetycznie lub nabyty, różni się zasadniczo od objawów uczuleniowych, przy któryc
dochodzi do reakcji Ag – przeciwciało
farmakokinetyka
farmakodynamika
uwalnianie (distribution)
wchłanianie (absorbation)
dystrybucja (distribution)
metabolizm (metabolism)
wydalanie (elimination)
wiązanie z receptorem
działanie leku
! Wchłanianie:
większość leków wykazuje działanie po dostaniu się do ustroju – wyjątek od tej reguły stanowią kremy, bądź
maści stosowane miejscowo na skórę, bądź środki przeczyszczające
aby substancja wykazała działanie farmakologiczne musi wniknąć do organizmu; może być podana różnymi
drogami:
doustnie
parenteralnie (dordzeniowo, dootrzewnowo)
dokomorowo, dordzeniowo, dopochwowo
substancja musi pokonać liczne bariery w organizmie – bariery lipidowe, czy też błony biologiczne (ściany
jelita, ściana naczyń krwionośnych, bariera krew-mózg, błony komórkowe)
czynniki wpływające na wchłanianie:
właściwości leków
masa cząsteczkowa substancji
stopień dysocjacji
lipofilność
postać leku
stan pacjenta
obecność i rodzaj pożywienia w żołądku
pasaż jelitowy
przepływ krwi przez jelita
pH w żołądku
schorzenia przewodu pokarmowego
transport przez błony komórkowe:
dyfuzja przez szczeliny pomiędzy komórkami (kłębuszki nerkowe = 68kDa, kapilarny = 30kDa)
transport przez błony komórkowe:
dyfuzja przez pory (bardzo małe cząsteczki)
wspomagany (specyficzny, ograniczony – Fe w jelitach, L-DOPA przez barierę krew-
mózg)
pinocytoza (insulina w OUN, toksyna botulinowa w jelitach)
dyfuzja poprzez lipidy błony komórkowej (zależy od powierzchni, gradientu, substancji
towarzyszących)

energia
dyfuzja
przez kanały przy udziale transport
jonowe
nośników
aktywny
! Kompartment:
obszar kinetycznie jednorodny, tzn. taki, na którym lek rozmieszcza się równomiernie z takim samym
stężeniem w danym momencie czasowym
pojęcie kompartmentu ma charakter czysto funkcjonalny, przeważnie niezwiązany z określonym obszarem
anatomicznym
układ jedno- i wielokompartmentowy:
układ jednokompartmentowy – podany lek ulega jednolitemu rozproszeniu w organizmie
układ wielokompartmentowy – lek nagromadził się np. tylko w układzie krążenia
! Wiązanie leków z białkami:
OSOCZE
lek związany z białkiem
wolna część leku
albuminy (60%)
γ-globuliny (18%)
α-globuliny (12%)
β-globuliny (10%)
TKANKI
lek związany z białkiem
wolna część leku
ligandyna – wątroba, nerki, jelita (kortykosteroidy)
DNA – cytostatyki
melanina, pochodne fenotiazyny, efedryna
tkanka kostka - tetracykliny
o czym informuje stopień wiązania z białkami?
silne wiązanie się leku z białkami
duża dawka początkowa (inicjująca)
mniejsze dawki podtrzymujące
wypieranie leku A z połączeń z białkami przez lek B
szczególnie niebezpieczne w przypadku leków o małym indeksie terapeutycznym
np. wypieranie warfaryny przez fenylobutazon
teikrytycznym objawem są krwotoki
stężenie fenylobutazonu [mg/l]
% warfaryny związanej
0
97,4
50
79,3
100
70,6
150
62,5
przyczyny prowadzące do zmian w wiązaniu leku z białkami:
spadek stężenia albumin
niedożywienie
marskość wątroby
oparzenia
zespół nerczycowy
niewydolność nerek
nadczynność tarczycy
obniżenie stężenia kwaśniej α
1
-glikoproteiny
doustne środki antykoncepcyjne
marskość wątroby
podwyższenie stężenia albumin
niedoczynność tarczycy
podwyższenie stężenia kwaśniej α
1
-glikoproteiny
reumatoidalne zapalenie stawów

choroba Cohna
oparzenia
otyłość
! Metabolizm leków:
zachodzi głównie w:
wątrobie
osoczu krwi
świetle przewodu pokarmowego
ścianie jelita
płucach
efekt pierwszego przejścia:
leki podane doustnie dostają się do krwioobiegu niemal wyłącznie przez układ krążenia
wrotnego, przez co cała wchłonięta dawka leku przechodzi najpierw przez wątrobę
w wątrobie leki poddane są działanie enzymów metabolicznych tzn. ułamek dawki zostaje
„wyekstrahowany” z krwi i ulega przemianom, zanim dostanie się do krążenia ogólnego, co
ewidentnie obniża jego dostępność biologiczną
typy reakcji biotransformacji:
reakcje I fazy:
zmiany aktywności leków
utworzenie grup chemicznych umożliwiających przeprowadzenie reakcji II fazy
reakcje hydrolizy, oksydacji, redukcji
reakcje II fazy:
sprzęganie z kwasem glukuronowym, siarkowym, glukozą, grupami metylowymi, resztą
acetylowi, glicyną, kwasem glutaminowym
powodują spadek aktywności leku, spadek lipofilowości, wzrost hydrofilowości przez
reakcje pozamikrosomalne:
esterazy
dehydrogenazy
czynniki wpływające na metabolizm:
wiek pacjenta:
noworodki
ludzie starsi
płeć
progesteron – hamuje procesy glukuronizacji
estradiol – hamuje procesy hydroksylacji
kortyzon
stan pacjenta
choroby wątroby i nerek
dieta
brak białka w pożywieniu
! Wydalanie:
zachodzi głównie z moczem
filtracja kłębuszkowa – związki chemiczne o małej masie cząsteczkowej <25kDa ulegają filtracji;
połączenia z białkami nie są filtrowane
wydzielanie kanalikowe – proces aktywny dla kationów i anionów
bierna reabsorpcja – lipofilne związki przenikają przez kanaliki nerkowe
wpływ pH:
związki o charakterze słabych kwasów – w moczu kwasy nie są zjonizowane, ulegają szybkiemu
wchłonięciu
związki o charakterze słabych zasad – w moczu są zjonizowane
wpływ lipofilności i pH na wchłanianie:
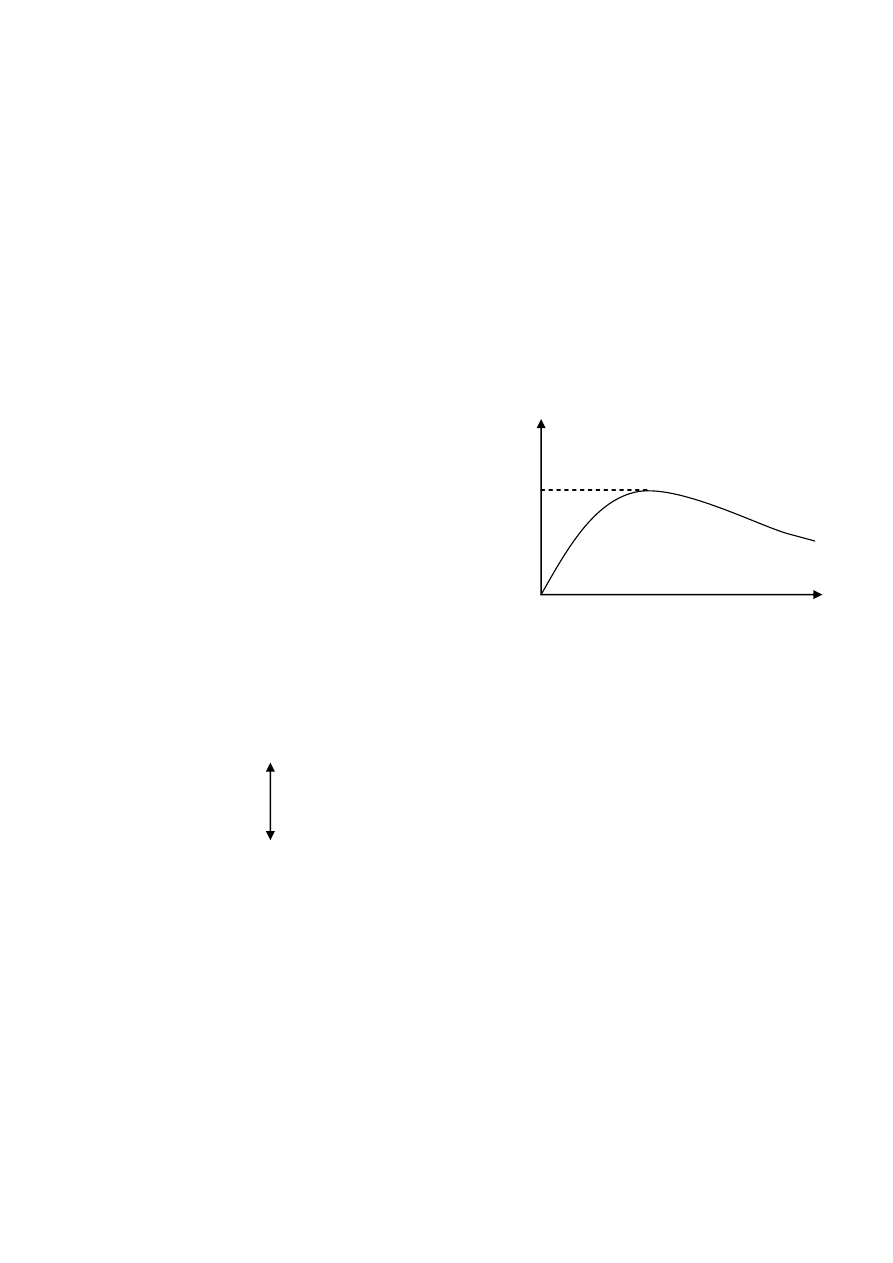
zjonizowane leki są słabiej rozpuszczalne w tłuszczach, 99% przesączu jest wchłanianych w kanalikach
nerkowych
wydalanie pozanerkowe:
z żółcią – substancje, które słabo wchłaniają się w jelitach, ze względu na znaczna dysocjację
bromosulfoftaleina, zieleń indocyjanianowa
ze śliną – substancja małe, nierozpuszczalne w tłuszczach
mocznik, acetamid
z potem – substancje niezjonizowane
alkohol etylowy, mocznik
przez płuca
alkohol
Przy podaniu doustnym stężenie leku rośnie, a następnie maleje
! Dostępność biologiczna:
biodostępność bezwzględna (F) – ułamek, procent dawki leki jaki przechodzi do krążenia ogólnego po
pozanaczyniowym podaniu leku
przyjmuje się, że po dożylnym podaniu leku wartość tego ułamka wynosi 1 (100%), a po pozanaczyniowym <1
parametry określające dostępność biologiczną:
AUC – pole stężeń pod krzywą – miara ilości leku,
jaka dociera do krążenia ogólnego w postaci
niezmienionej
C
max
T
max
! Wielokrotne podanie dożylne:
kumulacja – zachodzi, gdy maksymalna ilość substancji leczniczej w organizmie (C
max
w osoczu) obserwowana
po podaniu kilku dawek w odpowiednio dobranych przedziałach czasu jest większa niż ta sama ilość po
podaniu pojedynczej dawki
okno terapeutyczne – zawartość leku między C
max
a C
min
toksyczność
okno terapeutyczne
biodostępność
Leki mające wąskie okno terapeutyczne:
teofilina (ksantyny)
glikozydy nasercowe (digoksyna, digitoksyna)
leki p/arytmiczne (chinidyna, lidokaina, prokainamid)
aminoglikozydy (gentamycyna, tobramycyna)
leki immunosupresyjne
leki p/padaczkowe (karbamazepina, fenobarbital, fenytoina, kwas
walproinowy)
! Czynniki modulujące podanie leków:
choroby metaboliczne:
cukrzyca
nadczynność lub niedoczynność gruczołu tarczowego
niewłaściwe odżywanie
czynniki środowiskowe
insektycydy
choroby nerek:
zmniejszenie przesączu kłębuszkowego
zmiana pH w moczu
uszkodzenie hepatocytów
hipoalbuminemia
czynniki farmakodynamiczne
wiek
! Interakcje leków:
Tmax
Cmax
AUC

Farmakokinetyka
Farmakodynamika
wchłanianie
wiązanie z białkami
transport przez błony biologiczne
biotransformacja
wydalanie
synergizm
antagonizm
! Interakcje farmakokinetyczne w zakresie wchłaniania w jelitach:
adsorpcja na powierzchni (węgiel aktywny)
tworzenie się trudno rozpuszczalnych kompleksów (tetracykliny i jony wapniowe
zmiana napięcia powierzchniowego (kwasy żółciowe powodują wzmożone wchłanianie jelitowe leków)
zmiana pH treści jelitowej
leki alkalizujące obniżają wchłanianie leków kwaśnych
leki zakwaszające obniżają wchłanianie leków o odczynie alkalicznym
konkurencja o systemy przenośnikowe
uracyl – tymina
glukoza
zmniejszanie przepływu krwi przez jelita – leki naczyniozwężające będą obniżały wchłanianie
zwiększanie perystaltyki jelit – środki przeczyszczające obniżają wchłanianie leków w jelitach
! Interakcje w zakresie wiązania leków z białkami:
czynniki modyfikujące wiązania leków z białkami:
stężenie białek i stężenie leku
powinowactwo leków do białek
pH środowiska
zakwaszanie krwi podwyższa stopień wiązania leków o charakterze słabych kwasów
alkalizacja krwi podwyższa stężenie wolnej postaci tego leku w okolicy
wypieranie leków z wiązania z białkami:
a. lek silnie wiążący się z białkami:
fenyobutazon, salicylany
lek wypierany z wiązania z białkami:
sulfonamidy
b. lek silnie wiążący się z białkami:
fenylobutazon, salicylany
lek wypierany z wiązania z białkami:
leki hamujące krzepnięcie krwi (dikumarol)
leki p/cukrzycowe (tolbutamid)
penicyliny (nowobiocyna)
c. lek silnie wiążący się z białkami:
indometacyna, salicylany
lek wypierany z wiązania z białkami:
kortykosteroidy
! Interakcje w zakresie transportu leków przez błony biologiczne:
transport bierny:
zmiana pH płynów ustrojowych
zakwaszenie krwi powoduje wzrost przepuszczalności bariery krew – mózg wobec
barbituranów
alkalizacja krwi powoduje spadek przepuszczalności bariery krew-mózg wobec
barbituranów
zmiana przepuszczalności błon biologicznych
rozluźnienie struktury błon komórkowych
zmniejszenie napięcia powierzchniowego (DMSO, związki depolimeryzujące, hialuronidaza)
transport czynny:
ułatwienie
insulina, somatotropina, ACTH, wazopresyna
osłabienie
glikozydy nasercowe

! Interakcje w zakresie biotransformacji leków:
enzymy biorące udział w procesie biotransformacji:
p/pokarmowy: proteazy, lipazy, dekarboksylazy
wątroba: enzymy mikrosomalnej, esteraz, transferazy
drobnoustroje jelitowe: reduktazy, dekarboksylazy
łożysko: reduktazy
induktory enzymatyczne:
barbiturany – obniżają metabolizm doustnych leków p/krzepliwych
fenytoina – obniża metabolizm tolbutamidu
karbamazepina – obniża metabolizm prednizolonu
inhibitory enzymatyczne:
izoniazyd – wzrost dla fenytoiny
allopurynol – wzrost dla doustnych leków p/krzepliwych
fenylbutazon – wzrost dla tolbutamidu
! Interakcje w zakresie wydalania przez nerki:
leki zakwaszające mocz powodują spadek wydalania leków kwaśnych, wzrasta natomiast wydalanie leków
alkalicznych
leki alkalizujące mocz powodują spadek wydalania leków alkalicznych, wzrasta natomiast wydalanie leków
kwaśnych
MOCZ
MOCZ
kwaśny
(hamowanie wydalania)
alkaliczny
(przyspieszenie wydalania)
kwaśny
(przyspieszenie wydalania)
alkaliczny
(hamowanie wydalania)
substancje o charakterze kwaśnym:
ampicylina
barbiturany
fenylobutazon
penicylina
pochodne kumaryny
salicylany
streptomycyna
substancje o charakterze zasadowym:
amfetamina
aminofenazon
atropina
erytromycyna
gentomycyna
metyloksantyna
petydyna
prokaina
! Interakcje w zakresie konkurencji z czynnym wydalaniem kanalikowym:
probenecyd podnosi stężenie penicyliny we krwi oraz stężenie salicylanów we krwi
salicylany podnoszą stężenie metotreksatu we krwi
spironolakton podnosi stężenie digoksyny we krwi
! interakcje farmakodynamiczne:
synergizm:
addycyjny (propanolol – acebutanol)
hiperaddycyjny (propanolol – werapramil)
antagonizm:
konkurencyjny (kompetycyjny) (adrenalina – acebutanol)
niekonkurencyjny – niekompetycyjny
allosteryczny (acetylocholina – pirylamina)
czynnościowy (acetylocholina – adrenalina)
fizjologiczny (wazopresyna – satalol)
! Działania niepożądane leków:
hepatotoksyczne
neurotoksyczne
oto toksyczne
neurotoksyczne
kardiotoksyczne
mielotoksyczne
alergizujące
teratogenne
embriotoksyczne
karcinogenne (np. pabialgina – może wywołać
nowotwory po kilku latach)
Wyszukiwarka
Podobne podstrony:
w1.FARMAKOLOGIA OGÓLNA, wykłady PMWSZ w Opolu - Pielęgniarstwo, Farmakologia
Wykład Farmakologia ogólna 2, FARMAKOLOGIA
farmakologia ogólna
Farmakologia Ogólna
Farmakoterapia ogólna i miejscowa
FARMAKOLOGIA OGÓLNA ANALITYKA
farmakologia ogólna cz2
Farmakologia ogólna 7
FARMAKOLOGIA OGÓLNA LEKÓW P
więcej podobnych podstron