
1
IX Barwniki antocyjanowe
Barwniki to związki chemiczne absorbujące światło w zakresie widzialnym. Pod względem
budowy chemicznej stanowią grupę bardzo zróżnicowanych związków. Najogólniej można je
podzielić na związki zawierające azot – tutaj należą barwniki pochodne pirolu, a więc chlorofile, a
także barwniki pochodne pirymidyny oraz związki bezazotowe – chinoidy, flawonoidy i
karotenoidy. Charakterystyczną cechą barwników roślinnych jest to, że występują w komórkach w
postaci glikozydowej lub w połączeniu z białkiem.
Istnienie barwnych substancji organicznych jest przykładem wpływu rezonansu
elektronowego na właściwości substancji. Rozpatrując wzory barwników można zauważyć, że
każdy zawiera długi łańcuch na przemian zmieniających się pojedynczych i podwójnych wiązań
węgiel-węgiel, czyli układ tzw. sprzężonych wiązań podwójnych, który może występować w dwu
równoważnych formach. Obecność takich struktur rezonansowych jest koniecznym warunkiem, aby
związek organiczny był barwnikiem. Substancja jest barwna, ponieważ selektywnie absorbuje
światło widzialne. Barwa, którą obserwujemy jest barwą odbitą lub przepuszczoną przez daną
substancję barwną. W ten sposób substancja czerwona absorbuje światło niebieskie i zielone,
substancja zielona światło czerwone i niebieskie itd. Zdolność absorbowania światła jest
konsekwencją rezonansu elektronowego w układzie podwójnych wiązań sprzężonych. Absorpcja
światła widzialnego zachodzi przy podwyższeniu sprzężenia. Barwnikami są wszystkie produkty o
odpowiednio wystarczającym sprzężeniu na to, aby spowodować pojawienie się intensywnej barwy.
Antocyjany należące do barwników flawonoidowych są charakterystyczne tylko dla roślin
wyższych. Najbardziej istotną ich funkcją jest zmiana widma absorpcyjnego wnętrza komórki, a
zwłaszcza chloroplastów, co wiąże się z wykorzystaniem innych długości fal świetlnych do
fotosyntezy, a także tworzenie barw u roślin. Antocyjany charakteryzują się całą gamą barw, od
jasnoniebieskiej po purpurową. Występują w kwiatach, owocach, liściach, korzeniach i bulwach
roślin.
W roślinach antocyjany występują w postaci glikozydów. Glikozydy to związki chemiczne,
pochodne węglowodanów, których anomeryczny atom węgla jest związany przez kondensację do
atomu niecukrowej grupy. Kondensacja ta zachodzi najczęściej przez atom tlenu, rzadziej węgla,
siarki lub azotu. Wiązanie takie nazywa się wiązaniem glikozydowym. Część cukrową takiego
związku nazywa się glikonem, a cząsteczkę niecukrową aglikonem. W przypadku glikozydów
roślinnych część cukrowa składa się najczęściej z kilku (do 12) cząsteczek cukrów prostych.
W przypadku barwników antocyjanowych cześć aglikonowa nazywana jest antocjanidyn
ą
(około 15 typów). Cześć cukrową (glikon) antocyjan stanową z reguły krótkie 1- 3 cząsteczkowe
łańcuchy złożone z glukozy lub, rzadziej, innych cukrów np. ramnozy, arabinozy, ksylozy,
galaktozy. Przyłączenie cząsteczki cukru do aglikonu występuje najczęściej w pozycji C3,
wiązaniem β-glikozydowym. Glikozydowa postać jest korzystna, gdyż dzięki temu antocyjany są
dobrze rozpuszczalne w soku komórkowym, natomiast wolne są nierozpuszczalne w wodzie. Cukry
wpływają także na trwałość aglikonów.
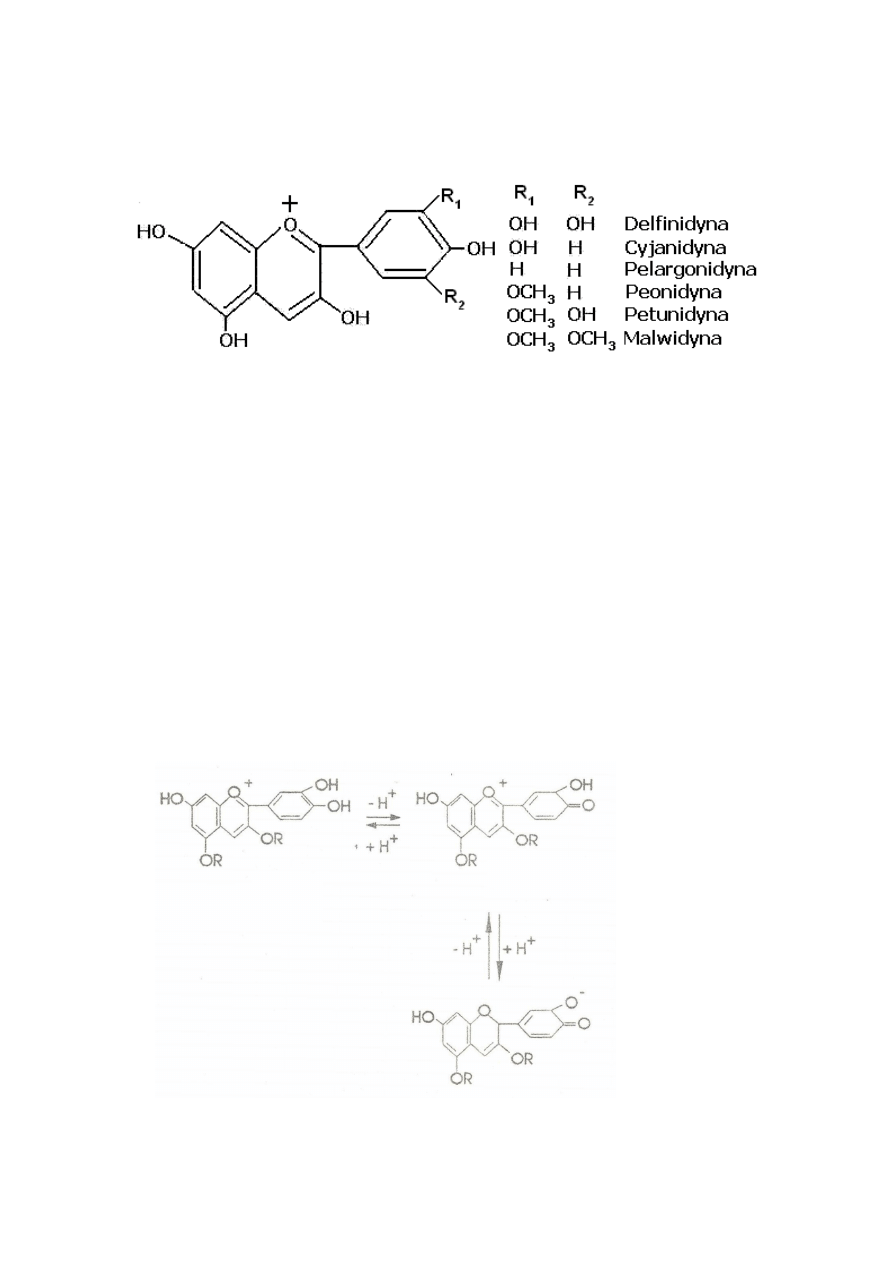
W grupie antocyjanów wyróżniono 15 typów antocyjanidyn (tych po odjęciu części
cukrowej), z których 6 spotykamy w naturze najczęściej. Są to: cyjanidyna (aronia, wiśnie,
czerwona kapusta, żurawina), delfinidyna (winogrona, czarne jagody, czarny bez, żurawina),
pelargonidyna (pelargonia, truskawka), peonidyna (czarny bez, peonia), malwidyna (winogrona,
2
malwa), petunidyna (petunia). Najbogatszym surowcem antocyjanowym są owoce aronii, które
obfitują w różne glikozydy cyjanidyny.
Ryc. 1. Antocyjanidyny
Przykładami powszechnie występujących antocyjanów są: cyjanidyno-3-glukozyd, cyjanidyno-
3-rutynozyd, malwidyno-3-glukozyd, malwidyno-3,5-diglukozyd.
Na barwę antocyjan mają wpływ:
1.
Metylacja niektórych grup hydroksylowych – zmiana barwy w kierunku czerwonej;
2.
Nagromadzenie antocyjanów w roślinach w stosunku do innych barwników – czyli zmiany
ilościowe w zależności od gatunku;
3.
Kopigmentacja – zmiana barwy w kierunku niebieskiej pod wpływem flawonów i
związków pokrewnych; patrz niżej;
4.
Kompleksy z metalami – czynnik wywołujący zmianę barwy w kierunku niebieskiej;
5.
Wpływ pH; patrz niżej (ryc.2).
Ryc. 2. Wpływ pH na barwę cyjanidyny
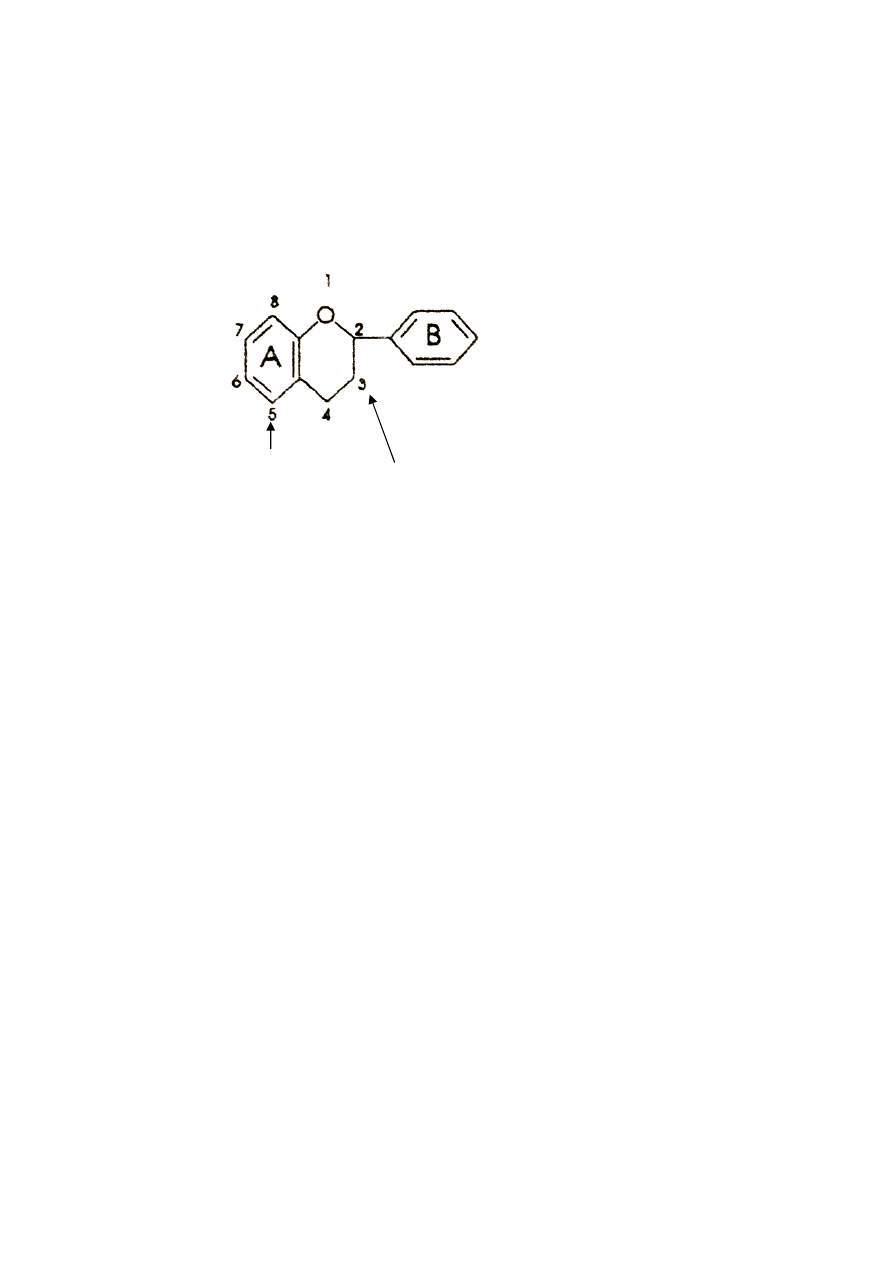
3
W ostatnich latach wzrosło zainteresowanie konsumentów żywnością barwioną naturalnymi
barwnikami. Zmusza to jej producentów do rezygnacji ze stosowania barwników syntetycznych i
zastosowania do barwienia żywności naturalnych barwników. Związane jest to ze znacznymi
ograniczeniami, gdyż barwniki antocyjanowe są bardzo niestabilne. Z tego powodu poszukuje się
bezpiecznej z punktu widzenia zdrowotnego metody stabilizacji antocyjanów. Takim sposobem
wydaje się kopigmentacja antocyjanów z innymi związkami np. flawonoidami (ryc. 3).
cukier
flawon
cukier
Ryc. 3. Najczęstsze połączenia antocyjanidyny z cukrem i kopigmentatorem
Barwa antocyjanów zależy od pH środowiska, w jakim się one znajdują; w przypadku pH
poniżej 7 (kwaśne) są one czerwone, a w pH obojętnym lub zasadowym (pH > 7) mają barwę
niebieską lub fioletową. Jeśli jednak występują one w kompleksie z jonami glinu, magnezu lub
żelaza III, to mimo kwaśnego odczynu środowiska, również mają barwę niebieską (tak jest np. w
kwiatach chabra bławatka).
Nagromadzenie cukru powoduje często wzmożone wytwarzanie antocyjanu. Okorowane lub
złamane gałęzie winorośli lub derenia uzyskują krwistoczerwone jesienne zabarwienie liści
wskutek przerwania odpływu cukru.
Antocyjany oprócz roli barwników mają prawdopodobnie także inne znaczenie dla roślin.
Przypuszcza się, że biorą udział w procesach oddychania. Przypisuje się im zdolność ochrony
organizmu przed szkodliwym działaniem promieni X. Flawonoidy wykazują pewne działanie
fizjologiczne na żywe organizmy typu: pobudzenie lub zahamowanie czynności serca, ruchów
oddechowych czynności mięśni, działanie obniżające lub podwyższające ciśnienie krwi,
przeciwwirusowe, bakteriobójcze.
Antocyjany występują szeroko w całym świecie roślinnym. Nie stwierdzono ich tylko u
glonów i w rodzinach roślin kaktusowatych i komosowatych (np. komosa, burak czerwony, szpinak).
Rodziny te mają swoją, odrębną grupę barwników zwanych betalainami, w skład których wchodzą
czerwonofioletowe betacyjany i żółte betaksantyny. Barwniki te występują nie tylko w korzeniu
buraka, ale także w kilku innych roślinach i grzybach niespożywanych przez człowieka. Wyjątkiem
jest opuncja figowa (Opuntia ficus-indica), która zawiera je w jadalnych owocach. W buraku
dominują betacyjany maskujące obecność betaksantyntynów. Barwniki buraka charakteryzują się
ograniczoną stabilnością, zależną od wielu czynników. Betacyjany są szczególnie nieodporne na
działanie podwyższonej temperatury, a także tlenu. Największą stabilność wykazują przy pH 4 – 5,
zaś odczyn zasadowy powoduje ich szybki rozpad. Podczas obróbki cieplnej czerwone barwniki
4
betacyjanowe rozkładają się szybciej niż żółte betaksantyny, zwłaszcza jeśli gotuje się buraki obrane
i rozdrobnione. Wywar i buraki nabierają wtedy zabarwienia czerwonobrunatnego, a przy
długotrwałym ogrzewaniu żółtobrązowego. Buraki gotowane w skórce zachowują dobrze barwniki, a
obniżenie pH roztworu przez zakwaszenie zwiększa intensywność i stopień zachowania barwy.
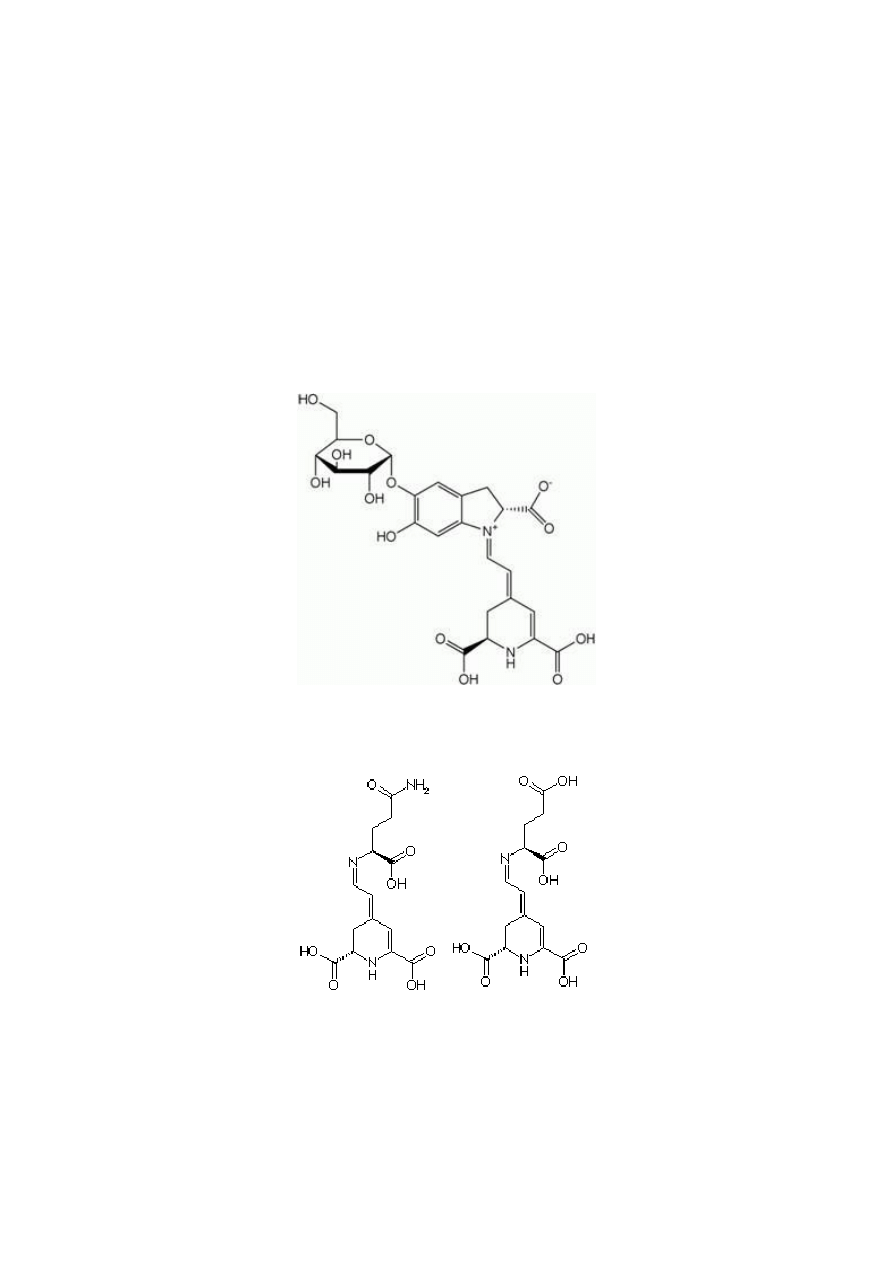
W burakach ćwikłowych głównym betacyjanem jest betanina (ryc. 4), a główną betaksantyną –
wulgaksantyna I i wulgaksantyna II (ryc. 5). Dwie wulgaksantyny różnią się jedynie pojedynczą
boczną grupą cząsteczki.
Ryc. 4. Betanina
Ryc. 5. Wulgaksantyna I (po lewej) i II (po prawej)

5
Antocyjany występują w wakuolach. Nadające barwy kwiatom znajdują się w komórkach
epidermy. Kwiaty białe swój efekt barwny uzyskują w wyniku obecności powietrza w tkankach
(odbija światło).
Przygotowanie wyci
ągów
Sprz
ęt i odczynniki
Zlewka 250 ml (2 sztuki), kolba erlenmajera (2 sztuki), bagietka, probówki (14 sztuk), cylinder
miarowy.
Wykonanie
a) antocyjany z kapusty:
Kapustę pokroić w drobniutkie kawałki, wsypać do zlewki 250 ml do poziomu 100 ml.
b) betacyjany z buraka:
Burak pokroić w drobną kostkę i wsypać do zlewki 250 ml do poziomu 100 ml.
Obie zlewki napełnić woda destylowaną do poziomu 250 ml i powoli ogrzewać do wrzenia
mieszając bagietką. Po zagotowaniu i ostudzeniu odsączyć roztwory do kolbek erlenmajera.
Ćwiczenia 1. Wpływ pH na barwę barwników
a)
Do 2 probówek nalać po 2 ml wyciągu z kapusty, następnie do pierwszej z nich dodać 1 ml
10% HCl, do drugiej dodać 1 ml 10% NaOH. Te same reakcje wykonać na wyciągu z buraka.
Opisać zmiany barwy roztworów w każdym z przypadków.
b)
Do 2 probówek nalać po 1 ml wyciągu z kapusty, a następniedo pierwszej probówki dodać 5
ml wody destylowanej (pH ok. 5,0), do drugiej dodać 5 ml wody wodociągowej (pH ok. 7,0)
Występuje wyraźna różnica w zabarwieniu obu roztworów.
Antocyjan czerwonej kapusty (rubrobrassycyna) jest szczególnie silnym i czułym indykatorem.
Ćwiczenie 2. Chemiczne reakcje antocyjanów
a) Reakcja z Pb(CH
3
COO)
2
Do 2 ml wyciągu z buraka i kapusty dodać po 0,5 ml nasyconego roztworu Pb(CH
3
COO)
2
.
Opisać barwy osadów.
b) Reakcja z AlCl
3
Do 5 ml wyciągu z kapusty i buraka dodać szczyptę krystalicznego AlCl
3
. Opisać zmiany barwy
roztworów.
c) Reakcja z FeCl
3
Do 2 ml wyciągu z kapusty i buraka dodać po kilka kropli 5% FeCl
3
. Opisać zmiany barwy
roztworów.

6
Ćwiczenie 3. Kwaśna hydroliza barwnika z buraka ćwikłowego
Do 5 ml wyciągu z buraka dodać 4 ml stężonego HCl i ogrzewać we wrzącej łaźni wodnej
przez 5 min. Następnie przeprowadzić 5-krotną ekstrakcję alkoholem n-amylowym (pod
dygestorium!). W tym celu do probówki należy dodać 1 ml alkoholu n-amylowego i wstrząsnąć
probówką. Po oddzieleniu się warstw należy odpipetować gruszką warstwę alkoholu (niepotrzebne).
Po ekstrakcji powinien pozostać jasno zabarwiony roztwór cukru (ekstrakcja: pozbycie się aglikonu).
Obecność cukru w roztworze wykazać znaną już ogólną reakcją na cukry. Scharakteryzować
zachodzące procesy i opisać równaniami reakcji chemicznych.
KATEDRA BIOTECHNOLOGII I BIOLOGII MOLEKULARNEJ
PRACOWNIA BIOCHEMII
BARWNIKI ANTOCYJANOWE
Imię i nazwisko:
Kierunek i rok:
Grupa: Termin zajęć:
1.
Cel ćwiczenia
2.
Obserwacje
1)
Wpływ pH na barwę barwników

7
2)
Chemiczne reakcje antocyjanów
a)
Reakcja z Pb(CH
3
COO)
2
b)
Reakcja z AlCl
3
c)
Reakcja z FeCl
3
3)
Kwaśna hydroliza barwnika z buraka ćwikłowego
3.
Reakcja chemiczna
Wyszukiwarka
Podobne podstrony:
ćw 4 Profil podłużny cieku
biofiza cw 31
Kinezyterapia ćw synergistyczne
Cw 1 ! komorki
Pedagogika ćw Dydaktyka
Cw 3 patologie wybrane aspekty
Cw 7 IMMUNOLOGIA TRANSPLANTACYJNA
Cw Ancyl strong
Cw 1 Zdrowie i choroba 2009
Rehabilitacja medyczna prezentacja ćw I
ćw 2b
Ćw 3 Elektorforeza Bzducha
ćw 3 Projektowanie drenowania
więcej podobnych podstron