
ANALIZA MIARECZKOWA
Opracowanie: dr inż. Krystyna Moskwa
Analiza miareczkowa jest klasyczną metodą analizy ilościowej. Polega ona na pomiarze objętości roztworu
o znanym stężeniu (tzw. roztworu mianowanego) zużytego do całkowitego przereagowania z substancją badaną.
Substancje te reagują ze sobą wg ściśle określonej reakcji chemicznej w ilościach równoważnikowych.
Stężenia roztworów wyraża się na kilka sposobów. W niniejszym ćwiczeniu roztwór miareczkujący
(mianowany) posiada ściśle określone stężenie molowe.
Stężenie molowe określa liczbę moli substancji zawartej 1 dm
3
roztworu tej substancji.
Podstawowym zagadnieniem w analizie miareczkowej jest określenie punktu równoważnikowego, tj punktu, w
którym przereagowały ze sobą jednakowe ilości równoważników roztworu mianowanego i substancji badanej.
Do określenia tego punktu stosuje się wskaźniki, które zmieniają swoją barwę w obecności niewielkiego nadmiaru
odczynnika miareczkującego. Zmiana pH roztworu jest gwałtowna w bezpośrednim sąsiedztwie punktu
równoważnikowego
W analizie miareczkowej mają zastosowanie dwa podstawowe typy reakcji:
1 - reakcje polegające na łączeniu się jonów
2 - reakcje podczas których zachodzi wymiana elektronów.
ALKALIMETRIA
Sprzęt: - biureta
Odczynniki:
- mianowany roztwór KOH
- kolby stożkowe -
fenoloftaleina
-
pipeta
- kolba miarowa o poj. 100 cm
3
W metodzie tej posługujemy się mianowanym roztworem zasady w celu oznaczenia ilości kwasu biorącego
udział w reakcji zobojętniania.
Wykonanie ćwiczenia.
Badany roztwór kwasu octowego CH
3
COOH przelać ilościowo do kolby miarowej o pojemności 100 cm
3
i
uzupełnić wodą destylowanądo kreski. Następnie odmierzyć pipetą 25 cm
3
badanego roztworu kwasu, przelać do
kolby stożkowej, rozcieńczyć wodą detylowaną, dodać 2 krople fenoloftaleiny. Fenoloftaleina jest bezbarwna w
roztworach kwaśnych, a więc jest bezbarwna w badanym roztworze. Badany roztwór należy zmiareczkować,
dodając kroplami mianowany roztwór KOH z biurety, aż do wystąpienia różowego-fioletowego zabarwienia.
Fenoloftaleina ma zabarwienie buraczkowe w roztworach zasadowych, a więc zabarwienie fenoloftaleiny w
badanym roztworze będzie pochodziło od kropli nadmiaru KOH po zakończonej reakcji zobojętniania. Odczytać z
biurety objętość zużytego mianowanego roztworu KOH. Próbę miareczkowania powtórzyć 2-krotnie.
ACYDYMETRIA
Sprzęt: - biureta
Odczynniki:
- mianowany roztwór HCl
- kolby stożkowe
- błękit bromotymolowy BBT
-
pipeta
- kolba miarowa o poj. 100 cm
3
W metodzie tej posługujemy się mianowanym roztworem kwasu w celu oznaczenia ilości zasady biorącej
udział w reakcji zobojętniania.
Wykonanie oznaczenia.
Badany roztwór NaOH przelać ilościowo do kolbki o pojemności 100 cm
3
i uzupełnić wodą do kreski.
Odmierzyć pipetą 25 cm
3
badanego roztworu do kolby stożkowej i dodać 2 krople BBT. Do drugiej kolbki stożkowej
wlać wodę destylowaną i 2 krople BBT. Jest to roztwór standardowy - barwa wskaźnika odpowiada pH=7. Do
badanego roztworu NaOH dodawać kroplami z biurety mianowanego roztworu HCl, aż do uzyskania barwy nieco
jaśniejszej niż w roztworze standardowym. Odczytać z biurety objętość zużytego mianowanego roztworu HCl.
Miareczkowanie wykonać 2-krotnie biorąc do obliczeń średnią wartość odczytanych objętości.
OKSYDYMETRIA
Sprzęt: - biureta
Odczynniki:
- mianowany roztwór KMnO
4
- kolby stożkowe
- 0,1 M roztwór H
2
SO
4
-
pipeta
-
kolba miarowa o poj. 100 cm
3
Jako
przykład zostanie tutaj omówione miareczkowanie manganometryczne. W metodzie tej używamy
mianowanego roztworu manganianu (VII) (nadmanganianu) potasu KMnO
4
wykorzystując jego właściwości
utleniające. Substancją oznaczaną jest roztwór soli żelaza(II), które zostaje utlenione do soli żelaza(III). Podczas
miareczkowania zachodzi następująca reakcja:

10FeSO
4
+2KMnO
4
+8H
2
SO
4
= 5Fe
2
(SO
4
)
3
+ K
2
SO
4
+ 2MnSO
4
+ 8H
2
O
Fe
2+
- 1e
→
Fe
3+
utlenianie
Mn
7+
+ 5e
→
Mn
2+
redukcja
Na skutek utleniania się jonów żelaza następuje redukcja jonów manganu z Mn
7+
, który ma zabarwienie
fioletowe do bezbarwnego Mn
2+
. Po całkowitym utlenieniu jonów żelaza dodana następna kropla KMnO
4
nie
wchodzi w reakcję chemiczną i barwi miareczkowany roztwór.
OBLICZENIA
Wykonanie oznaczenia.
Badany
roztwór,
zawierający jony Fe
2+
zakwasić 0,1 M H
2
SO
4
do pH = 4-5. Następnie przelać ilościowo do
kolby miarowej o pojemności 100 cm
3
i uzupełnić do kreski wodą destylowaną i wymieszać. Odmierzyć 25 cm
3
badanego roztworu do kolbki stożkowej i miareczkować dodając z biurety kroplami mianowany roztwór KMnO
4
, aż
do pojawienia się różowego zabarwienia roztworu badanego. Miareczkowanie wykonać 2-krotnie, biorąc do
obliczeń średnią wartość odczytanych z biurety objętości.
Obliczenia w alkalimetrii:
Na
przykład do zmiareczkowania25 cm
3
badanego roztworu kwasu octowego zużyto 5 cm
3
roztworu KOH
o stężeniu 0,1 mol/dm
3
. Podczas miareczkowania zachodzi następująca reakcja zobojętniania:
CH
3
COOH + KOH = CH
3
COOK
+ H
2
O
Jak
widać w reakcji tej 1 mol CH
3
COOH reaguje z 1 molem KOH. Obliczamy masy molowe reagentów,
przyjmując w obliczeniach masy atomowe pierwiastków zaokrąglone do jedności. Z obliczeń mamy: masa molowa
KOH = 56 g/mol, masa molowa CH
3
COOH = 60 g/mol.
Obliczamy następnie ile gramów KOH znajduje się w 5 cm
3
0,1 molowego roztworu zużytego do zmiareczkowania
kwasu octowego. Z definicji stężenia molowego roztworu wiemy, że w 1dm
3
czyli w 1000 cm
3
mianowanego
roztworu KOH znajduje się 0,1 mola czyli 5,6 grama KOH. Z prostej proporcji należy obliczyć szukaną wartość:
1000 cm
3
0,1 molowego roztworu zawiera 5,6 g KOH
5 cm
3
” ” ” ” x g KOH
x = 0,028 g KOH
Z
powyższej reakcji zobojętniania wiemy, że:
56 g KOH reaguje 60 g CH
3
COOH
0,028 g KOH ” y g CH
3
COOH
y = 0,3 g CH
3
COOH
Obliczona masa 0,3 g CH
3
COOH zawarta jest w 25 cm
3
roztworu, a więc w 1/4 badanego roztworu (całość
badanego kwasu octowego została rozcieńczona do objętości 100 cm
3
). Obliczoną masę CH
3
COOH należy
pomnożyć przez 4.
z = 0,3 g
⋅
4 = 1,2 g CH
3
COOH
W badanym zadaniu znajdowało się 1,2 g CH
3
COOH.
Można zastosowaać inną metodę w obliczeniach. Zostanie ona omówiona w następnym punkcie przy
miareczkowaniu acydymetrycznym.
Obliczenia w acydymetrii.
Jeśli do zmiareczkowania 25 cm
3
badanego roztworu NaOH zużyto na przykład 5 cm
3
mianowanego 0,1
molowego roztworu HCl, wykonać należy następujące obliczenia. Podczas miareczkowania zachodzi następująca
reakcja zobojętniania:
NaOH + HCl = NaCl + H
2
O
Z
powyższej reakcji wiemy, że 1 mol NaOH (40 g) reaguje z 1 molem HCl (36 g). Obliczamy liczbę moli
kwasu solnego zawartych w 5cm
3
0,1 molowego roztworu HCl.
1000 cm
3
roztworu zawiera 0,1 mola HCl
5cm
3
” ” x moli HCl
x = 0,0005 mola HCl
W reakcji z 0,0005 mola HCl weźmie udział 0,0005 mola NaOH. Obliczamy więc masę tej części mola
NaOH:
y = 0,0005 mol
⋅
40 g/mol = 0,02 g NaOH
Pamiętając, że do zmiareczkowania pobrano 25 cm
3
ze 100 cm
3
całości badanej próbki, wynik należy
pomnożyć przez 4.
z = 0,02g
⋅
4 = 0,08 g NaOH

Badana próbka zwierała 0,08 g NaOH
Można też zastosować omówioną już poprzednio metodę w obliczeniach. Obliczmy ile gramów HCl
znajduje się w 5 cm
3
0,1 molowego roztworu (znając df roztworu molowego oraz masę molową HCl).
1000 cm
3
roztworu zawiera 3,6 g HCl
5 cm
3
” ” x g HCl
x = 0,018 g HCl
Z
powyższej reakcji zachodzącej podczas miareczkowania wiemy, że:
36 g HCl reaguje z 40 g NaOH
0,018 g HCl ” y g NaOH
y = 0,02 g NaOH
Aby
odnieść obliczony wynik do całości badanej próbki należy pomnożyć go przez 4.
z = 0,02 g
⋅
4 = 0,08 g
Badana próbka zawierała 0,08 g NaOH.
Obliczenia w manganometrii:
Na
przykład do zmiareczkowania 25 cm
3
badanej próbki zawierającej roztwór FeSO
4
zużyto 5cm
3
0,1
molowego roztworu KMnO
4
. Obliczmy, ile moli KMnO
4
znajduje się w 5cm
3
mianowanego roztworu:
1000 cm
3
roztworu zawiera 0,1 mola KMnO
4
5cm
3
” ” x mola KMnO
4
x = 0,0005 mola KMnO
4
Z przebiegu reakcji zachodzącej podczas miareczkowania manganometrycznego wiemy, że 2 mole KMnO
4
z 10 molami FeSO
4
. Obliczmy liczbę moli FeSO
4
biorących udział w reakcji z 0,0005 molami KMnO
4
:
2 mole KMnO
4
reaguje z 10 moli FeSO
4
0,0005 moli KMnO
4
” y moli FeSO
4
y = 0,0025 mola FeSO
4
Masa molowa FeSO
4
wynosi 152g/mol, a więc masa 0,0025 mola wynosi:
z = 0,0025 mola
⋅
152 g/mol = 0,38 g FeSO
4
Pamiętając, że do zmiareczkowania pobrane zostało 25 cm
3
z całości rozcieńczonej do 100cm
3
badanej
próbki, wynik będzie czterokrotnie większy;
w = 0,38g FeSO
4
⋅
4 = 1,52 g FeSO
4
.
W badanej próbce znajdowało się 1,52 g FeSO
4
.
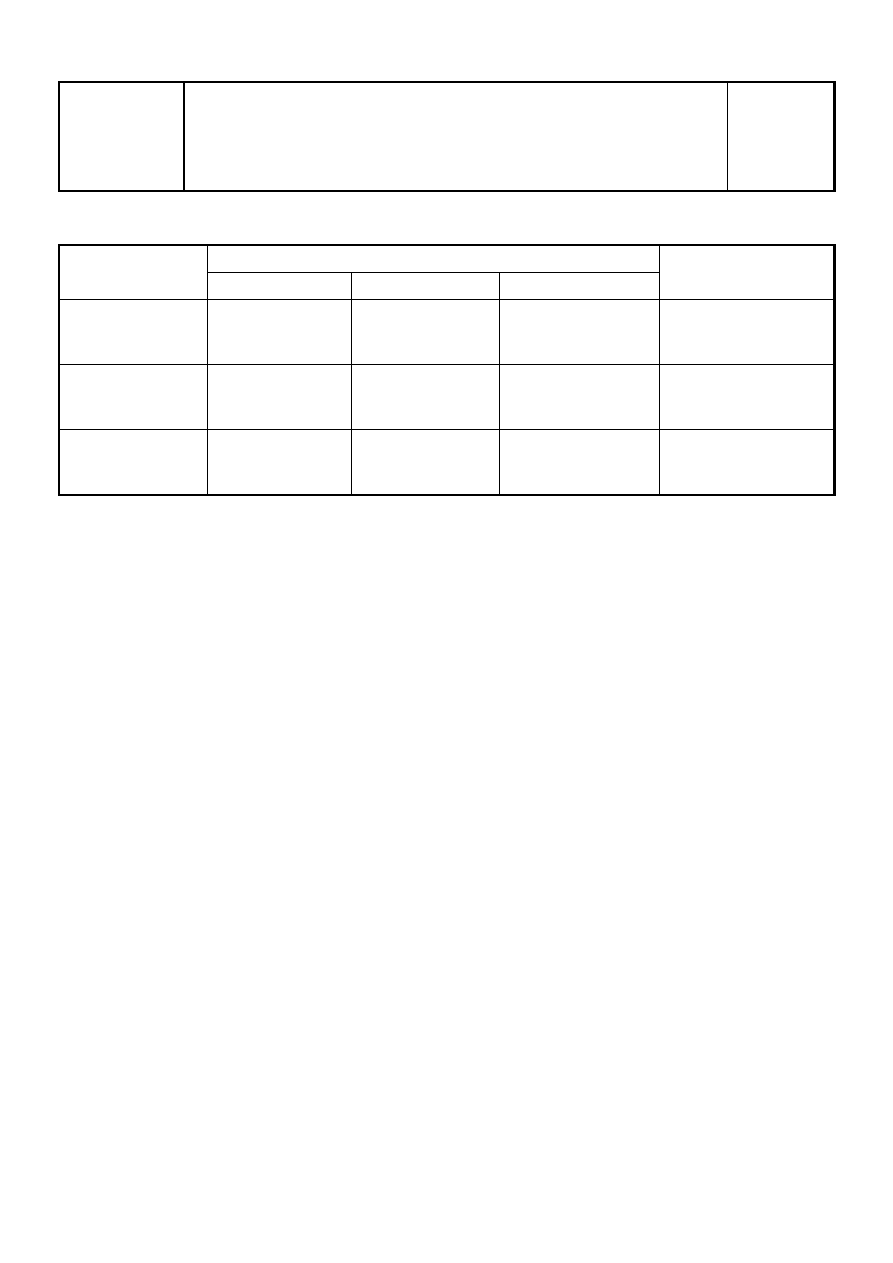
Wydz.
Gr.
Nazwisko, imię:
Temat:
ANALIZA MIARECZKOWA
Zaliczenie
objętość sustancji mianowanej [cm
3
]
V
1
V
2
V
śr
Zawartość substancji
miareczkowanej
[g]
Alkalimetria
Acydymetria
Oksydymetria
Obliczenia:
(ew. dokończyć na odwrocie strony)
Wyszukiwarka
Podobne podstrony:
Cw1 Analiza miareczkowa
ANALIZA MIARECZKOWA, Farmacja studium 2 letnie, I II semestr, analiza
CHEMIA ANALIZA MIARECZKOWA, PWR, chemia
Analiza Miareczkowa 1
Ćwiczenia z analizy miareczkowej 1
ANALIZA MIARECZKOWA. ALKACYMERIA, Biochemia, Biochemia
Ćwiczenia z analizy miareczkowej
podstawy analizy miareczkowej
ANALIZA MIARECZKOWA
Analiza miareczkowa
analiza miareczkowa2012
Analiza miareczkowa jest metodą ilościowego oznaczania substancji, Studia, Ogólne, Fiyzka, od romka,
Analiza miareczkowa, kompleksom Nieznany
sprawozdanie analiza miareczkowa 3
Cw1 Analiza miareczkowa
sprawozdanie analiza miareczkowa 2
więcej podobnych podstron