
• Zaburzenia hemostazy

Leki stosowane w
skazach
krwotocznych
•Leki działające miejscowo
•Leki działające na naczynia
krwionośne
•Leki w skazach płytkowych
•Leki w skazach osoczowych

Leki stosowane miejscowo
• Epinefryna
• Woda utleniona
• Tanina
• Trombina, gastrotrombina
• Prep. żelatynowe: spongostan
• Prep. okycelulozowe: oxycel, surgicel

Leki stosowane w skazach
naczyniowych
Leki działające na naczynia
– glikokortykosteroidy
– kwas askorbinowy
– etamsylat
– dobesylan wapnia
– rutozyd
– trokserutyna

Leki stosowane w skazach
krwotocznych płytkowych
• Glikokortykosteroidy
• Cyklofosfamid, azatiopryna
• Winkrystyna, winblastyna
• Immunoglobuliny
• Splenektomia
• Koncentraty płytek krwi

Leki stosowane w skazach
osoczowych
• Preparaty osoczowych czynników
krzepnięcia
• Wazopresyna i jej analogi
(desmopresyna,lipresyna)
• Witamina K

Leki zmniejszające krzepliwość
krwi
• Heparyny
• Doustne leki przeciwzakrzepowe
• Leki defibrynujące
• Leki hamujące czynność płytek krwi

Heparyny
•Dysponujemy obecnie dwoma
rodzajami heparyn
• Zastosowanie ma zarówno
dożylnie podawana heparyna
niefrakcjonowana (Unfractionated
Heparin, UFH)
•heparyny drobnocząsteczkowe
(Low Molecular Weight są Heparin,
LMWH)
•na polskim rynku obecnie
praktycznie 3 LMWH: dalteparyna
nadroparyna i
enoksaparyna.

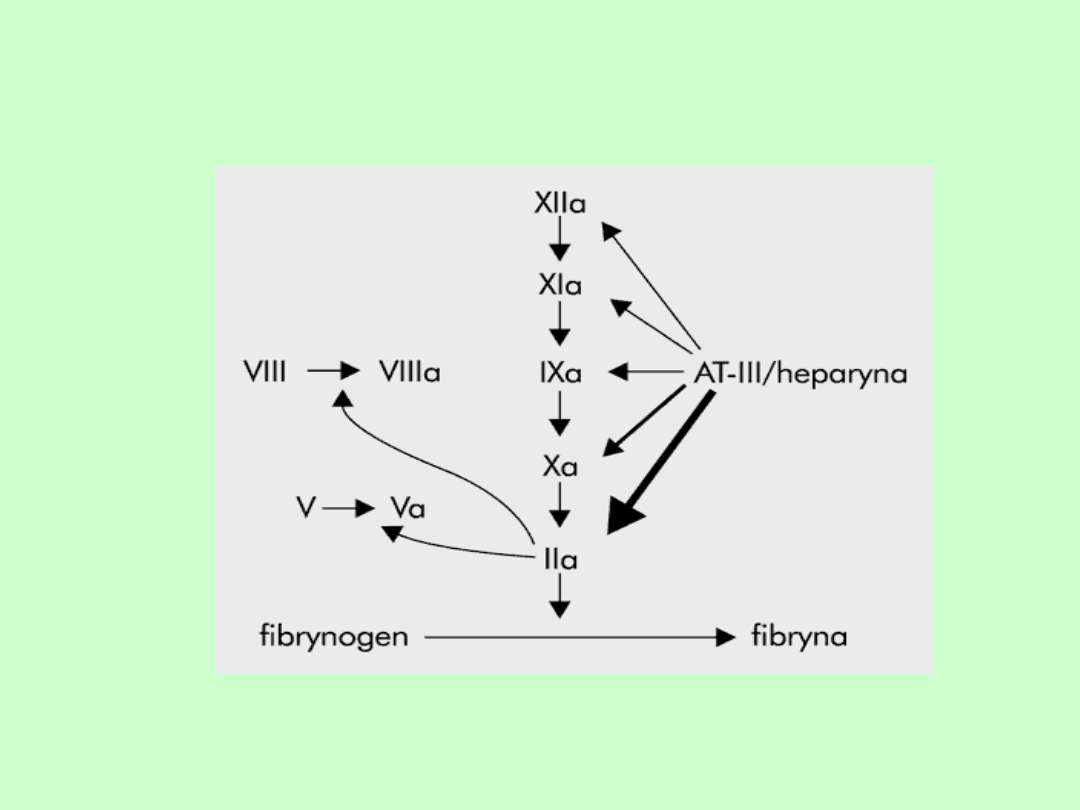
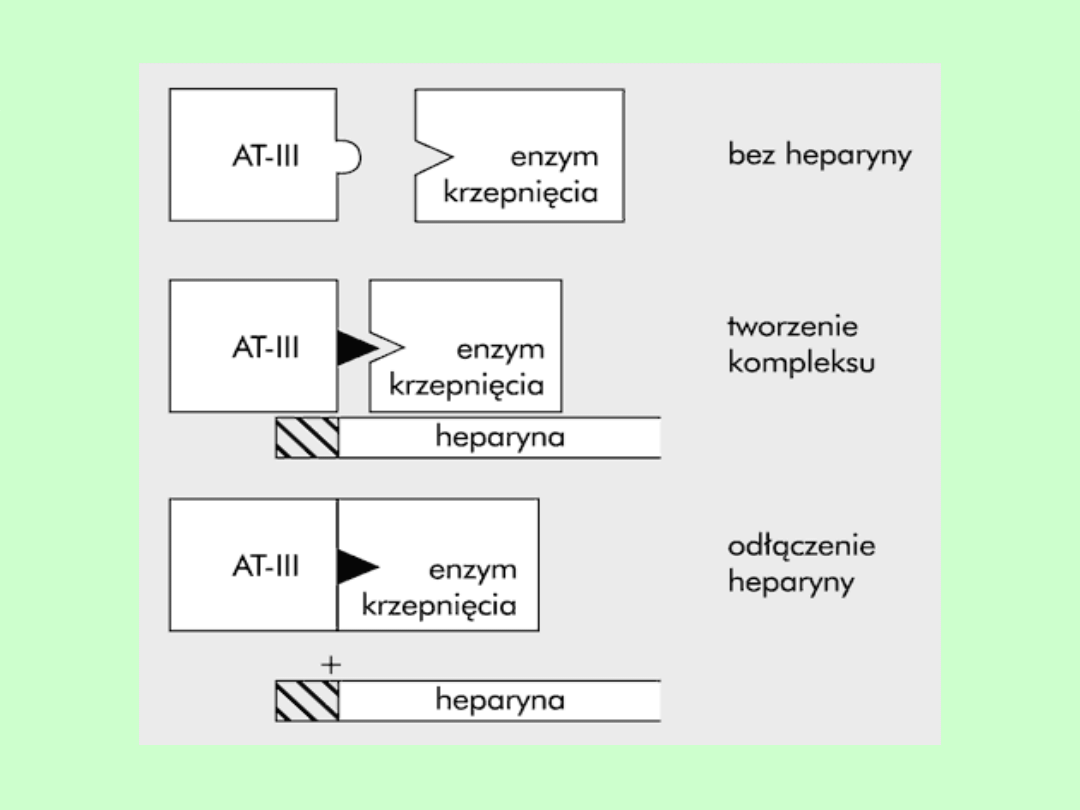
Mechanizm działania
heparyny
• wiąże się z AT-III i katalizuje inaktywację
czynników: IIa, Xa, IXa i XIIa
•

Farmakokinetyka heparyny
niefrakcjonowanej
• zalecane sposoby podawania to:
ciągły wlew dożylny i wstrzyknięcia
podskórne
• heparyna wiąże się z białkami
osocza (mała biodostępność przy
małych stężeniach)
• eliminacja
na komórkach śródbłonka i
makrofagach (ulega ona
depolimeryzacji)
wydalanie przez nerki (wolniejszy,
nieulegający wysyceniu mechanizm)

Monitorowanie laboratoryjne
•standardowym postępowaniem jest
korygowanie dawki i monitorowanie
efektu poprzez oznaczanie APTT, który
odzwierciedla hamujący wpływ
heparyny na trombinę oraz czynniki Xa
i IXa.
•powinno się oznaczać po upływie
około 6 godzin od wstrzyknięcia
dożylnego dawki nasycającej (bolus) i
na podstawie wyniku określić prędkość
ciągłego wlewu dożylnego

Przedawkowanie
heparyny
•Antykoagulacyjne działanie heparyny
(HMW) neutralizuje, wstrzyknięcie dożylne
protaminy
•Ryzyko działań niepożądanych protaminy,
hipotonia i bradykardia, można zmniejszyć,
wstrzykując lek powoli, w ciągu 1-3 minut
•Mogą wystąpić reakcje alergiczne

Oporność na heparynę
Niektórzy pacjenci wymagają
większych niż przeciętne dawek
heparyny dla odpowiedniego
przedłużenia APTT
•Oporność na heparynę jest wiązana z
niedoborem ATIII
•przyspieszoną eliminacją heparyny
•zwiększeniem stężeń białek
wiążących heparynę czynnika VIII,
fibrynogenu i czynnika płytkowego 4
(PF4).

Zastosowanie kliniczne
heparyny
•żylna choroba zakrzepowo-
zatorowa
•profilaktyka zakrzepicy żył
głębokich i zatorowości płucnej
•leczenie zakrzepicy żył głębokich
•dializa
•przetaczanie krwi

Zastosowanie kliniczne heparyny
• choroba niedokrwienna serca
• świeży zawał serca po leczeniu
trombolitycznym
• niestabilna dławica piersiowa lub
świeży zawał serca bez leczenia
trombolitycznego

Działania uboczne heparyny
tradycyjnej
• Krwawienie
• Małopłytkowość immunologiczna
(HIT) wywołana przez heparynę, która
może być przyczyną zakrzepicy żylnej
lub tętniczej
• Osteoporoza wywołana przez
heparynę

Przyjęto, że heparyna wpływa
na metabolizm kości:
•bezpośrednio hamując
czynność osteoblastów
•pobudzając czynność
osteoklastów
•obniżając stężenie
zjonizowanego wapnia w
surowicy i podwyższając
stężenie parathormonu

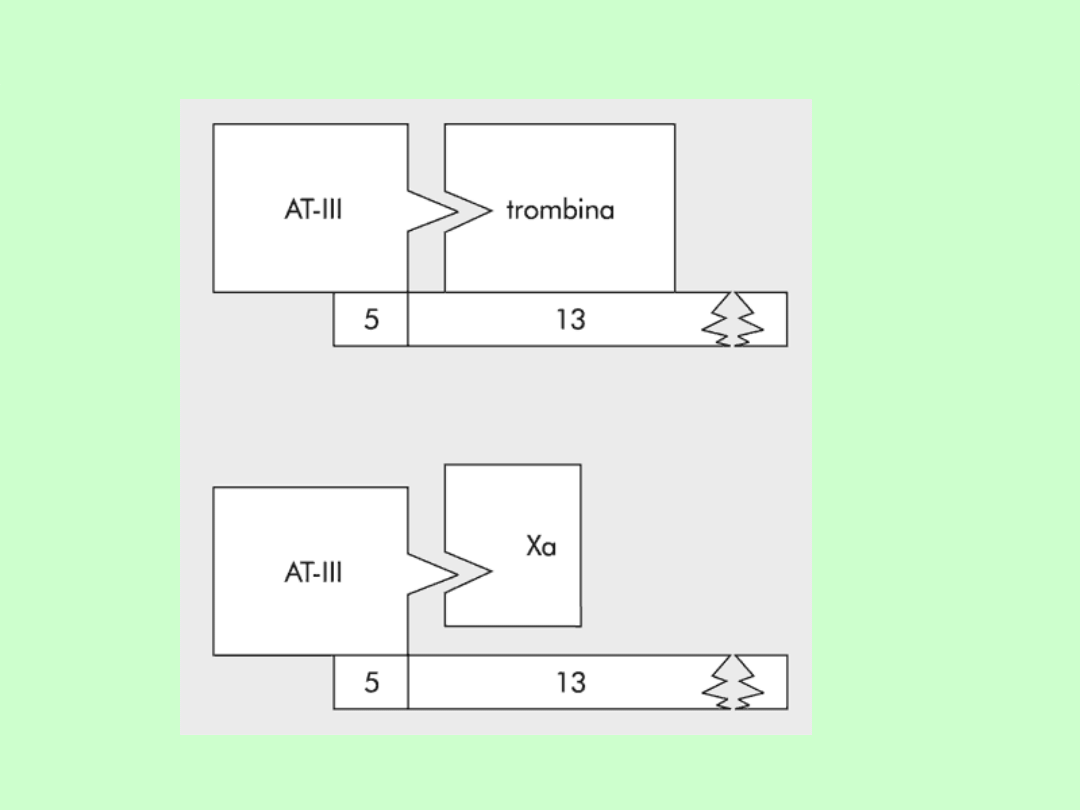
•Aby zablokować trombinę,
heparyna musi się związać
zarówno z enzymem, jak i z AT-III
•Zahamowanie czynnika Xa
wymaga jedynie związania
heparyny z AT-III przez
pentasacharyd"5"

Heparyny drobnocząsteczkowe
•powstają w procesie
depolimeryzacji heparyny
•cząsteczki mają wielkość około 1/3
cząsteczki heparyny
niefrakcjonowanej
•fragmenty te, prawie równie dobrze
jak większe cząsteczki, inaktywują
czynnik Xa,

Heparyny drobnocząsteczkowe
•charakteryzują się słabszym
wiązaniem z białkami osocza
•usuwane z ustroju głównie przez nerki
•laboratoryjne monitorowanie leczenia
LMWH zwykle nie jest konieczne

Heparyny drobnocząsteczkowe
•korzystną cechą LMWH jest łatwiejszy
do przewidzenia, w związek między
dawką a efektem antykoagulacyjnym
• daje to możliwość leczenia bez
monitorowania laboratoryjnego
• wyjątek stanowią chorzy z
niewydolnością nerek i otyłością (antyXa)

Lek
Producent/Miejsce
produkcji
Metoda syntezy
nadroparyna*
(Fraxiparin)
Sanofi/Gentilly,,
Francja
depolimeryzacja przy użyciu kwasu azotawego
enoksaparyna*
(Lovenox/ Clexane)
Aventis/Collegeville,,
PA,, USA
benzylacja,, a następnie depolimeryzacja w środowisku zasadowym
dalteparyna*
(Fragmin)
Pharmacia/Peakack,,
NJ,, USA
depolimeryzacja przy użyciu kwasu azotawego
ardeparyna
(Normiflo)
Wyeth-
Ayerst/Philadelphia,,
PA,, USA
depolimeryzacja przez utlenianie
tinzaparyna
(Innohep)
Leo
Laboratories/Dublin,,
Irlandia
enzymatyczna depolimeryzacja przy użyciu heparynazy
rewiparyna*
(Clivarine)
Knoll/Markham,,
Ontario,, Kanada
depolimeryzacja przy użyciu kwasu azotawego
danaparoid sodu
(Orgaran)
NV Organon/Oss,,
Holandia
izolowany z błony śluzowej jelita zwierzęcego; zawiera siarczan heparanu (84%),,
siarczan dermatanu (12%) i siarczan chondroityny (4%)
Heparyna stosowana w
postaci kremu ma
działanie miejscowe
przeciwzakrzepowe
(wysyca śródbłonek
naczyń i makrofagi) i
przeciwzapalne
(unieczynnia
hialuronidazę).
Stosowana w leczeniu
zakrzepowego zapalenia
żył. Leczenie blizn.

Doustne antykoagulanty
• Pochodne 4-hydroksykumaryny:
dikumarol, acenokumarol,
fenprokumor, warfaryna
• Pochodne indandionu: fenindion

Doustne antykoagulanty
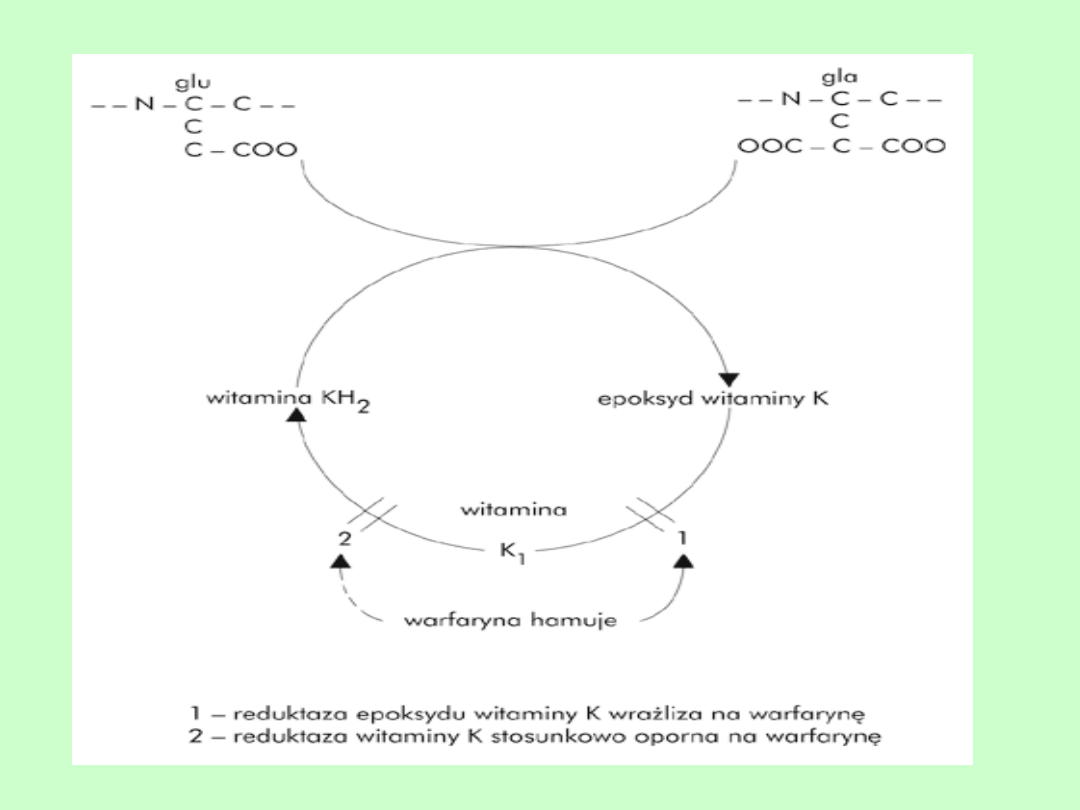
• Pochodne kumaryny są antagonistami witaminy K
• Witamina K jest kofaktorem karboksylacji reszt
kwasu glutaminowego do -karboksyglutaminowego
w czynnikach osoczowych krzepnięcia
• Efekt antykoagulacyjny pochodnych kumaryny
polega na hamowaniu cyklu przemian witaminy K
(przejście formy nieaktywnej epoksydu wit. K w
formę aktywną zredukowaną KH)
• w wątrobie powstają białka (cz. krzepnięcia) o
zmniejszonej aktywności prokoagulacyjnej (brak
zdolności wiązania Ca)

Ponadto antagoniści witaminy
K zaburzają karboksylację
białek regulatorowych - białka
C i białka S, mających
działanie antykoagulacyjne, i
dlatego mogą też wywierać
efekt prokoagulacyjny.

Kliniczne zastosowanie
doustnych antykoagulantów
•pierwotnej i wtórnej prewencji żylnej choroby
zakrzepowo-zatorowej
•w prewencji zatorów tętnic obwodowych u
chorych z migotaniem przedsionków bądź ze
sztucznymi zastawkami serca
•W prewencji zawału serca

Kliniczne zastosowanie doustnych
antykoagulantów
• W prewencji udaru mózgu,
ponownego zawału
• wskazane u chorych ze zwężeniem
mitralnym
• Dla większości wskazań powinno się
dążyć do uzyskania umiarkowanego
efektu antykoagulacyjnego (INR 2,0-
3,0).

Przedawkowanie doustnych
antykoagulantów
Jeśli INR przekracza 9,0 i nie wystąpiło
klinicznie istotne krwawienie, należy
podać doustnie witaminę K
1
U pacjentów z INR >20 i poważnym
krwawieniem należy :
•
wstrzymać leczenie warfaryną,
•
podać 10 mg witaminy K
1
w powolnym
wlewie dożylnym
•
przetoczyć świeżo mrożone osocze lub
koncentrat czynników zespołu
protrombiny

Osłabienie działania warfaryny
• barbiturany
• karbamazepina
• chlordiazepoksyd
• cholestyramina
• gryzeofulwina
• nafcylina
• ryfampicyna
• sukralfat
• pokarmy o dużej zawartości
witaminy K (duże ilości awokado)

Ciąża
Doustne antykoagulanty przechodzą
przez łożysko i mogą spowodować:
embriopatię
wady ośrodkowego układu
nerwowego
krwawienia u płodu
zwiększoną umieralność płodów

Działania uboczne
doustnych
antykoagulantów
• krwawienia
• działania teratogenne
• martwica skóry

Leki zmniejszające krzepliwość krwi
Leki defibrynujące
Ankrod batroksobina
Zawierają enzymy rozkładające
fibrynogen (powstają nieprawidłowe
monomery fibryny, łatwo trawione
przez plazminę)

Leki hamujące czynność płytek
Hamowanie agregacji płytek przez
hamowanie cyklooksygenazy
• Kwas acetylosalicylowy (1
mg/kg/d)
wskazania: świeży zawał serca,
CH.N.S., prewencja udaru mózgu

Kwas acetylosalicylowy
• Mechanizm działania
Hamowanie COX-1 co prowadzi do
zmniejszonej syntezy tromboxanu
TXA, prostacykliny
małe ilości ASA 30-70mg (nieodwracalna
inhibicja COX trwająca do końca życia
płytki, prostacyklina syntetyzowana
ponownie przez komórki śródbłonka
)

Leki hamujące czynność płytek
(poch. pirydyny)
tiklopidyna klopidogrel
Hamowanie agregacji płytek przez blokowanie
receptorów dla ADP (w konsekwencji
zmniejszona aktywacja glikoproteiny GPIIb/IIIa)
Tiklopidyna u 5%pacjentów powoduje
neutropenię
Klopidogrel działa silniej nie daje objawów
neutropeni

Leki hamujące czynność płytek
Abciximab- przeciwciała
monoklonalne
Hamowanie agregacji płytek przez
blokowanie glikoprotein płytkowych
GPIIb/IIIa

Leki wpływające na
fibrynolizę
• Leki trombolityczne
• Leki hamujące fibrynolizę

Leki trombolityczne
I generacja
• Streptokinaza
• Urokinaza
II generacja
• Tkankowy aktywator plazminogenu (t-
PA)
• Prourokinaza
• Acylowany kompleks strptokinaza-
plazminogen

SK – plazminogen
plazminogen plazmina
inaktywacja przez antyplazminę
fibrynoliza

Leki trombolityczne
Wskazania:
• Zawał serca
• Zatorowość płucna
• Zakrzepica żylna
Leczenie krótkotrwałe, kontynuacja
heparyną, antykoagulantami p.o.

Leki trombolityczne
Przeciwwskazania
• Skaza krwotoczna
• Udar mózgu
• Ciężkie nadciśnienie
• Operacja w ciągu 2-u tygodni
• Ciąża
• choroba wrzodowa
• Miesiączka
Powikłania-krwawienia (leki ham. fibrynolizę)

Stany przebiegające
ze zwiększoną fibrynolizą
• Przedawkowanie l. fibrynolitycznych
• Operacje na naczyniach, prostacie,
wątrobie, p.p.
• DIC
Postępowanie: leki hamujce
fibrynolizę

Leki hamujące fibrynolizę
• Kwas aminokapronowy
– inhibitor aktywatorów plazminogenu
– hamuje patologiczną fibrynolizę i
zwiększa stabilizację skrzepu
– p.o., i.v.
– działania niepożądane - osłabienie i bóle
mięśni, martwica mięśni, diureza
osmotyczna

Leki hamujące fibrynolizę
• Kwas traneksamowy
działa silniej i jest lepiej tolerowany

Leki hamujące fibrynolizę
• Aprotynina
hamuje fibrynolizę i układ krzepnięcia
Wskazania:
DIC z wtórnym uczynnieniem fibrynolizy
podawana i.v.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
Wyszukiwarka
Podobne podstrony:
LEKI WPLYWAJACE NA KRZEPNIECIE I HEMOSTAZE, 000-Nasze Zdrowko, Leki i Witaminy
Leki wpływające na układ autonomiczny
Leki wpływaj±ce na układ krzepnięcia
4 LEKI WPŁYWAJĄCE NA UKŁAD KRZEPNIĘCIA KRWI, Ratownictwo medyczne, Farmakologia, Farmakologia
Leki wplywajace na uklad krwiot Nieznany
Leki wpływające na układ renina
sprawdzian III Leki kardiologiczne i leki wplywajace na uklad wspolczulny
LEKI WPLYWAJACE NA KRZEPNIECIE I HEMOSTAZE
Leki wpływające na układ krwiotworczy i uklad krzepnięcia
w6 Leki wplywajace na uklad immunologiczny IIIL
Leki wpływające na układ autonomiczny, FARMACJA, FARMACJA
LEKI WPŁYWAJĄCE NA UKŁAD KOSTNY, V ROK, FARMACJA PRAKTYCZNA, osteooroza
Leki wpływaj±ce na układ krzepnięcia
LEKI WPLYWAJACE NA KRZEPNIECIE I HEMOSTAZE, 000-Nasze Zdrowko, Leki i Witaminy
więcej podobnych podstron