
Seminarium 8
Seminarium 8
Następstwa wirusowego
Następstwa wirusowego
zapalenia wątroby
zapalenia wątroby

Przewlekłe wirusowe zapalenie
Przewlekłe wirusowe zapalenie
wątroby
wątroby
wirusy pierwotnie
hepatotropowe:
HBV, HCV, HDV()
HGV, GB (A,B,C), TTV, SEN –
dyskusyjna rola w rozwoju PZW
wirusy pierwotnie nie
hepatotropowe
NIGDY
NIGDY

Epidemiologia zakażeń HBV
Epidemiologia zakażeń HBV
350 mln ludzi na świecie – przewlekłe
zakażenie HBV wg szacunków WHO
75% zakażonych to mieszkańcy Azji
> 2 miliardy ludzi ma dowody serologiczne
przebytego bądź trwającego zakażenia HBV
Ryzyko rozwoju marskości wątroby 30%
Ryzyko raka wątrobowokomórkowego 5-
10%

Epidemiologia zakażeń HBV
Epidemiologia zakażeń HBV
• Ponad 300 000 przypadków HCC rocznie
• Ponad 300 000 powikłań marskości
wątroby rocznie
(krwotok z przewodu pokarmowego,
wodobrzusze, encefalopatia)
• wg WHO ogólna śmiertelność związana
z
konsekwencjami zakażenia HBV
1 mln zgonów rocznie
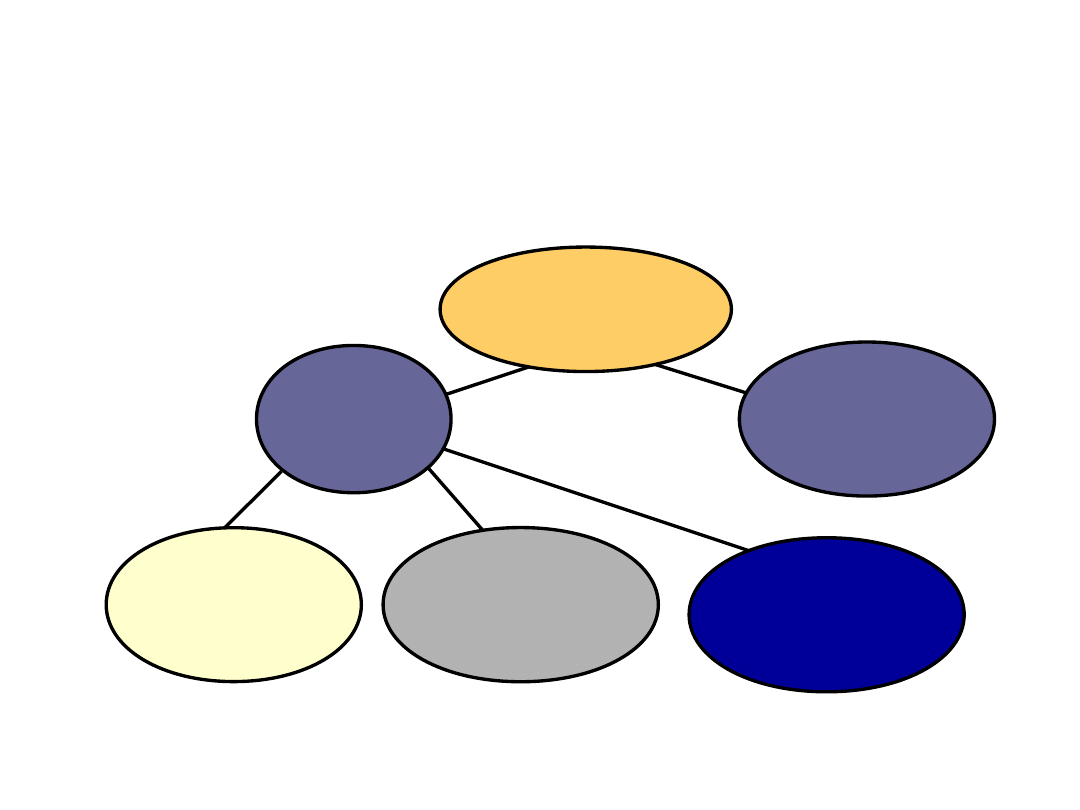
Prawdopodobne zejście PZW t.
Prawdopodobne zejście PZW t.
B HBeAg (+)
B HBeAg (+)
24% HBeAg
(-) PZW B z
wykrywalnym
HBV DNA
5%
nieokreślone
przypadki
67% trwała
remisja
Spontaniczna
serokonwersja
(n = 283)
33% wzrost
ALT
(> 2 x ULN)
4% rewersja
HBeAg

Naturalna eliminacja
Naturalna eliminacja
HBsAg
HBsAg
Występuje u ~ 0.5% nosicieli HBsAg
rocznie
Czas trwania zakażenia jako
pierwotna determinanta utraty
HBsAg
~ 50% nosicieli, u których zanika
HBsAg, ma wykrywalne HBV DNA w
surowicy w niskim mianie (1–2 log)

„
„
occult hepatitis B”
occult hepatitis B”
HBsAg (-) uj
Potwierdzona wiremia HBV
Wśród pacjentów dializowanych
większe ryzyko przy współzakażeniu
HCV
Ryzyko reaktywacji zakażenia HBV
związane z immunosupresją (np. stan
po przeszczepie) u pacjentów z
potwierdzeniem anty-HBc

Przewlekłe aktywne
Przewlekłe aktywne
zapalenie wątroby
zapalenie wątroby
HBeAg (-)
HBeAg (-)
Okresy zaostrzeń choroby i zacisza
Często agresywny przebieg choroby,
mały odsetek spontanicznych wyzdrowień
Wzrastająca częstość występowania:
~14% Płn. Europa, ~33% basen Morza
Śródziemnego
Mutacje w rejonie pre-C i promotorze
rdzeniowym wirusa HBV
Trudności w leczeniu
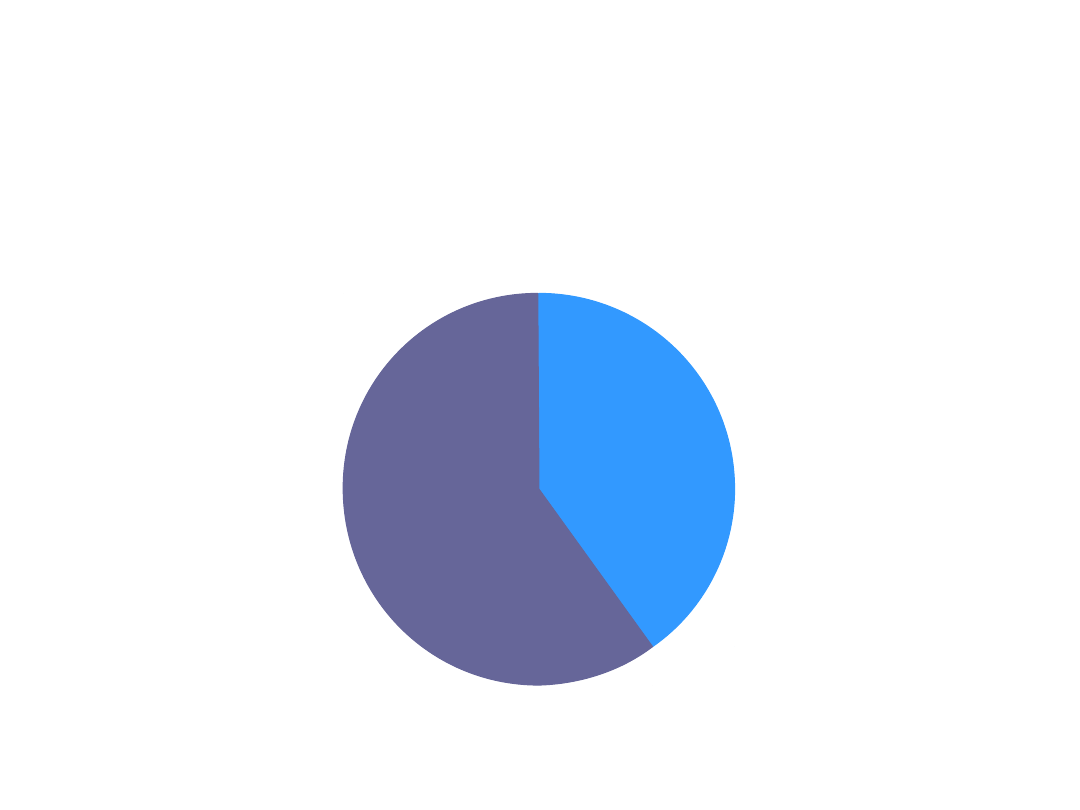
HBeAg+
60%
Przewlekłe zapalenie wątroby
Przewlekłe zapalenie wątroby
HBeAg
HBeAg
(+) i
(+) i
HBeAg
HBeAg
(-)
(-)
w USA
w USA
HBeAg-
40%

Znaczenie serokonwersji
Znaczenie serokonwersji
HBeAg
HBeAg
Dla pacjentów nie ulegających zakażeniu w
dzieciństwie (wiek młodzieńczy, dorośli – zwykle
biała rasa)
Brak postępu choroby po serokonwersji HBeAg
z HBV DNA < 10
5
kopii/mL (< 20,000 IU/mL)
Dla pacjentów ulegających zakażeniu w okresie
okołoporodowym lub we wczesnym dzieciństwie
(głównie mieszkańcy Azji)
Możliwy postęp choroby po serokonwersji HBeAg
z HBV DNA < 10
4
kopii/mL (< 2000 IU/mL)
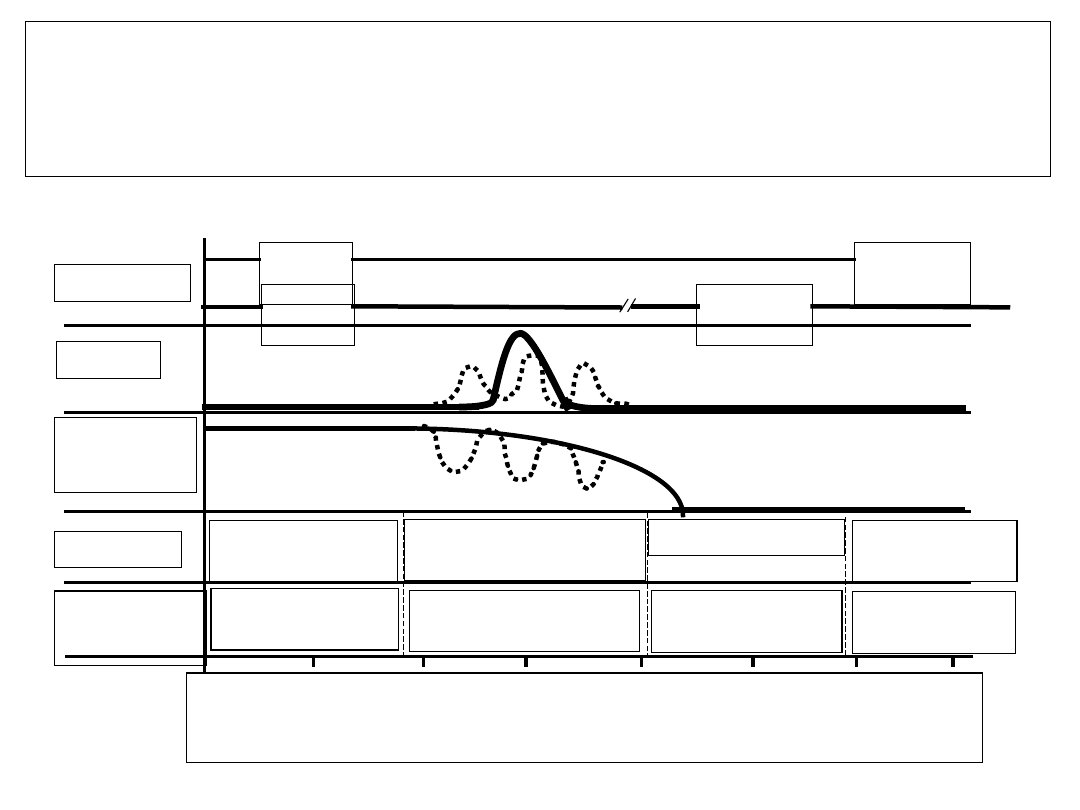
Natural
Natural
na
na
h
h
istor
istor
ia
ia
przewlekłego zakażenia
przewlekłego zakażenia
HBV
HBV
0 10 20 30 40 50 60
70
lata
Serologia
HBeA
g
anty-
HBe
ALT
HBV DNA l
(wiremia)
Choroba
Przewlekłe aktywne
zapalenie
Marskość/rak
immunotoleran
cja (faza I)
Aktywność
immunol. (faza II)
Niska replikacja
(faza III)
Faza przewl.
zakażenia
Minimalne
zapalenie
wyzdrowieni
e
normal./
marskość/rak
HBsA
g
anty-
HBs

Fazy przewlekłego
Fazy przewlekłego
zakażenia HBV
zakażenia HBV
replikacji z wykrywaniem markerów
„replikacji” (HBsAg, HBeAg, HBVDNA)
1. Tolerancja
2. Eliminacja – zaostrzenie kliniczne,
spadek ekspresji HBcAg, serokonwersja
HBeAg do anty-HBe
integracji z genomem hepatocytu
1. HBsAg (+)
2. Minimalna replikacja, możliwe wykrycie
jedynie HBVDNA; marskość, HCC

Postęp choroby i rozwój marskości wątroby
Postęp choroby i rozwój marskości wątroby
związany z natężeniem replikacji wirusa,
związany z natężeniem replikacji wirusa,
niezależny od obecności HBeAg
niezależny od obecności HBeAg
i aktywności biochemicznej aminotransferaz
i aktywności biochemicznej aminotransferaz
•
•
Skuteczne hamowanie replikacji wirusa
Skuteczne hamowanie replikacji wirusa
związane z poprawą histologiczną
związane z poprawą histologiczną
i częstością serokonwersji HBeAg/anty-HBe
i częstością serokonwersji HBeAg/anty-HBe
•Większe ryzyko rozwoju lekooporności
•Większe ryzyko rozwoju lekooporności
przy zastosowaniu leków
przy zastosowaniu leków
o średniej sile
o średniej sile
ham
ham
owania
owania
replikacj
replikacj
i
i
– ważne przy
– ważne przy
zakładanym długoterminowym leczeniu
zakładanym długoterminowym leczeniu

Inne czynniki ryzyka
Inne czynniki ryzyka
rozwoju marskości
rozwoju marskości
wątroby
wątroby
Współzakażenie HCV i HIV
Średni i starszy wiek
Płeć męska
Przebieg z częstymi
zaostrzeniami
Spożywanie alkoholu

Aktualne problemy
Aktualne problemy
leczenia PZW B i jego
leczenia PZW B i jego
następstw
następstw
Zaostrzenie choroby/ujawnienie przewlekłego
zakażenia u pacjentów leczonych z powodu
chorób nowotworowych, autoimmunologicznych,
po przeszczepach narządów
Marskość wątroby, rak wątrobowokomórkowy i
możliwości leczenia transplantacyjnego
Nieskuteczność stosowanych leków p/wirusowych
– selekcja lekoopornych mutantów wirusa
związana z progresją choroby; dostęp do nowych
leków

Kwalifikacja do leczenia
Kwalifikacja do leczenia
p/wirusowego
p/wirusowego
Aktywność aminotransferaz
Markery serologiczne: HBsAg, HBeAg
HBV DNA (IU/ml):
2,5pg/ml~700 000 kopii/ml ~125 000 IU/ml
Badanie histopatologiczne wycinka wątroby
z oceną aktywności zapalnej i włóknienia
Marskość wątroby i perspektywa leczenia
transplantacyjnego

Zasady postępowania – PZW
Zasady postępowania – PZW
B
B
bez objawów
bez objawów
dekompensacji funkcji
dekompensacji funkcji
wątroby
wątroby
HBeAg
HBV DNA
ALT leczenie
.
dodatni
<10
4
-10
5
norma
Kontrola 3-6 m-cy
dodatni
>10
4
-10
5
norma
Biopsja, ew.leczen
dodatni
>10
4
-10
5
>normy
IFN, PEG-IFN,
LAM,
inne
ujemny
<10
3
-10
4
Norma
Kontrola 3-6 m-cy
ujemny
>10
3
-10
4
Norma
Biopsja, leczenie
wieloletnie
?
ujemny
>10
3
-10
4
>normy
pegIFN, LAM,
inne

Zasady postępowania –
Zasady postępowania –
marskość wątroby
marskość wątroby
HBeAg HBV DNA IU/ml
marskość leczenie
dodatni lub
ujemny
<10
3
-10
4
wyrównana Obserwacja
lub
leczenie
LAM,
inne
dodatni lub
ujemny
>10
3
-10
4
wyrównana LAM, inne
dodatni lub
ujemny
<10
2
-10
3
niewyrównana
LAM,inne, Ltx
lub
>10
2
-10
3

Cele leczenia
Cele leczenia
p/wirusowego
p/wirusowego
Supresja replikacji HBV DNA
Normalizacja aktywności
aminotransferaz
Zmniejszenie nasilenia procesu
martwiczo-zapalnego w wątrobie
W odległej perspektywie: prewencja
marskości, niewydolności wątroby, HCC
Nie ustalono jednoznacznie jak długo
powinno się leczyć pacjenta

Leki hamujące replikację
Leki hamujące replikację
wirusa
wirusa
lek
lek
zarejestrowany
zarejestrowany
Faza 3
Faza 3
Faza 2
Faza 2
Analogi
Analogi
nukleozydó
nukleozydó
w
w
Lami
Lami
wudyna
wudyna
Entecavir
Entecavir
Cle
Cle
v
v
ud
ud
ine
ine
Emtricitabin
Emtricitabin
Telbivudine
Telbivudine
Elvucitabine
Elvucitabine
Valtorcitabin
Valtorcitabin
Amdoxovir
Amdoxovir
Racivir
Racivir
LB80380
LB80380
Analogi
Analogi
nukleotydó
nukleotydó
w
w
Adefovir dipivoxil
Adefovir dipivoxil
Tenofovir
Tenofovir
Alamifovir
Alamifovir
Pradefovir
Pradefovir
cytokiny
cytokiny
Interferon alfa
Interferon alfa
Peginterferon
Peginterferon
alfa-2a
alfa-2a

Główne czynniki związane
Główne czynniki związane
z opornością wirusa i selekcją
z opornością wirusa i selekcją
mutantów
mutantów
wirusowe
mutacje polimerazy wirusa
tworzenie dwuniciowego cccDNA o długim
czasie przetrwania w hepatocytach
hepatocytarne
długi czas przeżycia komórek zakażonych
zależne od gospodarza
leczenie p/wirusowe
odpowiedź immunologiczna
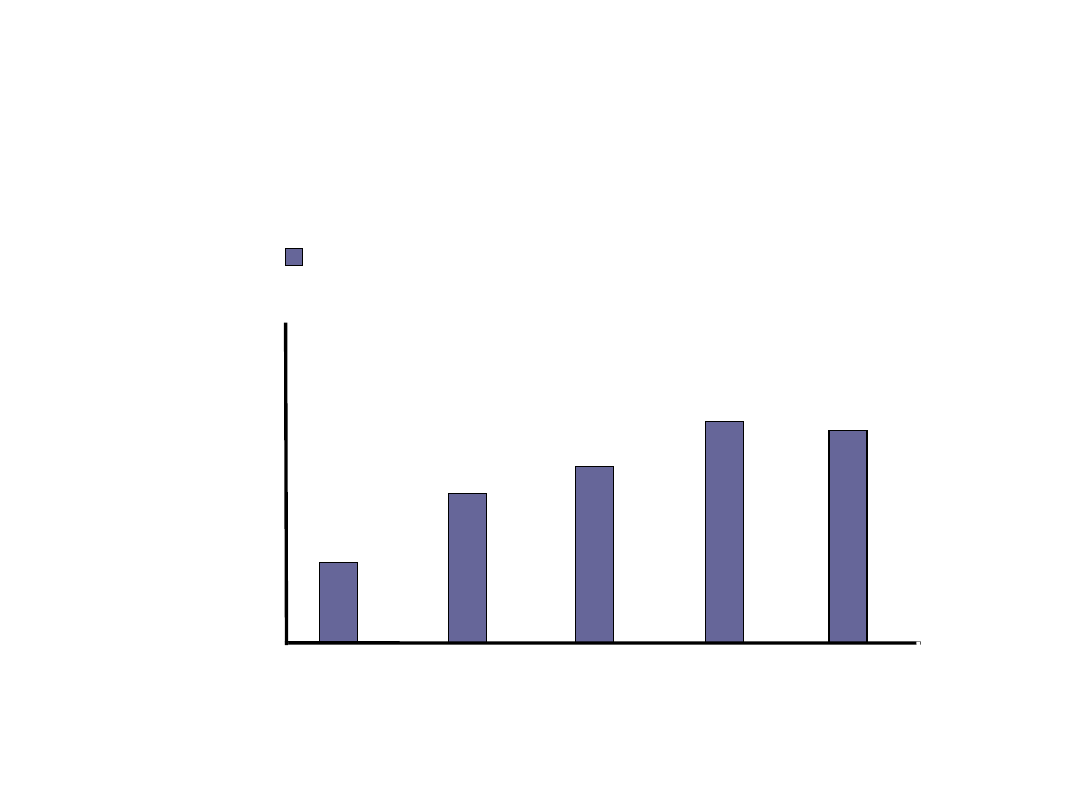
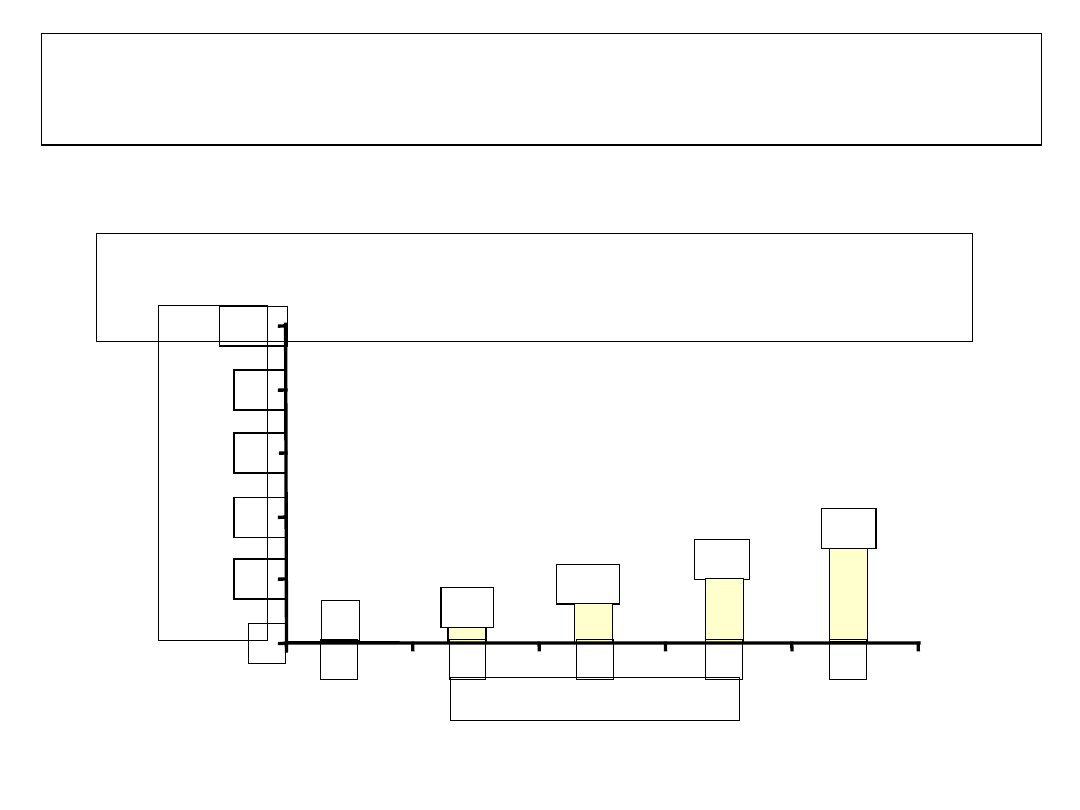
Występowanie lekooporności
Występowanie lekooporności
Lamiwudyna – pacjenci uprzednio nie
leczeni
23
55
71
65
46
rok
1
2
3
4
5
s
k
u
m
u
lo
w
a
n
a
c
z
ę
s
to
ś
ć
le
k
o
o
p
o
rn
o
ś
c
i
(%
)
0
80
40
60
20
100
Występowanie lekooporności
Występowanie lekooporności
Adefovir (pacjenci nieleczeni uprzednio analogami,
HBeAg(-))
0
3
11
18
29
rok
1
2
3
4
5
s
k
u
m
u
lo
w
a
n
a
c
z
ę
s
to
ś
ć
le
k
o
o
p
o
rn
o
ś
c
i
(%
)
0
80
40
60
20
100
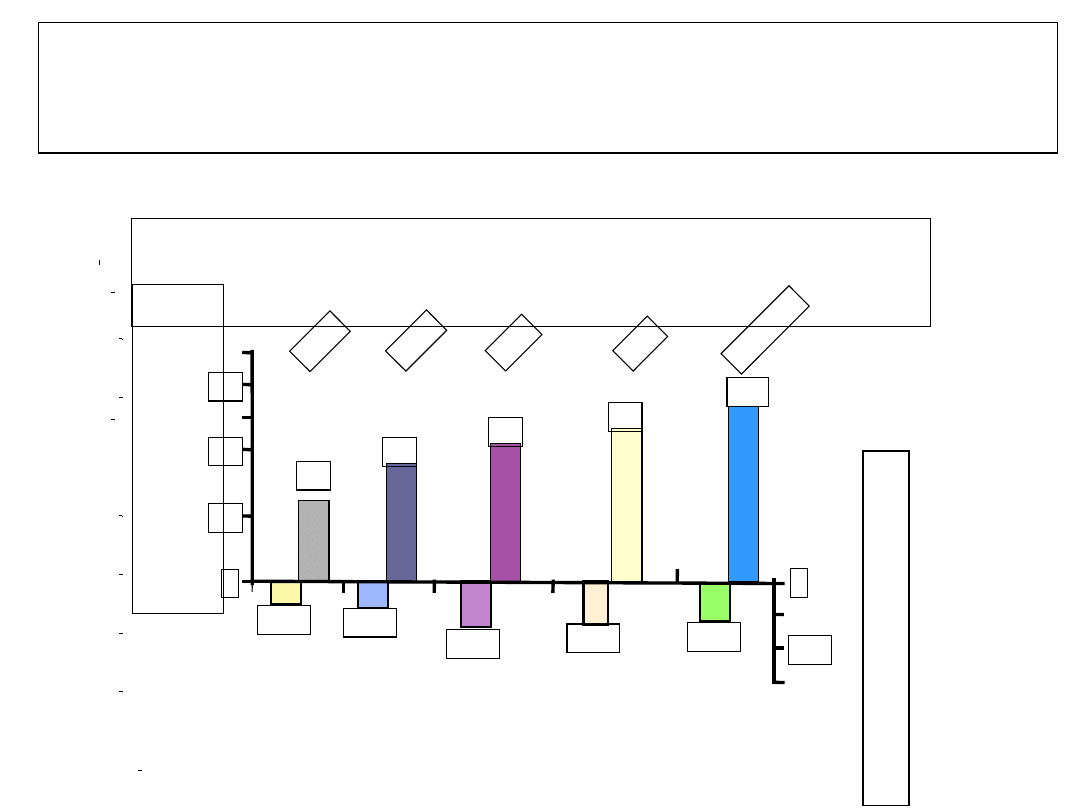
S
e
ro
k
o
n
w
e
rs
ja
H
B
e
A
g
%
S
p
a
d
e
k
H
B
V
D
N
A
L
o
g
1
0
-4.0
-3.6
-6.5
-6.9
-5.8
18
12
23
21
27
-10
0
10
20
30
LA
M
AD
V
Ld
T
ET
V
Pe
gI
FN
Dane z różnych badań różnych populacji, nie
będących bezpośrednimi porównaniami
0
HBV DNA
HBV DNA
i serokonwersja
i serokonwersja
HBeAg
HBeAg
po roku leczenia, pacjenci
po roku leczenia, pacjenci
HBeAg(+)
HBeAg(+)

Defini
Defini
cje oporności
cje oporności
Genotyp
Genotyp
owa
owa
oporność
oporność: mutacje w genomie HBV
powstające w czasie leczenia p/wirusowego
Wirusologiczny przełom
Wirusologiczny przełom
:
:
wzrost wiremii HBV
w ślad za rozwojem genotypowej opornoś
ci
ci
Kliniczny przełom
Kliniczny przełom
:
:
przełom wirusologiczny
ze wzrostem aktywności ALT lub progresją histologiczną
Fenotypowa oporność
Fenotypowa oporność
:
:
zmniejszona podatność
(badania in vitro) na inhibicję replikacji wywołaną
przez leki p/wirusowe, związaną z genotypową oporność
Krzyżowa oporność
Krzyżowa oporność: mutanty wyselekcjowane przez
jeden czynnik warunkują oporność w stosunku do innych
leków p/wirusowych

Kliniczne konsekwencje
Kliniczne konsekwencje
oporności
oporności
Utrata korzyści wynikających ze skutecznego
Utrata korzyści wynikających ze skutecznego
leczenia p/wirusowego
leczenia p/wirusowego
Zmniejszenie częstości serokonwersji HBeAg
„Pogorszenie” histologiczne
Progresja choroby
Ciężkie zaostrzenia u pacjentów z marskością wątroby
Ryzyko niepowodzenia u pacjentów po przeszczepie
wątroby
Potencjalny wpływ na zdrowie publiczne
Potencjalny wpływ na zdrowie publiczne
Transmisja szczepów lekoopornych
Mutacje HBsAg odpowiedzialne za nieskuteczność
szczepień
w 2-3% przypadków populacji szczepionej p/wzwB – występuje
mutant unikający immunologicznej odpowiedzi poszczepiennej

Selektywna
Selektywna
presja p/wirusowa
presja p/wirusowa
Związek pomiędzy natężeniem supresji
wirusa przez lek i możliwością rozwoju
lekooporności
Mała supresja→mała szansa rozwoju
lekooporności
Pełna supresja→mała szansa rozwoju
lekooporności
Idealna wielokierunkowa supresja?
Umiarkowana supresja jednokierunkowa→
duża szansa lekooporności

Monitor
Monitor
owanie
owanie
lekooporności
lekooporności
HBV DNA w surowicy jako najlepszy marker
Czuły i ten sam test PCR
Dostosowanie częstości oznaczeń do
Przebieg kliniczny
Łagodna choroba wątroby: badanie co 6 miesięcy
Choroba zaawansowana / marskość: kontrola co 3
miesiące
Profil lekooporności
Leczenie adefowirem lub entekawirem stwarza
możliwość rzadszego oznaczania wiremii w
porównaniu z lamiwudyną

1. Interferony
1. Interferony
Interferon alfa (Intron A, Roferon)
stosowanie 6 miesięcy; u 40%
pacjentów HBeAg (+) serokonwersja do
anty-HBe, często nietrwała
Interferon pegylowany alfa2a (40kD)
(Pegasys) – wyższa skuteczność
Wada – liczne objawy uboczne

2. Lamiwudyna (Zeffix)
2. Lamiwudyna (Zeffix)
Analog nukleozydu, inhibitor odwrotnej
transkryptazy HBV
Po 12 miesiącach stosowania u pacjentów
HBeAg (+) serokonwersja do anty-HBe
Mutanty lekooporne; możliwość powstania
już po 6 miesiącach terapii; do 20% rocznie
Dobra tolerancja

2. Lamiwudyna (Zeffix)
2. Lamiwudyna (Zeffix)
Mutanty regionu C genu polimerazy YMDD –
M204V/I/S powstają pod presją stosowania
lamiwudyny, telbivudyny, emtricitabiny oraz
entecawiru
Wolniejsze tempo replikacji w porównaniu ze
szczepem dzikim; efekt zwolnienia znoszony
przez często występujące jako dodatkowe
mutacje genu polimerazy L180M i V173L
oraz mutacje w rejonie pre-core G1896A

3. Adefowir (Hepsera)
3. Adefowir (Hepsera)
Analog nukleotydu adeniny
Wrażliwość dzikich szczepów HBV i mutantów
opornych na lamiwudynę w tym YMDD
Średni spadek wiremii o 3,4 log kopii/ml po 96
tyg.
Wolny rozwój lekooporności – do 2% po 96
tyg leczenia; N263T w genie polimerazy
nefrotoksyczność (pacjenci dializowani –
10mg [1 tabl] co 7 dni)

4. Entecawir (Baraclude)
4. Entecawir (Baraclude)
Analog nukleozydowy, selektywny inhibitor
odwrotnej transkryptazy HBV DNA
Najsilniejsze hamowanie replikacji wirusa
(supresja HBV DNA o blisko 7 log kopii/ml u
pacjentów wcześniej nieleczonych
wirostatykami)
Wyższe dawkowanie u pacjentów wcześniej
leczonych lamiwudyną z uwagi na możliwą
krzyżową oporność (1,0mg vs 0,5mg)

4. Entecawir (Baraclude)
4. Entecawir (Baraclude)
Nie obserwowano lekooporności po 96 tyg.
leczenia u pacjentów wcześniej nie
leczonych analogami nukleozydów
7% genotypowej oporności po 48 tyg
leczenia w przypadku lamiwudynooporności
Profil tolerancji porównywalny z profilem
lamiwudyny
Konieczność dostosowania dawki leku do
niewydolności nerek (dializowani 1tabl/tyg.)
Wybór leku I rzutu – jako
Wybór leku I rzutu – jako
strategia ochrony przed
strategia ochrony przed
lekoopornością
lekoopornością
Pacjenci z wyrównaną
chorobą wątroby
Monoterapia
ADV
–
LAM – ETV
–
PegIFN
Jeśli db profil odpowiedzi
stosować PegIFN
Jeśli w planie
długoterminowa terapia
rozważyć ADV / ETV
Pacjenci z marskością,
zdekompensowaną
chorobą wątroby,
oczekujący na Ltx
Terapia
kombinowana
Analogi nukleotydów
+
Analogi nukleozydów

Skrining HCC z PZW t. B -
Skrining HCC z PZW t. B -
brak jednoznacznych
brak jednoznacznych
wytycznych
wytycznych
W jakim wieku wdrażać badania
skriningowe?
U pacjentów zakażonych HBV HCC
może wystąpić w każdym wieku, także
w dzieciństwie
Nie ustalono jaki wiek jest optymalny
Większe ryzyko HCC u pacjentów ≥ 35
lat

Skrining HCC u pacjentów
Skrining HCC u pacjentów
z PZW t. B
z PZW t. B
U ponad 1/3 pacjentów z HCC AFP jest w
normie
AFP może być podwyższone u 1/3 pacjentów
z rozpoznaniem marskości bez obecności
HCC
Bardzo wysoka wartość AFP (> 1000 ng/mL)
jest diagnostyczna dla HCC
Rosnące wartości AFP mogą sugerować
HCC, ale nie jest to często obserwowane

Skrining HCC u pacjentów
Skrining HCC u pacjentów
z PZW t. B
z PZW t. B
Wysokie ryzyko
Wysokie ryzyko
-
-
AFP + USG co 6 miesięcy
marskość
rodzinne występowanie HCC
Średnie ryzyko
Średnie ryzyko
-
-
AFP + USG co 12 miesięcy
wiek > 30 - 40 lat
aktywna choroba (ALT ↑↑↑)
Jeśli AFP rośnie lub > 20 ng/ml, spiralne TK lub
MRI
Pozawątrobowe
Pozawątrobowe
manifestacje zakażenia
manifestacje zakażenia
HBV
HBV
Guzkowe zapalenie tętnic
(periarteritis nodosa)
Kłębuszkowe zapalenie nerek (błoniaste,
rozplemowo-błoniaste, rozplemowo-mezangialne)
Polimialgia reumatyczna
Krioglobulinemia mieszana – rzadziej niż w HCV
Zespół Guillain-Barre – opisy w literaturze
Zapalenie mięśnia sercowego – j.w.
Zespół Gianotti-Crosti – j.w.

Przewlekłe wirusowe
Przewlekłe wirusowe
zapalenie wątroby typu
zapalenie wątroby typu
B i D
B i D
Częstość zakażenia HDV wśród zakażonych
HBV ~ 5%
Trudności w rozpoznaniu (anty-delta, HDV
RNA)
Przebieg z szybką progresją, często z niską
lub niewykrywalną wiremią HBV; HBsAg +/- →
pułapka diagnostyczna
Możliwy przebieg z gwałtownym zaostrzeniem
PZW B – superinfekcja HDV
Leczenie PEG-IFN
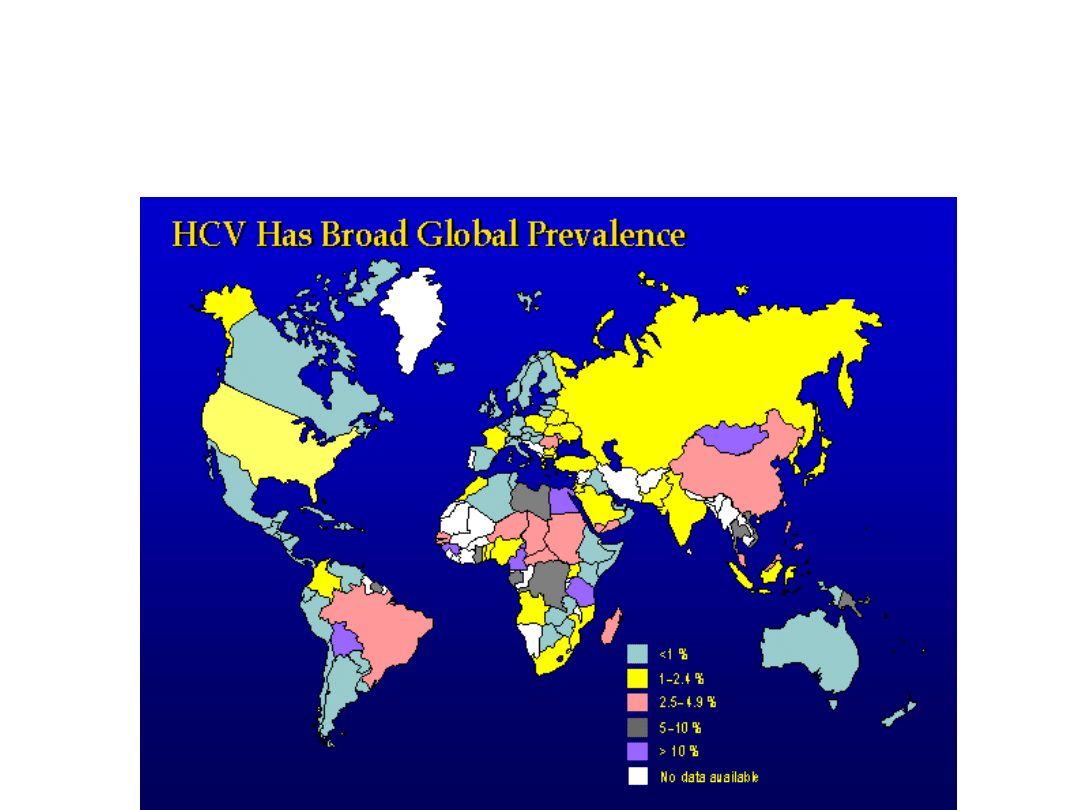
Występowanie zakażenia HCV
Występowanie zakażenia HCV
na świecie
na świecie

Przewlekłe WZW t. C –
Przewlekłe WZW t. C –
grupy ryzyka
grupy ryzyka
Transfuzje krwi przed 1992
IVDU oraz donosowe inhalacje kokainy
Przewlekła dializoterapia
Więzienia
Pracownicy służby zdrowia
Biorcy narządów, tkanek
Tatuowanie i „kolczykowanie”
Ryzykowne kontakty seksualne
Kontakty rodzinne z osobą HCV (+)
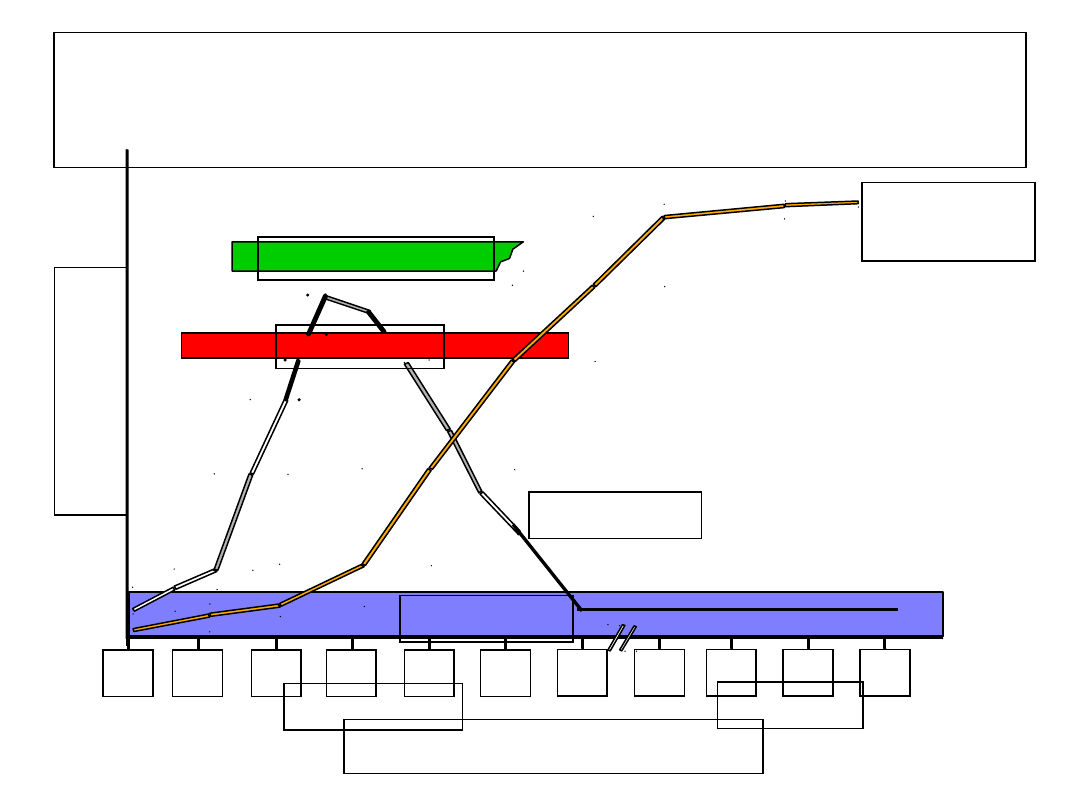
Przebieg ostrego WZW z
Przebieg ostrego WZW z
wyzdrowieniem
wyzdrowieniem
Objawy +/-
Czas od zakażenia
M
ia
n
o
p
rz
e
ci
w
ci
a
ł
anty-
HCV
ALAT
Norma
0
1
2
3
4
5
6
1
2
3
4
Lata
Miesiące
HCV RNA
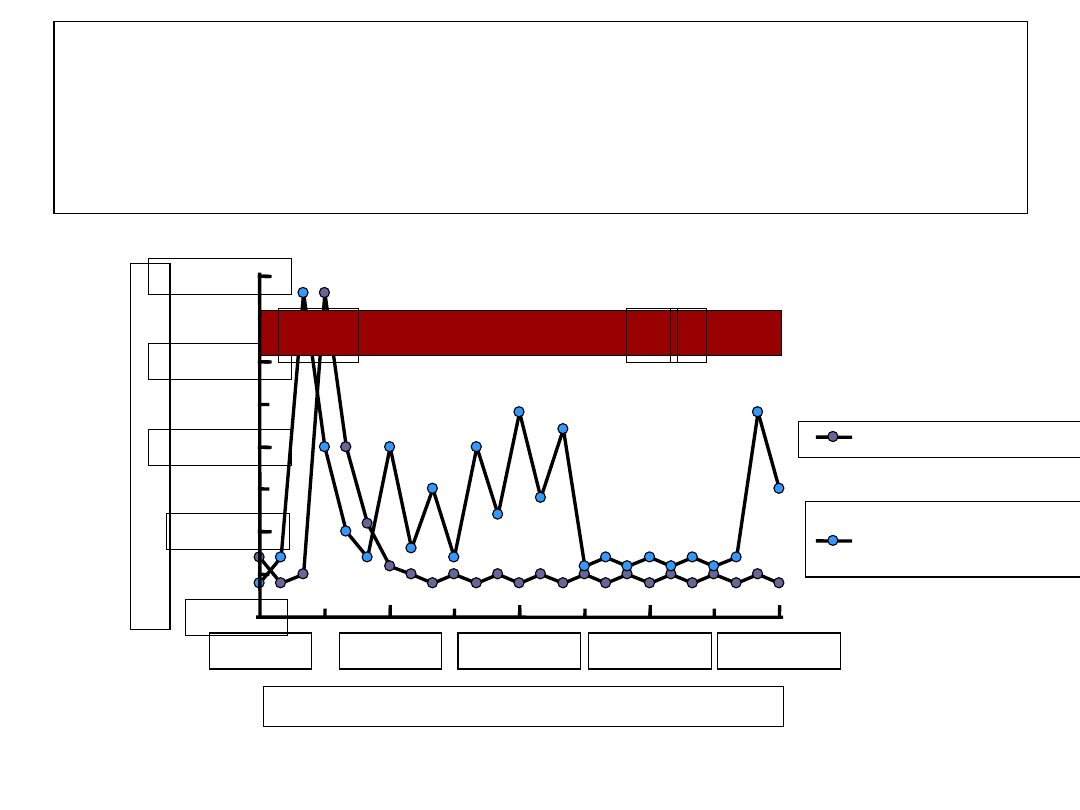
0
50
100
150
200
0
6
12
18
24
Miesiące
A
LT
(
IU
/l
)
Wyzdrowienie
Przewlekłe
Zakażenie HCV
HCV RNA
+/-
+ -
Przewlekłe wirusowe
Przewlekłe wirusowe
zapalenie wątroby H
zapalenie wątroby H
C
C
V
V

Autoimmunologiczna reakcja w wątrobie
Krioglobulinemia mieszana
Glomerulonephritis
Porphyria cutanea tarda (PCT)
Leukocytoclastic vasculitis
Mooren’s corneal ulcer
Non-Hodgkin’s lymphoma
Autoimmunologiczne zapalenie tarczycy
Cukrzyca t. 1
Zespół Sjögren’a
Przewlekłe WZW HCV:
pozawątrobowe manifestacje
choroby

PZW
PZW
H
H
C
C
V
V
a
a
uto
uto
-przeciwciała
-przeciwciała
HCV
HCV
(+)
(+)
, %
, %
HCV
HCV
(-)
(-)
, %
, %
Czynnik reumatyczny
Czynnik reumatyczny
70
70
8
8
Krioglobuliny
Krioglobuliny
36
36
< 1
< 1
ANA
ANA
> 1:40
> 1:40
> 1:180
> 1:180
21
21
13
13
10
10
2
2
SMA
SMA
> 1:40
> 1:40
> 1:180
> 1:180
21
21
7
7
2
2
< 1
< 1
LKM
LKM
5
5
< 1
< 1
Antithyroid
Antithyroid
7
7
2
2

PZW
PZW
H
H
C
C
V
V
a
a
uto
uto
-
-
przeciwciała
przeciwciała
Brak związku obecności autoprzeciwciał z:
Ciężkością PZW t.C
Genotypem HCV
Związek pomiędzy mianem RF a:
Krioglobulinemią
Ale nie bezobjawową krioglobulinemią
Autoprzeciwciała w surowicy mogą być
powodem fałszywie dodatnich anty-HCV
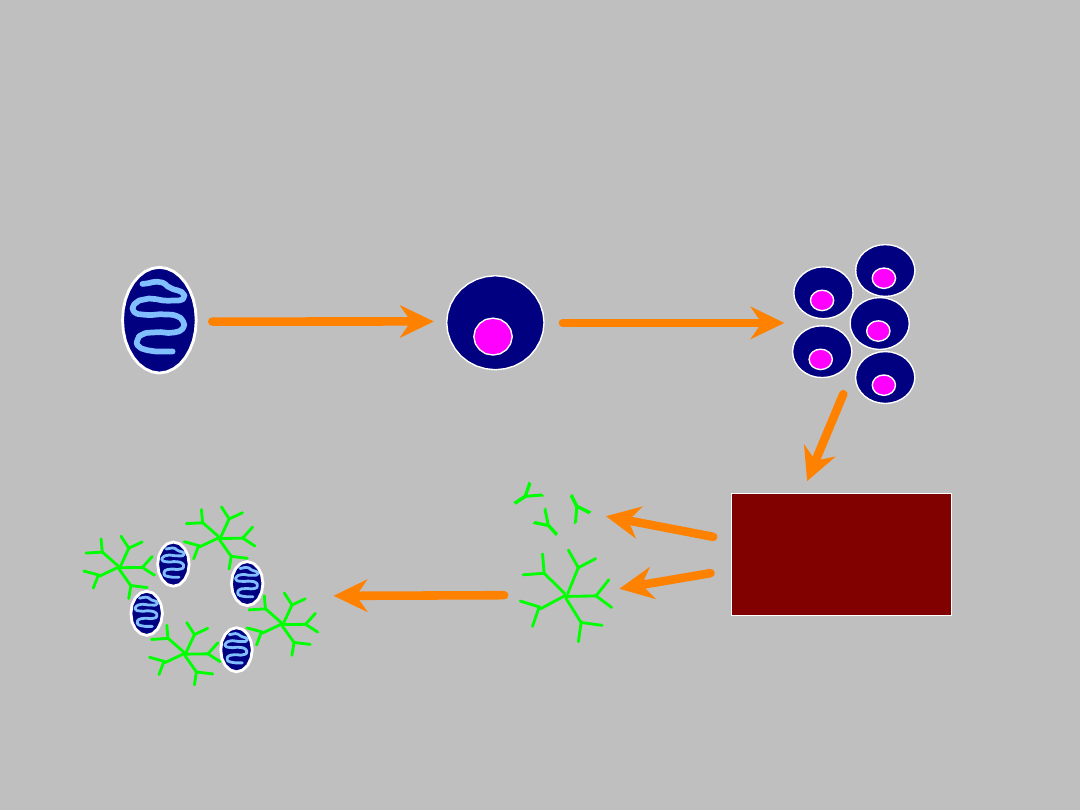
Patogeneza manifestacji
Patogeneza manifestacji
immunologicznej zakażenia
immunologicznej zakażenia
HCV
HCV
Monoclonal IgM
rheumatoid factor
Cryoglobulin
traps HCV
HCV evades the
immune response
Chronic immune
stimulation by
single HCV antigen
Polyclonal IgG
Y
Genetic and
environmental
factors

Zakażenie
Zakażenie
HCV
HCV
a
a
k
k
r
r
i
i
oglobulinemia
oglobulinemia
-
-
Dermatitis
Dermatitis
Występowanie w
typowych miejscach
Depozyty
krioglobulin w
małych naczyniach
Możliwość rozwoju
owrzodzeń
Świąd

Manifestacja
Manifestacja
krioglobulinemii
krioglobulinemii
i HCV
i HCV
Dermatitis
Vasculitis
Bóle mięśniowe (fibromyalgia?)
Bóle stawowe (RA i/lub ANA plus)
Błoniasto-rozplemowe zapalenie
kłębków
Neuropatia
Zespół przewlekłego zmęczenia (?)

Charakterysty
Charakterysty
ka
ka
HCV
HCV
Sialadenitis
Sialadenitis
Pierwotny
Pierwotny
zespół
zespół
Sj
Sj
ö
ö
gren’
gren’
a
a
SS-A, SS-B
SS-A, SS-B
nieobecny
nieobecny
obecne
obecne
Lymphocytic
Lymphocytic
capillaritis
capillaritis
łagodny
łagodny
około-
około-
naczyniowo
naczyniowo
głównie
głównie
CD
CD
8
8
nasilone
nasilone
około-przewodowo
około-przewodowo
głównie
głównie
CD
CD
4
4
Sicca syndrome:
Sicca syndrome:
Xerophthalmia
Xerophthalmia
Xerostomia
Xerostomia
nieobecny
nieobecny
8%-36%
8%-36%
obecny
obecny
obecny
obecny
Pozawątrobowa manifestacja
Pozawątrobowa manifestacja
zakażenia
zakażenia
HCV
HCV
-
-
Lymphocytic
Lymphocytic
Sialadenitis
Sialadenitis
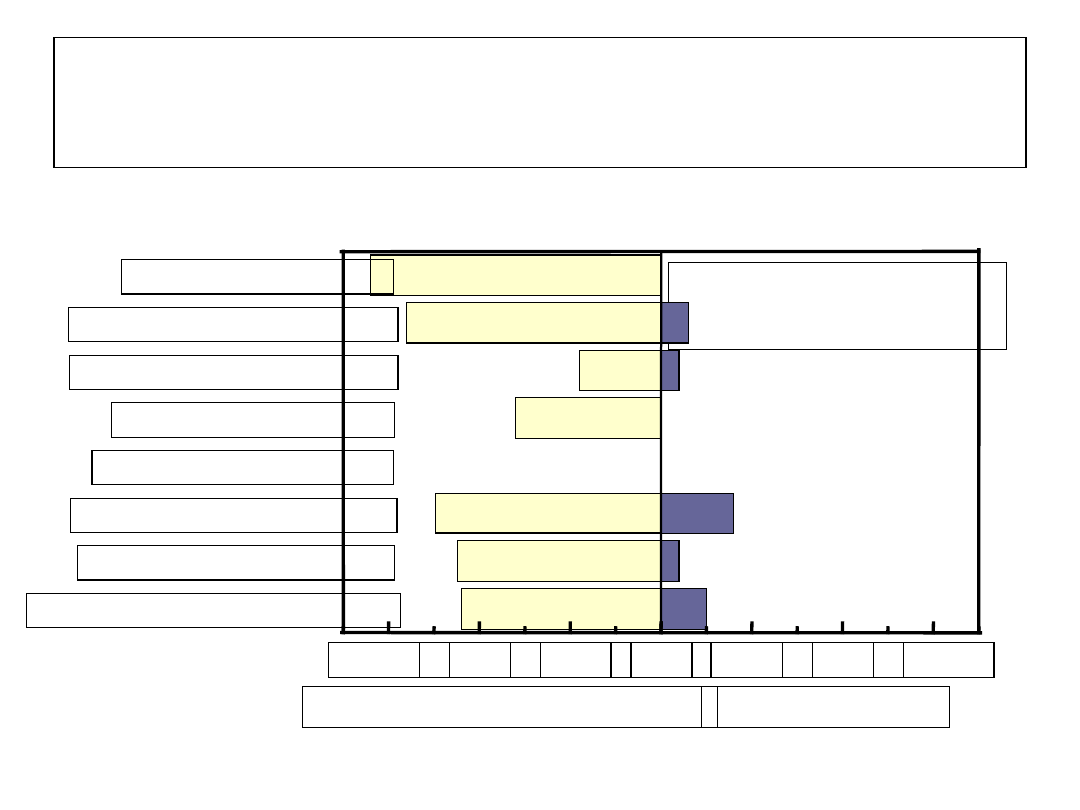
Pozawątrobowa manifestacja
Pozawątrobowa manifestacja
zakażenia
zakażenia
HCV
HCV
-
-
B-Cell
B-Cell
Lymphoma
Lymphoma
8 badań, 1754 pts
włączonych
Ferri (1994)
Mazzaro (1996)
Silvestri (1996)
Izumi (1996)
McColl (1996)
Zignego (1997)
DeRosa (1997)
Zuckerman (1997)
0
10
20
30
B Cell Lymphoma
0
10
20
30
Kontrola
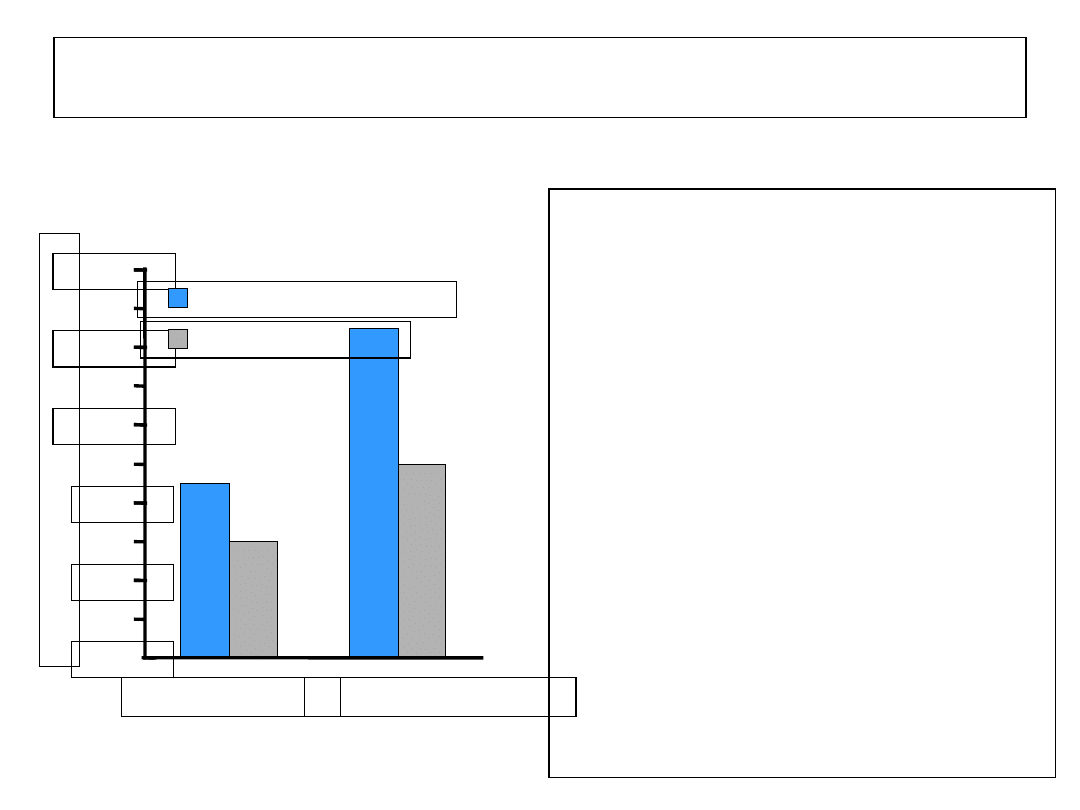
PZW
PZW
t.
t.
C
C
i
i
cukrzyca
cukrzyca
N = 179 z PZW t.C
Oceniono występowanie
DM i insulinooporności
Porównano z danymi z
bazy NHANES III badanie
po uwzględnieniu
zmiennej:
wiek
płeć
rasa
Występowanie DM lub IR
było wyższe u pacjentów
z PZW. T. C
0
4
8
12
16
20
kobiety
mężczyźni
L
ic
z
b
a
p
rz
y
p
a
d
k
ó
w
Obserwowane
Podejrzane
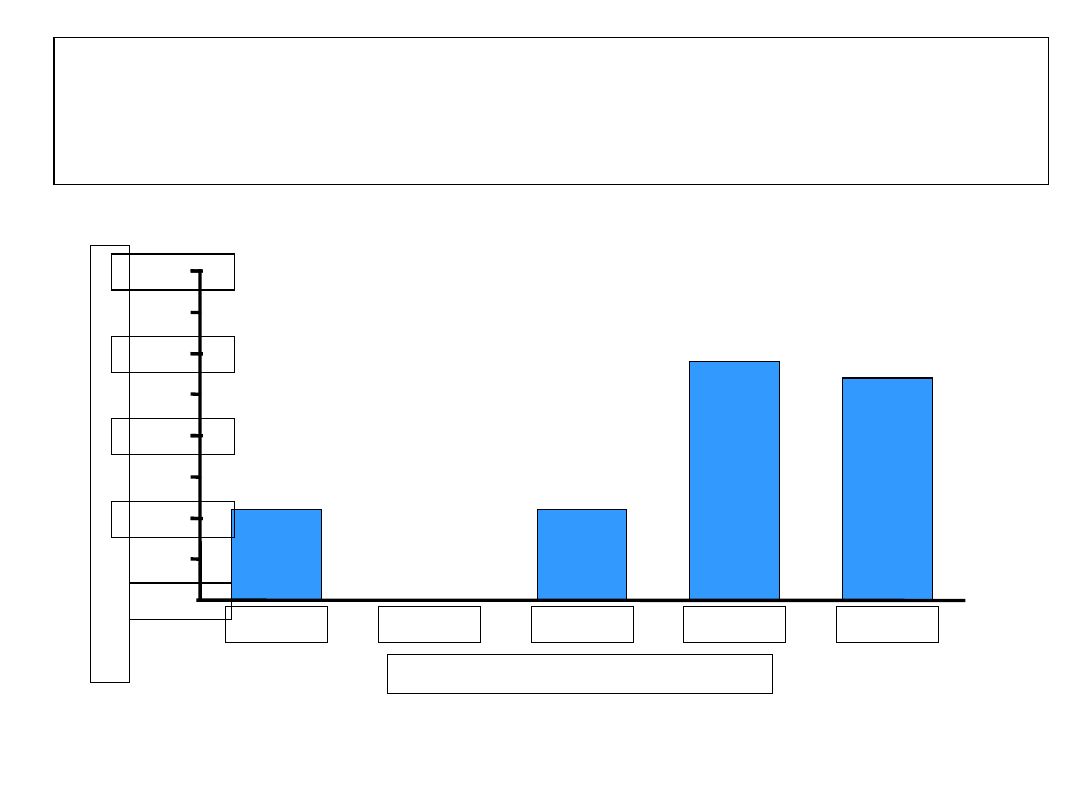
PZW
PZW
t.
t.
C
C
i
i
cukrzyca
cukrzyca
w relacji
w relacji
do
do
stopnia włóknienia
stopnia włóknienia
wątroby
wątroby
0
10
20
30
40
0
1
2
3
4
Histologic Stage
O
d
s
e
te
k
p
a
c
je
n
tó
w
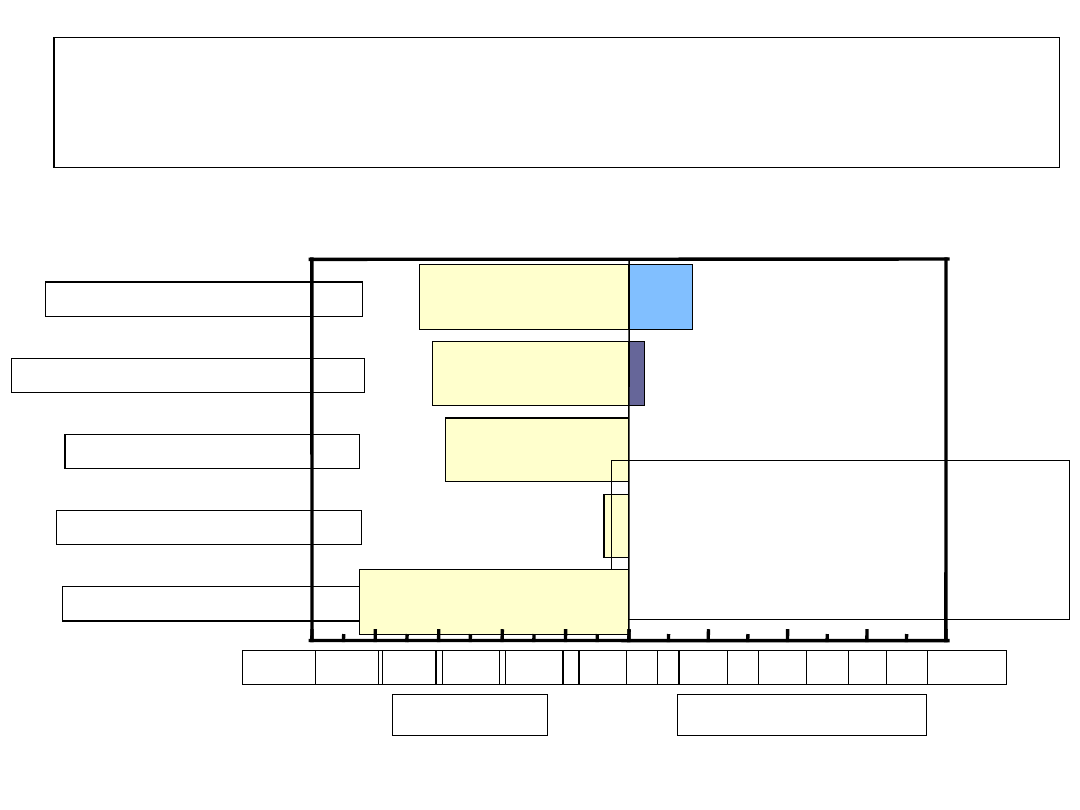
Pozawątrobowa manifestacja
Pozawątrobowa manifestacja
zakażenia
zakażenia
HCV
HCV
-
-
Porphyria Cutanea
Porphyria Cutanea
Tarda
Tarda
2 case series
3 niekontrolowane badania
280 pacjentów
Alkohol: 36%-77%
Fargion (1992)
De Castro (1993)
Criber (1995)
Stolzel (1995)
Kondo (1997)
0
20
40
60
80
100
PCT
0
5
10
15
20
Kontrola

Pozawątrobowa
Pozawątrobowa
manifestacja zakażenia
manifestacja zakażenia
HCV
HCV
-
-
Lichen Planus
Lichen Planus
Występuje u < 1% populacji ogólnej
U 10%-30% pacjentów z PZW t. C
Lokalizacja
Płasko-wyniosłe, fioletowawe, swędzące
grudki
W zagłębieniach ciała
Śluzówka jamy ustnej
Histologia
Gęste nacieki limfocytów T skóry właściwej
Kwalifikacja do leczenia PZW
Kwalifikacja do leczenia PZW
t. C
t. C
Ciężkość choroby
Ciężkość choroby
Odpowiedź na
Odpowiedź na
leczenie
leczenie
AST/ALT
AST/ALT
Bilirubin
Bilirubin
a
a
Albumin
Albumin
a
a
Pro-time (INR)
Pro-time (INR)
Liczba płytek
Liczba płytek
Histopatologia
Histopatologia
wątroby
wątroby
ALT
ALT
HCV RNA
HCV RNA
HCV genotype
HCV genotype
Histopatologia
Histopatologia
wątroby
wątroby
LFTs
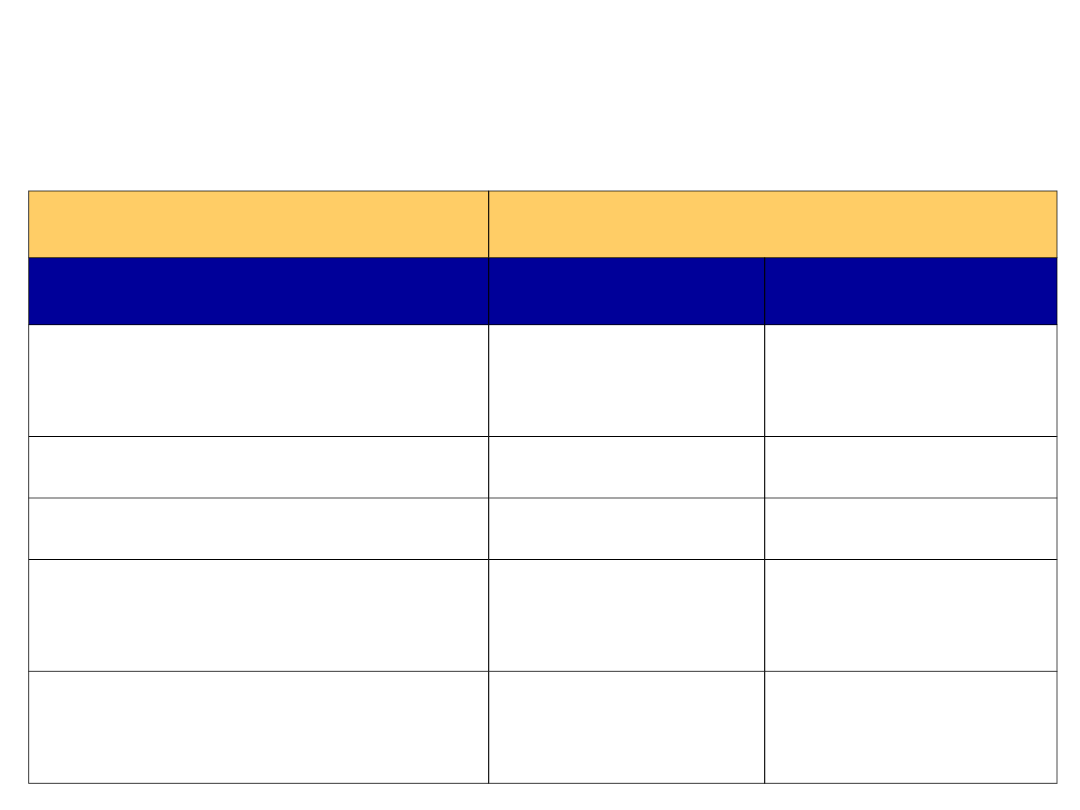
HCV – testy diagnostyczne
HCV – testy diagnostyczne
Typ testu
Typ testu
Charakterystyka
Charakterystyka
Serologia
Serologia
Wiremia
Wiremia
Rodzaj detekcji
Rodzaj detekcji
Przeciwciał
Przeciwciał
a
a
Wirus
Wirus
Czułość
Czułość
> 95%
> 95%
> 98%
> 98%
Specyficzność
Specyficzność
Zmienna
Zmienna
> 98%
> 98%
Dodatnie po
Dodatnie po
ekspozycji
ekspozycji
2-6
2-6
miesięcy
miesięcy
2-6
2-6
tygodni
tygodni
Zastosowanie
Zastosowanie
Skrining
Skrining
Potwierdzeni
Potwierdzeni
e
e
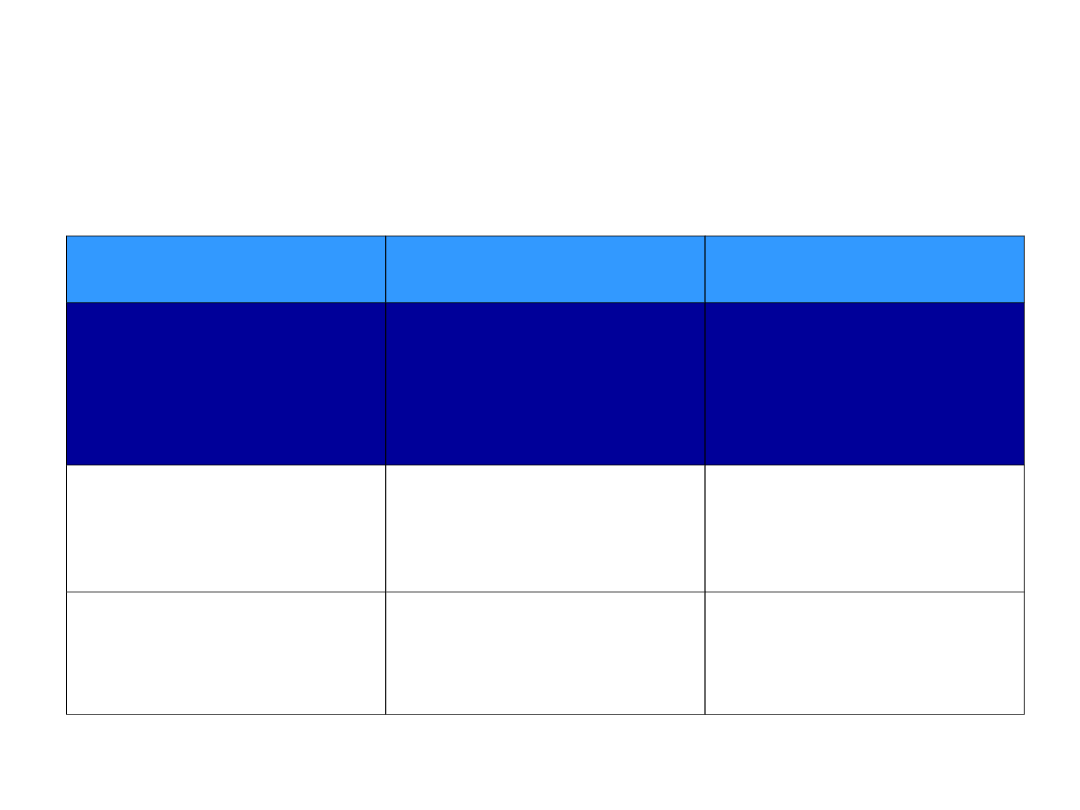
Rodzaj metod detekcji
Rodzaj metod detekcji
HCVRNA
HCVRNA
PCR
PCR
TMA
TMA
b-DNA
b-DNA
Polymerase
Polymerase
chain
chain
reaction
reaction
Transcription
Transcription
mediated
mediated
amplification
amplification
Branched
Branched
chain DNA
chain DNA
Amplifies
Amplifies
target
target
Amplifies
Amplifies
target
target
Amplifies
Amplifies
probe
probe
Jakościowy
Jakościowy
Ilościowy
Ilościowy
Jakościowy
Jakościowy
Ilościowy
Ilościowy

PZW t. C – biopsja
PZW t. C – biopsja
wątroby
wątroby
Jedyny test, który oceni:
Nasilenie zapalenia
Stopień włóknienia
Konieczna do oceny
Ryzyka rozwoju marskości w przyszłości
Potrzebna do leczenia
Umożliwia ocenę leczenia jeśli nie
uzyskano pierwotnej odpowiedzi na
leczenie
PZW t. C – biopsja wątroby
PZW t. C – biopsja wątroby
czy jest konieczna?
czy jest konieczna?
Nie
Nie
Pacjent akceptuje
Pacjent akceptuje
leczenie bez
leczenie bez
włóknienia
włóknienia
Pacjent nie
Pacjent nie
akceptuje leczenia
akceptuje leczenia
lub są
lub są
przeciwwskazania
przeciwwskazania
bezwzględne
bezwzględne
Badania sugerują
Badania sugerują
brak marskości
brak marskości
Pacjent osiągnął
Pacjent osiągnął
SV
SV
R
R
Tak
Tak
Pacjent akceptuje
Pacjent akceptuje
leczenie jeśli
leczenie jeśli
znaczne włóknienie
znaczne włóknienie
Badania sugerują
Badania sugerują
możliwość marskości
możliwość marskości
Pacjent nie osiągnął
Pacjent nie osiągnął
SVR
SVR
i nie miał
i nie miał
uprzednio biopsji
uprzednio biopsji
Porównanie biopsji wątroby i
Porównanie biopsji wątroby i
nieinwazyjnych testów
nieinwazyjnych testów
serologicznych
serologicznych
0
0.2
0.4
0.6
0.8
1.0
0
1
2
3
4
Stopień włóknienia
F
IB
R
O
T
E
S
T
0
0.2
0.4
0.6
0.8
1.0
0
1
2
3
Aktywność zapalna
A
C
T
IT
E
S
T
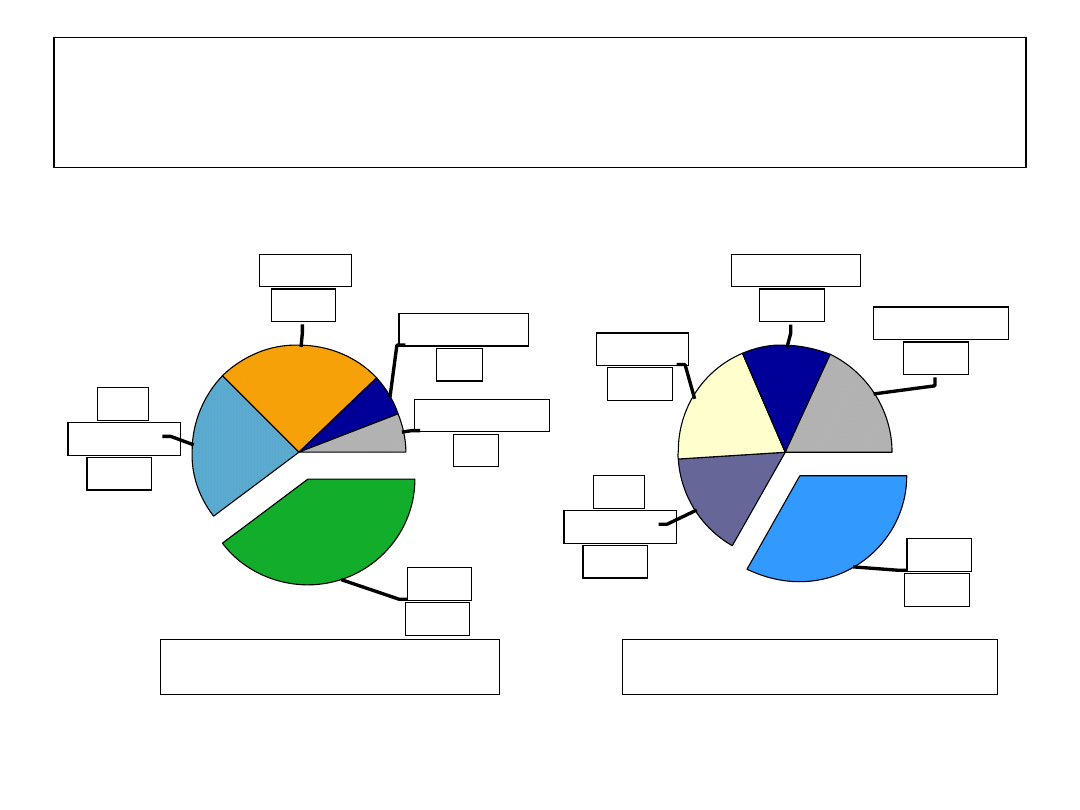
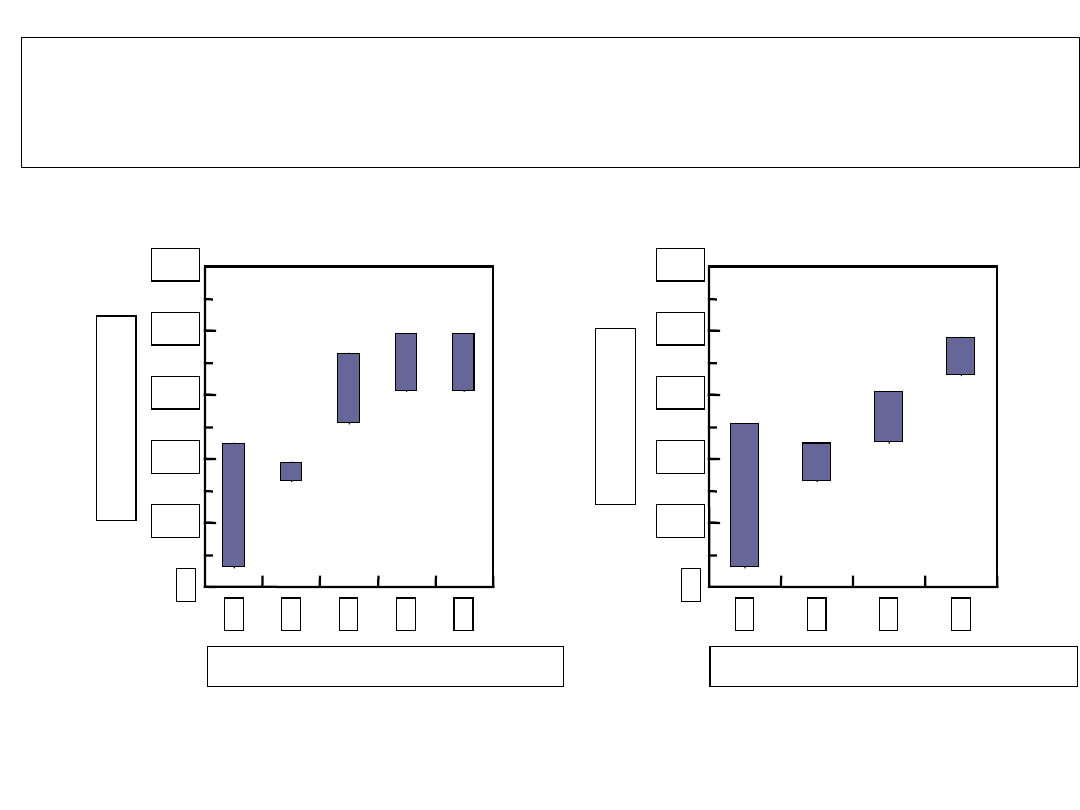
PZW t. C z prawidłową v/s
PZW t. C z prawidłową v/s
nieprawidłowa aktywnością
nieprawidłowa aktywnością
ALT
ALT
Prawidłowe ALT
Podwyższone ALT
Portal
26%
No
fibrosis
23%
Mild
39%
Cirrhosis
6%
Bridging
6%
Portal
20%
No
fibrosis
16%
Mild
33%
Cirrhosis
18%
Bridging
13%
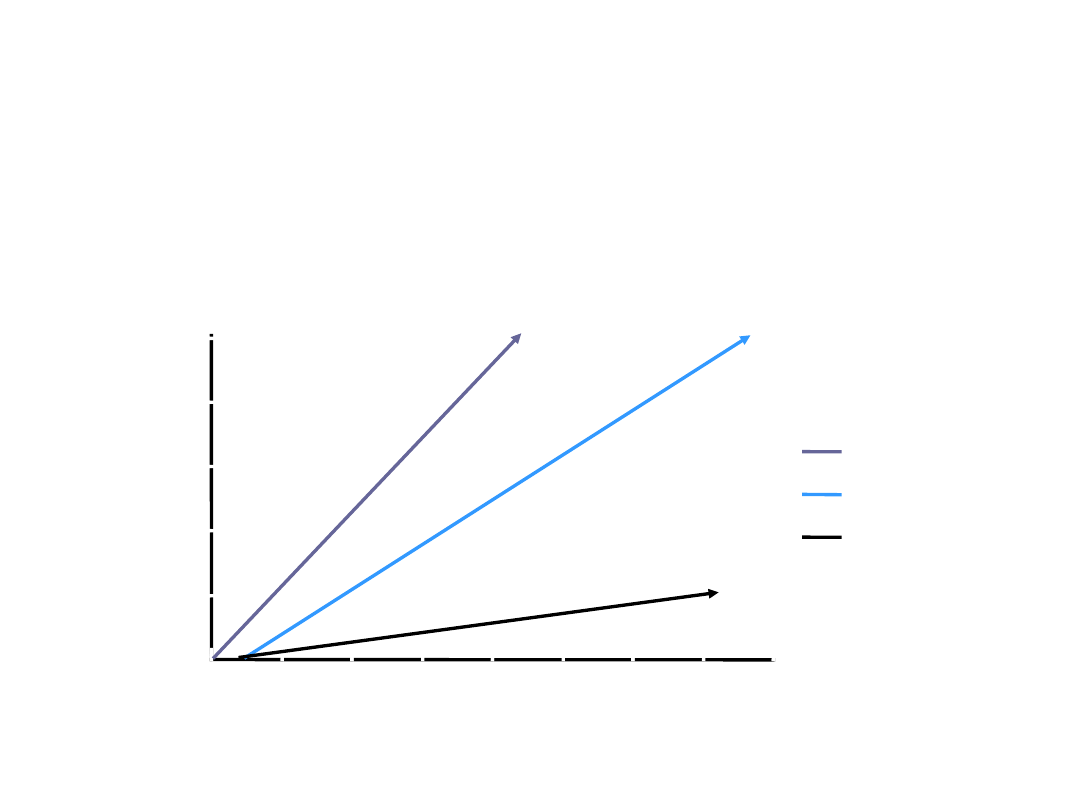
Progresja PZW t. C do
Progresja PZW t. C do
marskości zależnie od
marskości zależnie od
aktywności zapalnej
aktywności zapalnej
0
20
40
60
80
100
0
5
10
15
20
Czas (lata)
Bridging
Portal
Brak
S
za
c
u
n
k
o
w
y
o
d
s
e
te
k
p
a
c
je
n
tó
w
z
m
a
rs
k
o
ś
c
ią
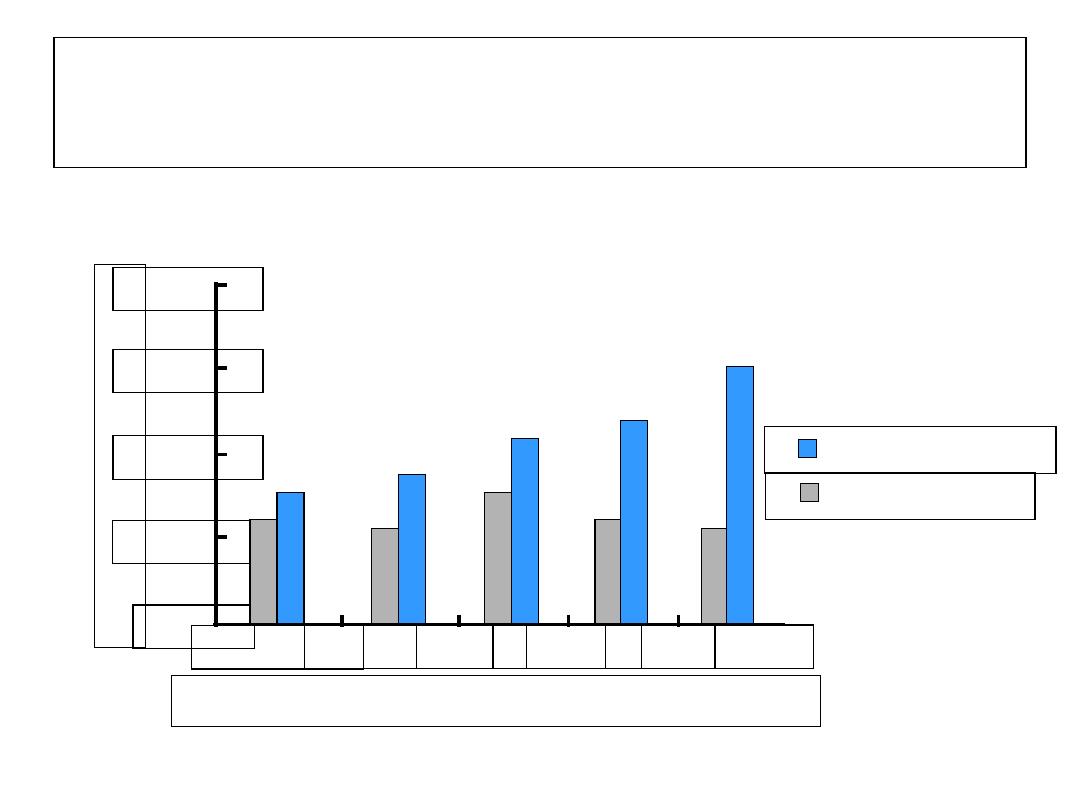
Progresja włóknienia w PZW t.
Progresja włóknienia w PZW t.
C
C
< 10
11-20 21-30 31-40 > 40
Czas trwania zakażenia (lata)
Włóknienie
Zapalenie
G
ra
d
e
o
r
S
ta
g
e
4.0
3.0
2.0
1.0
0
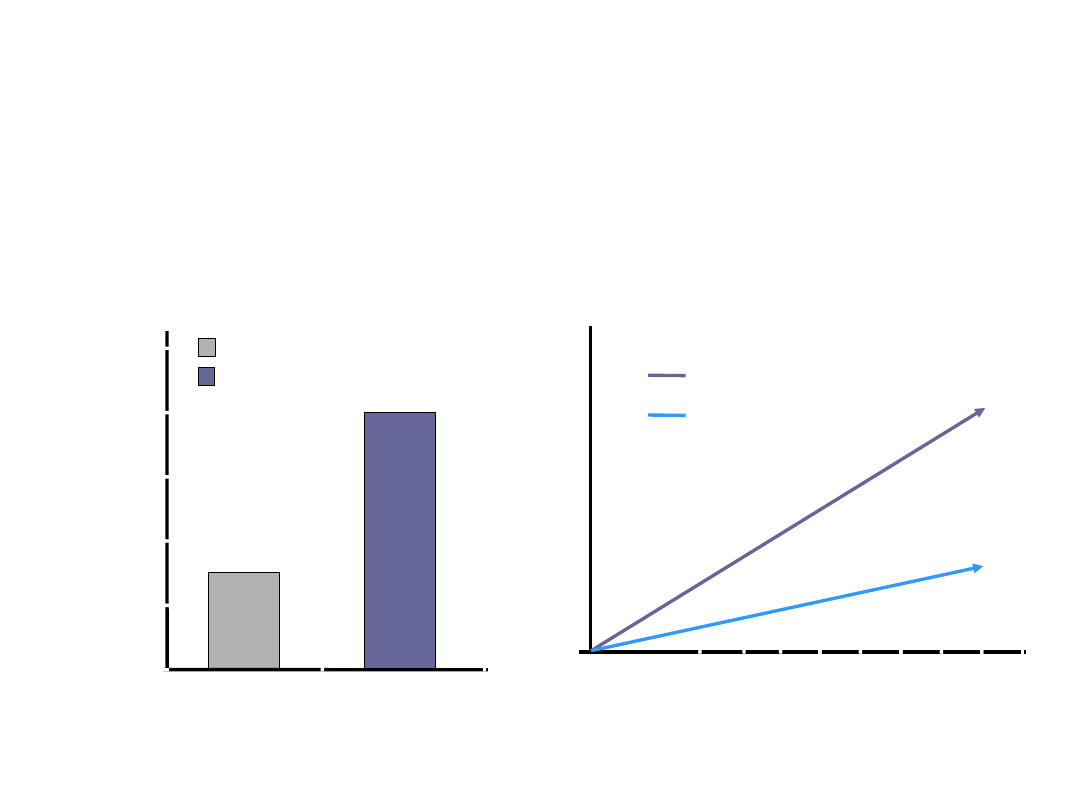
Przeżycie i odsetek dekompensacji
Przeżycie i odsetek dekompensacji
marskości u pacjentów zakażonych
marskości u pacjentów zakażonych
HCV
HCV
0
20
40
60
80
100
P
rz
e
ży
c
ie
(%
)
Stabilizacja
Dekompensacja
10-letnie skumulowane
przeżycie
0
10
20
30
40
50
0
2
4
6
8
10
Lata
O
d
s
e
te
k
p
a
c
je
n
tó
w
Dekompensacji
HCC
Skumulowane
prawdopodobieństwo

Leczenie przewlekłego
Leczenie przewlekłego
zapalenia wątroby HCV
zapalenia wątroby HCV

Cele terapii
Cele terapii
osoby
osoby
HCV
HCV
(+)
(+)
Pierwotnym celem jest eradykacja
HCV
Dodatkowe cele:
Zwolnienie progresji choroby
Zmniejszenie ryzyka rozwoju HCC
Poprawa obrazu histopatologicznego
wątroby
Poprawa jakości życia
Zapobieganie transmisji zakażenia HCV
Zmniejszenie nasilenia pozawątrobowej
manifestacji zakażenia
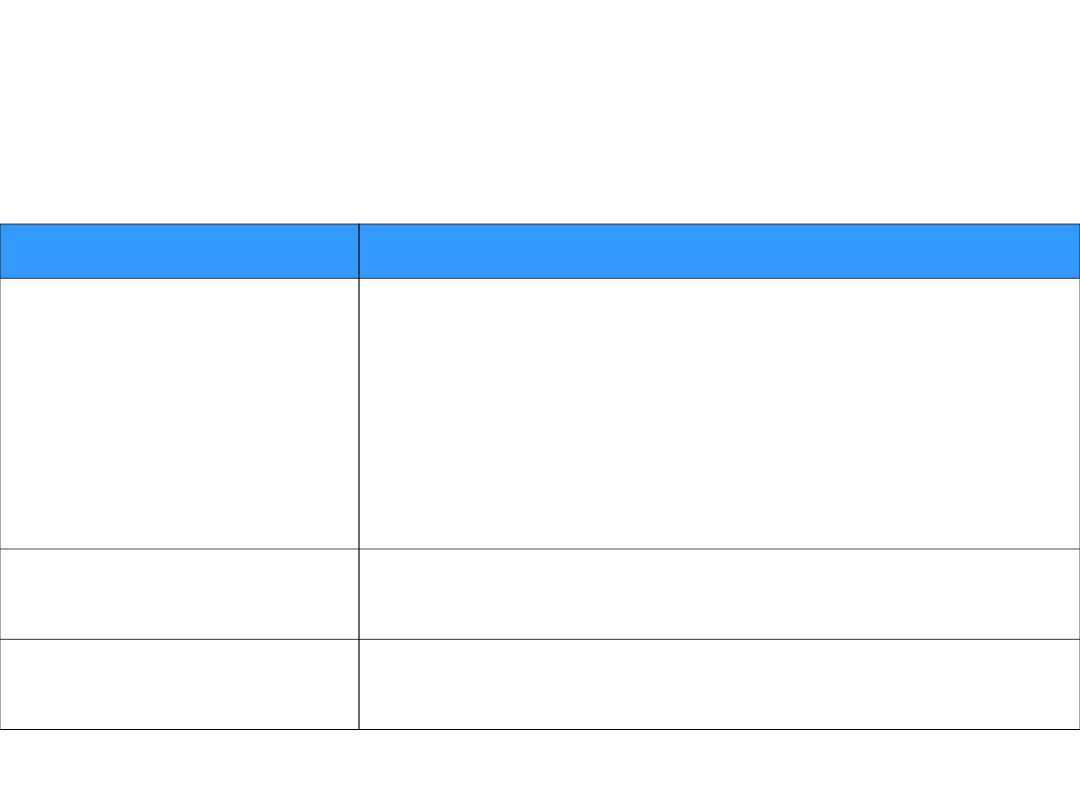
Lek
Lek
Zalecane dawkowanie
Zalecane dawkowanie
PEG-IFN
PEG-IFN
Peginterferon alfa-
Peginterferon alfa-
2b
2b
Peginterferon alfa-
Peginterferon alfa-
2a
2a
1.5
1.5
µ
µ
g/kg SQ
g/kg SQ
na tydzień w połączeniu z
na tydzień w połączeniu z
RBV;
RBV;
1.0
1.0
µ
µ
g/kg SQ
g/kg SQ
na tydzień w
na tydzień w
m
m
o
o
n
n
o
o
t
t
e
e
rap
rap
ii
ii
180
180
µ
µ
g SQ
g SQ
na tydzień w połączeniu z
na tydzień w połączeniu z
RBV
RBV
lub
lub
w
w
m
m
o
o
n
n
o
o
t
t
e
e
rap
rap
ii
ii
Interferon alfacon-1
Interferon alfacon-1
9
9
µ
µ
g SQ TIW; 15
g SQ TIW; 15
µ
µ
g TIW for
g TIW for
nonresponders
nonresponders
R
R
y
y
ba
ba
w
w
ir
ir
y
y
n
n
a (RBV)
a (RBV)
800-1400 mg PO
800-1400 mg PO
dziennie w 2 dawkach,
dziennie w 2 dawkach,
zależnie od wagi i genotypu
zależnie od wagi i genotypu
HCV
HCV
Leki zaaprobowane do
Leki zaaprobowane do
leczenia zakażenia HCV
leczenia zakażenia HCV
Pawlotsky JM. Hepatology. 2002;36(suppl 1):S65-S73.
Sethi A, et al. Clin Liver Dis. 2005;9:453-471.
Markery wirusologiczne i
Markery wirusologiczne i
definicje odpowiedzi na
definicje odpowiedzi na
leczenie
leczenie
Rapid Virologic
Rapid Virologic
Response
Response
(RVR)
(RVR)
HCV RNA
HCV RNA
niewykrywalne w
niewykrywalne w
4
4
tyg.
tyg.
terapii
terapii
Early Virologic
Early Virologic
Response (EVR)
Response (EVR)
Obniżenie HCVRNA o
Obniżenie HCVRNA o
≥ 2 log
≥ 2 log
w
w
12
12
tyg.
tyg.
terapii
terapii
End of
End of
Treatment
Treatment
(EOT) Response
(EOT) Response
Niewykrywalne
Niewykrywalne
HCV RNA
HCV RNA
na koniec
na koniec
terapii
terapii
Partial
Partial
Virologic
Virologic
Response
Response
Obniżenie HCVRNA o
Obniżenie HCVRNA o
≥ 2 log
≥ 2 log
w
w
12
12
tyg.
tyg.
terapii
terapii
,
,
ale
ale
HCV RNA
HCV RNA
(+) w
(+) w
24
24
tyg.
tyg.
terapii
terapii
Sustained
Sustained
Virologic
Virologic
Response
Response
(SVR)
(SVR)
HCV RNA
HCV RNA
ujemne
ujemne
12-24
12-24
tygodni po
tygodni po
EOT
EOT

Markery wirusologiczne i
Markery wirusologiczne i
definicje odpowiedzi na
definicje odpowiedzi na
leczenie
leczenie
Null Response
Null Response
HCV RNA
HCV RNA
obniżone
obniżone
< 2 log
< 2 log
10
10
IU/mL
IU/mL
w 1
w 1
2
2
tyg.
tyg.
terapii
terapii
Nonresponse
Nonresponse
Nie osiągnięcie
Nie osiągnięcie
nieoznaczalnego
nieoznaczalnego
HCV RNA
HCV RNA
w
w
każdym punkcie terapii
każdym punkcie terapii
Virologic
Virologic
Breakthrough
Breakthrough
Obniżenie
Obniżenie
HCV RNA
HCV RNA
do nieoznaczalnego
do nieoznaczalnego
przed
przed
powrotem wiremii w trakcie terapii
powrotem wiremii w trakcie terapii
Relapse
Relapse
Powrót wiremii HCV po osiągnięciu EOT
Powrót wiremii HCV po osiągnięciu EOT
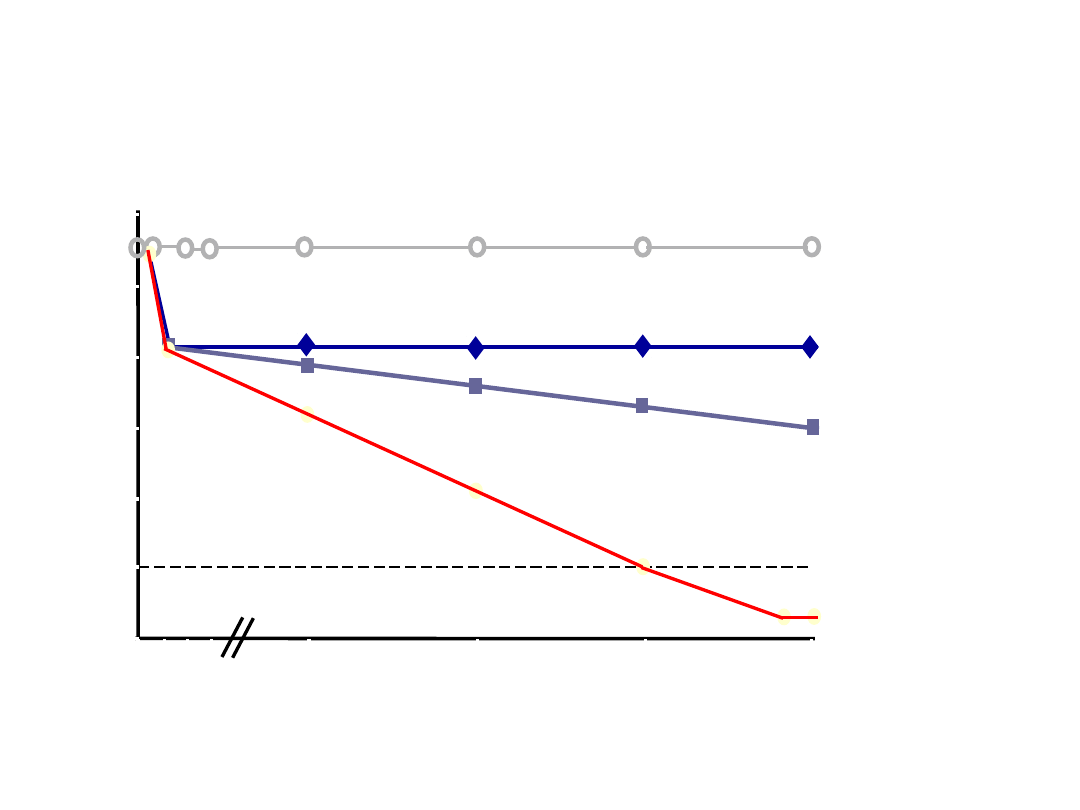
Wzory odpowiedzi
Wzory odpowiedzi
wirusologicznej
wirusologicznej
Dni terapii
1
2
3
4
5
6
7
0 1 2 3
7
14
21
28
Nonresponder
Flat-partial responder
Slow-partial responder
Rapid responder
Second phase
First phase
Próg
detekcji
HCVRNA
H
C
V
R
N
A
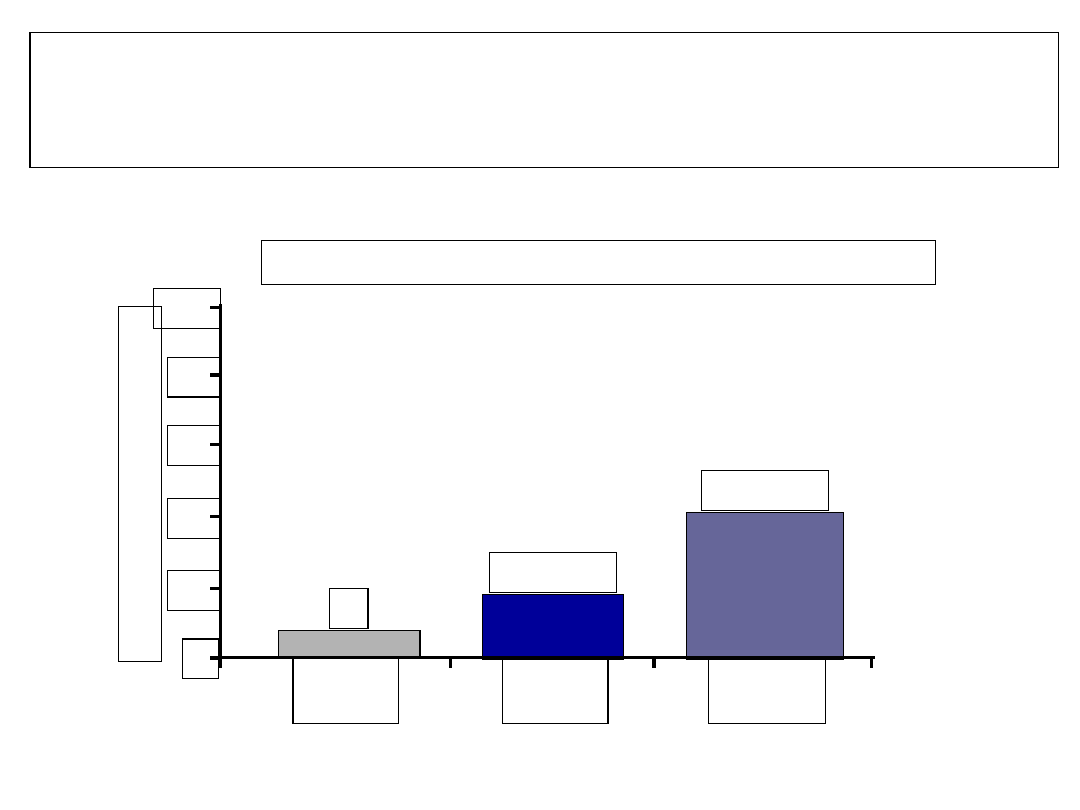
Trwała odpowiedź wirusologiczna
Trwała odpowiedź wirusologiczna
(
(
SVR
SVR
) w terapii zakażenia HCV
) w terapii zakażenia HCV
100
80
60
40
20
0
19
43
6
IFN
24 tyg.
IFN
48 tyg.
IFN/RBV
48 tyg.
SVR uzyskane w terapii standardowym IFN
P
a
c
je
n
c
i
(
%
)
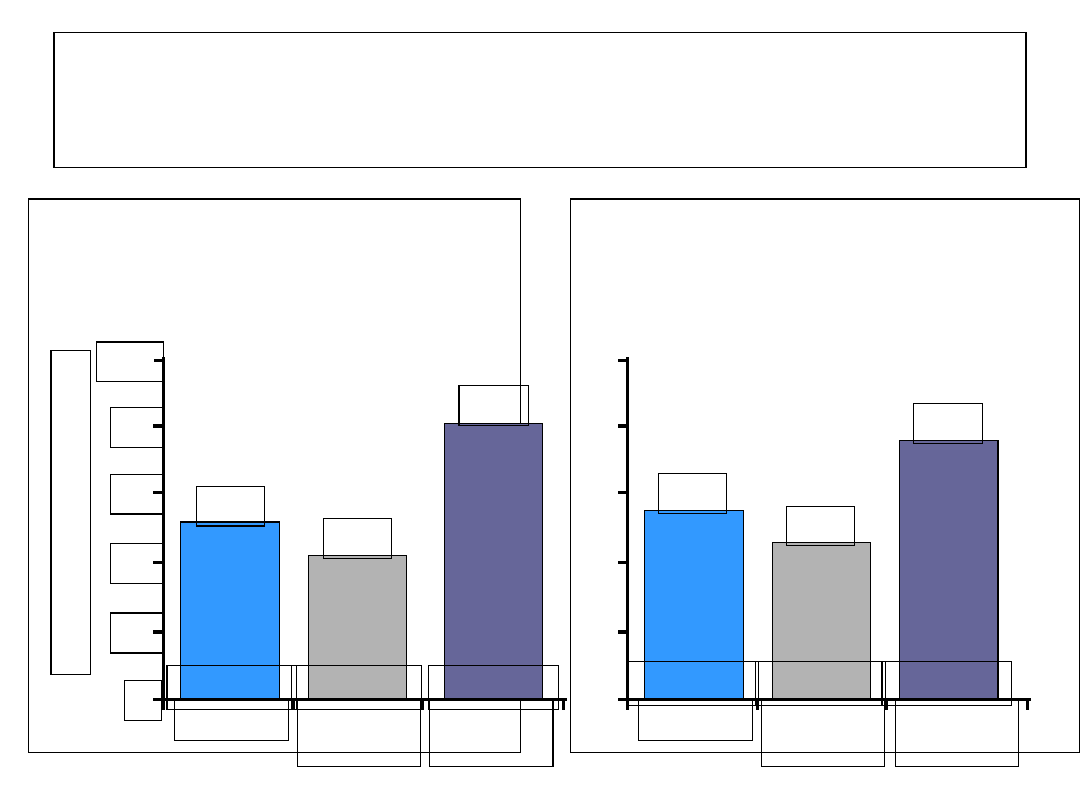
Peginterferon alfa-2b
Peginterferon alfa-2b
1.5
1.5
µg/kg/wk
µg/kg/wk
+
+
RBV
RBV
800 mg/d
800 mg/d
przez
przez
48
48
tygodni
tygodni
Peginterferon alfa-2a
Peginterferon alfa-2a
180
180
µg/wk +
µg/wk +
RBV
RBV
(1000
(1000
lub
lub
1200 mg/d
1200 mg/d
–
–
zależnie od wagi
zależnie od wagi
)
)
przez
przez
48
48
tygodni
tygodni
Trwała odpowiedź
Trwała odpowiedź
wirusologiczna (
wirusologiczna (
SVR
SVR
) w terapii
) w terapii
zakażenia HCV
zakażenia HCV
46
76
56
Ogólnie
Genotyp
1
Genotyp
2/3
n = 298 n = 140
n = 453
42
82
100
80
60
40
20
0
54
Ogólnie
Genotyp
1
Genotyp
2/3
S
V
R
(%
)
n = 348 n = 163
n = 511

Tydzień 4 RVR
osiągnięty
Genotyp 1/4
Genotyp 2/3
Tydzień 12
EVR nie
osiągnięty
Slow response
(EVR, brak
negatywizacji
HCV RNA w 24
tyg.)
Skrócenie terapii do
24 tygodni może
być stosowane
Zaleca się
kontynuować
terapię do 24 tyg.
jeśli
RVR osiągnięty
Rekomendacje
zalecają
zakończenie terapii
Rekomendacje
zalecają
zakończenie terapii
Przedłużenie terapii
do 72 tygodnia
może poprawić SVR
Zastosowanie
Zastosowanie
monitorowania wiremii w
monitorowania wiremii w
praktyce
praktyce

Wpływ leczenia PZW t. C
Wpływ leczenia PZW t. C
na rozwój HCC
na rozwój HCC
Leczenie interferonem alfa zmniejsza
ryzyko rozwoju HCC w porównaniu z grupą
nieleczonych (P = .002)
Przypadki Hepatocellular carcinoma
U nie leczonych: 38% (24%-58%)
Leczonych interferonem 4% (1%-15%)
HCC risk ratio: 0.067 (0.009-0.530; P = .
01)

Wniosek
Wniosek
Reguły terapii przeciwwirusowej
różnią się znacząco od zasad
stosowanych w
antybiotykoterapii…
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
Wyszukiwarka
Podobne podstrony:
Wirusowe zapalenie wątroby typu C klinika, leczenie i następstwa
WIRUSOWE ZAPALENIE WĄTROBY WZW, MEDYCYNA, Wykłady
Diagnostyka wirusowych zapaleń wątroby
Epidemiologia, etiopatogeneza i diagnostyka wirusowych zapaleń wątroby
Żywienie w wirusowym zapaleniu wątroby
WIRUSOWE ZAPALENIA WĄTROBY 3
Choroby zakaźne tekst, WIRUSOWE ZAPALENIE WĄTROBY WZW, WIRUSOWE ZAPALENIE WĄTROBY WZW
WZW, Wirusowe zapalenie wątroby (hepatitis viralis)
zakazy, w 11 WZW cz.II, WYKŁAD: WIRUSOWE ZAPALENIA WĄTROBY, CZĘŚĆ II
Przewlekłe wirusowe zapalenia wątroby typu B i C, Pomoce naukowe, studia, medycyna
WIRUSOWE ZAPALENIE WĄTROBY
Szkol Ostre wirusowe zapalenie wątroby
Wirusowe zapalenia wątroby, FIZJOTERAPIA, Demografia i epidemiologia
WIRUSOWE ZAPALENIE WĄTROBY WZW, Choroby zakaźne
WZW-Wirusowe zapalenia wątroby, zagrożenia, zapobieganie i leczenie
Wirusowe zapalenie wątroby typu A
Wirusowe zapalenie wątroby
WIRUSOWE ZAPALENIA WĄTROBY
więcej podobnych podstron