Fenol
Fenol, czyli inaczej…
hydroksybenzen,
hydroksybenzen,
karbol,
karbol,
benzofenol,
benzofenol,
monofenol,
monofenol,
kwas fenolowy
kwas fenolowy

Właściwości
W temperaturze pokojowej czysty
fenol jest bezbarwnym krystalicznym
ciałem stałym o charakterystycznym
ostrym zapachu
pod wpływem światła następuje
częściowe utlenienie fenolu, w wyniku
którego zmienia on barwę na różową,
brunatną lub czarną

Temp. topnienia 41°C
Temp. wrzenia 182 °C
gęstość 1,07 g/cm³
niezbyt dobrze rozpuszcza się w
wodzie (w temp. 20°C 8,2 g na 100
cm³ H
2
O), lepiej w rozpuszczalnikach
organicznych

Otrzymywanie
Najważniejszą metodą otrzymywania
fenolu jest obecnie metoda kumenowa.
Inne, obecnie głównie o znaczeniu
historycznym, to np.:
ekstrakcja ze smoły węglowej,
katalizowana hydroliza chlorobenzenu w
podwyższonej temperaturze,
stapianie kwasu benzenosulfonowego lub
jego soli z wodorotlenkiem sodu lub potasu
i zakwaszanie powstałych fenolanów
.
.

Zastosowanie
Obecnie głównie w produkcji:
żywic fenolowo-formaldehydowych (np. bakelitu),
leków (np. kwasu acetylosalicylowego),
detergentów,
herbicydów,
fungicydów
barwników
zmywaczy farb i pokostów, lakierów, gum, mydeł
A także jako:
środek wiążący w materiałach izolacyjnych,
płytach wiórowych i formach odlewniczych,
środek dezynfekcyjny i bakteriobójczy

Losy w organizmie
Wchłanianie fenolu odbywa się przez:
•
drogi oddechowe (retencja par fenolu w
drogach oddechowych wynosi około 70%)
•
skórę (zarówno jako ciecz i para:
współczynnik wchłaniania dermalnego par
fenolu wynosi
0,35 m
3
/h)
•
przewód pokarmowy
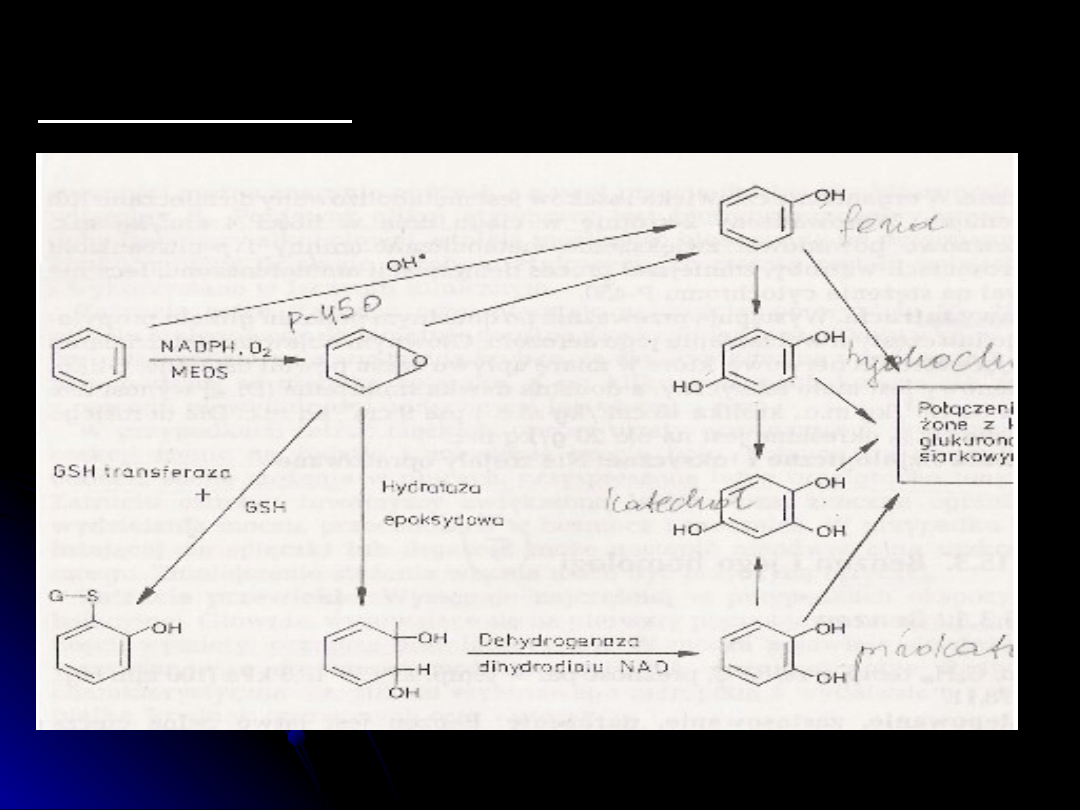
Metabolizm
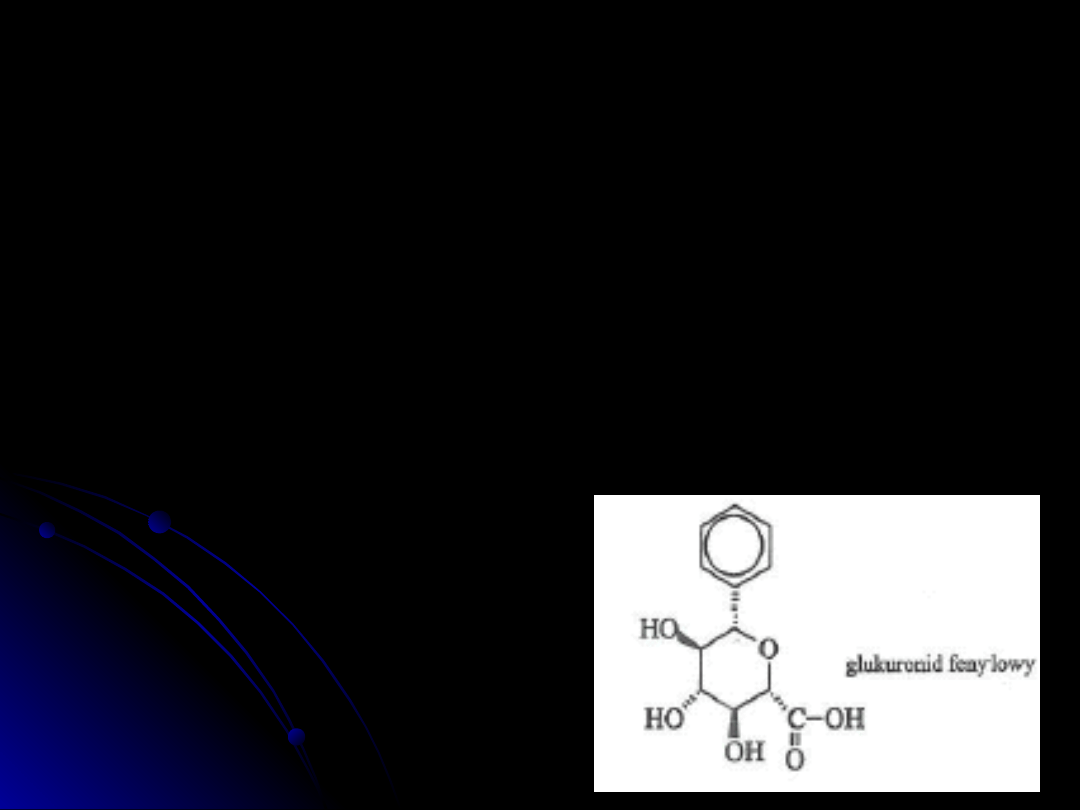
Biotransformacja fenolu polega
głównie na reakcjach sprzęgania
grupy –OH z kwasem siarkowym i
glukuronowym. W tej postaci fenol
jest szybko wydalany z moczem.
Obecny w moczu fenyloglukuronid
może
służyć do monitorowania
ekspozycji na fenol

W niewielkim stopniu fenol ulega także
hydroksylacji do katecholu i
hydrochinonu
Większa część przemian zachodzi w
wątrobie, jednak płuca, jelita i nerki
również odgrywają istotną rolę w tych
procesach, a względny udział
wymienionych narządów w
biotransformacji fenolu zależy od drogi
narażenia i dawki

Wydalanie
Główną drogą wydalania fenolu są nerki,
nieznaczna część może być wydalona z
kałem i powietrzem wydychanym.
U człowieka w ciągu 24h wydala się ok.
90% dawki fenolu, głownie w postaci
siarczanów.
Półokres wydalania fenolu z ustroju
człowieka wynosi 3-4 godziny.

Mechanizm działania
toksycznego fenolu
•
działa drażniąco na skórę i oczy
•
pary mogą powodować podrażnienie dróg
oddechowych
•
po wchłonięciu z przewodu pokarmowego w
większych dawkach wywiera działanie narkotyczne,
może powodować obrzęk mózgu, a także obrzęk
płuc i powodować uszkodzenie narządów
miąższowych, zwłaszcza wątroby i nerek.
•
wywołuje silną hemolizę krwi.

Zatrucia ostre - objawy
•
Przez skórę:
Wchłanianie przez skórę mgły, par i roztworu
wywołuje zawroty, ból głowy, dezorientację,
zaburzenia oddechowe, zapaść, utratę
przytomności.
Skażenie skóry substancją stałą lub ciekłą wywołuje
miejscowe zbielenie i oparzenia, które początkowo
nie są bolesne, oraz pęcherze, martwicę.
•
Drogą pokarmową:
Połknięcie roztworu wywołuje rozległe oparzenia
błon śluzowych jamy ustnej, gardła i dalszych
części przewodu pokarmowego, bóle i krwawienie,
perforację ścian przewodu pokarmowego,
uszkodzenie wątroby i nerek.

Zatrucia ostre – objawy
c.d.
•
Drogą inhalacyjną:
Pary i mgła powodują podrażnienie spojówek,
uszkodzenie rogówki, błon śluzowych nosa,
gardła, uczucie suchości w nosie, gardle,
kaszel.
W wysokich stężeniach: zawroty i ból głowy,
mdłości, wymioty, duszność, przyspieszenie i
pogłębienie oddechów, zaburzenia
oddychania, zaburzenia orientacji, zapaść,
utratę przytomności
Wdychanie par fenolu nie wywołuje zatruć
śmiertelnych.

Zatrucia przewlekłe -
objawy
•
W warunkach narażenia zawodowego
brak łaknienia, nudności, wymioty, biegunki,
zmniejszenie masy ciała, bóle i zawroty głowy,
nadmierne wydzielanie śliny, ciemne
zabarwienie moczu, zapalenie wątroby,
żółtaczka, zmiany w nerkach, białkomocz, stany
zapalne układu oddechowego, uporczywy kaszel
•
Wodą pitną skażoną fenolem:
biegunka, podrażnienie, poparzenie jamy ustnej

Bezpośrednim następstwem zatrucia
jest uszkodzenie wątroby z żółtaczką,
uszkodzenie nerek z ich ostrą
niewydolnością, zapalenie płuc.
Zgon następuje w skutek porażenia
ośrodka oddechowego

Pierwsza pomoc w wypadku
zatruć:
W przypadku zatruć inhalacyjnych wynieść poszkodowanego na
świeże powietrze. Zapewnić spokój i ciepło. Zapewnić drożność
dróg oddechowych. Podawać tlen do oddychania. Jeśli zachodzi
potrzeba, zastosować sztuczne oddychanie. Wezwać pomoc
lekarską.
W przypadku skażenia skóry zdjąć skażoną odzież. Skórę zmyć
dużą ilością letniej wody z mydłem, a następnie dużą ilością oleju
jadalnego. Założyć jałowy opatrunek. Niezbędna pomoc lekarska.
W przypadku skażenia oczu płukać je chłodną wodą przez około
15 minut. Niezbędna konsultacja lekarza okulisty.
W przypadku zatrucia drogą pokarmową podawać
poszkodowanemu do picia białko jaj kurzych. Nie prowokować
wymiotów. Wezwać lekarza.

Wartości toksykologiczne
Próg wyczuwalności zapachu – 0,2-20
mg/m
3
LD50 (szczur, doustnie) – 384 mg/kg m.c.
(przyjmuje się wartości 300-600 mg/kg m.c. dla różnych
gatunków zwierząt)
LC50 (szczur, inhalacja) – 316 mg/m
3
LD50 (królik, skóra) – 850 mg/kg m.c.

Wartości biologiczne i
toksyczne
NDS na stanowisku pracy – 10 mg/m
3
DSCh - 20 mg/m
3
Dopuszczalne stężenie w moczu
(DSB) wynosi 250 mg/g kreatyniny
Fizjologiczne stężenie w moczu osób
narażonych waha się w granicach
0,5-81.5 mg/dm
3

Oznaczanie fenolu
1.
Reakcje barwne
reakcja z wodnym roztworem chlorku żelaza-
zabarwienie
fioletowo-niebieskie
fenole monowodorotlenowe z odczynnikiem
Millona dają
czerwone
zabarwienie
reakcja nitrozowania (Liebermana)- nitrozowanie
w pozycji 4 w środowisku bezwodnym po dodaniu
kwasu nitrozylosiarkowoego daje zabarwienie
niebieskozielone
, po
dodaniu NaOH zmienia
się na
niebieskie.

2.
2.
Metodą chromatografii gazowej
Metodą chromatografii gazowej
Metoda polega na adsorpcji par fenolu na
żelu krzemionkowym, desorpcji
acetonitrylem i analizie metodą
chromatografii gazowej otrzymanego
roztworu
.

3.
Metodą spektrofotometryczną
Metodę stosuje się w zakresie stężeń 0.5 do 10.0
mg/dm
3
Oznaczanie fenolu w moczu polega na wydzielaniu
substancji z matrycy – najczęściej poprzez destylację z
para wodną z kwaśnego roztworu.
Następnie poddaje się go reakcji z 4-aminoantypiryną w
środowisku alkaicznym przy pH 9,8 ± 0,2 w obecności
heksacyjanożelazianu (III) potasu jako substancji
utleniającej.
W wyniku tej reakcji powstaje barwny związek
(indofenol) mający zabarwienie, w zależności od stężenia
fenolu, od
zielonożółtego
do
czerwonowiśniowego
.
Następnie określa się stężenie za
pomocą spektrofenometru UV-VIS
lub kolorymetru fotoelektrycznego.
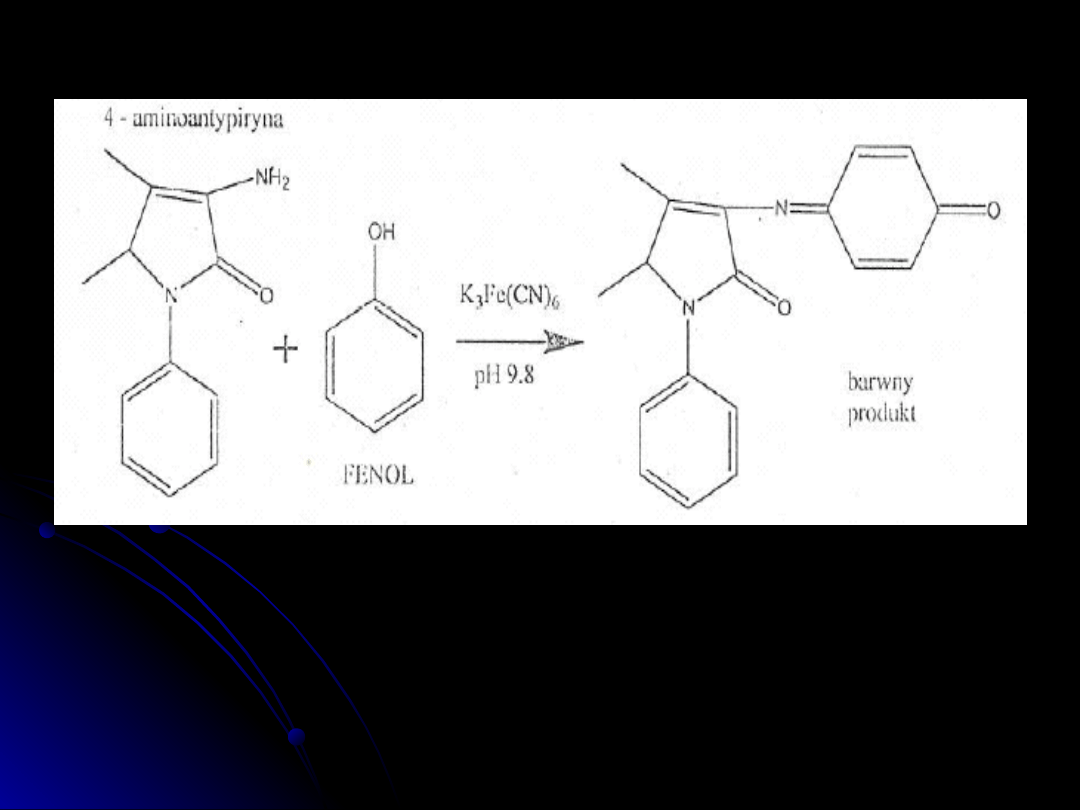
Reakcja 4-aminoantypiryny z fenolem.

Przygotowanie próbki do
analizy
1.
Utrwalenie próbki kwasem ortofosforowym (V) do
pH 4 dodanym bezpośrednio do moczu lub wody
oraz 1 g pięciowodnego siarczanu (VI) miedzi (II)
na 1 dm
3
próbki.
2.
Do roztworu fenolu dodaje się roztwór 4-
aminoantypiryny oraz roztworu
heksacyjanożelazianu (III) potasu.
3.
Następnie dodaje się roztworu buforu amonowego
lub wodnego 25% roztworu amoniaku i dopełnia
wodą destylowaną do odpowiedniej objętości.
4.
Pomiar absorbancji przeprowadza się po ok. 5-10
minutach (nie dłużej niż po 30 min.) przy długości
fali 510 nm.
5.
Zawartość fenolu obliczamy na podstawie odczytu
wartości z krzywej wzorcowej.

Dziękuję
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
Wyszukiwarka
Podobne podstrony:
FENOL ppt
fenol spektro ppt
03 Sejsmika04 plytkieid 4624 ppt
Choroby układu nerwowego ppt
10 Metody otrzymywania zwierzat transgenicznychid 10950 ppt
10 dźwigniaid 10541 ppt
03 Odświeżanie pamięci DRAMid 4244 ppt
Prelekcja2 ppt
2008 XIIbid 26568 ppt
WYC4 PPT
rysunek rodziny ppt
więcej podobnych podstron