
FENOL
właściwości, działanie na
organizm, toksyczność
J Ł
Farmacja, gr. d

Właściwości
Fenol (C
6
H
5
OH): hydroksybenzen, benzenol, kwas
karbolowy, karbol
W temperaturze pokojowej czysty fenol jest bezbarwnym
krystalicznym ciałem stałym (pod wpływem światła
następuje częściowe utlenienie fenolu, w wyniku którego
zmienia barwę na różową, brunatną lub czarną)
Jest silnie higroskopijny
Zapach: ostry, słodkawy
Gęstość: 1,07 g/cm³
Rozpuszczalność: niezbyt dobrze rozpuszcza się w
wodzie, lepiej w rozpuszczalnikach organicznych np.:
alkohol etylowy, eter etylowy, gliceryna, chloroform,
benzen
Temperatura topnienia: 41°C
Temperatura wrzenia: 182°C

Fenol od alkoholi odróżnia to, że
grupa hydroksylowa połączona jest
bezpośrednio z pierścieniem
aromatycznym, co wpływa na
właściwości związku - m. in. na wzrost
właściwości kwasowych (stała
dysocjacji K
a
= 1,3 · 10).
Tworzy sole i estry - fenolany.
Po raz pierwszy został wydzielony ze
smoły węglowej w 1832 r. przez
chemika niemieckiego
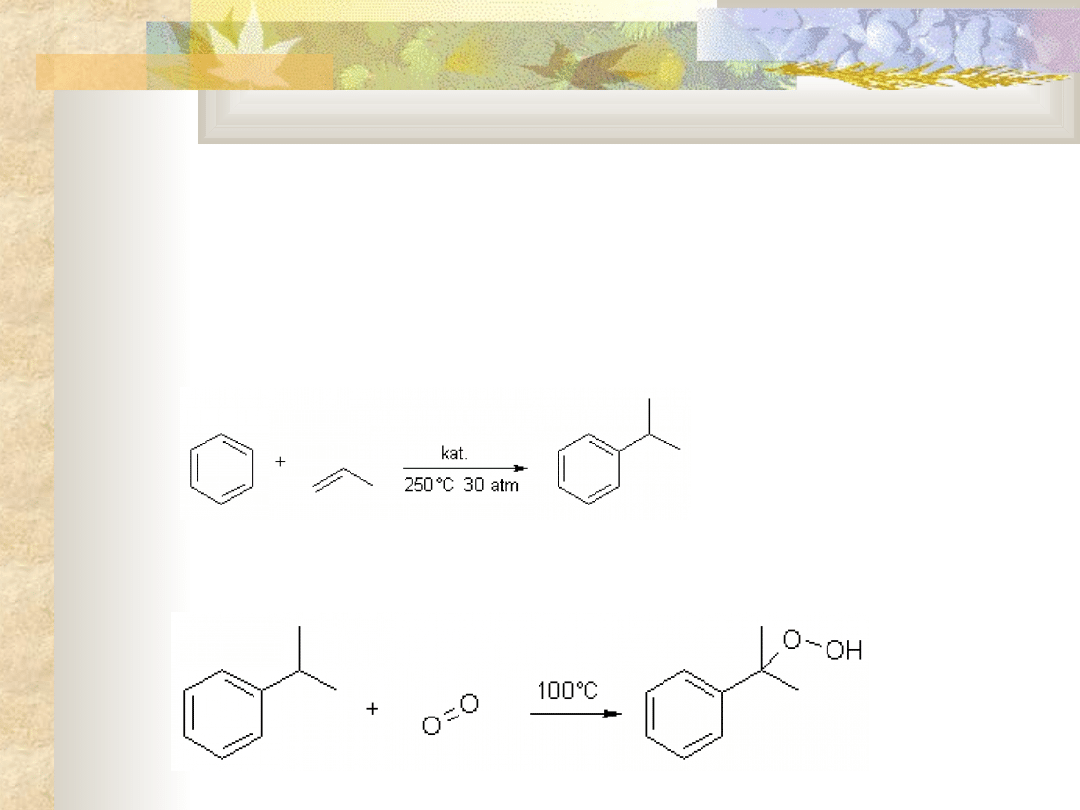
Otrzymywanie – metoda kumenowa
To trójetapowa metoda otrzymywania fenolu i acetonu z benzenu i propenu.
Nazwa tej metody pochodzi od kumenu (izopropylobenzenu), który jest
produktem pośrednim.
etap I - alkilacja benzenu propenem w temp. 250°C pod zwiększonym
ciśnieniem w obecności kwasu Lewisa (np. chlorku glinu) jako
katalizatora:
etap II – utlenianie kumenu tlenem w temp. 100°C do wodoronadtlenku
kumenu
:
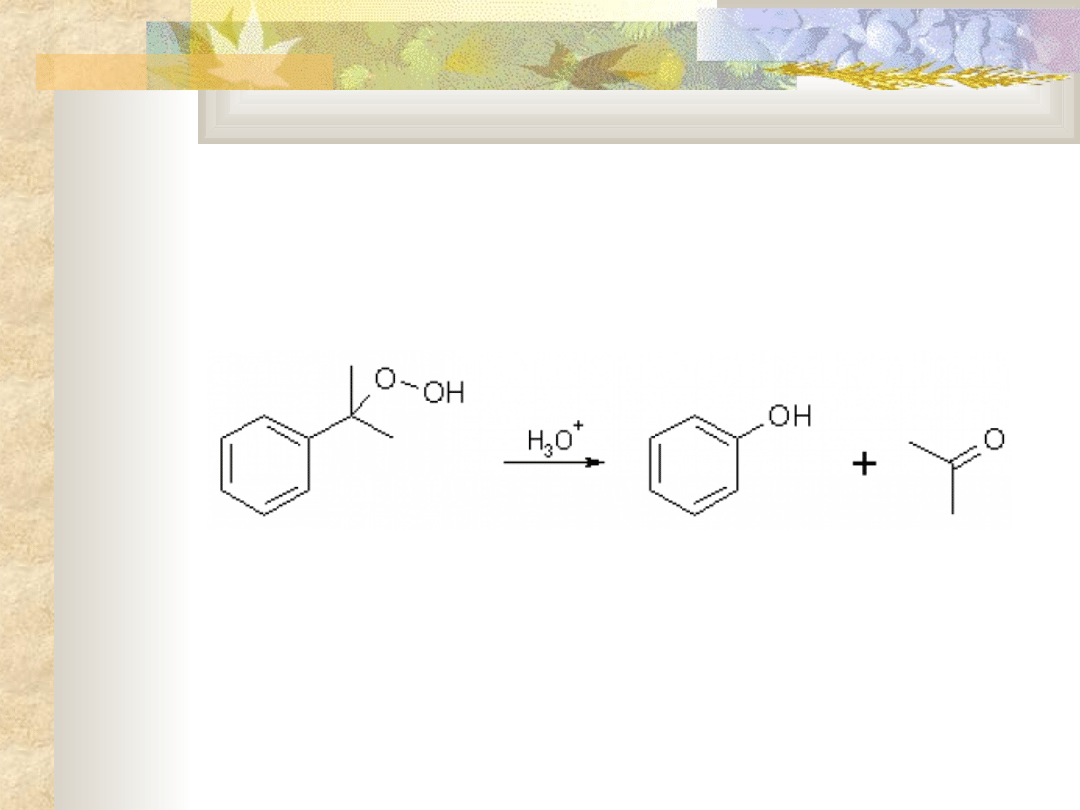
Otrzymywanie – metoda kumenowa
etap III - kwasowa hydroliza otrzymanego
hydronadtlenku kumenu:
Produkty są następnie rozdzielane przez
destylację.
Zdecydowana większość światowej produkcji
fenolu i acetonu oparta jest na tej metodzie.

Zastosowanie
Używany do produkcji:
żywic fenolowo-formaldehydowych,
bisfenolu, kaprolaktamu, alkilowych
pochodnych fenoli i chlorofenoli
leków (np. kwasu acetylosalicylowego),
detergentów, herbicydów, fungicydów i
barwników,
zmywaczy farb, pokostów, lakierów, gum,
perfum i mydeł
w XIX w. stosowany był jako środek
antyseptyczny i dezynfekujący.

Zastosowanie
był jednym z najwcześniej stosowanych środków
przeciwbakteryjnych. W stężeniu 0,2% działa
bakteriostatycznie, 1,3% grzybobójczo, powyżej 2%
bakteriobójczo. Dzisiaj nie stosowany, ze względu
na dużą liczbę zatruć
stosowany w kosmetyce do tzw. peelingu
chirurgicznego. Fenol to najsilniejszy wśród
związków chemicznych używanych do złuszczania
skóry. Wykazuje właściwości keratokoagulacyjne. Po
peelingu stężenie fenolu we krwi dochodzi do 0,68
mg/ml- znacznie niższe niż śmiertelne. Opisywano
przypadki śmierci po peelingach fenolowych- z
powodu kardiotoksyczności (arytmie serca).

Toksyczność
Klasa toksyczności:
Substancja toksyczna oraz żrąca wg wykazu
substancji niebezpiecznych.
Substancja nieumieszczona w wykazie substancji
i preparatów o działaniu rakotwórczym lub
mutagennym.
Substancja nie może być sklasyfikowana jako
rakotwórcza dla ludzi
Drogi wchłaniania:
drogi oddechowe,
skóra,
z przewodu pokarmowego
metabolit benzenu

Toksyczność
Pary fenolu dobrze wchłaniają się zarówno przez
układ oddechowy jak i przez skórę (wchłanianie
przez skórę może być nawet przyczyną zatruć
śmiertelnych).
Fenol stały lub w roztworach wchłania się przez
skórę, jednak denaturacja białek naskórka
powoduje opóźnienie wchłaniania
.

Stężenia oraz dawki
śmiertelne i toksyczne
LD50 (szczur, doustnie) – 384 mg/kg
LC50 (szczur, inhalacja) – 316 mg/m3
LD50 (królik, skóra) – 850 mg/kg
Dawka śmiertelna doustna wynosi ok. 50-
500 mg/kg

Objawy zatrucia ostrego:
pary i mgła powodują podrażnienie spojówek, błon
śluzowych nosa, gardła, uczucie suchości w nosie,
gardle, kaszel. W wysokich stężeniach: zawroty i ból
głowy, mdłości, wymioty, duszność, przyspieszenie i
pogłębienie oddechów, zaburzenia oddychania,
zaburzenia orientacji, zapaść, utratę przytomności.
wchłanianie przez skórę mgły, par i roztworu
wywołuje zawroty, ból głowy, dezorientację,
zaburzenia oddechowe, zapaść, utratę przytomności.
skażenie skóry substancją stałą lub ciekłą wywołuje
miejscowe zbielenie i oparzenia, które początkowo
nie są bolesne, oraz pęcherze, martwicę.
skażenie oczu powoduje ostry stan zapalny,
uszkodzenie rogówki.

bezpośrednim następstwem zatrucia jest
uszkodzenie wątroby z żółtaczką, uszkodzenie
nerek z ich ostrą niewydolnością, zapalenie płuc.
połknięcie roztworu wywołuje rozległe oparzenia
błon śluzowych jamy ustnej, gardła i dalszych
części przewodu pokarmowego, bóle i
krwawienie, perforację ścian przewodu
pokarmowego, uszkodzenie wątroby i nerek.
Objawy zatrucia przewlekłego:
zaburzenia ze strony układu pokarmowego:
wymioty, bóle gardła, utrata łaknienia, ślinotok,
biegunka i jadłowstręt.
występuje ochronoza (ciemne zabarwienie skóry
i moczu) i wykwity skórne.
może wystąpić uszkodzenie wątroby i nerek.

NDS- 7,8-10 mg/m3
Dopuszczalne stężenie w moczu- 250 mg/g
kreatyniny
Narażenie zawodowe na fenol występuje
głównie w trakcie stosowania żywic
fenolowych oraz ich obróbki cieplnej. Są one
wykorzystywane jako materiał wiążący w
materiałach izolacyjnych, płytach wiórowych,
formach odlewniczych.
Narażenie na fenol może także występować
podczas produkcji koksu, produkcji fenolu i
jego pochodnych oraz kaprolaktamu
(poliamid, nylon).
Źródłem narażenia mogą być wędzone
produkty spożywcze oraz woda pitna.

Przykład: Płock 1999-2003
Przeprowadzono analizę zanieczyszczeń
fenolem powietrza atmosferycznego w
Płocku w latach 1999-2003. Przedstawiono
średnioroczne stężenia oraz zanalizowano
ich dynamikę w badanym okresie. Analiza
danych wykazała, że w latach 1999-2002
stężenie fenolu w Płocku wyniosło 3,3 ug/m3
i przekraczało wartość dopuszczalnego
stężenia, które wynosi 2,5 ug/m3. Źródłem
fenolu mogła być wytwórnia fenolu i
acetonu Petrochemii Płock S.A.

Losy w organizmie
Biotransformacja fenolu polega głównie na
sprzęganiu z kwasem siarkowym i
glukuronowym w wątrobie, jednak płuca,
jelita i nerki również odgrywają istotną rolę
w metabolizmie tego związku
Główną drogą wydalania fenolu są nerki, w
ciągu 24 h wydala się ok. 90% dawki
fenolu głównie w postaci siarczanu
Część fenolu metabolizowana jest w
wątrobie do hydrochinonu i katecholu,
wydalanych przez nerki
Półokres wydalania fenolu z ustroju po
narażeniu inhalacyjnym wynosi 3-4 h

Mechanizm działania
toksycznego
Fenol i jego metabolity wiążą się kowalencyjnie z
białkami tkanek, głównie wątroby, z białkami osocza,
a także z DNA
Powodują denaturację i ścięcie białek komórkowych
Uszkadzają wątrobę i nerki, wywołują kwasicę
metaboliczną
Pary fenolu mogą powodować podrażnienie dróg
oddechowych
Działa neurotoksycznie, powodując demielenizację
włókien nerwowych
Może doprowadzić do methemoglobinemii
Przeprowadzone badania wykazują, że fenol może
mieć działanie genotoksyczne oraz powodować
uszkodzenie szpiku

Oznaczanie fenolu w wodzie i
moczu:
Polega na wydzieleniu go z matrycy – najczęściej
poprzez destylację z parą wodną z kwaśnego
roztworu i następnie reakcji z 4-aminoantypiryną
w środowisku alkalicznym przy pH = 9,8 w
obecności heksacyjanożelazianu(III) potasu jako
substancji utleniającej
W wyniku tej reakcji powstaje barwny związek
(indofenol) mający zabarwienia w zależności od
stężenia fenolu od zielonożółtego do
czerwonowiśniowego
Następnie określa się stężenie za pomocą
spektrofotometru UV-Vis lub kolorymetru
fotoelektrycznego
Metodę stosuje się w zakresie stężeń 0,5 – 10,00
mg/dm
3
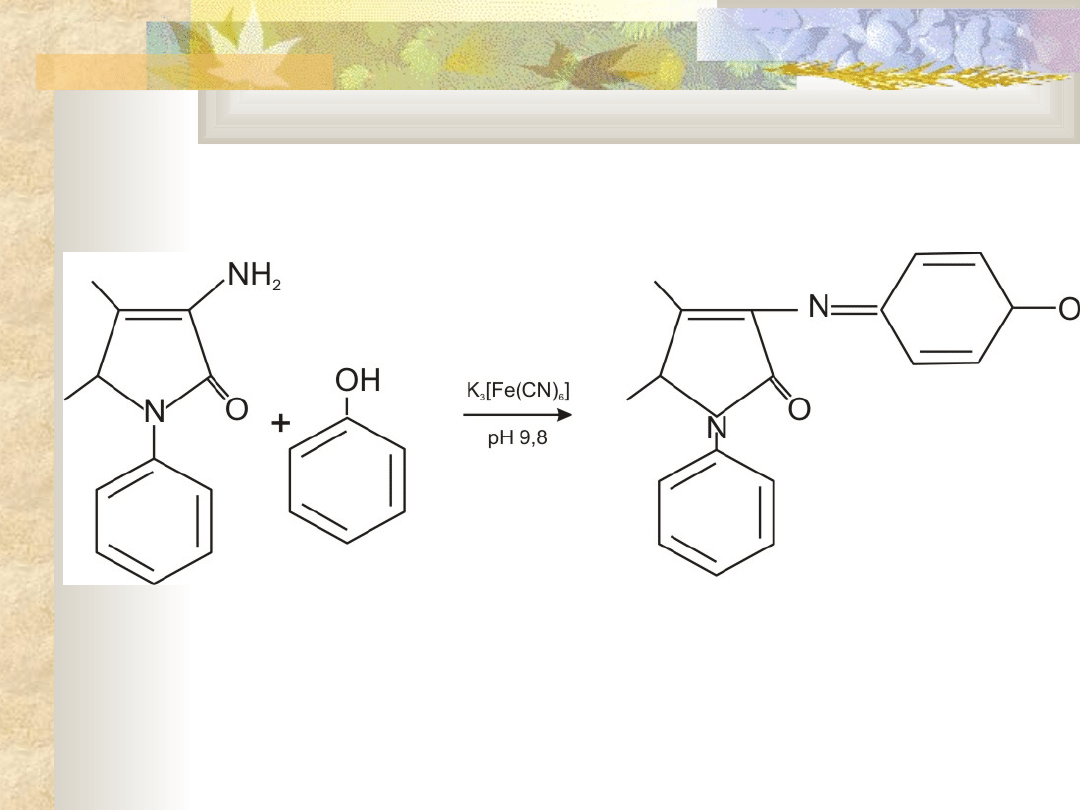
4-
aminoantypiryna
fenol
indofenol

Bibliografia
http://toxnet.nlm.nih.gov/cgi-bin/sis/search
http://portalwiedzy.onet.pl/12011,,,,fenol,haslo.ht
http://pl.wikipedia.org/wiki/Fenol
„Toksykologia współczesna” pod red. W. Seńczuka
Dermatologia kliniczna 2004, 6 (2): „Właściwości
biologiczne, zastosowanie i działania
niepożądane peelingów kwasem
trójchlorooctowym i fenolem”
Medycyna Środowiskowa 2005, 8 (2):
„Zanieczyszczenie powietrza atmosferycznego
fenolem w Płocku w latach 1999-2003”

Dziękuję za uwagę
Document Outline
- FENOL właściwości, działanie na organizm, toksyczność
- Właściwości
- Fenol od alkoholi odróżnia to, że grupa hydroksylowa połączona jest bezpośrednio z pierścieniem aromatycznym, co wpływa na właściwości związku - m. in. na wzrost właściwości kwasowych (stała dysocjacji Ka = 1,3 · 10). Tworzy sole i estry - fenolany. Po raz pierwszy został wydzielony ze smoły węglowej w 1832 r. przez chemika niemieckiego
- Otrzymywanie – metoda kumenowa
- Slide 5
- Zastosowanie
- Zastosowanie
- Toksyczność
- Slide 9
- Stężenia oraz dawki śmiertelne i toksyczne
- Objawy zatrucia ostrego: pary i mgła powodują podrażnienie spojówek, błon śluzowych nosa, gardła, uczucie suchości w nosie, gardle, kaszel. W wysokich stężeniach: zawroty i ból głowy, mdłości, wymioty, duszność, przyspieszenie i pogłębienie oddechów, zaburzenia oddychania, zaburzenia orientacji, zapaść, utratę przytomności. wchłanianie przez skórę mgły, par i roztworu wywołuje zawroty, ból głowy, dezorientację, zaburzenia oddechowe, zapaść, utratę przytomności. skażenie skóry substancją stałą lub ciekłą wywołuje miejscowe zbielenie i oparzenia, które początkowo nie są bolesne, oraz pęcherze, martwicę. skażenie oczu powoduje ostry stan zapalny, uszkodzenie rogówki.
- bezpośrednim następstwem zatrucia jest uszkodzenie wątroby z żółtaczką, uszkodzenie nerek z ich ostrą niewydolnością, zapalenie płuc. połknięcie roztworu wywołuje rozległe oparzenia błon śluzowych jamy ustnej, gardła i dalszych części przewodu pokarmowego, bóle i krwawienie, perforację ścian przewodu pokarmowego, uszkodzenie wątroby i nerek. Objawy zatrucia przewlekłego: zaburzenia ze strony układu pokarmowego: wymioty, bóle gardła, utrata łaknienia, ślinotok, biegunka i jadłowstręt. występuje ochronoza (ciemne zabarwienie skóry i moczu) i wykwity skórne. może wystąpić uszkodzenie wątroby i nerek.
- NDS- 7,8-10 mg/m3 Dopuszczalne stężenie w moczu- 250 mg/g kreatyniny Narażenie zawodowe na fenol występuje głównie w trakcie stosowania żywic fenolowych oraz ich obróbki cieplnej. Są one wykorzystywane jako materiał wiążący w materiałach izolacyjnych, płytach wiórowych, formach odlewniczych. Narażenie na fenol może także występować podczas produkcji koksu, produkcji fenolu i jego pochodnych oraz kaprolaktamu (poliamid, nylon). Źródłem narażenia mogą być wędzone produkty spożywcze oraz woda pitna.
- Przykład: Płock 1999-2003
- Losy w organizmie
- Mechanizm działania toksycznego
- Oznaczanie fenolu w wodzie i moczu:
- PowerPoint Presentation
- Bibliografia
- Dziękuję za uwagę
Wyszukiwarka
Podobne podstrony:
fenol(1) ppt
fenol spektro ppt
03 Sejsmika04 plytkieid 4624 ppt
Choroby układu nerwowego ppt
10 Metody otrzymywania zwierzat transgenicznychid 10950 ppt
10 dźwigniaid 10541 ppt
03 Odświeżanie pamięci DRAMid 4244 ppt
Prelekcja2 ppt
2008 XIIbid 26568 ppt
WYC4 PPT
rysunek rodziny ppt
więcej podobnych podstron