
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH I
PURYNOWYCH I
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
Adrianna Opalska
Wydział Nauk Medycznych
Kierunek lekarski
grupa IV

NUKLEOTYDY I ICH ROLA
NUKLEOTYDY I ICH ROLA
aktywne
prekursory
kwasów nukleinowych
(RNA, DNA)
środki
wymiany energii
(ATP – uniwersalny,
GTP – dla określonej grupy procesów)
ich pochodne uczestniczą w reakcjach
biosyntezy (np. powstawanie glikogenu –
UDP-glukoza, synteza tłuszczów – CDP-
acyloglicerol)
zasadnicze elementy szlaków
przekaźnictwa sygnałów
(cAMP, cGMP, ATP)

NUKLEOTYDY I ICH ROLA
NUKLEOTYDY I ICH ROLA
komponenty
koenzymów
FAD, NAD⁺, NADP⁺
allosteryczne regulatory aktywności
enzymatycznej
ich syntetyczne analogi naturalne są
stosowane w chemioterapii
(inhibitory
enzymów)
allopurynol – analog puryny, stosowany w
leczeniu hiperurykemii i w skazie
moczanowej

SZLAKI BIOSYNTEZY
SZLAKI BIOSYNTEZY
synteza de novo
( zasady nukleotydowe
składane z prostszych związków)
•
PIRYMIDYNY - najpierw szkielet zasady,
następnie przyłączany do rybozy
•
PURYNY - poszczególne fragmenty
dobudowywane do rybozy
synteza rezerwowa
(przyłączanie do
rybozy zasad odzyskanych z innych
procesów)

SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
W SKRÓCIE…
najpierw syntetyzowany jest
pierścień zasady składający się z 2
cząsteczek wodorowęglanu, kwasu
asparaginowego i NH₄⁺
następnie przyłączany jest do rybozy
powstaje nukleotyd pirymidynowy
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
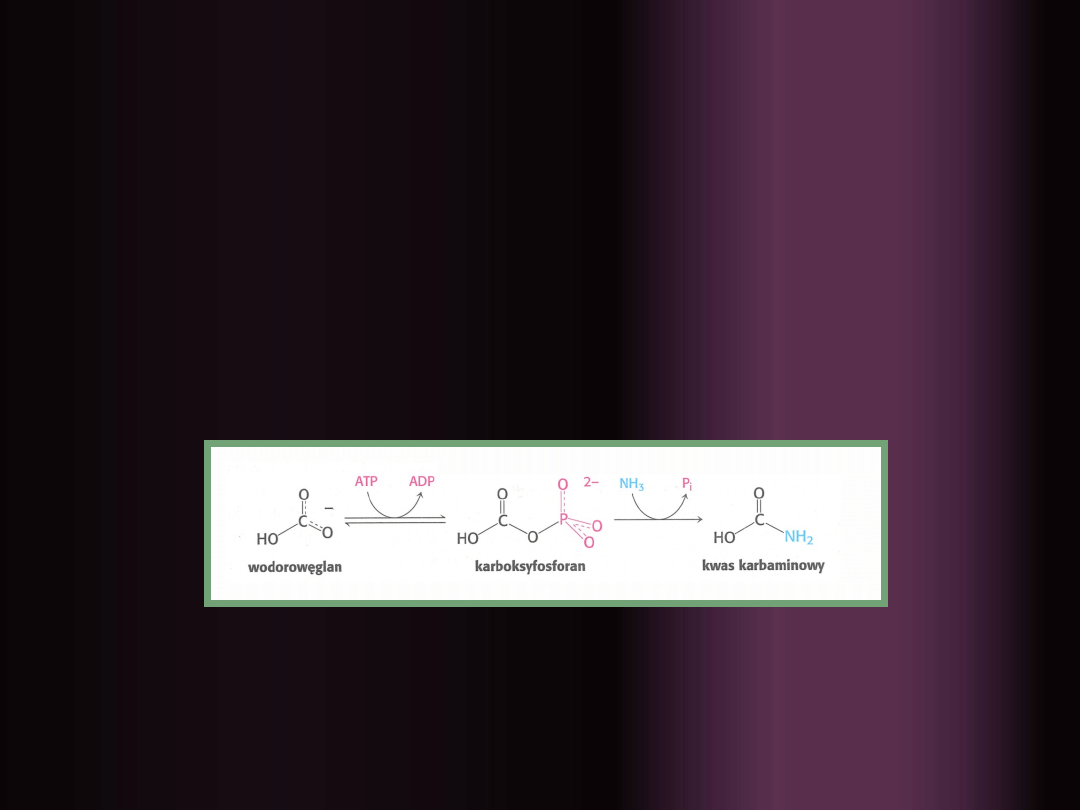
…POCZĄTEK :
kilkuetapowa synteza
karbamoilofosforanu z glutaminy, ATP i CO₂
katalizowana przez cytoplazmatyczną syntetazę
karbamoilofosforanową
I ETAP:
fosforylacja jonu wodorowęglanowego z
wykorzystaniem cząsteczki ATP, powstaje
karboksyfosforan i ADP
II ETAP:
karboksyfosforan reaguje z amoniakiem, w
wyniku czego powstaje kwas karbaminowy i
nieorganiczny fosforan

SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
III ETAP:
kwas karbaminowy ulega
fosforylacji z udziałem drugiej
cząsteczki ATP, powstaje
karbamoilofosforan
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
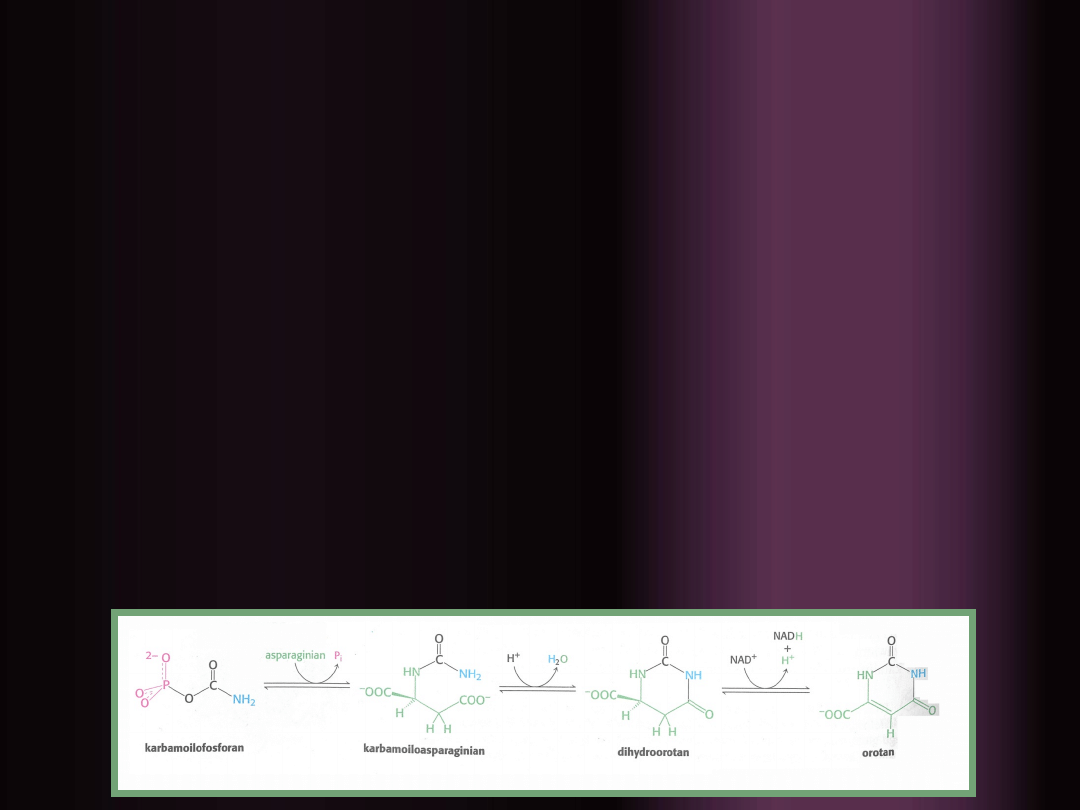
Kondensacja
karbamoilofosforanu
z
asparaginianem
katalizowana przez
karbamoilotransferazę
asparaginianową tworzy
karbamoiloasparaginian
Karbamoiloasparaginian
ulega
cyklizacji do
dihydroorotanu
, który z
udziałem NAD⁺ zostaje utleniony do
orotanu
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
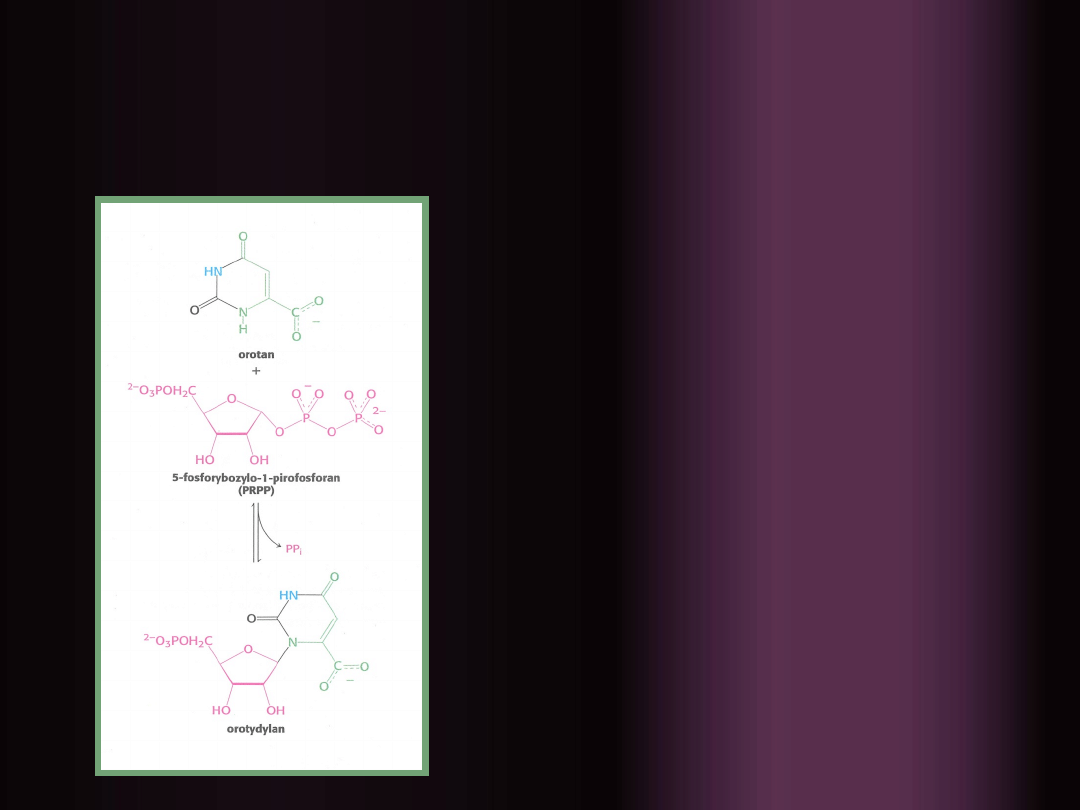
Na tym etapie
orotan
wiąże się z
rybozą
, która
jest elementem
składowym
5-fosforybozylo-1-
pirofosforanu (PRPP)
Po tej reakcji katalizowanej
przez
fosforybozylotransferazę
pirymidynową
orotan
tworzy nukleotyd
pirymidynowy –
orotydylan
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
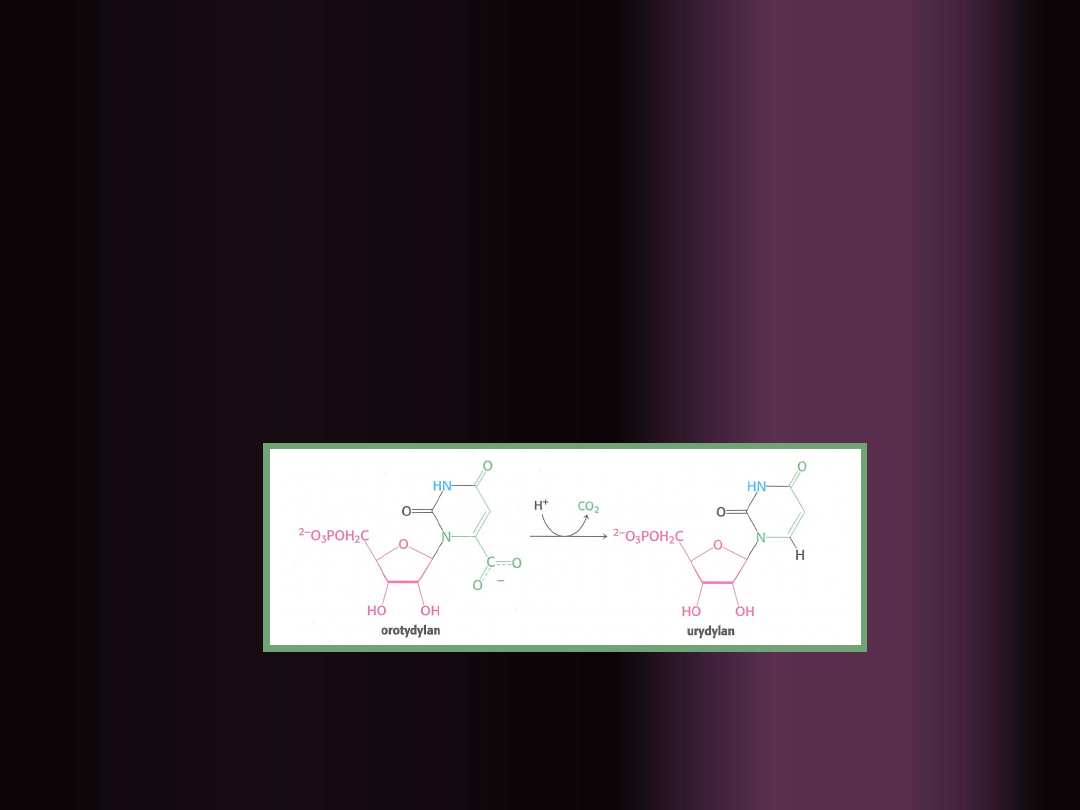
Orotodylan
ulega następnie
dekarboksylacji
dzięki dekarboksylazie
orotydylanowej, w wyniku czego powstaje
urydylan
(UMP)
, główny nukleotyd
pirymidynowy – prekursor RNA
z UMP mogą powstawać kolejne
podstawowe rybonukleotydy pirymidynowe

POWSTAWANIE
POWSTAWANIE
TRIFOSFORANUCYTYDYNY
TRIFOSFORANUCYTYDYNY
Cytydyna powstaje w wyniku przekształcenia
zasady - uracylu obecnego w UMP
Reakcja poprzedzona jest zamianą UMP w
UTP
I.
UMP
+
ATP
↔
UDP
+
ADP
II.
UDP
+
ATP
↔
UTP
+
ADP
CTP
powstanie z UTP po wymianie tlenu
grupy karbonylowej na grupę aminową

REAKCJE REZERWOWE
REAKCJE REZERWOWE
PIRYMIDYN
PIRYMIDYN
Przemieniają rybonukleozydy pirymidynowe,
URYDYNĘ
I
CYTYDYNĘ
oraz
deoksyrybonukleozydy,
TYMIDYNĘ
I
DEOKSYCYTYDYNĘ
w
nukleotydy
Np.: kinaza deoksycytydynowa przekształca
deoksycytydynę
do
monofosforanu
deoksycytydyny (dCMP)
deoksycytydyna
+
ATP
→
dCMP
+
ADP

REGULACJA BIOSYNTEZY
REGULACJA BIOSYNTEZY
NUKLEOTYDÓW
NUKLEOTYDÓW
PIRYMIDYNOWYCH
PIRYMIDYNOWYCH
Dwa pierwsze enzymy biorące udział w
syntezie nukleotydów pirymidynowych są
wrażliwe na
regulację allosteryczną
3 pierwsze i 2 ostatnie enzymy regulowane są
przez
skoordynowaną represję i derepresję
syntetaza karbamoilofosforanowa
hamowana przez UTP i nukleotydy purynowe,
aktywowana przez PRPP
karbamoilotransferaza asparaginianowa
wrażliwa na hamujące działanie CTP
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
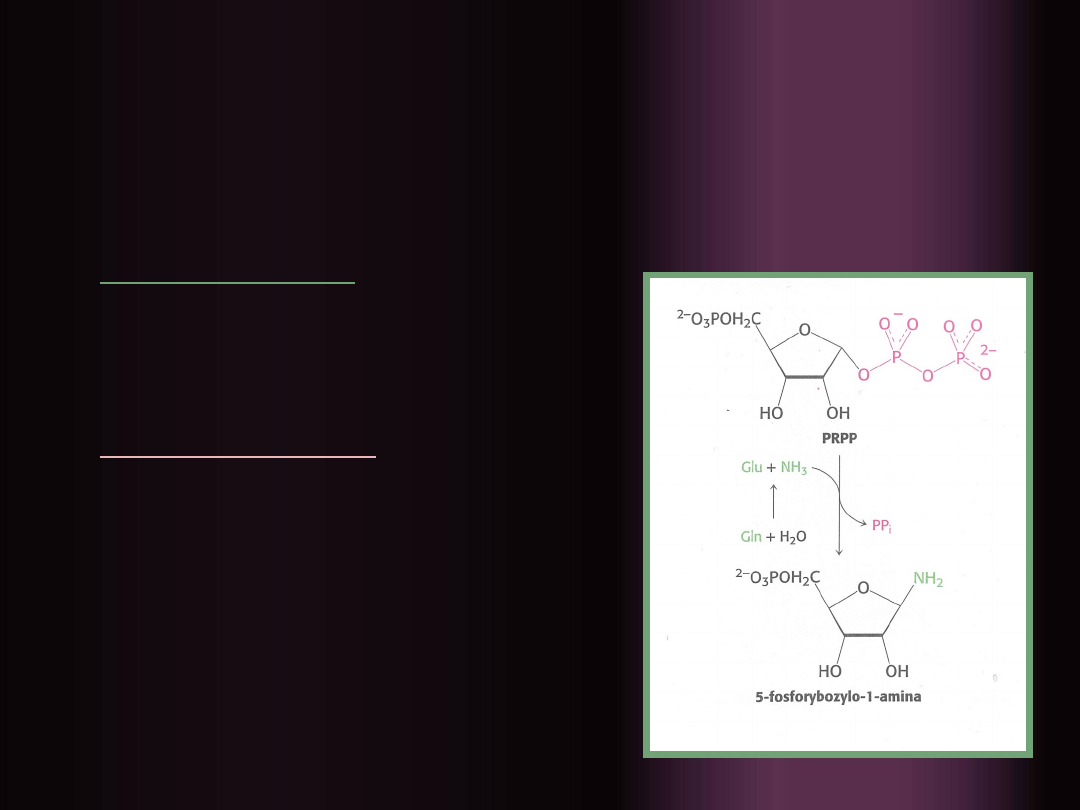
Reakcja syntezy puryn
wymaga PRPP
,
stanowiącego szkielet, na
którym stopniowo
budowana jest zasada
I etap syntezy:
wymiana
pirofosforanu z PRPP na
azot amidowy glutaminy, w
efekcie czego powstaje 5-
fosforybozylo-1-amina, z
grupą aminową w
konfiguracji β
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
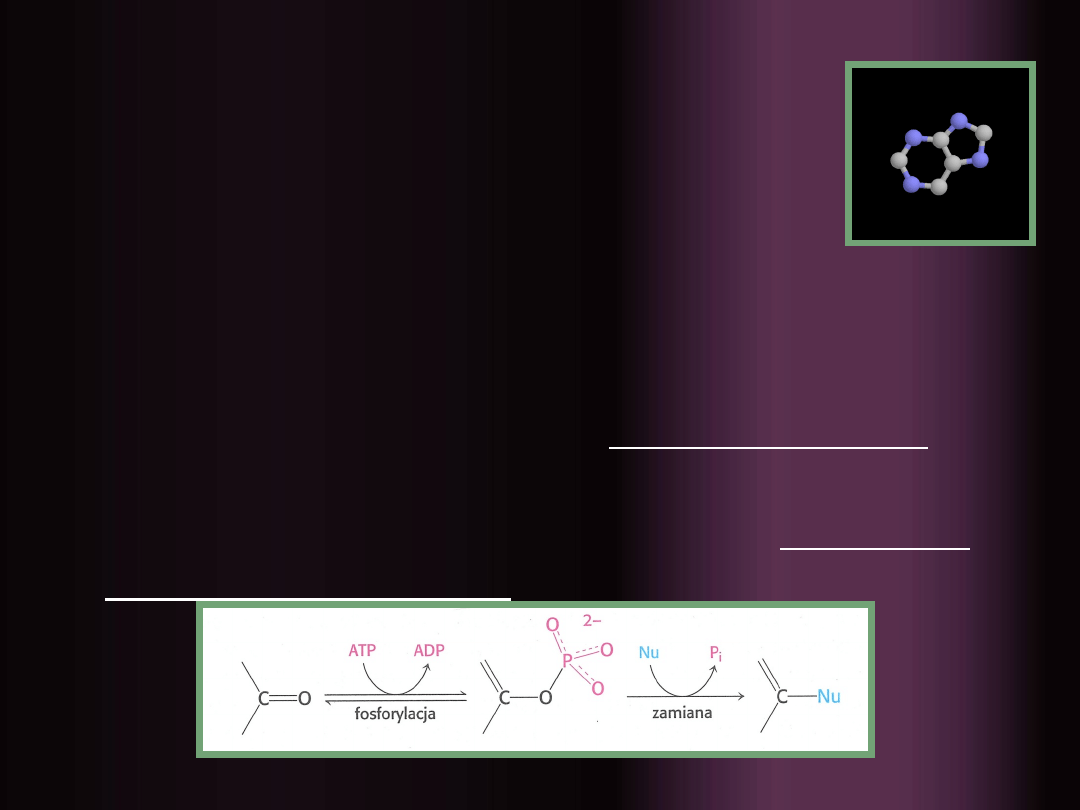
Synteza zachodzi w kolejnych
9 etapach
Pierwsze sześć z nich to reakcje
analogiczne, katalizowane przez enzymy
zawierające domeny wiążące ATP
Każdy etap składa się z aktywacji tlenu
związanego z atomem węgla na drodze
fosforylacji, po której następuje wymiana
grupy fosforanowej
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
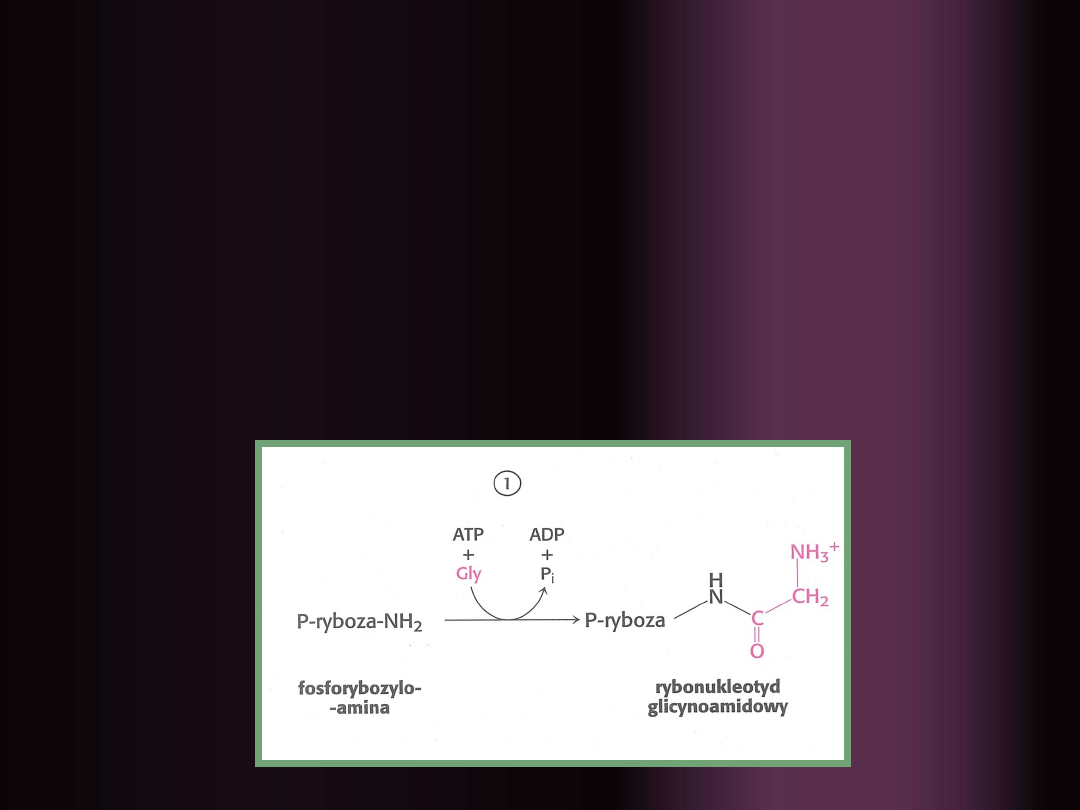
1.
Grupa karboksylowa glicyny
ulega
aktywacji przez fosforylację, następnie
zostaje przyłączana do
grupy aminowej
fosforybozyloaminy
(5-fosfo-β-D-
rybozyloaminy)
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
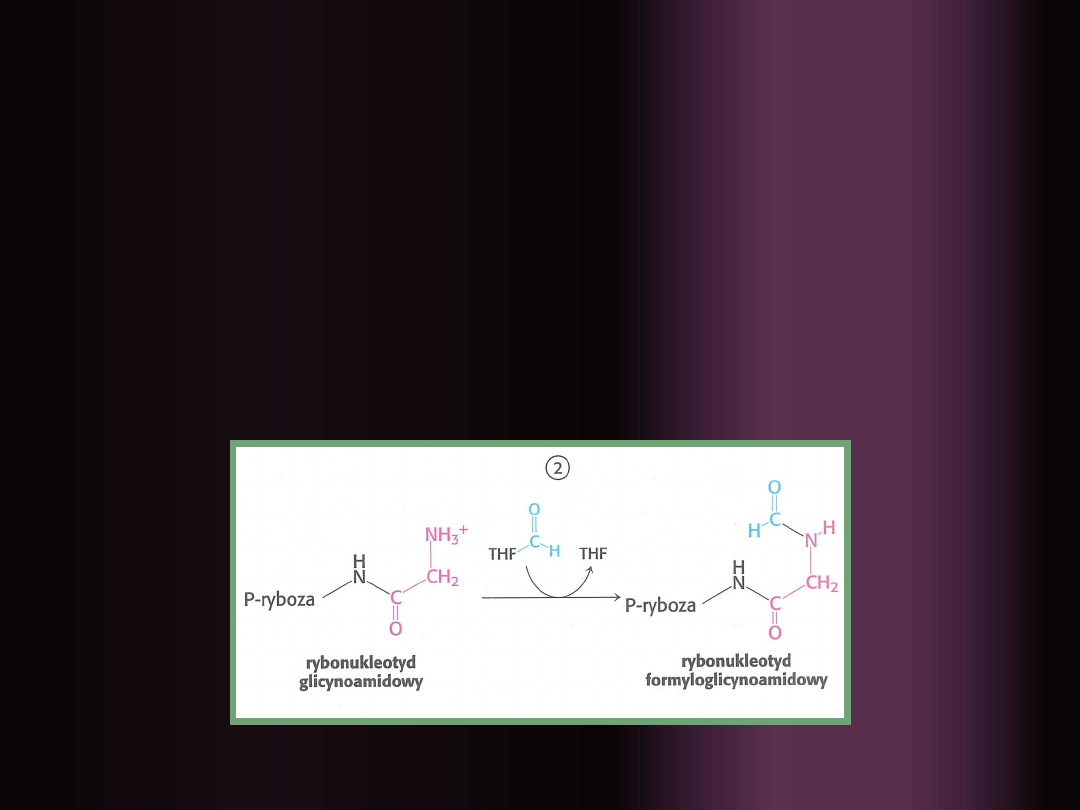
2.
Aktywacja i przyłączenie
mrówczanu
do
grupy aminowej glicyny, powstaje
rybonukleotyd formyloglicynoamidowy
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
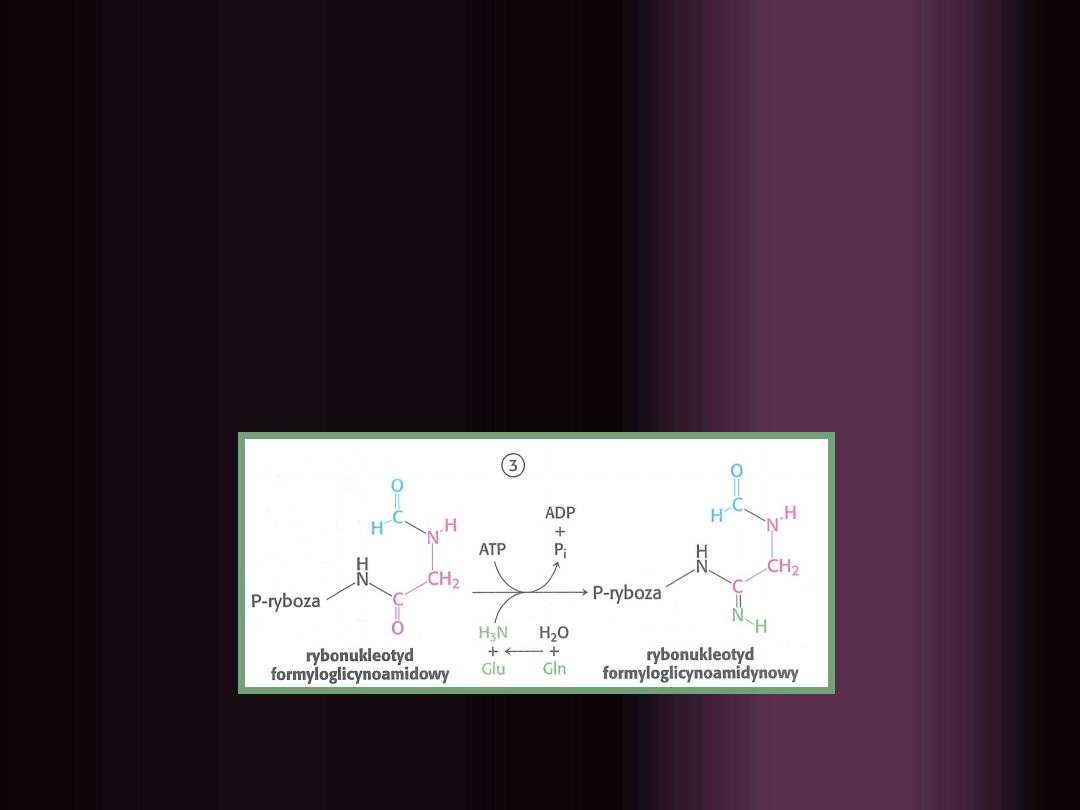
3.
Podstawienie tlenu karbonylowego grupą
NH, powstanie
rybonukleotydu
formyloglicynoamidynowego
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
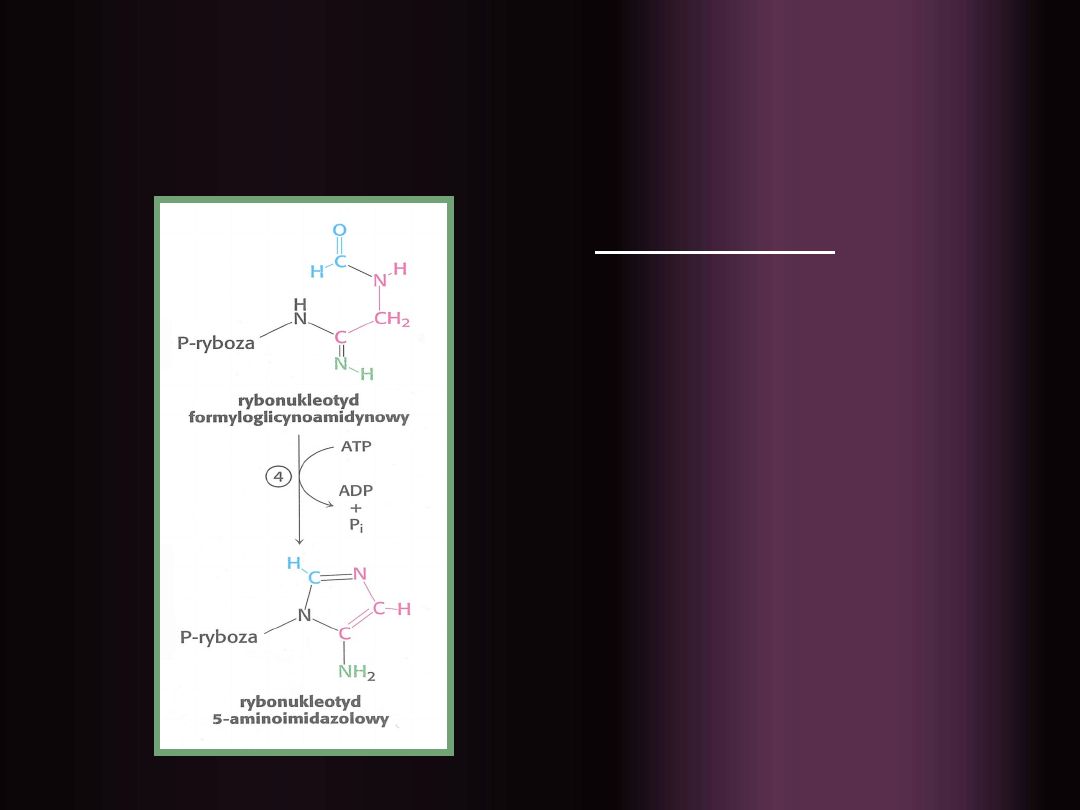
4.
Cyklizacja
rybonukleotydu
formyloglicynoa
midy nowego
,
powstaje
pięcioskładnikow
y
pierścień
imidazolowy
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
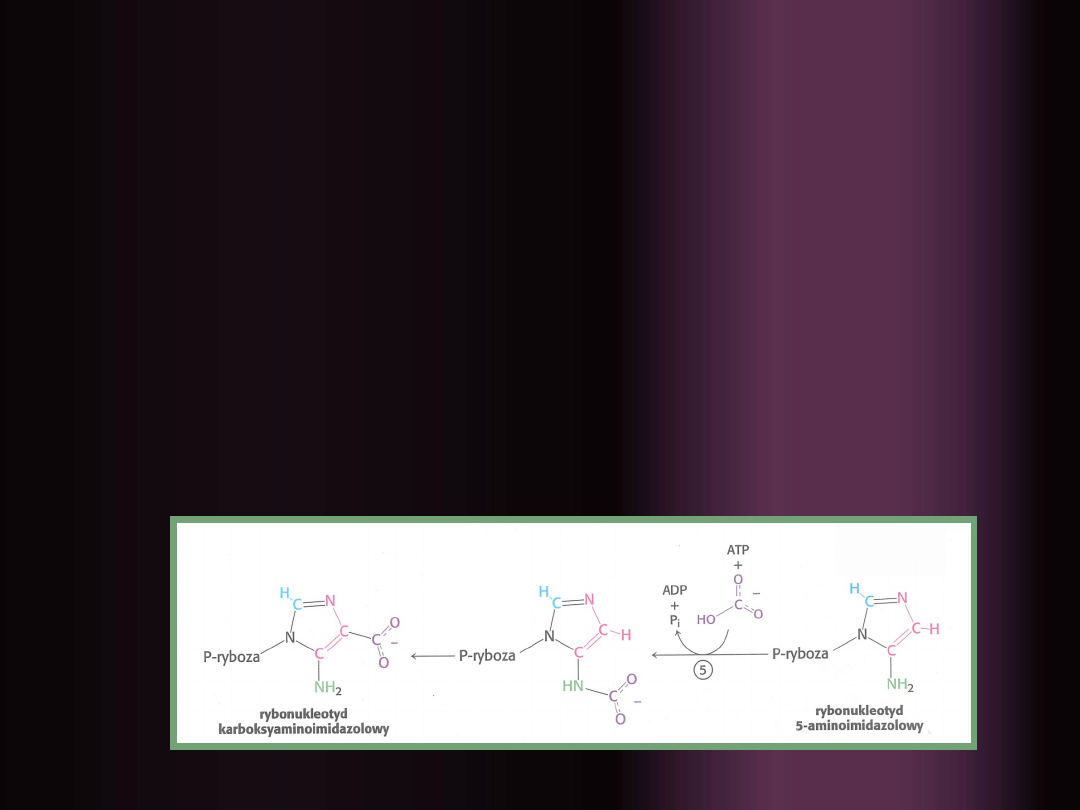
5.
Aktywacja jonu wodorowęglanowego
i atakowanie go przez egzocykliczną
grupę aminową, powstały produkt
ulega rearanżacji i przeniesieniu
grupy karboksylowej na pierścień
imidazolowy
SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
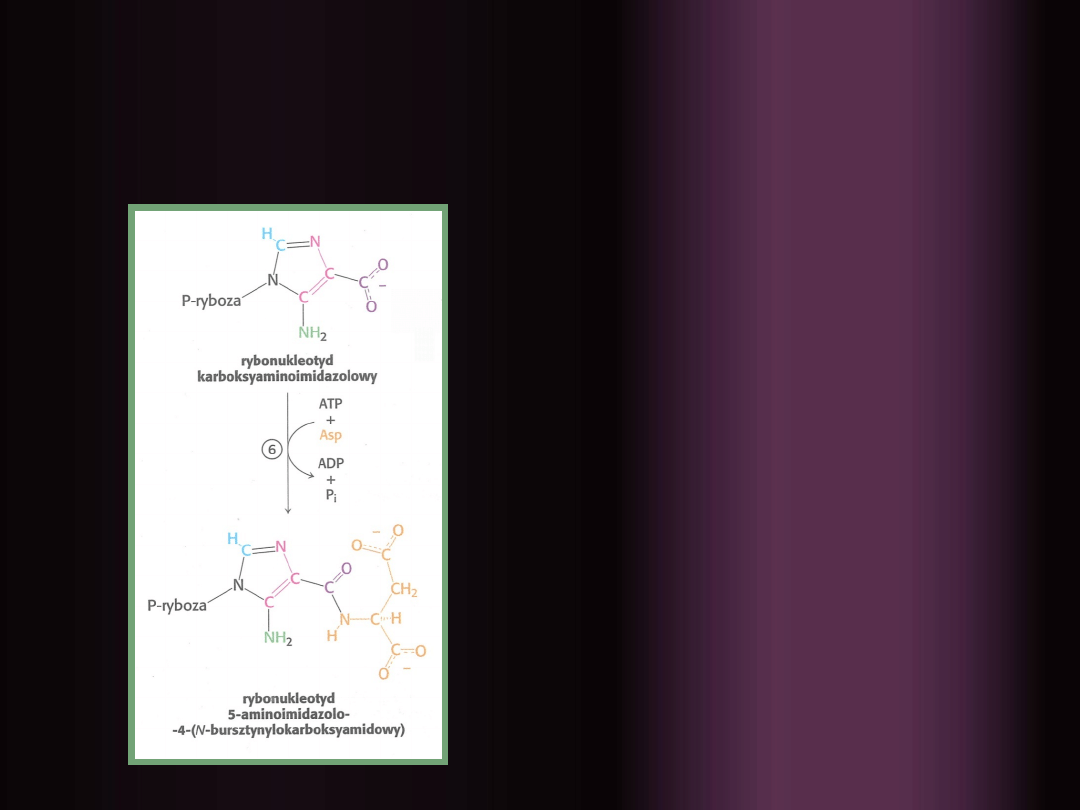
6.
Fosforylacja grupy
karboksylowej
imidazolu, powstała
grupa fosforanowa
zostaje zamieniona na
grupę aminową
będącą częścią
asparaginianu

SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
7.
Oddzielenie się od związku fumaranu i
powstanie
rybonukleotydu 5-
aminoimidazolo-4-karboksyamidowego
8.
Przyłączenie grupy formylowej z N¹⁰-
formylotetrahydrofolianu do azotu, powstaje
rybonukleotyd 5-foraminoimidazolo-4-
karboksyamidowy
9.
Cyklizacja, utrata cząsteczki wody i
przekształcenie produktu w
inozynian (IMP)
Zamiana
IMP
w
AMP
lub
GMP
wymaga
kilku dodatkowych etapów

SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
ZAMIANA IMP W AMP
Przyłączenie
kwasu asparaginowego
do
IMP
W następnym etapie odłącza się fumaran
i powstaje
AMP
Enzym odpowiedzialny za reakcję :
syntaza adenylobursztynianowa

SYNTEZA NUKLEOTYDÓW
SYNTEZA NUKLEOTYDÓW
PURYNOWYCH
PURYNOWYCH
ZAMIANA IMP W GMP
Utlenienie IMP do
ksantylanu
,
wprowadzenie grupy aminowej przy
węglu C-2. Ksantylan zostaje aktywowany
przez przeniesienie grupy AMP z ATP na
atom tlenu nowo powstałej grupy
karbonylowej. Zastąpienie AMP przez jon
amonowy z hydrolizy glutaminy i powstaje
guanylan
Enzym katalizujący: syntetaza GMP

SZLAK REZERWOWY SYNTEZY
SZLAK REZERWOWY SYNTEZY
NUKLEOTYDÓW PURYNOWYCH
NUKLEOTYDÓW PURYNOWYCH
przyłączanie
wolnych zasad
pochodzących z rozpadu nukleotydów lub
przyjmowanych z pożywieniem do
PRPP
Enzymy odpowiedzialne za odzysk zasad
purynowych:
•
Fosforybozylotransferaza adeninowa
adenina
+
PRPP
→
adenylan
+
PP
i
•
Fosforybozylotransferaza hipoksantyno-
guaninowa
guanina
+
PRPP
→
guanylan
+
PP
i
hipoksantyna
+
PRPP
→
inozynian
+
PP
i

REGULACJA BIOSYNTEZY
REGULACJA BIOSYNTEZY
NUKLEOTYDÓW PURYNOWYCH
NUKLEOTYDÓW PURYNOWYCH
Głównym determinantem
nasilenia
syntezy
de novo nukleozydów purynowych jest
stężenie PRPP
(determinowane przez
względną szybkość syntezy PRPP, jego
zużytkowanie i degradację)
Hamowanie 2 pierwszych enzymów
odbywa się przez
IMP
,
GMP
(blok przemiany
inozynianu w ksantylan),
AMP
(blok
przemiany inozynianu w adenylan)

NAD
NAD
⁺, FAD I KOENZYM A
⁺, FAD I KOENZYM A
POWSTAJĄ Z ATP
POWSTAJĄ Z ATP
NAD⁺
- nukleotyd nikotynoamidoadeninowy
I etap syntezy: powstanie
rybonukleotydu
nikotynianu
z
nikotynianu
i
PRPP
II etap syntezy: przeniesienie reszty AMP
z ATP na rybonukleotyd nikotynianowy i
powstanie
deamino-NAD⁺
III etap syntezy: przyłączenie jonu
amonowego od grupy amidowej
glutaminy do grupy karboksylowej
nikotynianu, powstanie
NAD⁺

NAD
NAD
⁺, FAD I KOENZYM A
⁺, FAD I KOENZYM A
POWSTAJĄ Z ATP
POWSTAJĄ Z ATP
FAD
– dinukleotyd flawinoadeninowy; powstaje
z ryboflawiny i dwóch cząsteczek ATP
I etap syntezy:
ryboflawina
+
ATP
→
ryboflawino-5’-fosforan
+
ADP
II etap syntezy:
ryboflawino-5’-fosforan
+
ATP
→
FAD
+
PP
i

BIBLIOGRAFIA…
BIBLIOGRAFIA…
• Berg Jeremy, Tymoczko John, Streyer Lubert, BIOCHEMIA,
Warszawa 2007, PWN.
• Murray Robert, Granner Daryl, Mayes Peter, Biochemia
Harpera, wyd.3, Warszawa 1995.
• Davidson Victor, Sittman Donald, Biochemia wydanie
polskie pod redakcją Janiny Kwiatkowskiej - Korczak,
Wrocław 2002.

DZIĘKUJĘ ZA UWAGĘ !
DZIĘKUJĘ ZA UWAGĘ !
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
Wyszukiwarka
Podobne podstrony:
synteza puryn pirymidyn, medycyna, Biochemia
06 Podstawy syntezy polimerówid 6357 ppt
Pirymidyny 2003
8a Syntezy prostych aminokwasów
Wykład VIII Synteza układów sekwencyjnych
pirymidyny 2003
02 Metody syntezy organicznej VI s1id 3675
Ćwiczenia usprawniające analizę i syntezę wzrokową oraz orientację przestrzenną(1), Ćwiczenia uspraw
Zastosowanie enzymow w syntezie- wyniki, PWR, III semestr
d4 synteza aztreonamu
Synteza jodku ołowiu sprawozdanie
kwasy i pochodne Synteza kwasu?etylosalicylowego1
NANOC W Nano Wyklad 05 Synteza Metodami Chemicznymi II (1)
Synteza Zach Organizacyjne 2010
Syntezy alkenów i alkinów przykłady zadań, Chemia, Organiczna
Prawo+cywilne+-+synteza, DSFIR 1 rok, prawo cywilne i handlowe
VII, Lekarski WLK SUM, lekarski, biochemia, cykl crebsa, puryny i pirymidyny
Budowa chemiczna i synteza lopo Nieznany
GAZ SYNTEZOWY 2009
więcej podobnych podstron